 |
 |
| J Korean Ophthalmol Soc > Volume 64(6); 2023 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ĒÖśņ×ÉņØś 3ļģä ņØ┤ņāü ņ×äņāü Ļ▓░Ļ│╝ ļ░Å ATN (A: atrophy, T: traction, N: neovascularization) classification systemņŚÉ ļö░ļźĖ ņ£äņČĢņä▒ ļ│ĆĒÖöņÖĆ Ļ▓¼ņØĖņä▒ ļ│ĆĒÖöļź╝ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ē ņŗĀņāØĒśłĻ┤Ćņ£╝ļĪ£ ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēļ░øĻ│Ā 3ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢ£ ĒÖśņ×ÉļōżņØś ņØśļ¼┤ĻĖ░ļĪØņØä ĒøäĒ¢źņĀüņ£╝ļĪ£ ņĪ░ņé¼ĒĢśņśĆļŗż. ņ╣śļŻī ņĀäĻ│╝ ļ¦łņ¦Ćļ¦ē Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŗ£ņĀÉņŚÉņä£ņØś ņ£äņČĢņä▒ ņÜöņØĖĻ│╝ Ļ▓¼ņØĖņä▒ ņÜöņØĖņØä ATN classification systemņŚÉ ļö░ļØ╝ ĒÅēĻ░ĆĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
ņ┤Ø 21ļ¬ģ 21ņĢłņØ┤ ļīĆņāüņØ┤ ļÉśņŚłĻ│Ā ĒÅēĻĘĀ ņŚ░ļĀ╣ņØĆ 52.29 ┬▒ 14.6ņäĖņśĆĻ│Ā, ĒÅēĻĘĀ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØĆ 57.65 ┬▒ 18.8Ļ░£ņøöņØ┤ņŚłņ£╝ļ®░ ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼ ĒܤņłśļŖö ĒÅēĻĘĀ 2.9 ┬▒ 1.9ĒÜīņśĆļŗż. 7ņĢł(33.3%)ņŚÉņä£ ņ×¼ļ░£ņØ┤ ļ░£ņāØļÉśņŚłņ£╝ļ®░, 5ņĢł(23.8%)ņŚÉņä£ ļ░śļīĆņĢłņŚÉ ļ░£ņāØĒĢśņśĆļŗż. ņ┤łĻĖ░ ĒÅēĻĘĀ ņŗ£ļĀźņØĆ logarithm of the minimum angle of resolution (logMAR) 0.44 ┬▒ 0.30, ņĄ£ņóģ ņŗ£ļĀźņØĆ 0.33 ┬▒ 0.39ņśĆņ£╝ļ®░, 15ņĢł(71.4%)ņŚÉņä£ ņŗ£ļĀźņØ┤ ņ£Āņ¦ĆļÉśĻ▒░ļéś ĒśĖņĀäļÉśņŚłļŗż. ņ┤łĻĖ░ ņŗ£ļĀźņØĆ ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ ņŗ£ļĀźĻ│╝ ņ£ĀņØśĒĢśĻ▓ī ņŚ░Ļ┤ĆļÉ£ ņØĖņ×ÉļĪ£ ļéśĒāĆļé¼ļŗż(p=0.026). ņ£äņČĢņä▒ ņÜöņØĖņØś ļŗ©Ļ│äĻ░Ć ņ¦äĒ¢ēļÉ£ Ļ▓ĮņÜ░Ļ░Ć 4ņĢł(19.0%)ņØ┤ņŚłņ£╝ļ®░, Ļ▓¼ņØĖņä▒ ņÜöņØĖņŚÉņä£ļŖö 1ņĢł(4.8%)ņŚÉņä£ļŖö ĒśĖņĀäņØä ļ│┤ņśĆņ£╝ļ®░ 5ņĢł(23.8%)ņŚÉņä£ ņ¦äĒ¢ēņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż.
ABSTRACT
Purpose
To evaluate the clinical outcomes of myopic choroidal neovascularization (CNV) and atrophic and tractional changes according to the ATN (A: atrophy, T: traction, N: neovascularization) classification system.
Methods
This was a retrospective review of the medical records of myopic CNV patients treated with intravitreal anti-vascular endothelial growth factor (anti-VEGF) injections and followed up for at least 3 years. Atrophic and tractional components were graded according to the ATN system at baseline and the last visit.
Results
The study included 21 eyes in 21 patients. The mean age was 52.29 ┬▒ 14.6 years, the mean follow-up duration was 57.65 ┬▒ 18.8 months, and the mean number of injections was 2.9 ┬▒ 1.9. Recurrence occurred in seven eyes (33.3%). Five patients (23.8%) developed myopic CNV in the contralateral eye. The mean initial and final logarithm of the minimum angle of resolution (logMAR) visual acuities were 0.44 ┬▒ 0.30 and 0.33 ┬▒ 0.39, respectively. Visual acuity was maintained or improved compared to baseline in 15 eyes (71.4%). Baseline visual acuity was significantly associated with the final visual acuity (p = 0.026). Based on the ATN classification system, the atrophic component progressed in four eyes (19.0%), while the tractional component improved in one eye (4.8%) and progressed in five eyes (23.8%).
ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņØĆ ļ│æņĀü ĻĘ╝ņŗ£ ņżæ 5-11%ņŚÉņä£ ļ░£ņāØĒĢśļ®░ ņŗ£ļĀźņĀĆĒĢśļź╝ ņØ╝ņ£╝ĒéżļŖö ĒØöĒĢ£ ņøÉņØĖņ£╝ļĪ£ 50ņäĖ ņØ┤ĒĢśņŚÉņä£ ļ░£ņāØĒĢ£ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņØś 62%ļź╝ ņ░©ņ¦ĆĒĢ£ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż. ņĀÉņ¦äņĀüņØĖ ņżæņŗ¼ ņŗ£ļĀźņĀĆĒĢśļź╝ ņØ╝ņ£╝Ēé¼ ņłś ņ׳ņ£╝ļ®░ ņ╣śļŻīĒĢśņ¦Ć ņĢŖņØä Ļ▓ĮņÜ░ ļ▓ĢņĀü ņŗżļ¬ģņ£╝ļĪ£ ņØ┤ņ¢┤ņ¦ł ņłśļÅä ņ׳ļŗż. ļ░śļīĆņĢłņŚÉ ļ░£ņāØ ļ╣łļÅäĻ░Ć ĒØöĒĢ£ ĒÄĖņØĖļŹ░ ņןĻĖ░Ļ░ä ņŚ░ĻĄ¼ļź╝ ĒåĄĒĢ┤ ņĢĮ 34.8%ņŚÉņä£ ļ░£ņāØĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż.1,2
Ļ│╝Ļ▒░ņŚÉļŖö Ļ┤æņŚŁĒĢÖņ╣śļŻīĻ░Ć ņŗ£Ē¢ēļÉśņŚłņ£╝ļéś ņżæņŗ¼ņÖĆņĢäļל ņŗĀņāØĒśłĻ┤ĆņŚÉ ļīĆĒĢ┤ņä£ļŖö ņןĻĖ░Ļ░ä ņŗ£ļĀź ņśłĒøäĻ░Ć ņóŗņ¦Ć ņĢŖņĢä Ēśäņ×¼ļŖö ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼Ļ░Ć ņØ╝ņ░© ņ╣śļŻīļĪ£ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż.3,4
ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×ÉļĪ£ ļ▓Āļ░öņŗ£ņŻ╝ļ¦Ö(Avastin┬«, Genentech, Inc., South San Francisco, CA, USA), ļØ╝ļŗłļ╣äņŻ╝ļ¦Ö(Lucentis┬«, Genentech, Inc.), ņĢĀĒöīļ”¼ļ▓äņģēĒŖĖ(Eylea┬«, Regeneron, Rensselaer, NY, USA)Ļ░Ć ĻĄŁļé┤ņŚÉņä£ ņØ┤ņÜ® Ļ░ĆļŖźĒĢśļŗż. ļ▓Āļ░öņŗ£ņŻ╝ļ¦Ö ņ╣śļŻīņŚÉ ļīĆĒĢ£ ņןĻĖ░ ņŚ░ĻĄ¼ņŚÉņä£ ņŻ╝ļĪ£ ĒĢäņÜöĒĢĀ ļĢī ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ 5ļģä ņØ┤ņāü ņŚ░ĻĄ¼ņŚÉņä£ ĒÅēĻĘĀ 4.9ĒÜī, 10ļģä ņØ┤ņāü ņŚ░ĻĄ¼ņŚÉņä£ ĒÅēĻĘĀ 6.8ĒÜī ņŻ╝ņé¼ ņ╣śļŻīĻ░Ć ņŗ£Ē¢ēļÉśņŚłĻ│Ā ņ╣śļŻī ņĀäĻ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ņ¢æĒśĖĒĢ£ ņŗ£ļĀź Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż.5,6
ĻĄŁļé┤ ļ│┤Ļ│ĀņŚÉņä£ļŖö Seo and Chang7ņØ┤ ļ▓Āļ░öņŗ£ņŻ╝ļ¦Ö ņ╣śļŻīņØś 2ļģä ņןĻĖ░ Ļ▓░Ļ│╝ļź╝ ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░ Lee et al8ņØĆ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņŚÉņä£ ļ▓Āļ░öņŗ£ņŻ╝ļ¦Ö ņ╣śļŻīņØś 1ļģä ņØ┤ņāü ņןĻĖ░ ņ╣śļŻī Ļ▓░Ļ│╝ļź╝ ļ│┤Ļ│ĀĒĢśņśĆļŗż.
RuizŌĆÉMedrano et al9ņØĆ ņ╣╝ļØ╝ņĢłņĀĆņé¼ņ¦äĻ│╝ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņ£äņČĢņä▒ ņÜöņØĖ(atrophic component, A), Ļ▓¼ņØĖņä▒ ņÜöņØĖ(tractional component, T), ņŗĀņāØĒśłĻ┤Ćņä▒ ņÜöņØĖ(neovascular component, N)ņØä ĒÅēĻ░ĆĒĢĀ ņłś ņ׳ļŖö ATN classification and grading systemņØä ņåīĻ░£ĒĢśņśĆļŗż. ATN systemņØĆ ĻĘ╝ņŗ£ņä▒ ĒÖ®ļ░śļ│æņ”Ø ĒÅēĻ░ĆņŚÉņä£ Ļ░äļŗ©ĒĢśļ®┤ņä£ļÅä ļåÆņØĆ ņŗĀļó░ļÅäņÖĆ ņ×¼Ēśäņä▒ņØä ļ│┤ņŚ¼ ņŚ¼ļ¤¼ ņŚ░ĻĄ¼ņŚÉņä£ ņØ┤ņÜ®ļÉśĻ│Ā ņ׳ļŗż.10
Ēśäņ×¼Ļ╣īņ¦Ć ĒĢ£ņĢłņ¦ĆņŚÉņä£ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņŚÉ ļīĆĒĢ£ 3ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŚ░ĻĄ¼Ļ░Ć ņŚåņŚłĻ│Ā ĻĄŁļé┤ņÖĖņĀüņ£╝ļĪ£ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ņŚ░ĻĄ¼ņŚÉņä£ ATN classification systemņØä ņØ┤ņÜ®ĒĢ£ ņŚ░ĻĄ¼ļŖö ļō£ļ¼Ė Ļ▓āņ£╝ļĪ£ ņĢīĻ│Ā ņ׳ļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ņ╣śļŻī Ēøä 3ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņŚÉņä£ņØś ņ×äņāü Ļ▓░Ļ│╝ ļ░Å ATN classification systemņŚÉ ļö░ļźĖ ņ£äņČĢņä▒ ņÜöņØĖĻ│╝ Ļ▓¼ņØĖņä▒ ņÜöņØĖņØś ļ│ĆĒÖöļź╝ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢśņśĆļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ļŗ©ņØ╝ĻĖ░Ļ┤ĆņŚÉņä£ ņŗ£Ē¢ēļÉ£ ĒøäĒ¢źņĀü Ļ┤Ćņ░░ ņŚ░ĻĄ¼ļĪ£ ĒŚ¼ņŗ▒ĒéżņäĀņ¢ĖņŚÉ ņ×ģĻ░üĒĢśņŚ¼ ņŗ£Ē¢ēļÉśņŚłņ£╝ļ®░ ļłäļäżņĢłĻ│╝ļ│æņøÉ ņ×äņāüņŚ░ĻĄ¼ņ£żļ”¼ņ£äņøÉĒÜī(Institutional Review Board, IRB) ņŖ╣ņØĖņØä ĒÜŹļōØĒĢśņśĆļŗż(ņŖ╣ņØĖļ▓łĒśĖ: N-2211-002-999). ņØśļ¼┤ĻĖ░ļĪØ Ļ▓ĆņāēņØä ĒåĄĒĢ┤ -6.0ļööņśĄĒä░ ņØ┤ņāüņØś ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņ╣ś ļśÉļŖö ņĢłņČĢņן ĻĖĖņØ┤Ļ░Ć 26 mm ņØ┤ņāüņØś ĒÖśņ×É ņżæ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ćņ£╝ļĪ£ ņ¦äļŗ©ļÉśņ¢┤ ĒĢäņÜöĒĢĀ ļĢīļ¦łļŗż ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É(anti-VEGF) ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēļ░øņØĆ Ļ▓ĮņÜ░ļź╝ ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆļŗż. ļśÉĒĢ£, ņ▓½ ņ╣śļŻī ņŗ£ ņ╣╝ļØ╝ ņĢłņĀĆņé¼ņ¦ä, ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØ┤ ņŗ£Ē¢ēļÉśņŚłņ£╝ļ®░ ņ▓½ ņ╣śļŻī Ēøä 36Ļ░£ņøö ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņØ┤ ļÉśņŚłļŹś Ļ▓ĮņÜ░ļź╝ ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆļŗż. ņĀ£ņÖĖ ĻĖ░ņżĆņØĆ ļŗżņØīĻ│╝ Ļ░Öļŗż. 1) ņØ┤ņĀä ņ£Āļ”¼ņ▓┤ļ¦Øļ¦ēņłśņłĀņØä ņŗ£Ē¢ēļ░øņØĆ Ļ▓ĮņÜ░, 2) ļŗżļźĖ ņøÉņØĖņŚÉ ņØśĒĢ£ ņĢłĻĄ¼ ļé┤ ņŻ╝ņé¼ ļśÉļŖö Ļ┤æņŚŁĒĢÖņÜöļ▓Ģ ņ╣śļŻī ļ│æļĀźņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░, 3) ņĢĮņŗ£, 4) Ļ│ĀĒśłņĢĢņä▒ ļ¦Øļ¦ēļ│æņ”Ø, ļŗ╣ļć©ļ¦Øļ¦ēļ│æņ”Ø, ņŖĄņä▒ ļéśņØ┤Ļ┤ĆļĀ©ĒÖ®ļ░śļ│Ćņä▒ņØ┤ ļÅÖļ░śļÉ£ Ļ▓ĮņÜ░ ļō▒ņØ┤ļ®░, Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ļÅÖņĢł ņ¢æņĢłņØ┤ ņ¦äļŗ©ļÉ£ Ļ▓ĮņÜ░ļŖö ļ©╝ņĀĆ ļ░£ņāØĒĢ£ ņĢłņØä ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆļŗż.
ņ▓½ ņ╣śļŻī ņŗ£ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź, ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼, ņĢłņĀĆĻ▓Ćņé¼, ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü(optical coherence tomography; SpectralisTM Heidelberg Engineering, Dossenheim, Germany) ļ░Å ĒśĢĻ┤æņĢłņĀĆĒśłĻ┤ĆņĪ░ņśüņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ ņØĖļÅäņŗ£ņĢäļŗīĻĘĖļ”░ĒśłĻ┤ĆņĪ░ņśüņłĀņØĆ ņØśņé¼ņØś ĒīÉļŗ©ņŚÉ ļö░ļØ╝ ņØ╝ļČĆņŚÉņä£ ņŗ£Ē¢ēļÉśņŚłļŗż. ĒÖśņ×ÉļŖö ņ¦äļŗ© Ēøä 1ĒÜī Ēś╣ņØĆ ņŚ░ņåŹņĀüņ£╝ļĪ£ 2-3ĒÜī ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼ļź╝ ņŗ£Ē¢ēļ░øņĢśļŗż. ņŻ╝ņé¼ Ēøä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ļÅÖņĢł ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņŚÉņä£ ļ¦Øļ¦ēĒĢśņĢĪ, ļ¦Øļ¦ēļé┤ņĢĪņØ┤ ļ░£ņāØļÉ£ Ļ▓ĮņÜ░ļéś ņĢłņĀĆĻ▓Ćņé¼ņŚÉņä£ ļ¦Øļ¦ēņČ£ĒśłņØ┤ ļ░£ņāØļÉ£ Ļ▓ĮņÜ░ļź╝ ņ×¼ļ░£ļĪ£ ĒīÉļŗ©ĒĢśņŚ¼ ņČöĻ░ĆņĀüņØĖ ņŻ╝ņé¼ ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż.
ņ×ÉļŻī ļČäņäØņØĆ ņ▓½ ņ╣śļŻī ņŗ£ņÖĆ ļ¦łņ¦Ćļ¦ē Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŗ£ņĀÉņŚÉņä£ņØś ļéśņØ┤, ņä▒ļ│ä, ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņ╣ś, ĻĖ░ņĀĆ ņ¦łĒÖś, ņłśņĀĢņ▓┤ ņāüĒā£, ĻĄ┤ņĀłĻĄÉņĀĢņłśņłĀ ņŚ¼ļČĆ, ņŻ╝ņé¼ Ēܤņłś, ņ×¼ļ░£ ņŚ¼ļČĆ, ņ×¼ļ░£ Ēܤņłś, ņ×¼ļ░£Ļ╣īņ¦ĆņØś ĻĖ░Ļ░ä, Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ļō▒ņØ┤ ĒżĒĢ©ļÉśņŚłļŗż. ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü ņåīĒöäĒŖĖņø©ņ¢┤ņŚÉņä£ ļČäņĀł(segmentation)ņØ┤ ņĀĢĒÖĢĒĢśņ¦Ć ņĢŖņĢä ņżæņŗ¼ņÖĆ ņ£äņ╣śņŚÉņä£ ņłśļÅÖ ņĖĪņĀĢĒĢ£ ĻĖĖņØ┤ļź╝ ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗śļĪ£ ņĀĢņØśĒĢśņśĆņ£╝ļ®░, ĒÖ®ļ░śĒĢś ļ¦Øļ¦ēņāēņåīņāüĒö╝ņĖĄņØś ņÖĖņĖĪ Ļ▓ĮĻ│äņÖĆ ļ¦źļØĮļ¦ēĻ│Ąļ¦ē Ļ▓ĮĻ│äĻ╣īņ¦Ć 1:1 ╬╝m ļ¬©ļō£ļĪ£ ņĖĪņĀĢĒĢ£ ņłśņ¦ü ĻĖĖņØ┤ļź╝ ļ¦źļØĮļ¦ēļæÉĻ╗śļĪ£ ņĀĢņØśĒĢśņśĆļŗż. ņ▓½ ņ╣śļŻī ņŗ£ņĀÉĻ│╝ ļ¦łņ¦Ćļ¦ē Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŗ£ņĀÉņŚÉņä£ ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗ś, ļ¦źļØĮļ¦ēļæÉĻ╗śļź╝ 2ļ¬ģņØś ņĢłĻ│╝ņØśņé¼Ļ░Ć ņĖĪņĀĢĒĢśņśĆļŗż. ļśÉĒĢ£, ATN grading systemņØä ņ░ĖĻ│ĀĒĢśņŚ¼ ņ╣╝ļØ╝ņĢłņĀĆņé¼ņ¦ä ļ░Å ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņ▓½ ņ╣śļŻī ņŗ£ņÖĆ ļ¦łņ¦Ćļ¦ē Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŗ£ņĀÉņŚÉņä£ņØś ņ£äņČĢņä▒ ņÜöņØĖ, Ļ▓¼ņØĖņä▒ ņÜöņØĖņØä ĒÅēĻ░ĆĒĢśņśĆļŗż(Table 1). ĒÅēĻ░ĆļŖö Ļ░ü ĒÖśņ×ÉņØś ņĀĢļ│┤ļź╝ ņĀ£Ļ│ĄĒĢśņ¦Ć ņĢŖĻ│Ā ņĢłņĀĆ ļ░Å ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü ņé¼ņ¦äļ¦īņØä Ļ┤Ćņ░░ņ×ÉņŚÉĻ▓ī ļ¼┤ņ×æņ£ä ņł£ņä£ļĪ£ ņĀ£Ļ│ĄĒĢśņŚ¼ ĒīÉļÅģņØä ĒĢśņśĆņ£╝ļ®░ ņØśĻ▓¼ņØ┤ ļŗżļźĖ Ļ▓ĮņÜ░ ļ¦Øļ¦ē ņĀäļ¼ĖņØśņØś Ļ▓░Ļ│╝Ļ░ÆņØä ņé¼ņÜ®ĒĢśņśĆļŗż.
ĒåĄĻ│äļČäņäØņØĆ IBM SPSS Statistics version 29.0 (IBM Corp., Armonk, NY, USA)ņØä ņØ┤ņÜ®ĒĢśņśĆļŗż. ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ĒåĄĻ│äĒĢÖņĀü ļČäņäØņØä ņ£äĒĢ┤ logarithm of minimal angle of resolution (logMAR) Ļ░Æņ£╝ļĪ£ ļ│ĆĒÖśĒĢśņśĆļŗż. ļ│ĆņłśļōżĻ│╝ ņĄ£ņóģ ņŗ£ļĀźĻ│╝ņØś ņŚ░Ļ┤Ćņä▒ņØä ņĢīņĢäļ│┤ĻĖ░ ņ£äĒĢ┤ ļŗ©ļ│Ćļ¤ē ļČäņäØĻ│╝ ļŗżļ│Ćļ¤ē ļČäņäØņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņ▓½ ņ╣śļŻī ņŗ£ ĒÖśņ×ÉņØś ļéśņØ┤ļź╝ ĻĖ░ņżĆņ£╝ļĪ£ 50ņäĖ ņØ┤ņĀäņŚÉ ļ░£ņāØĒĢ£ ĻĄ░Ļ│╝ 50ņäĖ ņØ┤ņāüņŚÉņä£ ļ░£ņāØĒĢ£ ĻĄ░ņ£╝ļĪ£ ļČäļźśĒĢśņŚ¼ ņČöĻ░ĆņĀüņØĖ ļ╣äĻĄÉ ļČäņäØņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņŚ░ņåŹļ│ĆņłśņØś Ļ▓ĮņÜ░ Mann-Whitney U testļź╝ ņØ┤ņÜ®ĒĢśņśĆņ£╝ļ®░, ļ¬ģļ¬®ļ│ĆņłśņØś ļ╣äĻĄÉņŚÉņä£ļŖö chi-square testļź╝ ņØ┤ņÜ®ĒĢśņśĆļŗż. pĻ░ÆņØ┤ 0.05 ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░ļź╝ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ Ļ░Æņ£╝ļĪ£ ņĀĢņØśĒĢśņśĆļŗż.
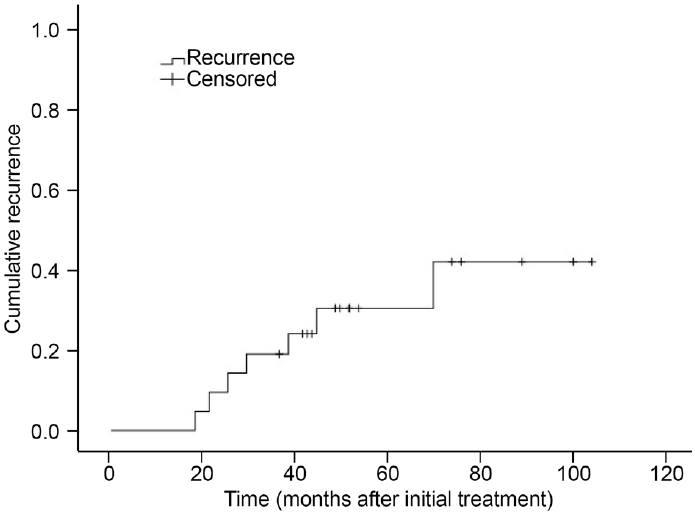
ņ┤Ø 21ļ¬ģņØś ĒÖśņ×ÉĻ░Ć ĒżĒĢ©ļÉśņŚłņ£╝ļ®░ ĒÅēĻĘĀ ņŚ░ļĀ╣ņØĆ 52.29 ┬▒ 14.6ņäĖ, ĒÅēĻĘĀ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØĆ 57.65 ┬▒ 18.8Ļ░£ņøöņØ┤ņŚłļŗż. ņŚ¼ņä▒ņØ┤ 18ļ¬ģ(85.7%)ņØ┤ņŚłņ£╝ļ®░ 12ņĢł(57.1%)ņØĆ ņóīņĢłņŚÉņä£ ļ░£ņāØļÉśņŚłļŗż. ĻĄ┤ņĀłĻĄÉņĀĢņłśņłĀņØä ņŗ£Ē¢ēļ░øņĢśļŹś ĒÖśņ×ÉļŖö 9ļ¬ģ(42.9%)ņØ┤ņŚłņ£╝ļ®░ ļ░▒ļé┤ņןņłśņłĀņØä ņŗ£Ē¢ēļ░øņĢśļŹś ĒÖśņ×ÉļŖö 5ļ¬ģ(23.8%)ņØ┤ņŚłļŗż. ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņ╣śļŖö -5.98 ┬▒ 6.4ļööņśĄĒä░, ņ▓½ ņ╣śļŻī ņŗ£ logMAR ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ 0.44 ┬▒ 0.30ņØ┤ņŚłļŗż. Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ļÅÖņĢł ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼ ĒܤņłśļŖö ĒÅēĻĘĀ 2.9 ┬▒ 1.9ĒÜīņśĆņ£╝ļ®░ 7ņĢł(33.3%)ņŚÉņä£ ņ×¼ļ░£ņØ┤ ļ░£ņāØļÉśņŚłņ£╝ļ®░ ņ▓½ ņ×¼ļ░£Ļ╣īņ¦ĆņØś ļ░£ņāØ ĻĖ░Ļ░äņØĆ 37.71 ┬▒ 16.5Ļ░£ņøöņØ┤ņŚłļŗż(Fig. 1.). 5ļ¬ģ(23.8%)ņŚÉņä£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ļÅÖņĢł ļ░śļīĆņĢłņŚÉņä£ļÅä ļ░£ņāØļÉśņŚłļŗż. ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ņĀÉņŚÉņä£ņØś logMAR ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ 0.33 ┬▒ 0.39ņśĆļŗż(Table 2). ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ņĀÉņŚÉņä£ļŖö logMAR ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźĻ│╝ ļŗ©ļ│Ćļ¤ē ļČäņäØņŚÉņä£ ņ▓½ ņ╣śļŻī ņŗ£ logMAR ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØ┤ ļéśņüĀņłśļĪØ(r=0.528, p=0.017), ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņ╣śĻ░Ć ļé«ņØäņłśļĪØ(r=-0.446, p=0.043) ļéśņü£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż. ļŗżļ│Ćļ¤ē ļČäņäØņŚÉņä£ ņ▓½ ņ╣śļŻī ņŗ£ logMAR ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź(p=0.026)ņØ┤ ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ņĀÉņŚÉņä£ņØś ņŗ£ļĀźĻ│╝ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ Ļ┤ĆĻ│äļź╝ ļ│┤ņśĆļŗż(Table 3).
ATN grading systemņŚÉ ļö░ļźĖ ļČäņäØņŚÉņä£ ļæÉ ļ¬ģņØś ĒÅēĻ░Ćņ×É Ļ░ä ņØ╝ņ╣śļÅäļŖö ņ£äņČĢņä▒ ņÜöņØĖņŚÉņä£ 85.7% (kappa=0.732, p<0.001), Ļ▓¼ņØĖņä▒ ņÜöņØĖņŚÉņä£ 83.3% (kappa=0.709, p<0.001)ņśĆļŗż. ņ▓½ ņ╣śļŻī ņŗ£ ņ£äņČĢņä▒ ņÜöņØĖņØĆ A0 2ņĢł(9.5%), A1 5ņĢł(23.8%), A2 5ņĢł(23.8%), A3 9ņĢł(42.9%)ņØ┤ņŚłņ£╝ļ®░ ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ņĀÉņŚÉņä£ļŖö A0 1ņĢł(4.8%), A1 3ņĢł(14.3%), A2 7ņĢł(33.3%), A3 10ņĢł(47.6%)ņØ┤ņŚłļŗż. ņ£äņČĢņä▒ ņÜöņØĖņŚÉņä£ gradingņØ┤ ņ¦äĒ¢ēļÉ£ Ļ▓ĮņÜ░ļŖö 4ņĢł(19.0%)ņØ┤ņŚłņ£╝ļ®░ 17ņĢł(81.0%)ņŚÉņä£ļŖö gradingņØś ļ│ĆĒÖöĻ░Ć ņŚåņŚłļŗż. Ļ▓¼ņØĖņä▒ ņÜöņØĖņØĆ ņ▓½ ņ╣śļŻī ņŗ£ T0 19ņĢł(90.5%), T1 1ņĢł(4.8%), T2 1ņĢł(4.8%)ņØ┤ņŚłņ£╝ļ®░, ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ņĀÉņŚÉņä£ļŖö T0 14ņĢł(66.7%), T1 5ņĢł(23.8%), T2 1ņĢł(4.8%), T3 1ņĢł(4.8%)ņ£╝ļĪ£ ĒÅēĻ░ĆļÉśņŚłļŗż. Ļ▓¼ņØĖņä▒ ņÜöņØĖņŚÉņä£ 5ņĢł(23.8%)ņŚÉņä£ gradingņØś ņ¦äĒ¢ēņØ┤ ņ׳ņŚłņ£╝ļ®░, 1ņĢł(4.8%)ņŚÉņä£ gradingņØ┤ ĒśĖņĀäļÉśņŚłĻ│Ā 15ņĢł(71.4%)ņŚÉņä£ļŖö gradingņØś ļ│ĆĒÖöļŖö ņŚåņŚłļŗż(Table 4, Fig. 2). ņ£äņČĢņä▒ ņÜöņØĖĻ│╝ Ļ▓¼ņØĖņä▒ ņÜöņØĖņØś ņ¦äĒ¢ē ņŚ¼ļČĆņŚÉ ļö░ļźĖ ņŻ╝ņé¼ Ēܤņłś, ņ×¼ļ░£ Ēܤņłś, ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ņĀÉņŚÉņä£ņØś ņŗ£ļĀź ļō▒ņØä ļČäņäØĒĢ£ Ļ▓░Ļ│╝ ĒåĄĻ│äĒĢÖņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļéś ņāüĻ┤ĆĻ┤ĆĻ│äļŖö ļéśĒāĆļéśņ¦Ć ņĢŖņĢśļŗż.
ļéśņØ┤ņŚÉ ļö░ļźĖ ņ¦æļŗ© ļČäņäØņŚÉņä£ 50ņäĖ ļ»Ėļ¦ī ĒÖśņ×ÉĻĄ░Ļ│╝ 50ņäĖ ņØ┤ņāü ĒÖśņ×ÉĻĄ░ņŚÉņä£ ņ▓½ ņ╣śļŻī ņŗ£ logMAR ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ Ļ░üĻ░ü 0.39 ┬▒ 0.34, 0.47 ┬▒ 0.26ņØ┤ņŚłņ£╝ļ®░, ņĄ£ņóģ ļ░®ļ¼Ė ņŗ£ logMAR ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ Ļ░üĻ░ü 0.36 ┬▒ 0.39, 0.30 ┬▒ 0.41ļĪ£ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż. ņ▓½ ņ╣śļŻī ņŗ£ ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö 50ņäĖ ļ»Ėļ¦ī ĒÖśņ×ÉĻĄ░ņŚÉņä£ 111.5 ┬▒ 91.87 ╬╝m, 50ņäĖ ņØ┤ņāü ĒÖśņ×ÉĻĄ░ņŚÉņä£ 52.30 ┬▒ 36.49 ╬╝mļĪ£ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśņ£╝ļéś ļ¦łņ¦Ćļ¦ē ļ░®ļ¼Ė ņŗ£ ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö 50ņäĖ ļ»Ėļ¦ī ĒÖśņ×ÉĻĄ░ņŚÉņä£ 85.00 ┬▒ 65.02 ╬╝m, 50ņäĖ ņØ┤ņāü ĒÖśņ×ÉĻĄ░ņŚÉņä£ 32.09 ┬▒ 24.70 ╬╝mņ£╝ļĪ£ ĒåĄĻ│äĒĢÖņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņśĆļŗż(p=0.043). ņŻ╝ņé¼ ĒܤņłśļŖö 50ņäĖ ļ»Ėļ¦ī ĒÖśņ×ÉĻĄ░ņŚÉņä£ 2.60 ┬▒ 1.71ĒÜī, 50ņäĖ ņØ┤ņāü ĒÖśņ×ÉĻĄ░ņŚÉņä£ 3.18 ┬▒ 2.27ĒÜīļĪ£ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņŚåņŚłļŗż. 50ņäĖ ļ»Ėļ¦ī ĒÖśņ×ÉĻĄ░ņŚÉņä£ļŖö 6ņĢł(60%)ņŚÉņä£ ņ×¼ļ░£, 50ņäĖ ņØ┤ņāü ĒÖśņ×ÉĻĄ░ņŚÉņä£ļŖö 1ņĢł(9.1%)ņŚÉņä£ ņ×¼ļ░£ļÉśņŚłņ£╝ļ®░ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤Ļ░Ć ņ׳ņŚłļŗż(p=0.013) (Table 5).
ĻĘ╝ņŗ£ļŖö ĒØöĒĢ£ ņĢłĻ│╝ ņןņĢĀņØś ĒĢ£ ņ£ĀĒśĢņ£╝ļĪ£ ĒŖ╣Ē׳ ļÅÖņĢäņŗ£ņĢäņŚÉņä£ ņ£Āļ│æļźĀņØ┤ ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż. ĻĄŁļé┤ 5ņäĖņŚÉņä£ 18ņäĖņØś 983ļ¬ģņØä ĻĖ░ņżĆņ£╝ļĪ£ ņŗżņŗ£ĒĢ£ ĻĄŁļ»╝Ļ▒┤Ļ░Ģņśüņ¢æņĪ░ņé¼ 7ĻĖ░ ņ×ÉļŻīņŚÉņä£ 65.4%ņŚÉņä£ ĻĘ╝ņŗ£Ļ░Ć ņ׳ņŚłņ£╝ļ®░, ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņ╣śĻ░Ć -6.0ļööņśĄĒä░ ņØ┤ĒĢśļĪ£ ņĀĢņØśĒĢ£ Ļ│ĀļÅäĻĘ╝ņŗ£ņØś ļ╣äņ£©ņØĆ 6.9%ņśĆļŗż.11 ņØ┤ļŖö ĻĖ░ņĪ┤ 4, 5ĻĖ░ ĻĄŁļ»╝Ļ▒┤Ļ░Ģņśüņ¢æņĪ░ņé¼ ņ×ÉļŻīņŚÉņä£ Ļ│ĀļÅäĻĘ╝ņŗ£ņØś ļ╣äņ£©ņØ┤ 5.9%ņśĆļŹś Ļ▓āĻ│╝ ļ╣äĻĄÉĒĢśļ®┤ ĻĄŁļé┤ņŚÉņä£ Ļ│ĀļÅäĻĘ╝ņŗ£ņØś ļ╣äņ£©ņØ┤ ņ”ØĻ░ĆĒĢśļŖö ņČöņäĖļĪ£ Ē¢źĒøä ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć, ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”ØĻ│╝ Ļ░ÖņØĆ ĻĘ╝ņŗ£ņä▒ ĒÖ®ļ░śņ¦łĒÖś ļśÉĒĢ£ ņ”ØĻ░ĆĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.12,13
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņŚ¼ņä▒ņØ┤ 85.7%ļĪ£ ņŚ¼ņä▒ņØś ļ╣äņ£©ņØ┤ ļåÆņĢśļŖöļŹ░ ņØ┤ļŖö Lee et al8ņØś ņŚ░ĻĄ¼ņØś ņŚ¼ņä▒ ļ╣äņ£©(83.7%)Ļ│╝ ļ╣äņŖĘĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż. ĒĢśņ¦Ćļ¦ī ļŗżļźĖ ņØĖņóģņØś ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļé©ņä▒ņØś ļ╣äņ£©(50.9%)ņØ┤ ļŹö ļåÆņØĆ ņŚ░ĻĄ¼ļÅä ņ׳ņ¢┤ ņØĖņóģļ│ä ņ░©ņØ┤Ļ░Ć ņ׳ņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.14 ļ»ĖĻĄŁ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļé©ņä▒ļ│┤ļŗż ņŚ¼ņä▒ņØś ņ£Āļ│æļźĀņØ┤ ļåÆņØīņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż.15 ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņØ┤ ņŻ╝ļĪ£ ņŚ¼ņä▒ņŚÉņä£ ļ╣łļ▓łĒĢ£ ņøÉņØĖņØĆ Ļ│ĀļÅäĻĘ╝ņŗ£ņĢłņØś ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņŚÉ ņŚÉņŖżĒŖĖļĪ£Ļ▓É ņłśņÜ®ņ▓┤Ļ░Ć ļ░£ĒśäļÉśņ¢┤ ņŗĀņāØĒśłĻ┤ĆņØś ļ░£ņāØņØä ņ┤ēņ¦äĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.16
ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ņ╣śļŻīļŖö ņŻ╝ļĪ£ ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼Ļ░Ć ņØ┤ņÜ®ļÉ£ļŗż. ļØ╝ļŗłļ╣äņŻ╝ļ¦ÖĻ│╝ ņĢĀĒöīļ”¼ļ▓äņģēĒŖĖņØś ĒÜ©Ļ│╝ļŖö 3ņāü ņ×äņāüņŗ£ĒŚśņŚÉņä£ ĒÖĢņØĖļÉśņŚłņ£╝ļ®░ ņ╣śļŻī ļ¬®ņĀüņ£╝ļĪ£ Ļ│ĄņØĖļÉ£ ņĢĮņĀ£ņØ┤ļŗż. ļØ╝ļŗłļ╣äņŻ╝ļ¦Ö ņ×äņāü ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ĒÖśņ×ÉļōżņØä ļīĆņāüņ£╝ļĪ£ ņŻ╝ņé¼ ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ 6Ļ░£ņøö ņŗ£ņĀÉņŚÉņä£ 48ļ¬ģņØś ĒÖśņ×ÉļōżņØä ļČäņäØĒĢ£ Ļ▓░Ļ│╝ Early Treatment Diabetic Retinopathy Study (ETDRS) ņ░©ĒŖĖļĪ£ ĒÅēĻĘĀ 12.2 ĻĖĆņ×ÉņØś ņŗ£ļĀźņØ┤ Ē¢źņāüļÉśņŚłĻ│Ā ņżæņŗ¼ļ¦Øļ¦ēļæÉĻ╗śļŖö Ļ░ÉņåīĒĢśņśĆņØīņØä ļ│┤Ļ│Ā ĒĢśņśĆļŗż.17 ņĢĀĒöīļ”¼ļ▓äņģēĒŖĖ ņ×äņāü ņŚ░ĻĄ¼ņŚÉņä£ļÅä 48ņŻ╝ ļÅÖņĢł ņĢĀĒöīļ”¼ļ▓äņģēĒŖĖ ņ╣śļŻīĻĄ░ņØĆ ĒÅēĻĘĀ 4.2ĒÜīņØś ņŻ╝ņé¼ ņ╣śļŻīļź╝ ļ░øņĢśņ£╝ļ®░, ĒÅēĻĘĀ 13.5 ĻĖĆņ×ÉņØś ņŗ£ļĀź Ē¢źņāü ĒÜ©Ļ│╝ļź╝ ļ│┤ņśĆĻ│Ā, ļīĆņĪ░ĻĄ░ņŚÉņä£ļŖö 3.9 ĻĖĆņ×ÉņØś ņŗ£ļĀź Ļ░£ņäĀņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż.18 ļ▓Āļ░öņŗ£ņŻ╝ļ¦Ö ļśÉĒĢ£ ņ×äņāüņŚÉņä£ ļ¦ÄņØ┤ ņé¼ņÜ®ļÉśļ®░ ņןĻĖ░ ņŚ░ĻĄ¼ ļśÉĒĢ£ ļ¦ÄņØ┤ ņØ┤ļŻ©ņ¢┤ņĪīļŗż. ņäĖ Ļ░Ćņ¦Ć ņĢĮņĀ£ Ļ░ä ĒÜ©Ļ│╝ļź╝ ļ╣äĻĄÉĒĢśĻĖ░ ņ£äĒĢ£ ļīĆĻĘ£ļ¬© ņĀäĒ¢źņĀü ņŚ░ĻĄ¼ Ļ▓░Ļ│╝Ļ░Ć ļČĆņĪ▒ĒĢśņŚ¼ ņ¦üņĀæņĀüņØĖ ļ╣äĻĄÉļŖö ņ¢┤ļĀżņÜ┤ ņāüĒā£ļŗż. Cha et al19ņØĆ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ņ╣śļŻīļĪ£ ļ▓Āļ░öņŗ£ņŻ╝ļ¦ÖĻ│╝ ļØ╝ļŗłļ»ĖņŻ╝ļ¦Ö ļ╣äĻĄÉ ņŚ░ĻĄ¼ņŚÉņä£ 1ļģä Ēøä ļ╣äņŖĘĒĢ£ ĻĖ░ļŖźņĀü Ļ▓░Ļ│╝ņÖĆ ĒĢ┤ļČĆĒĢÖņĀü Ļ▓░Ļ│╝ļź╝ ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░, Pham et al20ņØĆ ļ¦Øļ¦ē ņāüĒā£ņŚÉ ļö░ļØ╝ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņ╣śļŻīņŚÉ ļīĆĒĢ£ ļ®öĒāĆļČäņäØņØä ņŗ£Ē¢ēĒĢśņśĆļŖöļŹ░ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņŚÉņä£ ļ▓Āļ░öņŗ£ņŻ╝ļ¦ÖĻ│╝ ļØ╝ļŗłļ╣äņŻ╝ļ¦Ö ņé¼ņØ┤ņŚÉ ņŗ£ļĀźĒ¢źņāüņŚÉ ļīĆĒĢ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłĻ│Ā ļ▓Āļ░öņŗ£ņŻ╝ļ¦ÖņØ┤ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņŚÉņä£ ļØ╝ļŗłļ╣äņŻ╝ļ¦ÖĻ│╝ ņĢĀĒöīļ”¼ļ▓äņģēĒŖĖņØś ĒĢ®ļ”¼ņĀüņØĖ ļīĆņ▓┤ņ╣śļŻīņĀ£ļĪ£ ņé¼ņÜ®ļÉĀ ņłś ņ׳ļŗżĻ│Ā ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņŻ╝ļĪ£ ļ▓Āļ░öņŗ£ņŻ╝ļ¦ÖņØ┤ ņ╣śļŻīņŚÉ ņé¼ņÜ®ļÉśņŚłņ£╝ļ®░ 2ļ¬ģņØś ĒÖśņ×ÉņŚÉņä£ ļØ╝ļŗłļ╣äņŻ╝ļ¦ÖņØ┤ ņé¼ņÜ®ļÉśņŚłļŖöļŹ░ ņ╣śļŻīņĢĮņĀ£Ļ░Ć ņŗ£ļĀźņŚÉ ļīĆĒĢ┤ ņ£ĀņØśĒĢĀ ņĀĢļÅäņØś ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ļ▓Āļ░öņŗ£ņŻ╝ļ¦Öņ£╝ļĪ£ ĒĢäņÜöĒĢĀ ļĢīļ¦łļŗż ņ╣śļŻīĒĢ£ ņŚ░ĻĄ¼ļź╝ ņé┤ĒÄ┤ļ│┤ļ®┤ 1ļģä ņØ┤ņāü ĒÖśņ×ÉņŚÉņä£ ņĢĮ 2.7ĒÜīņØś ņ╣śļŻīĻ░Ć ņŗ£Ē¢ēļÉśņŚłņ£╝ļ®░ 5ļģä ņØ┤ņāü ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒÅēĻĘĀ 4.9ĒÜī, 10ļģä ņØ┤ņāü ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒÅēĻĘĀ 6.8ĒÜī ņŻ╝ņé¼ ņ╣śļŻīĻ░Ć ņŗ£Ē¢ēļÉśņŚłļŗż.5,6,19 ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 3ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĒÖśņ×ÉņŚÉņä£ 2.9ĒÜī ņŗ£Ē¢ēļÉśņŚłļŖöļŹ░ ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼ ĒܤņłśļŖö Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØ┤ ņ”ØĻ░ĆĒĢ©ņŚÉ ļö░ļØ╝ ņ”ØĻ░ĆļÉĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņŚÉņä£ ļ░śļīĆņĢłņŚÉ ļ░£ņāØĒĢśļŖö ļ╣łļÅäļŖö ņןĻĖ░Ļ░ä(8-10ļģä) ņŚ░ĻĄ¼ņŚÉņä£ ņĢĮ 30% ņĀĢļÅäļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż.1,6 ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 5ņĢł(23.8%)ņŚÉņä£ ļ░£ņāØĒĢśņśĆļŖöļŹ░ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņØ┤ ĻĖĖņ¢┤ņ¦äļŗżļ®┤ ļ░śļīĆņĢłņŚÉņä£ ļ░£ņāØ ļ╣łļÅäļŖö ņĪ░ĻĖł ļŹö ņś¼ļØ╝Ļ░ł Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņØĆ ņ╣śļŻī Ēøä ņ×¼ļ░£ĒĢĀ ņłś ņ׳Ļ│Ā ņ×¼ļ░£ ĻĖ░Ļ░äņØĆ Ļ░£ņØĖļ¦łļŗż ņ░©ņØ┤Ļ░Ć ņ׳ļŗż. Lee et al8ņØĆ 1ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŚ░ĻĄ¼ņŚÉņä£ 43ņĢł ņżæ 17ņĢł(39.5%)ņŚÉņä£ ņ×¼ļ░£ņØä ļ│┤Ļ│Ā ĒĢśņśĆņ£╝ļ®░ ĻĘĖņżæ 6ņĢłņØ┤ 24Ļ░£ņøö ņØ┤ĒøäņŚÉ ļ░£ņāØĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 21ņĢł ņżæ 7ņĢł(33.3%)ņŚÉņä£ ņ×¼ļ░£ĒĢśņśĆļŖöļŹ░ ņØ┤ļŖö ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ĒÖśņ×ÉņŚÉņä£ ļ░śļīĆņĢł Ļ▓Ćņé¼ļź╝ ņåīĒÖĆĒ׳ ĒĢśņ¦ĆņĢŖņĢäņĢ╝ ĒĢśļ®░ ņןĻĖ░Ļ░ä ņ×¼ļ░£ņØ┤ ņŚåļŹöļØ╝ļÅä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņØ┤ ĒĢäņÜöĒĢ©ņØä ņŗ£ņé¼ĒĢ£ļŗż.
ļéśņØ┤ņŚÉ ļö░ļźĖ ņ╣śļŻī ĒÜ©Ļ│╝ļź╝ ļČäņäØĒĢ£ ĻĖ░ņĪ┤ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļéśņØ┤Ļ░Ć ņĀüņØĆ ĻĄ░ņŚÉņä£ ļéśņØ┤Ļ░Ć ļ¦ÄņØĆ ĻĄ░ļ│┤ļŗż ļŹö ņĀüņØĆ ņŻ╝ņé¼ ĒܤņłśņÖĆ ņŗ£ļĀźĒśĖņĀäņØä ļ│┤ņśĆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.21,22 ļśÉĒĢ£ ņ×¼ņ╣śļŻīņŚÉ ļīĆĒĢ£ ĒĢäņÜöĻ░Ć ļéśņØ┤ņŚÉ ņśüĒ¢źņØä ļ░øļŖöļŗżĻ│Ā ĒĢśņśĆļŗż.22 ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 50ņäĖ ņØ┤ņāü ĒÖśņ×ÉĻĄ░ņŚÉņä£ ņ×¼ļ░£ņØ┤ ļŹö ņĀüņŚłņ£╝ļéś ĒÅēĻĘĀ ņŻ╝ņé¼ ĒܤņłśļŖö ļŹö ļ¦ÄņĢśļŖöļŹ░, Ēæ£ļ│ĖņØ┤ ņĀüņŚłņ£╝ļ®░ 50ņäĖ ņØ┤ņāüņŚÉņä£ ņ×¼ļ░£ļÉ£ 1ļ¬ģņØś ĒÖśņ×ÉņŚÉņä£ ņ┤Ø 9ĒÜīņØś ņŻ╝ņé¼Ļ░Ć ĒĢäņÜöĒĢśņŚ¼ ņ×¼ļ░£ ņŗ£ ļ¦ÄņØĆ ņŻ╝ņé¼ ņ╣śļŻīĻ░Ć ĒĢäņÜöĒĢśņśĆļŹś ņĀÉņØ┤ ņśüĒ¢źņØä ņŻ╝ņŚłņØä ņłś ņ׳ļŗż.
OhnoŌĆÉMatsui et al23ņØĆ ļ│æņĀüĻĘ╝ņŗ£ ĒÅēĻ░ĆņÖĆ Ļ┤ĆļĀ©ĒĢśņŚ¼ International Photographic Classification and Grading System for myopic maculopathy (METAŌĆÉPM) ļČäļźś ņŗ£ņŖżĒģ£ņØä ļ░£Ēæ£ĒĢśņśĆļŗż. ņŻ╝ļĪ£ ņ£äņČĢņØä ĒÅēĻ░ĆĒĢśĻ│Ā ņŗĀņāØĒśłĻ┤ĆņØĆ ļČĆņłśņĀüņ£╝ļĪ£ ĒÅēĻ░ĆĒĢśņśĆņ£╝ļ®░ ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”Ø(myopic tractional maculopathy)ņŚÉ ļīĆĒĢ£ ĒÅēĻ░ĆļŖö ņĀ£ņÖĖļÉśņŚłļŗż. ĻĘĖ Ēøä RuizŌĆÉMedrano et al9ņØ┤ ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”ØņØä ĒÅēĻ░ĆĒĢĀ ņłś ņ׳ļŖö ATN classification and grading systemņØä ļÅäņ×ģĒĢśņŚ¼ Ēśäņ×¼ ļ¦ÄņØĆ ņŚ░ĻĄ¼ņŚÉ ņØ┤ņÜ®ļÉśĻ│Ā ņ׳ļŗż. Kurt et al10ņØĆ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņ╣śļŻīļź╝ ņÜöĒĢśņ¦Ć ņĢŖļŖö ĒØēĒä░ĒÖöļÉ£ Ļ▓ĮņÜ░ļź╝ ĒżĒĢ©ĒĢ£ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ņŚ░ĻĄ¼ņŚÉņä£ ATN systemņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļČäņäØņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņ£äņČĢņä▒ ņÜöņØĖĻ│╝ Ļ▓¼ņØĖņä▒ ņÜöņØĖ ņé¼ņØ┤ņØś ņ£ĀņØśĒĢ£ ņāüĻ┤ĆĻ┤ĆĻ│äļŖö ņŚåņŚłņ£╝ļ®░ ņŗĀņāØ ĒśłĻ┤Ćņä▒ ņÜöņØĖĻ│╝ Ļ▓¼ņØĖņä▒ ņÜöņØĖ ņé¼ņØ┤ņØś ņ£ĀņØśĒĢ£ ņāüĻ┤ĆĻ┤ĆĻ│äļŖö ņŚåņŚłņ¦Ćļ¦ī ņ£äņČĢņä▒ ņÜöņØĖĻ│╝ ņŗĀņāØĒśłĻ┤Ćņä▒ ņÜöņØĖ ņé¼ņØ┤ņŚÉņä£ļŖö ņ£ĀņØśĒĢ£ ņāüĻ┤ĆĻ┤ĆĻ│äĻ░Ć ņ׳ņØīņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. ņ£äņČĢņØ┤ ņŗĀņāØĒśłĻ┤Ć ĒØēĒä░ņØś ļÅģļ”ĮņĀüņØĖ ņśłņĖĪņØĖņ×ÉņØ┤ļ®░ patchy ļ¦źļØĮļ¦ēļ¦Øļ¦ēņ£äņČĢņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņØ┤ Ļ░Ćņן ņ×ÉņŻ╝ ļ░£ņāØļÉśņ¢┤ ņäĖņŗ¼ĒĢ£ Ļ▓Ćņé¼ņÖĆ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņØ┤ ĒĢäņÜöĒĢśļŗżĻ│Ā ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ¬©ļōĀ ĒÖśņ×ÉņŚÉņä£ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ ATN classification and grading systemņŚÉ ļö░ļźĖ ņ£äņČĢņØś ņ¦äĒ¢ēņØĆ 4ņĢł(19.0%)ņŚÉņä£ ņ׳ņŚłļŗż. Chhablani et al5ņØĆ ņĢäļ░öņŖżĒŗ┤ ņ╣śļŻīļĪ£ 5ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņŚÉņä£ ņ▓½ ņ╣śļŻī ņŗ£ 12.5%ņŚÉņä£, ļ¦łņ¦Ćļ¦ē ļ░®ļ¼ĖņØĆ 29.1%ņŚÉņä£ ņżæņŗ¼ņÖĆ ņ£äņČĢņØ┤ ļ░£ņāØĒĢśņśĆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░, Mallone et al6ņØĆ ņĢäļ░öņŖżĒŗ┤ ņ╣śļŻī Ēøä 10ļģä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŚ░ĻĄ¼ņŚÉņä£ 80%ņŚÉņä£ ļ¦źļØĮļ¦ēļ¦Øļ¦ēņ£äņČĢņØ┤ ļ░£ņāØ ļ░Å ņ¦äĒ¢ēĒĢśņśĆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż. ņØ┤ņ▓śļ¤╝ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņ£äņČĢņØś ņ¦äĒ¢ēņØ┤ ņĀüĻ▓ī ļéśĒāĆļéśļŖö Ļ▓āņØĆ ATN classification and grading systemņØ┤ patchy atrophyņØś Ēü¼ĻĖ░Ļ░Ć ņ”ØĻ░ĆĒĢśļŖö Ļ▓āņØä ļ░śņśüĒĢśņ¦Ć ļ¬╗ĒĢśņŚ¼ ņŗżņĀ£ļĪ£ ņ£äņČĢņØ┤ ņ¦äĒ¢ēļÉśļŖö Ļ▓ĮņÜ░ņŚÉļÅä Ļ░ÖņØĆ ļō▒ĻĖēņ£╝ļĪ£ ļČäļźśļÉśņŚłĻĖ░ ļĢīļ¼ĖņØ┤ļØ╝Ļ│Ā ņāØĻ░üļÉ£ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö Ļ▓¼ņØĖņä▒ ņÜöņØĖņŚÉ ļīĆĒĢ£ ĒÅēĻ░ĆņŚÉņä£ļŖö 5ņĢł(23.8%)ņŚÉņä£ ņ¦äĒ¢ēņØ┤ ņ׳ņŚłņ£╝ļ®░, 1ņĢł(4.8%)ņŚÉņä£ ĒśĖņĀäļÉśņŚłļŗż. Shimada et al24ņØĆ ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”ØņŚÉ ņśüĒ¢źņØä ņżä ņłś ņ׳ļŖö ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ļ░Å ļ¦źļØĮļ¦ēļ¦Øļ¦ēņ£äņČĢņØä ņĀ£ņÖĖĒĢ£ 2ļģä ņØ┤ņāü ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”Ø Ļ┤Ćņ░░ ņŚ░ĻĄ¼ņŚÉņä£ 11.6%ņŚÉņä£ ņ¦äĒ¢ē, 3.9%ņŚÉņä£ ņÖäĒÖö ļśÉļŖö ņÖäņĀäĒĢ£ ĒśĖņĀäņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. ĒśĖņĀäļÉśļŖö ļ╣äņ£©ņØĆ ļ╣äņŖĘĒĢśņśĆņ£╝ļ®░ ņ¦äĒ¢ēņŚÉ ļīĆĒĢ£ ļ╣äņ£©ņØĆ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļŹö ļåÆĻ▓ī ļéśĒāĆļé¼ļŗż. ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņ╣śļŻī Ēøä ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”ØĻ│╝ ļ¦Øļ¦ēņĖĄĻ░äļČäļ”¼ņØś ņ¦äĒ¢ēņØĆ ļō£ļ¼╝ņ¦Ćļ¦ī ļÅģĒŖ╣ĒĢ£ ĒĢ®ļ│æņ”Ø ņżæ ĒĢśļéśņØ┤ļŗż.25 ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤ĆņŚÉņä£ ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ņŻ╝ņé¼Ļ░Ć ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ļ¦Øļ¦ēļ│æņ”ØņØä ņĢģĒÖöņŗ£ĒéżļŖö ļ¬ģĒÖĢĒĢ£ ĻĖ░ņĀäņØĆ ļČłļČäļ¬ģĒĢśņ¦Ćļ¦ī Shimada et al26ņØĆ ņŗĀņāØĒśłĻ┤ĆņØś Ēć┤Ē¢ē ņ£äņ╣śņŚÉņä£ ļé┤Ļ▓ĮĻ│äļ¦ēņØ┤ ņłśņČĢļÉśņ¢┤ ņØ╝ņ¢┤ļéĀ ņłś ņ׳ņØīņØä ņäżļ¬ģĒĢśņśĆļŗż. Wei et al27ņØĆ ņä¼ņ£Āļ¬©ņäĖĒżļź╝ ĒżĒĢ©ĒĢ£ ņłśņČĢļĀźņØä Ļ░Ćņ¦ä ļŗżņ¢æĒĢ£ ņäĖĒżņŚÉ ĒżĒĢ©ļÉśņ¢┤ ņ׳ļŖö ņĢīĒīī ĒÅēĒÖ£ĻĘ╝ ņĢĪĒŗ┤ņØ┤ ņŚ¼ļ¤¼ ņ░©ļĪĆ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼ Ēøä ņ£Āļ”¼ņ▓┤ņĢĪņŚÉņä£ ļ░£ĒśäņØ┤ ņ”ØĻ░ĆĒĢśņŚ¼ ļé┤Ļ▓ĮĻ│äļ¦ēņØ┤ļéś Ēøäņ£Āļ”¼ņ▓┤ļ¦ēņØś ņłśņČĢņØä ņ£Āļ░£ņŗ£ņ╝£ ļ¦Øļ¦ēņĖĄĻ░äļČäļ”¼Ļ░Ć ņ¦äĒ¢ēļÉĀ ņłś ņ׳ļŗżĻ│Ā ĒĢśņśĆļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ćņ£╝ļĪ£ ņ£Āļ”¼ņ▓┤Ļ░Ģ ļé┤ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼ ņ╣śļŻīļź╝ ļ░øĻ│Ā 3ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ļÉ£ ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ĻĄŁļé┤ ņŚ░ĻĄ¼ ņżæ ņ▓śņØīņ£╝ļĪ£ ATN classification and grading systemņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņןĻĖ░ ņ×äņāü Ļ▓░Ļ│╝ ļ░Å ļ│ĆĒÖöļź╝ ĒÖĢņØĖĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņØś ņĀ£ĒĢ£ņĀÉņ£╝ļĪ£ļŖö ĒøäĒ¢źņĀü ļ░®ļ▓Ģņ£╝ļĪ£ ņŗ£Ē¢ēļÉśņ¢┤ ļČäņäØņØ┤ ņØ┤ļŻ©ņ¢┤ņĪīĻ│Ā Ēö╝ĒŚśņ×ÉņłśĻ░Ć ņĀüņ£╝ļ®░ ĻĖ░ņĪ┤ ĻĄ┤ņĀłĻĄÉņĀĢņłśņłĀņØ┤ļéś ļ░▒ļé┤ņןņłśņłĀļĪ£ ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņ╣śļź╝ ņĀĢĒÖĢĒĢśĻ▓ī ļ░śņśüĒĢśņ¦Ć ļ¬╗ĒĢśņŚ¼ Ļ│ĀļÅäĻĘ╝ņŗ£ņØś ĻĖ░ņżĆņØĖ -6.0ļööņśĄĒä░ļź╝ ļ¦īņĪ▒ņŗ£Ēéżņ¦Ć ļ¬╗ĒĢśņśĆļŗż. ļśÉĒĢ£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņØ┤ ĻĘ£ņ╣ÖņĀüņ£╝ļĪ£ ļÉśņ¦Ć ļ¬╗ĒĢśņśĆņ£╝ļ®░ ņ┤łĻĖ░ ņ╣śļŻī ņŗ£ ņŻ╝ņé¼ ĒܤņłśĻ░Ć ĒåĄņØ╝ļÉśņ¦Ć ļ¬╗ĒĢśņśĆļŹś ņĀÉņØ┤ Ļ▓░Ļ│╝ņŚÉ ņśüĒ¢źņØä ņŻ╝ņŚłņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
Ļ▓░ļĪĀņĀüņ£╝ļĪ£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ćņ£╝ļĪ£ ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņ╣śļŻīļź╝ ļ░øĻ│Ā 3ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ļÉ£ ĒÖśņ×ÉļŖö 71.4%ņŚÉņä£ ņŗ£ļĀźņØ┤ ņ£Āņ¦ĆļÉśĻ▒░ļéś ĒśĖņĀäļÉśļŖö Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ņ£╝ļ®░ ņØ╝ļČĆņŚÉņä£ ļ¦źļØĮļ¦ēļ¦Øļ¦ēņ£äņČĢĻ│╝ ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”ØņØ┤ ņ¦äĒ¢ēĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ļŗż. ņØ┤ļŖö ĒĢŁĒśłĻ┤Ćļé┤Ēö╝ņä▒ņןņØĖņ×É ņŻ╝ņé¼Ļ░Ć ĻĘ╝ņŗ£ņä▒ ļ¦źļØĮļ¦ēņŗĀņāØĒśłĻ┤Ć ņןĻĖ░ ņ╣śļŻīņŚÉ ĒÜ©Ļ│╝ņĀüņØĖ ļ░®ļ▓Ģņ×äņØä ļÆĘļ░øņ╣©ĒĢśļ®░, Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŗ£ ĻĘ╝ņŗ£ņä▒ Ļ▓¼ņØĖņä▒ ĒÖ®ļ░śļ│æņ”ØĻ│╝ ļ¦źļØĮļ¦ēļ¦Øļ¦ēņ£äņČĢ ļ│ĆĒÖöņŚÉ ļīĆĒĢ£ ĒÅēĻ░Ć ļśÉĒĢ£ ņåīĒÖĆĒĢśņ¦Ć ņĢŖļÅäļĪØ ĒĢ┤ņĢ╝Ļ▓Āļŗż.
Figure┬Ā1.
A Kaplan-Meier curve showing the cumulative recurrence of the myopic choroidal neovascularization after initial treatment. Among the 21 eyes, 7 eyes (33.3%) showed recurrence during the follow-up period.
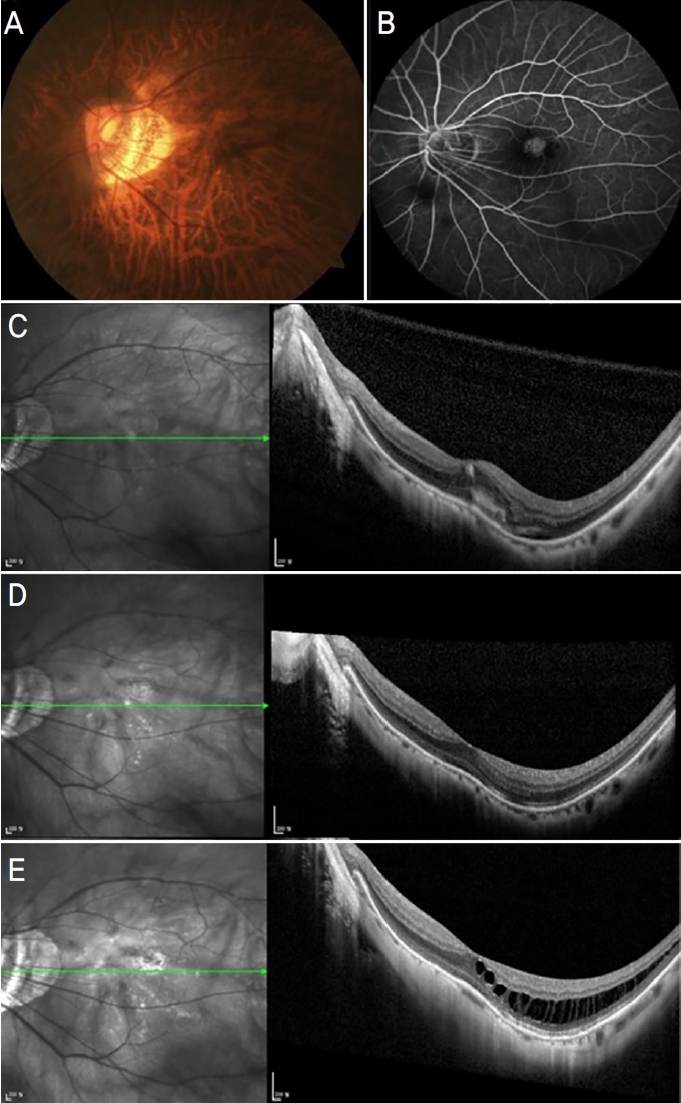
Figure┬Ā2.
Clinical course of a 59 year-old female patient who was diagnosed with myopic choroidal neovascularization (CNV) in the left eye. At baseline, tessellated fundus (A) and leakage from CNV was noted on fluorescein angiography (B), and subretinal fluid with hyper-reflective material was detected on optical coherence tomography (C). The patient was treated with 2 monthly intravitreal bevacizumab injections. One month after the second injection, the fluid and hyper-reflective material were disappeared (D). At 44 months after the initial treatment, myopic retinoschisis was noted on optical coherence tomography (E).
Table┬Ā1.
ATN classification system, which considers atrophic (A), tractional (T) and neovascular (N) components
Table┬Ā2.
Demographics and clinical outcomes of myopic choroidal neovascularization patients (n = 21)
Table┬Ā3.
Associations between parameters and final logMAR best corrected visual acuity in myopic choroidal neovascularization patients (n = 21)
| Parameters |
Univariate |
Multivariate |
|
|---|---|---|---|
| Correlation coefficient (Spearman) | p-value* | p-valueŌĆĀ | |
| Age (years) | 0.015 | 0.947 | 0.832 |
| Baseline logMAR best corrected visual acuity | 0.528 | 0.017 | 0.026 |
| Follow up period | 0.041 | 0.864 | 0.256 |
| Spherical equivalents | -0.446 | 0.043 | 0.990 |
| Number of anti-VEGF injections | 0.195 | 0.398 | 0.557 |
Table┬Ā4.
Changes of the funduscopic and tomographic parameters according to a novel myopic maculopathy classification system (atrophy [A], traction [T], neovascularization [N]; ATN) during follow up period (n = 21)
Table┬Ā5.
Univariate comparisons between young age group and old age group (n = 21)
| Parameters | Young age (< 50 years) group (n = 10) | Old age (Ōēź 50 years) group (n = 11) | p-value* |
|---|---|---|---|
| Baseline logMAR BCVA | 0.39 ┬▒ 0.34 | 0.47 ┬▒ 0.26 | 0.503 |
| Final logMAR BCVA | 0.36 ┬▒ 0.39 | 0.30 ┬▒ 0.41 | 0.387 |
| Follow-up period (months) | 58.90 ┬▒ 20.51 | 57.65 ┬▒ 18.84 | 0.912 |
| Number of anti-VEGF injections | 2.60 ┬▒ 1.71 | 3.18 ┬▒ 2.27 | 0.512 |
| Number of recurrence | 0.80 ┬▒ 0.91 | 0.09 ┬▒ 0.30 | 0.043 |
| Baseline CRT (╬╝m) | 243.80 ┬▒ 55.71 | 282.2 ┬▒ 82.66 | 0.393 |
| Final CRT (╬╝m) | 196.00 ┬▒ 48.95 | 209.90 ┬▒ 43.53 | 0.481 |
| Baseline choroidal thickness (╬╝m) | 111.5 ┬▒ 91.87 | 52.30 ┬▒ 36.49 | 0.123 |
| Final choroidal thickness (╬╝m) | 85.00 ┬▒ 65.02 | 32.09 ┬▒ 24.70 | 0.043 |
| Recurrence | 6 (60.0) | 1 (9.1) | 0.013 |
| Bilateral involvement | 3 (30.0) | 2 (18.2) | 0.525 |
| History of refractive surgery | 5 (50.0) | 4 (36.4) | 0.528 |
| Baseline lens status | 0.696 | ||
| ŌĆāPhakia | 8 (80.0) | 8 (82.7) | |
| ŌĆāEudophakia | 2 (20.0) | 3 (27.3) |
REFERENCES
1) Ohno-Matsui K, Yoshida T, Futagami S, et al. Patchy atrophy and lacquer cracks predispose to the development of choroidal neovascularisation in pathological myopia. Br J Ophthalmol 2003;87:570-3.



2) Yoshida T, Ohno-Matsui K, Yasuzumi K, et al. Myopic choroidal neovascularization: a 10-year follow-up. Ophthalmology 2003;110:1297-305.


3) Hayashi K, Ohno-Matsui K, Shimada N, et al. Long-term results of photodynamic therapy for choroidal neovascularization in Japanese patients with pathologic myopia. Am J Ophthalmol 2011;151:137-47.e1.


4) Willis J, Morse L, Vitale S, et al. Treatment patterns for myopic choroidal neovascularization in the United States: analysis of the IRIS registry. Ophthalmology 2017;124:935-43.


5) Chhablani J, Paulose RM, Lasave AF, et al. Intravitreal bevacizumab monotherapy in myopic choroidal neovascularisation: 5-year outcomes for the PAN-American collaborative retina study group. Br J Ophthalmol 2018;102:455-9.


6) Mallone F, Giustolisi R, Franzone F, et al. Ten-year outcomes of intravitreal bevacizumab for myopic choroidal neovascularization: analysis of prognostic factors. Pharmaceuticals (Basel) 2021;14:1042.



7) Seo YS, Chang MH. Long-term therapeutic effect of intravitreal bevacizumab (Avastin) on myopic choroidal neovascularization. J Korean Ophthalmol Soc 2011;52:34-40.

8) Lee JM, Kim JW, Lee DW, Kim JH. Long-term treatment outcomes of intravitreal bevacizumab treatment for myopic choroidal neovascularization. J Korean Ophthalmol Soc 2019;60:547-54.


9) Ruiz-Medrano J, Montero JA, Flores-Moreno I, et al. Myopic maculopathy: current status and proposal for a new classification and grading system (ATN). Prog Retin Eye Res 2019;69:80-115.


10) Kurt RA; Sar─▒g├╝l Sezen├Čz A, Akkoyun I, Y─▒lmaz G. The correlation of atrophy, traction and neovascularization in myopic choroidal neovascularization according to a novel myopic maculopathy classification system (atrophy (A), traction (T), neovascularization (N): ATN). Int Ophthalmol 2022;42:2925-32.



11) Kim H, Seo JS, Yoo WS, et al. Factors associated with myopia in Korean children: Korea National Health and Nutrition Examination Survey 2016-2017 (KNHANES VII). BMC Ophthalmol 2020;20:31.




12) Jung SI, Han J, Kwon JW, et al. Analysis of myopic progression in childhood using the Korea National Health and Nutrition Examination Survey. J Korean Ophthalmol Soc 2016;57:1430-4.


13) Lee DH, Choi EY, Kang HG, Kim M. Current concepts in myopic choroidal neovascularization: a review. J Retin 2020;5:1-11.

14) Jain M, Narayanan R, Jana P, et al. Incidence, predictors and re-treatment outcomes of recurrent myopic choroidal neo-vascularization. PLoS One 2022;17:e0271342.



15) Willis JR, Vitale S, Morse L, et al. The prevalence of myopic choroidal neovascularization in the United States: analysis of the IRIS(®) Data Registry and NHANES. Ophthalmology 2016;123:1771-82.


16) Kobayashi K, Mandai M, Suzuma I, et al. Expression of estrogen receptor in the choroidal neovascular membranes in highly myopic eyes. Retina 2002;22:418-22.


17) Tufail A, Patel PJ, Sivaprasad S, et al. Ranibizumab for the treatment of choroidal neovascularisation secondary to pathological myopia: interim analysis of the REPAIR study. Eye (Lond) 2013;27:709-15.




18) Ikuno Y, Ohno-Matsui K, Wong TY, et al. Intravitreal aflibercept injection in patients with myopic choroidal neovascularization: the MYRROR study. Ophthalmology 2015;122:1220-7.


19) Cha DM, Kim TW, Heo JW, et al. Comparison of 1-year therapeutic effect of ranibizumab and bevacizumab for myopic choroidal neovascularization: a retrospective, multicenter, comparative study. BMC Ophthalmol 2014;14:69.




20) Pham B, Thomas SM, Lillie E, et al. Anti-vascular endothelial growth factor treatment for retinal conditions: a systematic review and meta-analysis. BMJ Open 2019;9:e022031.



21) Yoshida T, Ohno-Matsui K, Ohtake Y, et al. Long-term visual prognosis of choroidal neovascularization in high myopia: a comparison between age groups. Ophthalmology 2002;109:712-9.


22) Karagiannis D, Kontadakis GA, Kaprinis K, et al. Treatment of myopic choroidal neovascularization with intravitreal ranibizumab injections: the role of age. Clin Ophthalmol 2017;11:1197-201.




23) Ohno-Matsui K, Kawasaki R, Jonas JB, et al. International photographic classification and grading system for myopic maculopathy. Am J Ophthalmol 2015;159:877-83.e7.


24) Shimada N, Tanaka Y, Tokoro T, Ohno-Matsui K. Natural course of myopic traction maculopathy and factors associated with progression or resolution. Am J Ophthalmol 2013;156:948-57.e1.


25) Ng DSC, Ho M, Iu LPL, Lai TYY. Safety review of anti-VEGF therapy in patients with myopic choroidal neovascularization. Expert Opin Drug Saf 2022;21:43-54.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 784 View
- 42 Download
- Related articles
-
Recurrent Idiopathic Choroidal Neovascularization in an Adolescent2023 February;64(2)
Choroid in Myopic Choroidal Neovascularization Measured Using SD-OCT.2014 September;55(9)
Long-term Natural Course of Idiopathic Choroidal Neovascularization.2005 May;46(5)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



