진행성 위암으로 인한 중증 빈혈이 동반된 망막분지정맥폐쇄안에서 발생한 신생혈관녹내장 1예
A Case of Neovascular Glaucoma with Branch Retinal Vein Occlusion Accompanied by Severe Anemia
Article information
Abstract
목적
망막분지정맥폐쇄, 중증 빈혈 등의 인자를 동반한 환자에서 발생한 신생혈관녹내장 증례에 관하여 보고를 하고자 한다.
증례요약
고혈압이 있는 79세 남자 환자로, 9개월 전 우안의 망막분지정맥폐쇄로 타원에서 부분적 망막광응고술 치료를 시행받은 과거력이 있으며, 내원 7일 전부터 타원에서 우안의 안허혈증후군 의심하에 경과 관찰 도중 발생한 우안의 통증 및 안압상승을 주소로 본원 응급실로 전원되었다. 내원 당시 최대교정시력은 우안 안전수동, 좌안 1.0으로 측정되었고 안압은 골드만압평안압계로 우안 28 mmHg, 좌안 15 mmHg로 측정되었으며, 세극등현미경검사상 우안 홍채신생혈관 및 전방출혈이 관찰되어 신생혈관녹내장 진단 하에 아메드밸브삽입술을 계획하였다. 술 전 혈액검사상 헤모글로빈 7.8 g/dL의 중등도 빈혈 소견이 관찰되었고, 위장관계 관련 출혈이 의심되어 시행한 내시경 및 조직검사 결과상 진행성 위암을 진단받았다. 본과에서 우안의 아메드밸브삽입술 시행 후 안압은 안정적으로 유지되었고 외과에서 위부분 절제술을 시행하였다.
결론
망막분지정맥폐쇄 환자에서 심한 신생혈관녹내장이 발생하는 경우, 전신검사 및 평가를 시행하여 망막의 혈액 공급을 악화시킬 수 있는 동반 요인에 대해 고려하여야 한다.
Trans Abstract
Purpose
Here we report a case of neovascular glaucoma in a patient with branch retinal vein occlusion and severe anemia due to advanced gastric cancer.
Case summary
A 79-year-old hypertensive male was transferred to the emergency room because of ocular pain and high intraocular pressure (IOP) in the right eye. He had a history of sectoral retinal photocoagulation for branch retinal vein occlusion in the right eye at a local hospital 9 months previously, and was suspected of having ocular ischemic syndrome for the past 7 days. At the time of admission, his best-corrected visual acuity was hand motion in the right eye and 1.0 in the left eye. His IOP was 28 mmHg in the right eye and 15 mmHg in the left eye, measured using a Goldman applanation tonometer. Neovascularization was observed in the iris on slit-lamp examination; detailed fundus examination and gonioscopy could not be performed because of hyphema in the right eye. Ahmed valve implantation was planned based on a diagnosis of neovascular glaucoma. Preoperative blood tests showed severe anemia (hemoglobin: 7.8 g/dL), indicating gastrointestinal bleeding. Advanced gastric cancer was confirmed on endoscopy and biopsy. Ahmed valve implantation was performed in the right eye and the IOP was maintained within the normal range. Distal gastrectomy was performed by the general surgery department.
Conclusions
Severe neovascular glaucoma in branch retinal vein occlusion patients requires careful systemic examination for concomitant factors that may worsen the retinal blood supply.
신생혈관녹내장의 주된 병인은 당뇨망막병증, 망막중심정맥폐쇄, 안허혈증후군으로 알려져 있으며 이들은 공통적으로 망막 후극부 부분의 허혈을 일으켜 저산소증에 의해 발생된 혈관내피생성인자의 분비를 야기하여 홍채 및 전방각에 신생혈관 형성을 촉진시키고, 증식성 섬유혈관막에 의해 전방각이 폐쇄되어 속발녹내장을 유발한다. 신생혈관녹내장의 예방과 치료로는 전 단계에 범망막광응고를, 녹내장 단계에 범망막광응고 및 약물, 수술적 치료를 시행하고 있다. 그러나 이러한 치료에도 불구하고 안과적으로는 난치성 질환에 해당하며 이는 홍채와 전방각 표면에 생성된 섬유혈관막 및 주변홍채유착으로 인해 안압하강제의 효과가 적기 때문이다. 또한 술 중 또는 술 후 출혈 및 섬유혈 관막에 의한 여과 수포 형성의 실패로 인해 섬유주절제술 및 방수유출장치삽입술 시행에도 예후가 불량한 것으로 알려졌다[1]. 망막분지정맥폐쇄의 경우 망막 허혈 범위가 충분히 넓지 않다면 신생혈관녹내장의 단독 발생이 매우 드물며[2] 망막분지동맥폐쇄와 같은 망막 허혈을 악화시키는 다른 요인이 함께 동반된 경우의 증례들은 보고된 적이 있다[3]. 현재까지 망막분지동맥폐쇄와 동반된 국내 증례는 있었지만 전신 질환과 동반되어 나타난 사례는 드물며 눈 이외 부위의 암 발생과 동반되어 나타난 사례의 보고는 지금까지 없었다. 본 증례의 환자는 진행성 위암으로 인한 중증 빈혈이 동반되었고 넓지 않은 부위의 망막분지정맥폐쇄안에서 신생혈관녹내장이 발생하여 이를 보고하고자 한다.
증례보고
기저 질환으로 고혈압을 지닌 78세 남자 환자가 내원 1주일 전 타원에서 우안의 안허혈증후군 의심하에 경과 관찰 도중 발생한 점진적인 시력저하, 통증 및 안압상승으로 의뢰되었다. 본원 내원 9개월 전 타 병원에서 우안 망막분지정맥폐쇄 진단 후 부분적 망막광응고술을 시행받았으며 2년전 양안 초음파 수정체유화술 및 후방 인공수정체삽입술을 시행한 병력이 있었다.
본원 내원 당시 최대 교정시력은 우안 안전수동, 좌안 1.0이었으며, 안압은 골드만압평안압계로 우안 28 mmHg, 좌안 15 mmHg였다. 우안 홍채 신생혈관과 전방출혈 소견 관찰되었으며 좌안은 특이 소견이 관찰되는 바 없었다. 본원 내원 당시 우안의 전방출혈로 인한 전방흐림으로 인하여 자세한 안저검사 및 전방각경검사가 불가하였다(Fig. 1).
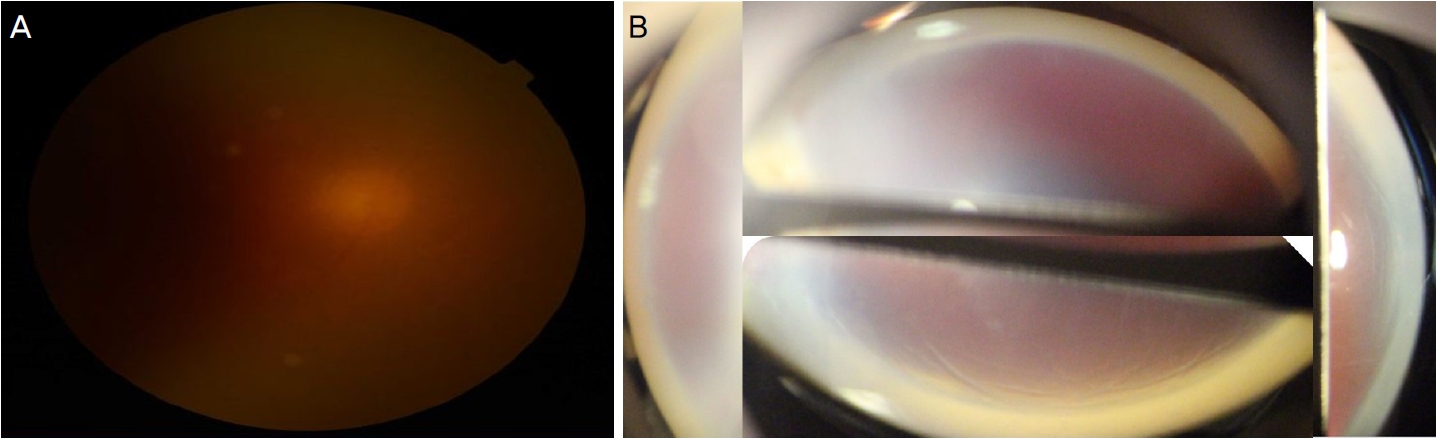
Blurred imaging of fundus and anterior chamber angle due to anterior chamber flare and hyphema. (A) Fundus photograph of the right eye at the time of first visit. (B) Gonioscopic examination of the right eye at the time of first visit.
그러나 내원 1주 전 타원에서 촬영한 안저 사진에서 우안 상이측 1/4 가량 망막 부위의 망막분지정맥폐쇄 후의 혈관성 변화 및 부분적 망막광응고술 반흔을 확인할 수 있었다(Fig. 2).
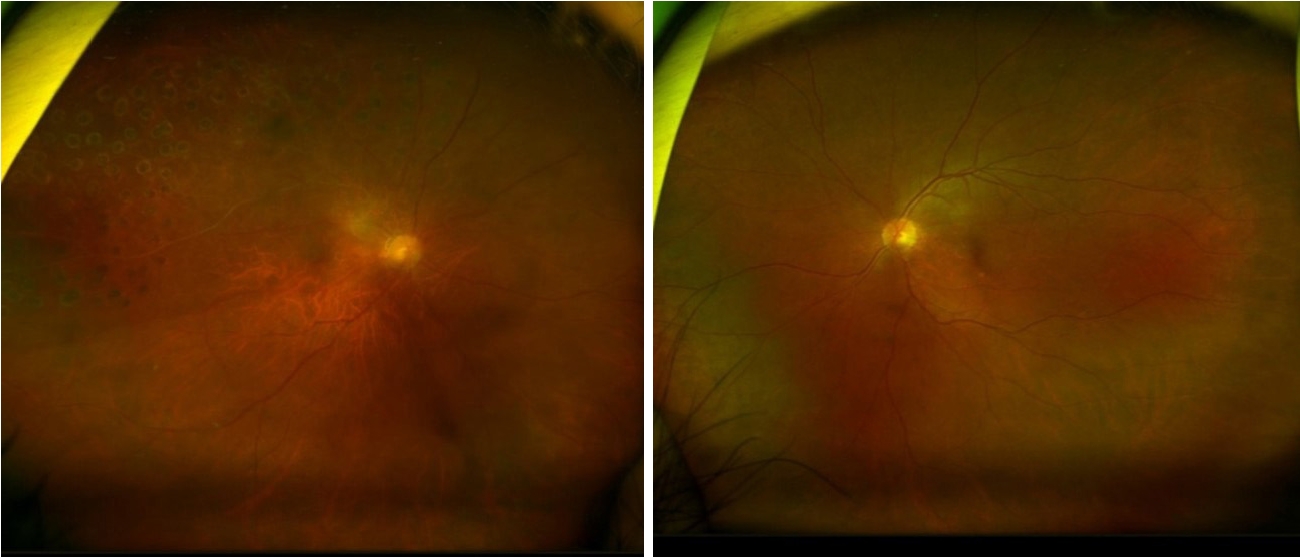
Ultra-Widefield fundus photographs of both eyes presenting ghost vessels and scatter laser photocoagulation scar at superotemporal retina of the right eye, 1 week before the first visit.
우안 신생혈관녹내장으로 진단하에 1주 뒤 전방 내 및 유리체강 내 베바시주맙(1.25 μg/0.03 mL, 0.05 mL, Avastin, Genetech Inc., San Francisco, CA, USA) 주입술 뒤 아메드밸브삽입술을 계획하였으며 dorzolamide 2%/timolol 0.5% 병합제제 2회, brimonidine 0.2% 3회, bimatoprost 0.01% 1회 점안으로 최대약물 치료를 시행하였다. 수술을 위해 동일 시행한 혈액검사 결과상 hemoglobin 7.8 g/dL (정상 14-18 g/dL)의 중등도 빈혈 소견이 관찰되었으며 신생혈관녹내장의 원인을 알아보기 위해 촬영한 경부 전산화단층촬영 혈관조영술(computed tomography angiography) 결과 우측 내 측속목동맥의 중등도 협착 소견 및 좌측 내측속목동맥의 중증 협착 소견이 관찰되었다(Fig. 3). 이후 본원 순환기내과에 의뢰하에 시행한 혈액검사상 hemoglobin 7.8 g/dL (정상 14-18 g/dL), hematocrit 26.3% (정상 38-52%), MCV 78.4 fL (정상 80-95 fL), MCH 23.2 pg (정상 26-32 pg), MCHC 29.7 g/dL (정상 32-36 g/dL), ferritin 11.3 ng/mL (정상 22-322 ng/mL), transferrin 327 mg/dL (정상 200-360 mg/dL), 말초혈액펴바른표본검사상 감소된 적혈구 수 및 크기가 관찰되어 중증의 철 결핍성 빈혈 소견을 보이고 있었으며 특이사항으로는 carcinoembryonic antigen 수치가 6.89 ng/mL (정상 0-5 ng/mL)로 증가되어 있었다. 하지만 2년 전 백내장수술을 위한 검사 시 hemoglobin은 15 g/dL 로 정상 수치였다. 철 결핍성 빈혈의 가장 흔한 원인 중에 하나인 위장관계 출혈 의심 하에[4] 본원 소화기내과 의뢰하여 술 전 위대장 내시경검사를 의뢰하였다. 시행한 결과 위체부 내의 소만곡 부위에 4 cm 크기의 침윤형 궤양성 종괴가 관찰되어(Fig. 4) 조직검사를 시행하였으며, 익일 예정대로 아메드밸브삽입술을 시행하였다.
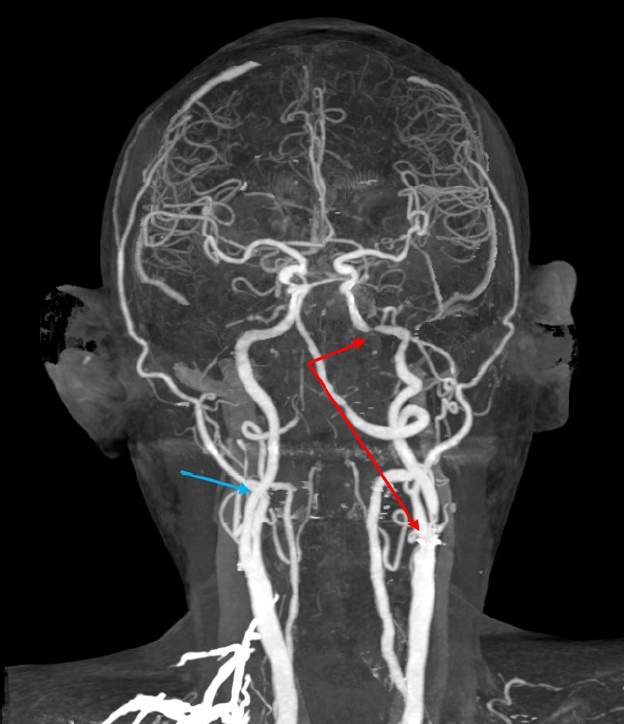
Brain-neck computed tomography angiography imaging modality presenting left proximal and distal internal carotid artery severe stenosis (red arrows), and right distal internal carotid artery moderate stenosis (blue arrow).
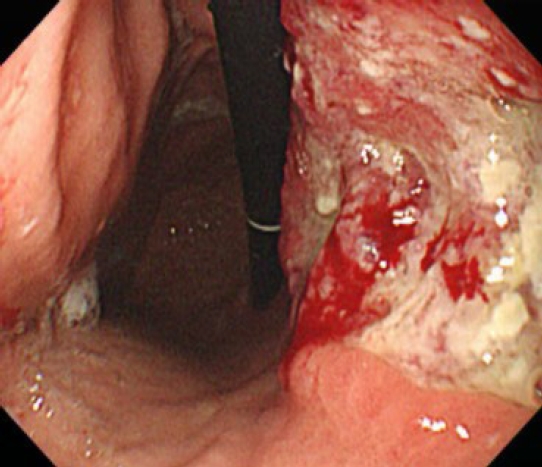
Gastrofiberscopy shows about a 4 cm sized ulceroinfiltrative mass seen on the posterior wall of the lower curvature of the lower gastric body.
아메드밸브삽입술 술 후 1일째에 우안 안압은 골드만압평안압계로 14 mmHg, 최대교정시력은 안전수지로 측정되었다. 동일 앞서 시행하였던 조직검사 결과상 위샘암종 소견이 확인되었으며 익일 촬영한 양전자 방출 전산화단층촬영(positron emission tomography computed tomography)검사상에서도 비정상 세포의 움직임을 시사하는 음영 증강 소견을 위각 부위에서만 관찰할 수 있었다. 이에 본원 일반 외과에 의뢰하여 전복강경하 원위부 위절제술을 시행하였다. 술 후 1년 뒤 우안 안압은 골드만압평안압계로 10 mmHg, 최대교정시력은 0.02로 측정되었으며 안저 사진상 이전과 동일한 부위에 가늘어진 동맥 및 비어 있는 정맥혈관 소견이 수술 전과 유사하게 관찰되고 있다. 망막의 주변부는 신생혈관녹내장 치료를 위한 추가적인 망막광응고술 반흔을 관찰할 수 있으며(Fig. 5), 위절제술 부위는 재발 소견 없이 안정적 양상을 보였다.
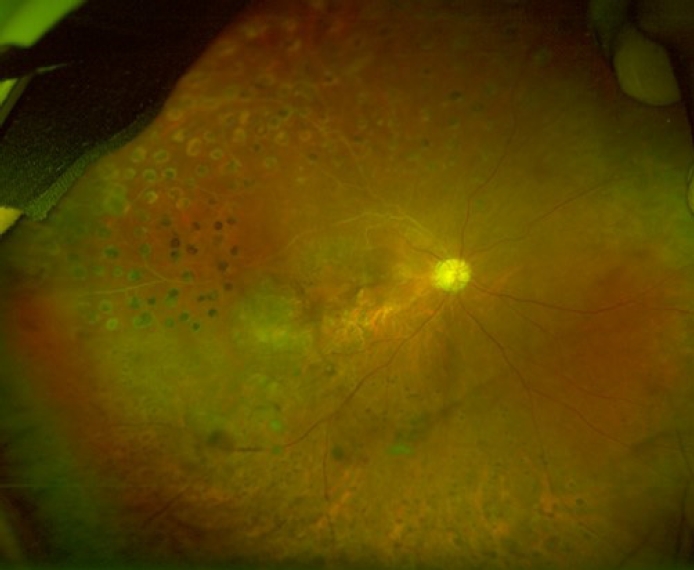
Ultra-Widefield fundus photograph of the right eye 1 year after ahmed glaucoma valve implantation, showing narrowed arteries and ghost vessels in the same superotemporal area as before surgery. Additional panretinal photocoagulation scars for the treatment of neovascular glaucoma are observed in the peripheral retina.
고 찰
신생혈관녹내장은 발생 기전으로 여러 원인에 따른 망막 허혈이 가장 중요한 부분이다. 따라서 여러 가지 질환 중 광범위하게 망막 허혈을 야기할 수 있는 당뇨망막병증, 망막중심정맥폐쇄, 안허혈증후군등이 주요 원인 질환이 될 수 있다[5]. 하지만 망막분지정맥폐쇄의 경우 신생혈관녹내장의 발생 가능성이 아주 낮은 것으로 되어 있다[6]. Hayreh et al [2]은 총 264안의 망막분지정맥폐쇄안 중 망막의 1/2 이상을 포함하는 허혈 부위를 지닌 한 증례만에서 신생혈관녹내장으로의 진행을 관찰할 수 있었다고 보고하였으며 Magargal et al [7]은 망막의 1/4 부위만을 포함하는 허혈 범위를 가졌음에도 50세 이상의 나이, 전신 혈관 질환 및 고안압증 소인을 지닌 환자에서 발생한 신생혈관녹내장 증례 1예를 보고한 바 있다. An and Kwon [3]은 망막분지정맥폐쇄 및 망막분지동맥폐쇄가 동반된 환자에서 신생혈관녹내장을 일으킬 가능성이 매우 낮은 두 질환이 망막의 각각 다른 부위에 영향을 주어 시너지 효과로 인하여 신생혈관녹내장이 발생한 증례를 보고한 바 있다. 이처럼 망막분지정맥폐쇄의 경우 망막 절반 이하의 허혈 범위를 가져 신생혈관녹내장으로의 진행 가능성이 매우 낮으며 본 증례의 환자 또한 상이측 1/4 부위만의 망막분지정맥폐쇄 침범 소견만을 보였기에 단독 요인으로 고려하기에는 맞지 않아 신생혈관 녹내장으로 진행하기 위해선 동반된 타 허혈성 요인이 필요했음을 추측할 수 있다.
빈혈의 경우 유형과 관계없이 단독 요인으로 망막 영역에 허혈성 변화를 일으킬 수 있으며[8] 빈혈만으로도 망막의 혈액 순환이 악화되어 신생혈관녹내장이 발생한 경우의 증례도 보고된 바 있다. Yahia et al [9]은 당뇨망막병증, 망막정맥폐쇄등의 다른 요인이 없는 순수한 판코니 빈혈을 지닌 11세 여아에서 시행한 형광안저혈관조영술 결과 이측 망막 부위의 광범위한 허혈 범위를 발견할 수 있었고 이로 인한 신생혈관녹내장으로의 진행을 보고하였다. 빈혈성 망막병증의 경우 망막의 저산소증을 야기하여 망막 출혈, 연성 삼출물 등의 소견을 나타낼 수 있으며 철 결핍성 빈혈 환자 37명을 조사한 결과 9명에서 빈혈성 망막병증 소견이 관찰되었으며 헤모글로빈 수치가 8 g/dL보다 낮은 중증 빈혈 소견을 지닌 33명 중 23명에서 빈혈성 망막병증 소견이 관찰됨을 보고한 바 있다[10]. Xue et al [11]은 철 결핍성 빈혈 환자의 hemoglobin 수치에 따라 중증도를 분류하여 혈중 적혈구생성인자의 수치를 조사하였으며 철 결핍성 빈혈 환자군에서의 치료 전과 치료 시작 후 1-2개월의 기간 동안 대조군인 정상군보다 적혈구생성인자의 수치가 높았고 또한 빈혈이 악화되거나 중증일수록 수치의 증가에 기여함을 보고한 바 있다. 적혈구생성인자는 신생혈관의 발생을 촉진시키는 허혈로 유도된 혈관생성인자에 해당하며 증식당뇨망막병증 환자의 유리체 내에서 그 증가 수치를 찾아볼 수 있다[12]. Raman and Lambley [13]는 1형 당뇨병을 지닌 환자에서 적혈구생성인자가 관상동맥 우회로 이식술로 유리체강내 및 전안부로의 공급이 증가되어 신생혈관녹내장의 진행을 가속화시킨 증례를 보고한 바 있다.
본 증례는 망막분지정맥폐쇄 과거력과 속목동맥중등도 협착을 가졌고 이후 진행성 위암으로 인하여 발생한 중증의 철 결핍성 빈혈로 인하여 신생혈관녹내장으로 이어졌으나 초기의 적절한 약물 치료 및 유리체강 내 베바시주맙 주입술, 방수유출장치삽입술 등을 시행하여 이후 추가적인 안압하강제의 사용 없이 안정적으로 안압이 유지되고 있는 증례이다. 특이점으로는 우측 속목동맥의 중등도 협착 소견이 관찰되었으나 좌측은 심한 중증의 속목동맥협착이 관찰되었다는 점이다. 속목동맥협착과 빈혈 모두 양안에 영향을 미칠 수 있지만 좌안은 망막 소견이 정상이고 신생혈관 관찰이 없으나, 좌안보다 우안의 속목동맥협착 정도가 낮음에도 불구하고 우안에만 신생혈관녹내장이 발생한 것으로 보아, 본 증례에서는 우안에만 국한된 요인인 망막분지정맥폐쇄가 신생혈관녹내장의 발생에 가장 큰 기여를 했을 것으로 유추해 볼 수 있다. 하지만 본 증례의 망막분지정맥폐쇄의 비관류 부위는 망막 전영역의 1/4 범위의 넓지 않은 침범을 보이고 있으며 타원에서 이미 9개월 전 부분적 망막 광응고술을 시행한 뒤 내원한 상태였다. 따라서 기존의 연구에 따르면 단독으로 신생혈관녹내장을 발생시킬 가능성은 낮다고 여겨진다. 그리고 내원 당시에 진행성 위암으로 인해 나타난 중증 철 결핍성 빈혈은 약 18개월 전 타원에서 시행한 혈액검사에서 15 g/dL의 정상 hemoglobin 수치를 보였으므로 급성으로 철 결핍성 빈혈이 진행했음을 알려준다. 따라서 본 증례의 환자는 hemoglobin 수치 8 g/dL 이하의 중증의 철 결핍성 빈혈 소견으로 급격히 증가한 체내의 적혈구생성인자가 안구 내로 전달되었고 망막분지정맥폐쇄 소견과 맞물리어 신생혈관녹내장으로 진행하였을 것으로 생각된다. 하지만 본 증례의 한계점으로는 전방출혈로 인하여 내원 시 안저 소견을 확인하지 못했고 형광안저혈관조영술을 시행하지 못하여 망막정맥폐쇄로 인한 정확한 허혈 범위를 측정하지 못하였다는 점으로, 이전 안저 소견만으로 예측하였기에 안저의 1/4 범위보다 더 넓은 허혈 범위가 존재하였을 가능성이 있다. 또한 속목동맥협착으로 인한 안허혈증후군의 가능성을 완전히 배제할 수 없으며 망막 허혈에 대한 취약점으로 작용했을 수 있으나 정상안보다 덜 심한 협착과 술 후 사진에서 다른 부위의 혈관 변화가 동반되지 않아 이번 신생혈관녹내장 발생을 유발한 주된 원인은 아님을 추정해 볼 수 있다.
결론적으로, 넓지 않은 허혈 범위의 망막분지정맥폐쇄안에서 신생혈관이 발생한 환자에서 빈혈이 동반되어 전신검사를 통해 진행성 위암을 발견할 수 있었던 점에서 임상적 의의가 있다. 급성으로 진행한 중증의 빈혈로 의해 높아진 망막의 산소요구에 기존의 망막분지정맥폐쇄로 인하여 망막허혈에 취약해진 우안에서 신생혈관녹내장이 발생한 것으로 추측된다. 따라서 망막병변으로 작은 허혈 부위를 가지는 환자에서 신생혈관녹내장이 발생하는 경우, 반드시 전신검사 및 평가를 함께 실시하여 망막의 허혈 상태를 급격하게 악화시킬 수 있는 다른 전신적, 안과적 동반 질환에 대하여 충분히 고려하여야 한다.
Notes
Conflicts of Interest
The authors have no conflicts to disclose.
References
Biography
김형주 / Hyeong Ju Kim
울산대학교 의과대학 울산대학교병원 안과학교실
Department of Ophthalmology, Ulsan Uni versi ty H ospital, U niversi ty o f Ulsan College of Medicine
