항인지질항체증후군에서 발생한 양안 언가지혈관염
Bilateral Frosted Branch Angiitis in Anti-phospholipid Antibody Syndrome
Article information
Abstract
목적
항인지질항체증후군에서 발생한 양안 언가지혈관염 증례를 경험하였기에 보고한다.
증례요약
60세 여자 환자가 악화되는 양안 비문증 및 시력저하로 내원하였다. 초진 시 교정시력 우안 0.8, 좌안 0.05였고, 양안 전방과 유리체의 염증, 후극부 및 주변부 망막에 전체적으로 퍼져 있는 언가지 모양의 혈관초가 관찰되었으며, 빛간섭단층촬영에서 좌안의 황반부종, 형광안저혈관조영술에서 양안의 혈관초가 형성된 망막혈관에서 형광색소의 염색 및 누출이 관찰되었다. 혈액검사 및 경구 스테로이드 치료를 시작하였으며 항인지질항체검사에서 항카디오리핀항체(anticardiolipin antibody), 항베타2당단백 I 항체(anti-ß2 glycoprotein-I antibody)가 양성으로 원발항인지질항체증후군에서 발생한 언가지혈관염으로 진단하였다. 경과 관찰 기간 동안 교정시력 우안 0.5, 좌안 0.3으로 큰 변화 없이 유지 중이며 재발의 소견은 보이지 않았다.
결론
양안 언가지혈관염은 드문 질환으로 전신 스테로이드 치료에 잘 반응한다고 알려져 있으나 본 증례와 같이 원발항인지질항체증후군과 동반될 경우 비전형적인 예후를 보일 수 있다.
Trans Abstract
Purpose
We report a case of bilateral frosted branch angiitis caused by anti-phospholipid antibody syndrome.
Case summary
A 60-year-old female complained of worsening vitreous floaters and decreased visual acuity in both eyes. The initial best-corrected visual acuity (BCVA) was 0.8 in the right eye and 0.05 in the left. On slit-lamp examination, inflammatory findings were observed in the anterior chamber and vitreous body of both eyes. On fundus examination, vascular sheathing in the shape of a frosted branch was observed in the posterior pole and peripheral retina in both eyes. Optical coherence tomography indicated macular edema in the left eye. Staining and leakage of dye along the vascular sheathing were observed in both eyes with fluorescein angiography. On suspicion of panuveitis, we conducted a blood test and started eye drops and oral steroid therapy. However, vitreous inflammation, macular edema, and vascular sheathing increased; thus, we proceeded with systemic steroid therapy. We conducted blood tests at 8-week intervals; lupus anticoagulant was negative but anticardiolipin antibody and anti- ß2 glycoprotein-I antibody were positive. We diagnosed the patient with bilateral frosted branch angiitis caused by anti-phospholipid antibody syndrome. During the follow-up period, the BCVA remained steady at 0.5 in the right eye and 0.3 in the left eye, without symptom recurrence.
Conclusions
Bilateral frosted branch angiitis, a rare disease, is known to respond well to systemic steroid treatment. However, if accompanied by primary anti-phospholipid antibody syndrome, as in the case presented, it may have an atypical prognosis.
항인지질항체증후군(antiphospholipid syndrome)은 혈청학적으로 루프스항응고인자(lupus anticoagulant), 항카디오리핀 항체(anticardiolipin antibody), 항베타2당단백 I 항체(anti-ß2 glycoprotein-I antibody)의 항인지질항체가 양성이며, 재발성 정맥 및 동맥의 혈전증, 습관성 유산, 혈소판 감소 등의 증상을 보이는 후천성 자가면역 질환이다[1]. Utz and Tang [2]은 항인지질항체증후군 환자의 임상에서 심부정 맥혈전증이 가장 흔한 첫 증상(38.9%)이었고, 혈전증이 다른 모든 장기에서 발생이 가능하며, 안과적으로는 일과성 흑암시(amaurosis fugax, 5.4%), 망막동맥혈전증(retinal artery thrombosis, 1.5%)도 가능하다고 보고하였다. 항인지질항체증후군이 안구에 이환되는 발생률은 8-88%로 연구마다 상이한 차이를 보이며, Utz and Tang [2]은 후안부가 항인지질항체증후군이 주로 이환되는 장소로 망막혈관폐쇄, 유리체 염증, 허혈시신경병증 등이 동반될 수 있고, 흔하지 않지만 건성안증후군과 상피각막병증, 필라멘트각막병증 등 전안부에도 증상이 나타난다고 보고하였다[2,3]. 언가지혈관염(frosted branch angiitis)은 대부분 건강한 젊은이에서 발생하고, 양안을 침범하며 심한 시력저하를 보이지만, 대부분 전신적 스테로이드 치료에 잘 반응하고 재발 없이 좋은 예후를 가지고 있는 것으로 알려져 있다[4,5]. 또한 발병 전에 대부분 감기 증상을 앓거나 바이러스 감염질환을 앓기도 하며, 다른 전신적인 질환[4,5]과 연관성이 언급되기도 한다[4]. Wood and Wong [6]은 2016년 항인지질항체증후군과 관련된 양안의 언가지혈관염에 대해 스테로이드 치료 후 좋은 결과를 보였다고 보고하였는데, 이에 저자들은 국내에서 원발항인지질항체증후군 환자에서 양안 언가지혈관염이 보고된 바 없으며, 비전형적인 예후를 보인 증례를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
증례보고
60세 여자 환자가 내원 3일 전부터 시작되는 우안 비문증을 주소로 내원하였다. 환자는 3주 전부터 시작된 좌안의 비문증으로 타병원 방문하였으며, 타병원 초진 시 양안 시력 1.0, 좌안은 유리체혼탁 소견을 보였다. 경과 관찰하는 중 톡소플라스마 면역글로블린 M (immunoglobulin M, IgM) 항체 양성 판정을 받아 톡소플라즈마 맥락망막염 의증으로 진단 후 경구 트리메토프림-설파메톡사졸(Septrin®; Samil Pharm., Seoul, Korea) 복용하였으나 악화되는 염증으로 테논낭하 스테로이드주입술을 시행받았다. 이후 지속적으로 악화되는 비문증 및 시력저하로 본원으로 전원되었으며, 본원 초진 당시 교정시력 우안 0.8, 좌안 0.05였고, 양안에 경미한 전방 염증세포와 우안 유리체내 1+ 염증세포, 좌안 유리체내 2+ 염증세포, 양안 후극부 및 주변부 망막에 전체적으로 퍼져 있는 언가지 모양의 혈관초가 관찰되었다. 빛간섭단층촬영에서 좌안 낭포황반부종 및 좌안 망막내층의 두꺼워짐, 형광안저혈관조영술에서 양안의 혈관초가 형성된 망막혈관에서 형광색소의 염색 및 누출이 관찰되었다(Fig. 1). 양안 전체 포도막염 진단하 스테로이드 점안액(Predbell®; ChongKunDang Pharm., Seoul, Korea)과 경구 스테로이드(Prednisolone acetate, Solondo®; Yuhan, Seoul, Korea) 30 mg을 처방하였으며, 다양한 감염성 및 염증성 병인에 대한 전신검사를 시행하였다. 환자는 특이적인 과거력 및 류마티스질환도 가지고 있지 않고 유산 경험도 없었으며, 개, 염소, 닭을 키우고 생식은 하지 않는다고 진술하였다. 생체활력징후는 정상이었으며, 일반 혈액검사는 정상, 적혈구 침강속도 35 mm/hr (참고치 0-20), C-반응단백질 0.1 mg/L (참고치 0-0.5)였고, 간기능, 혈중 요소 질소, 크레아티닌, 전해질 수치, 소변검사 수치 등은 정상이었다. 혈액응고검사에서 PT (prothrombin time), INR (international normalized ratio), aPTT (activated partial thromboplastin time)는 정상 범위 내에 있었고, protein C, protein S, antithrombin III도 정상 범위였다. 혈청학적 검사에서 간염표지자, 항핵항체, VDRL (veneral disease research laboratory), ANCA (antineutrophil cytoplasmic antibody) 등은 음성이었으며, 혈청 보체 C3 116 mg/dL (정상 범위 90-180), C4 29 mg/dL (정상 범위 10-40)도 정상 범위였다. 항인지질항체검사에서 루푸스 항응고인자는 음성이었으나 항카디오리핀 항체 IgM 43.1 GPL (정상 범위 <12.0), IgG 3.4 GPL (정상 범위 <12.0), 항베타2당단백 I 항체 IgM 32.0 U/mL (정상 범위 <20.0), 항베타2당단백 I 항체 IgG 8.0 (정상 범위 <20.0)으로 양성반응을 보였다. 그 외 흉부 X선검사, 결핵, 단순포진바이러스, 대상포진바이러스, 거대세포바이러스, 톡소플라즈마에 대한 면역글로블린검사, B27과 B51을 포함한 백혈구항원검사도 모두 정상 범위이거나 음성이었다. 경구 스테로이드 복용을 지속하면서 나온 검사 결과와 임상양상을 통해서 원발항인지질항체증후군에서 발생한 양안 언가지혈관염으로 추정 진단하였으나 교정시력 우안 0.6, 좌안 안전수동으로 시력저하, 유리체염증 및 혈관초가 증가하는 악화 양상(Fig. 2)을 보여 3일간의 고용량 스테로이드 충격요법 및 류마티스 내과에 의뢰 후 아스피린을 같이 복용하였다. 전신 스테로이드 용법 이후 경구 스테로이드 50 mg 및 아스피린을 지속적으로 복용하였고, 좌안의 황반부종과 유리체염증은 감소하였으나 우안 교정시력 안전수동으로 저하, 황반부종 및 유리체염증이 증가하는 소견이 관찰되었다(Fig. 3). 초진 당시 염증이 적고 시력이 좋았던 우안의 지속적 악화로 유리체강내 덱사메타손 임플란트(Ozurdex®; Allergan, Irvine, CA, USA) 주입술을 시행하였으며, 아스피린 복용을 유지하면서 전신 스테로이드는 5 mg을 2주 간격으로 감량하였다. 전신 스테로이드를 감량하는 도중 교정시력 양안 0.3으로 호전, 혈관초 및 유리체염증, 황반부종은 호전되어 유지하였으나 내원 2개월째에 좌안에 망막출혈 및 황반부종이 관찰되어 유리체강내 덱사메타손 임플란트주입술을 시행하였다. 이후 6개월간 교정시력 우안 0.5, 좌안 0.3으로 유지되었고, 혈액검사에서는 지속적으로 항인지질 항체가 상승된 소견이 보였으며(항카디오리핀 항체 IgM 31.2 GPL, 항카디오리핀 항체 IgG 3.4 GPL, 항베타2당단백 I 항체 IgM 53.0 U/mL), 상태는 안정되어 아스피린 복용을 유지하며 외래 통해 경과 관찰 중이다(Fig. 4).
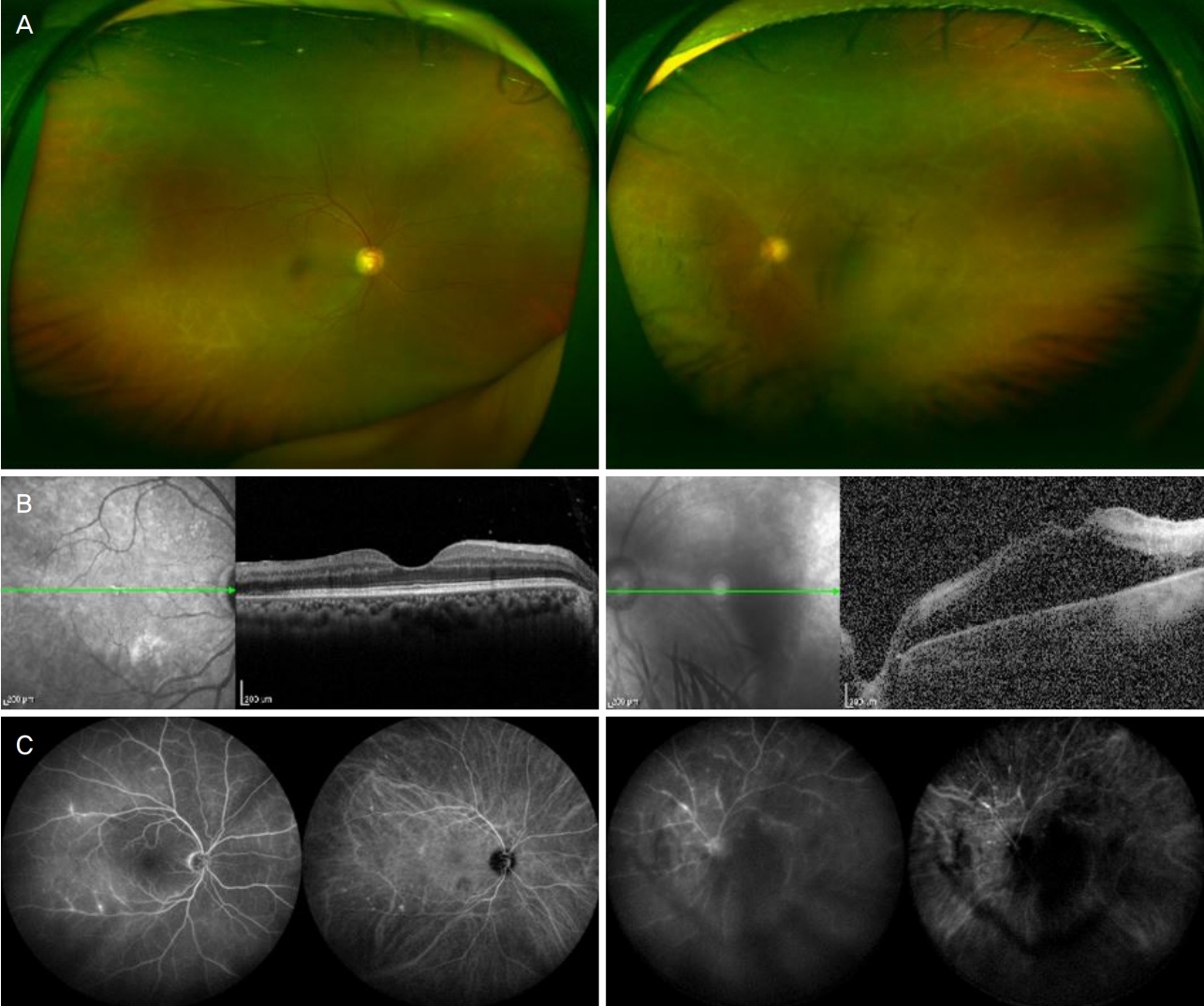
These figure show fundus photography, optical coherence tomography, fluorescein angiography and indocyanine angiography of the patient at first visit to our clinic. (A) Bilateral frosted branch vascular sheathing was observed at baseline. (B) Cystoid macular edema in the left eye and inner retinal layer thickening in the left eye. The central macular thickness in left eye was 422 µm. (C) The leakage and staining of fluorescein dye in the late stages at fluorescein angiography and the leakage from choroidal vessels at indocyanine angiogram.

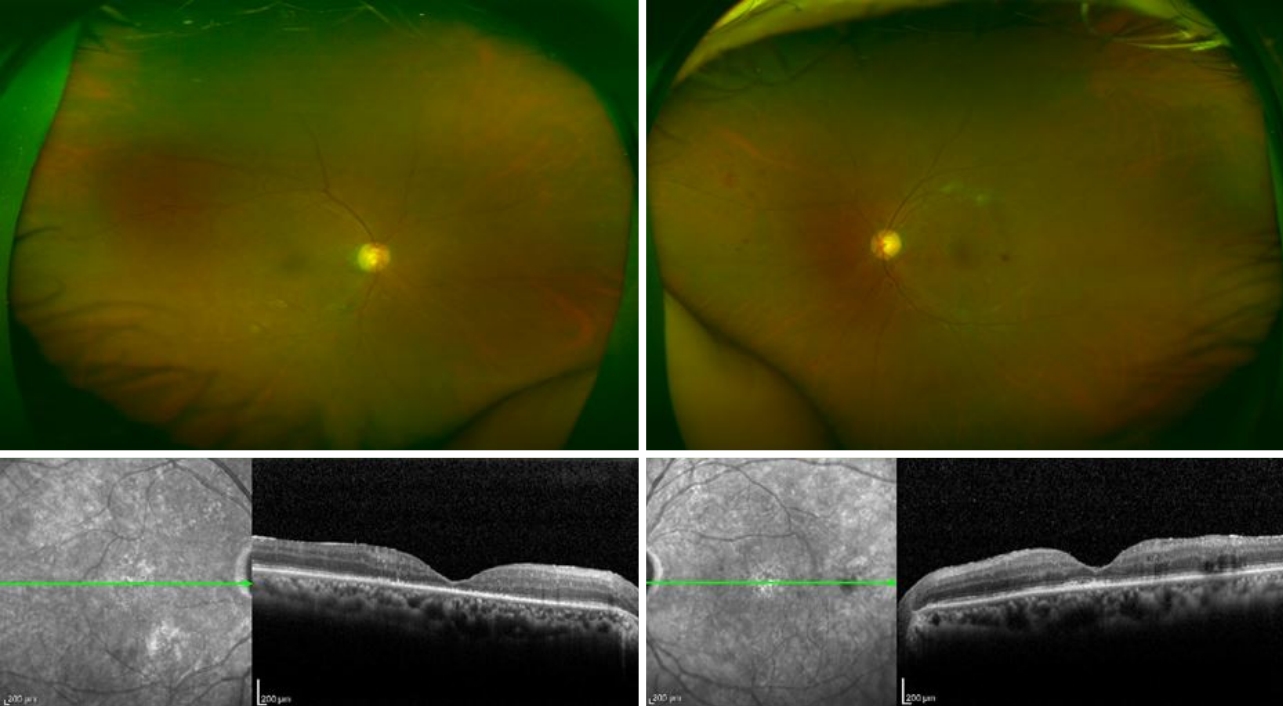
Fundus photography and optical coherence tomography of the patient. Vitreous inflammation and vascular sheathing was aggravated in the left eye. The central macular thickness in left eye was 675 µm. Ten days after the initial diagnosis, the macular edema increased and visual loss worsened.
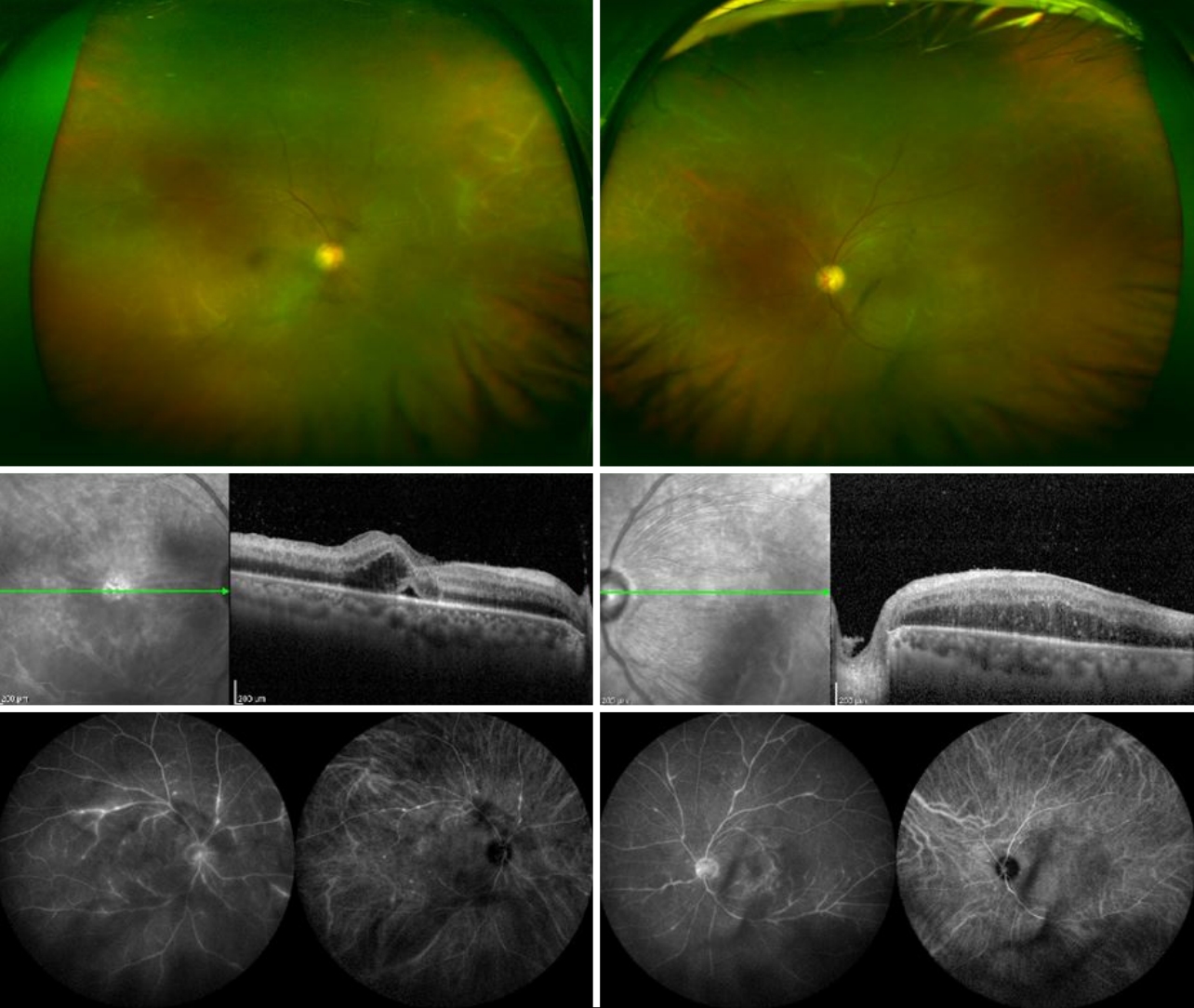
Fundus photography, optical coherence tomography, fluorescein angiography and indocyanine angiography of the patient at 15 days after the initial diagnosis. On fundus photo, the vascular obstruction and sheathing were increased in the right eye, while decreased in the left eye. On optical coherence tomography, the thickness of the central macula was reduced to 575 µm and vitreous inflammation was decreased in the left eye. But in the right eye, the thickness of the central macula has been increased to 419 µm compared to initial inspection, at that time, the thickness of the central macula was 259 µm. And the vitreous inflammation was increased. On fluorescein angiography and indocyanine angiography, the leakage and staining of dye were increased in the right eye.
고 찰
항인지질항체증후군은 많은 임상 분야에서 대단한 관심을 끌고 있으며, 항인지질항체와 관련하여 여러 조직이나 기관에 혈전을 일으킴으로써 다양한 임상증상을 야기한다[5]. 항인지질항체증후군의 진단은 항인지질항체가 12주 이상 지속되는 항베타2당단백 I IgM 또는 IgG 양성, 항카디오리핀항체 양성, 루프스항응고인자 양성의 세 가지 항목 중 적어도 한 가지 이상을 만족시켜야 한다. 또한 명백한 기저질환이 없는 경우를 원발항인지질항체증후군, 루프스 등의 자가면역질환과 동반되는 경우를 이차항인지질항체증후군이라고 구분한다[1].
언가지혈관염은 1976년 Ito [4]가 6세 남아에서 급성으로 망막혈관을 따라 생기는 초형성(sheathing)을 특징으로 한 포도막염을 처음 보고하였고, 나뭇가지에 서리가 내린 모양을 닮아 명명된 특징적인 망막혈관염을 일컫는다. 호발 연령은 어린이나 30대의 양봉분포(bimodal distribution)를 보이고, 남성보다 여성에서 더 발병률이 높다고 알려져 있다[4]. 대부분의 경우 양측성(75%)이며, 시력은 병이 진행할수록 감소하여 광각까지 감소하기도 한다[4]. 특징적인 안저와 홍채염 및 유리체염, 망막부종을 동반하기도 하며, 회복기에는 미세출혈을 동반하기도 한다[4]. 병인은 명확하게 밝혀지지 않았으나 면역 저하 환자들의 경우 거대세포바이러스 감염과 연관이 있다고 알려져 있으며 정상 면역 환자의 경우 톡소플라즈마증(toxoplasmosis), 크론병(Crohn’s disease), 전신홍반루프스(systemic lupus erythematosus) 질환과 연관이 되어 발병한다[4]. 이러한 다양한 감염원에 의한 과민반응(hypersensitivity reaction)으로 언가지혈관염이 생기기 전의 전구증상(감기증상)을 앓을 수 있으며, 면역 복합체 침착(immune complex deposition)이 생겨 병이 발병하는 것으로 생각하기도 한다[7]. 또한 이로 인해 전신 스테로이드 치료를 시행하는 경우 회복이 빠르며 좋은 예후를 보이는 것으로 알려져 있으나, 황반부 반흔(macular scarring)이 발생하여 시력예후가 안 좋은 경우가 발표되기도 하였다[4-7].
본 증례에서 환자는 이전 기저질환이 없으며, 유산 경험도 없는 과거력이 없는 상태로 안과적 질환이 발병하였다. 처음 내원 당시 타병원에서 톡소플라즈마 항체 양성 소견이 보여 톡소플라즈마 맥락망막염 의증으로 치료를 하였으나 호전 양상 보이지 않고 진행성의 언가지혈관염이 관찰되었다. 또한 본원에서 시행한 혈액검사상 항인지질항체 양성 이외 다른 감염이나 루푸스 등의 면역질환을 의심할만한 소견은 발견되지 않았으므로 원발항인지질항체증후군에 의한 언가지혈관염이라고 판단하였다. 항인지질항체증후군과 관련된 언가지혈관염의 증례는 Wood and Wong [6]이 최초로 보고하였으며, 국내에서는 항인지질항체증후군과 관련된 망막혈관폐쇄 증례는 수차례 있었으나 언가지혈관염과 관련된 증례는 보고된 바 없어 임상적으로 의의가 있을 것으로 생각된다[8,9].
항인지질항체증후군은 다양한 형태의 인지질(phospholipids)과 인지질-결합 단백질(phospholipid-binding proteins)과 반응하여 자가면역항체가 생산되는 후천성 혈전장애(acquired thrombophilic disorder)이지만, 혈관 병변은 대개 혈전증(thrombosis)이나 미세혈관병증(microangiopathy)과 관련되어 염증(inflammation)과는 큰 관련은 없는 것으로 알려져 있다[5,10]. 그러나 혈관염(vasculitis)도 항인지질항체증후군에 드물게 나타나기도 하며, 전신혈관염이 있는 환자에게서 항인지질항체 양성을 보이기도 하고 속발항인지질항체증후군이 생기기도 한다[10-12]. 항인지질항체증후군에서의 혈전증이 생기는 병인에 대해서는 아직 완전히 밝혀지지 않았지만 면역반응에 의해 혈관내피 활성화, 염증성 싸이토카인(inflammatory cytokines)의 생성, 혈관세포부착 인자(vascular adhesion molecules)의 기능항진(upregulation)이 발생하여 혈관내강(vascular lumen)에 호중구와 단핵구의 동원(recruitment)을 촉진하게 된다[13]. Lally and Sammaritano [14]는 항인지질항체증후군에서 이러한 염증세포의 침윤이 혈전증과 동시에 생길 수 있지만, 혈관벽이 병리학적인 염증 변화(pathognomic inflammation)가 일어나는 진정한 의미의 혈관염은 나타내지는 않는다고 한다. 또한 망막혈전증의 유무와 관련 없이 망막혈관염만 나타나기도 한다[15]. 망막혈관염은 형광안저촬영에서 특징적인 형광누출과 모세혈관비관류를 관찰할 수 있는데, Lally and Sammaritano [14]는 항인지질항체증후군에서 망막혈관염은 조직병리학적(histopathology)인 근거가 없기 때문에 근본적인 원인으로 미세혈전(microthrombi)의 존재를 완전히 배제할 수 없으며, 이전의 연구에서도 스테로이드 치료 없이 항응고 치료로도 성공적으로 회복된 사례가 있듯이 혈전이 원인일 가능성이 있다[15]. 본 증례에서도 항인지질항체와 관련된 자가면역항체가 증가함으로 인해 혈관내피 세포, 혈소판, 단핵구 등 혈액응고 체계 및 보체 체계에서도 영향[3]을 받아 미세혈전과 관련된 혈관초를 보이는 망막혈관염이 발생한 것으로 생각된다. 따라서 초기 언가지혈관염이 확인되어 경구용 스테로이드 치료를 시도하였으나 양안의 진행되는 시력저하와 염증 증가를 보이는 비전형적인 경과를 보였으며, 류마티스 내과에 의뢰한 이후 항인지질항체증후군과의 관련성을 확인한 후 스테로이드 치료와 더불어 항응고제 투여(아스피린)를 동시에 시행하면서 안정된 것으로 생각된다.
항인지질항체증후군에서의 일차적인 치료는 항응고제를 통한 혈전증의 재발을 예방하는 데 있으며, 항인지질항체 확인 시 평생 항응고제 복용이 권장된다[5]. 또한 하이드록시클로로퀸(hydroxychloroquine)이 항인지질항체 양성인 환자에서 혈전증을 예방하는 것으로 알려져 있으며, 다른 치료에 반응하지 않을 경우 추가적인 치료 옵션으로 고려되기도 한다[5]. Wood and Wong [6]은 항인지질항체증후군을 동반하는 언가지혈관염에서 단기간의 전신적 고용량 스테로이드 치료와 더불어 장기간의 스테로이드 투여와 항응고제 병용 치료 이후 좋은 예후를 보였고, 재발 위험을 방지할 수 있다고 발표했다. 따라서 본 증례에서도 장기간의 스테로이드 투여와 항응고제 병용 치료가 좋은 예후를 보인 것으로 생각된다.
본 저자들은 국내 최초로 항인지질항체증후군과 동반한 양안의 언가지혈관염을 보고하는 바이며, 언가지혈관염의 증례에서 드물지만 항인지질항체증후군의 가능성을 항상 염두하고 항인지질항체를 포함한 다양한 항체인자에 대한 검사가 필요하다. 또한 혈액 내과 및 류마티스 내과와의 협진을 통해 전신적인 치료가 동반되어야 좋은 예후를 보일 수 있을 것으로 생각한다.
Notes
Conflicts of Interest
The authors have no conflicts to disclose.
References
Biography
이용민 / Yong Min Lee
건양대학교 의과대학 안과학교실
Department of Ophthalmology, Konyang University College of Medicine