Ļ░üļ¦ēņØ┤ņŗØņłśņłĀņØĆ Ļ░üļ¦ēņŚÉ ĻĖ░ļŖźņĀüņ£╝ļĪ£ļéś ĻĄ¼ņĪ░ņĀüņ£╝ļĪ£ ĒÜīļ│Ą ļČłĻ░ĆļŖźĒĢ£ ņåÉņāüņØ┤ ļ░£ņāØĒĢśņŚ¼ ņŗ£ļĀźņØ┤ ņĀĆĒĢśļÉ£ ĒÖśņ×ÉņØś Ļ░üļ¦ēņØä ņĀ£Ļ▒░ĒĢśĻ│Ā Ļ│ĄņŚ¼ņ×ÉļĪ£ļČĆĒä░ ĻĖ░ņ”Øļ░øņØĆ Ēł¼ļ¬ģĒĢ£ Ļ░üļ¦ēņØä ņØ┤ņŗØĒĢśļŖö ņłśņłĀņØ┤ļŗż.1 Ļ░üļ¦ēņØ┤ņŗØ ņĀä ĻĖ░ņ”ØĻ░üļ¦ēņØś ņāüĒā£ņŚÉ ļīĆĒĢ£ ņĀĢĒÖĢĒĢ£ ĒÅēĻ░ĆļŖö ņłśņłĀņØś ņśłĒøäņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö ņÜöņåī ņżæ Ļ░Ćņן ņżæņÜöĒĢ£ ņÜöņØĖņØ┤ļŗż. ĻĖ░ņĪ┤ņŚÉ ĻĖ░ņ”ØĻ░üļ¦ēņØĆ ĻĖ░ņ”Øņ×ÉņŚÉ ļīĆĒĢ£ ņ×äņāüņĀü ĻĖ░ņ┤ł ņĀĢļ│┤ņÖĆ Ļ░üļ¦ēļé┤Ēö╝ņäĖĒż ļ░Å Ļ░üļ¦ēļæÉĻ╗ś ņĖĪņĀĢ, ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ņØ┤ņŗØ ņĀüĒĢ®ņä▒ņØä ĒÅēĻ░ĆĒĢśņŚ¼ ņłśņłĀņØä ņŗ£Ē¢ēĒĢ┤ņÖöļŗż.2,3
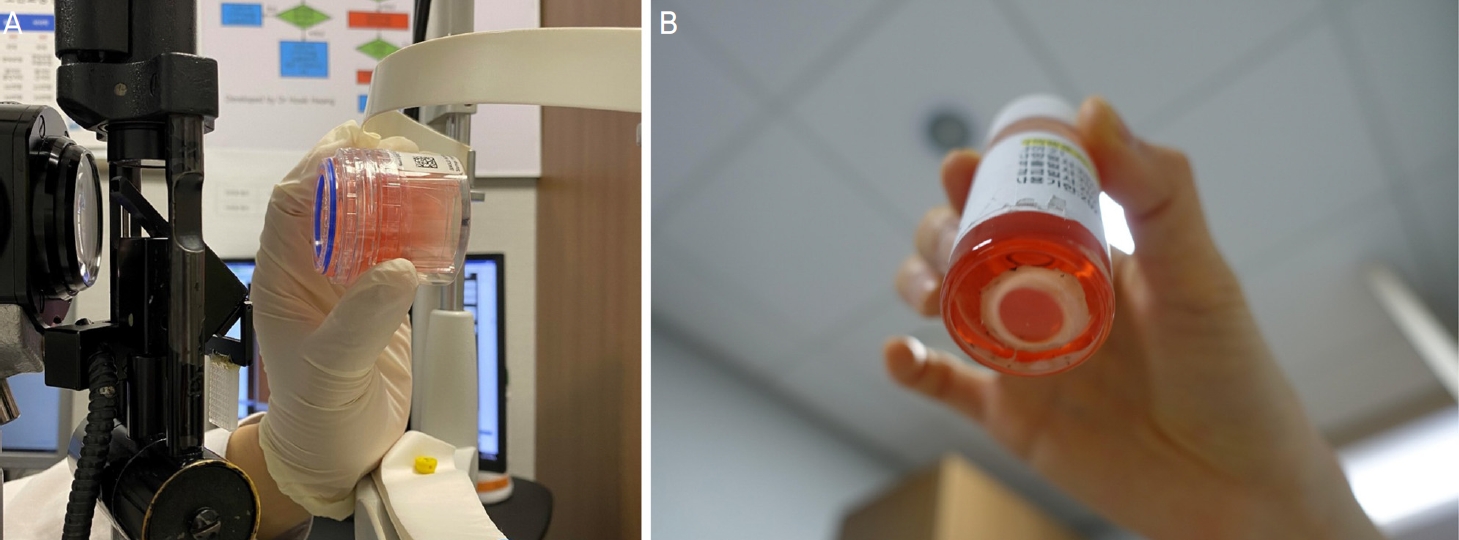
ņłśņ×ģ ĻĖ░ņ”ØĻ░üļ¦ēņØś Ļ▓ĮņÜ░ņŚÉļŖö Ļ░üļ¦ē ļ│┤ņĪ┤ņĢĪņØ┤ ļŗ┤Ļ▓©ņ׳ļŖö corneal viewing chamber (Krolman, Boston, MA, USA)ņŚÉ Ļ░üļ¦ēņĀłĒÄĖņØ┤ Ļ│ĀņĀĢļÉ£ ņāüĒā£ļĪ£ ļ│┤Ļ┤ĆņØ┤ ļÉśņ¢┤, ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØä ņØ┤ņÜ®ĒĢśņŚ¼ ĻĖ░ņ”ØĻ░üļ¦ēņØś ņĀäļ®┤ ļ░Å Ēøäļ®┤ņØä ļ│┤ļŗż ņÜ®ņØ┤ĒĢśĻ▓ī Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ļŗż(Fig. 1A).4 ĻĘĖļ¤¼ļéś ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņØś Ļ▓ĮņÜ░ Ļ░üļ¦ē ļ│┤ņĪ┤ņĢĪ(Optisol-GS, Bausch & Lomb Inc., Rochester, NY, USA)ņŚÉ ļ│äļÅäņØś Ļ│ĀņĀĢņןņ╣ś ņŚåņØ┤ ļŗ┤ĻĖ┤ ņāüĒā£ļĪ£ ļ│┤Ļ┤ĆĒĢśņŚ¼, Ļ░üļ¦ēņØ┤ Ļ│ĀņĀĢļÉśņ¢┤ ņ׳ņ¦ĆļŖö ņĢŖĻĖ░ ļĢīļ¼ĖņŚÉ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ Ļ┤Ćņ░░ņØ┤ ņ¢┤ļĀĄĻ│Ā, ļīĆņŗĀņŚÉ ļ│æņØä ļōżĻ│Ā Ļ░üļ¦ēņØä ņ£ĪņĢłņ£╝ļĪ£ļ░¢ņŚÉ Ļ┤Ćņ░░ĒĢĀ ņłś ņŚåļŗż(Fig. 1B).
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤ĻĖ┤ ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņØä ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ ņēĮĻ▓ī Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ļÅäļĪØ ĒĢ£ ņןņ╣śļź╝ ņĀĆņ×ÉļōżņØ┤ Ļ░£ļ░£ĒĢśņśĆņ£╝ļ®░, ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņØś ņØ┤ņŗØņłśņłĀ ņĀä Ļ▓Ćņé¼ ņŗ£ ņןņ╣śņØś ĒÜ©ņÜ®ņä▒ņØä ĒÅēĻ░ĆĒĢśņŚ¼ ņØ┤ļź╝ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
2023ļģä 2ņøöļČĆĒä░ 2023ļģä 3ņøöĻ╣īņ¦Ć ņŚ¼ņØśļÅäņä▒ļ¬©ļ│æņøÉņŚÉņä£ ĻĖ░ņ”Øļ░øļŖö ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ē 2ņĢłņØä ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆļŗż. ņ▓½ ļ▓łņ¦Ė ĻĖ░ņ”ØĻ░üļ¦ēņØĆ ĻĖ░ņĀĆ ņ¦łĒÖśņ£╝ļĪ£ Ļ│ĀĒśłņĢĢņØ┤ ņ׳ņ£╝ļ®░ ņĢłĻ│╝ņĀü ļ│æļĀźņØ┤ ņŚåļŖö 52ņäĖ ļćīņé¼ņ×ÉņØś Ļ░üļ¦ēņØ┤ļ®░, ļæÉ ļ▓łņ¦Ė ĻĖ░ņ”ØĻ░üļ¦ēņØĆ ļé┤Ļ│╝ņĀü, ņĢłĻ│╝ņĀü ļ│æļĀźņØ┤ ņŚåļŖö 21ņäĖņØś ņé¼Ēøä ĻĖ░ņ”ØĻ░üļ¦ēņØ┤ņŚłļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĒŚ¼ņŗ▒ĒéżņäĀņ¢Ė(Declaration of Helsinki)ņØä ņżĆņłśĒĢśņśĆņ£╝ļ®░, ņŚ¼ņØśļÅäņä▒ļ¬©ļ│æņøÉ ņ×äņāüņŚ░ĻĄ¼ņ£żļ”¼ņ£äņøÉĒÜī(Institutionary Review Board, IRB)ņØś ņŗ¼ņé¼ Ēøä ņŖ╣ņØĖņØä ļ░øņĢśļŗż(ņŖ╣ņØĖļ▓łĒśĖ: 2023-0384-0001). ņé¼ņĀäņŚÉ ņ¦üĻ│äĻ░ĆņĪ▒ņØś ņןĻĖ░ĻĖ░ņ”Ø ņä£ļ®┤ ļÅÖņØśĻ░Ć ņŗ£Ē¢ēļÉ£ ņ×ÉņŚÉ ļīĆĒĢśņŚ¼ ņĢłĻĄ¼ņĀüņČ£ņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, ĻĖ░ņ”Øļ░øļŖö ļ│æņøÉņØ┤ļéś ņןĻĖ░ĻĖ░ņ”Øņ×ÉļĪ£ļČĆĒä░ ĻĖ░ņ”Øņ×ÉņØś ņä▒ļ│ä/ļéśņØ┤, ņé¼ņØĖ ļ░Å ĻĖ░ņĀĆ ļ│æļĀź(ņĀäņŗĀ ļ░Å ņĢłĻ│╝ņĀü ļ│æļĀź), ņé¼ļ¦Øņŗ£Ļ░ü ļō▒ņØś ņĀĢļ│┤ļź╝ ņĀ£Ļ│Ąļ░øņĢśļŗż.
ļ©╝ņĀĆ ņĀüņČ£ļÉ£ ĻĖ░ņ”Øņ×É ņĢłĻĄ¼ļź╝ Ļ▒░ņ”łļĪ£ Ļ░Éņŗ╝ ņ▒ä ņåÉņ£╝ļĪ£ ļōżĻ│Ā ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņŚÉņä£ Ļ░üļ¦ēņāüĒö╝Ļ▓░ņåÉ, ĻĖ░ņ¦łļČĆņóģ ļ░Å ĻĖ░ņ¦łĒś╝Ēāü, ļģĖņØĖĒÖś, ļŹ░ņŖżļ®öļ¦ē ņŻ╝ļ”äĻ│╝ ĻĘĖ ņĀĢļÅäļź╝ ĒÅēĻ░ĆĒĢśņśĆļŗż. Ļ░üļ¦ē ļ▓äĒŖĖļŗØ(corneal buttoning) ņŗ£ Ļ░üļ¦ēņ£żļČĆļĪ£ļČĆĒä░ ņĢĮ 3 mm ļé©ļÅäļĪØ Ļ│Ąļ¦ēņØä ņלļØ╝ Ļ░üĻ│Ąļ¦ē ņØ┤ņŗØĒÄĖņØä ļ¦īļōżņŚłņ£╝ļ®░, Ļ░üļ¦ē ļ│┤ņĪ┤ņĢĪņØĖ Optisol-GS (Bausch & Lomb Inc.) ņÜ®ņĢĪņŚÉ Ļ░üļ¦ēļé┤Ēö╝Ļ░Ć ņ£äļĪ£ Ē¢źĒĢśļÅäļĪØ ļŗ┤ņĢä 4┬░C ļāēņן ņāüĒā£ļĪ£ ļ│┤Ļ┤ĆĒĢśņśĆļŗż. ĻĖ░ņ”ØĻ░üļ¦ēņØ┤ ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤ĻĖ┤ ņāüĒā£ņŚÉņä£ ņä£ņÜĖņä▒ļ¬©ļ│æņøÉ ņĢłņØĆĒ¢ēņŚÉ ņ׳ļŖö ĻĖ░ņ”ØĻ░üļ¦ēņÜ® Ļ▓Įļ®┤Ēśäļ»ĖĻ▓Į(Eye Bank Kerato Analyzer; EKA-10, Konan Medical Inc., Hyogo, Japan)ņ£╝ļĪ£ ļé┤Ēö╝ņäĖĒżļ░ĆļÅäņÖĆ Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢśņśĆļŗż.
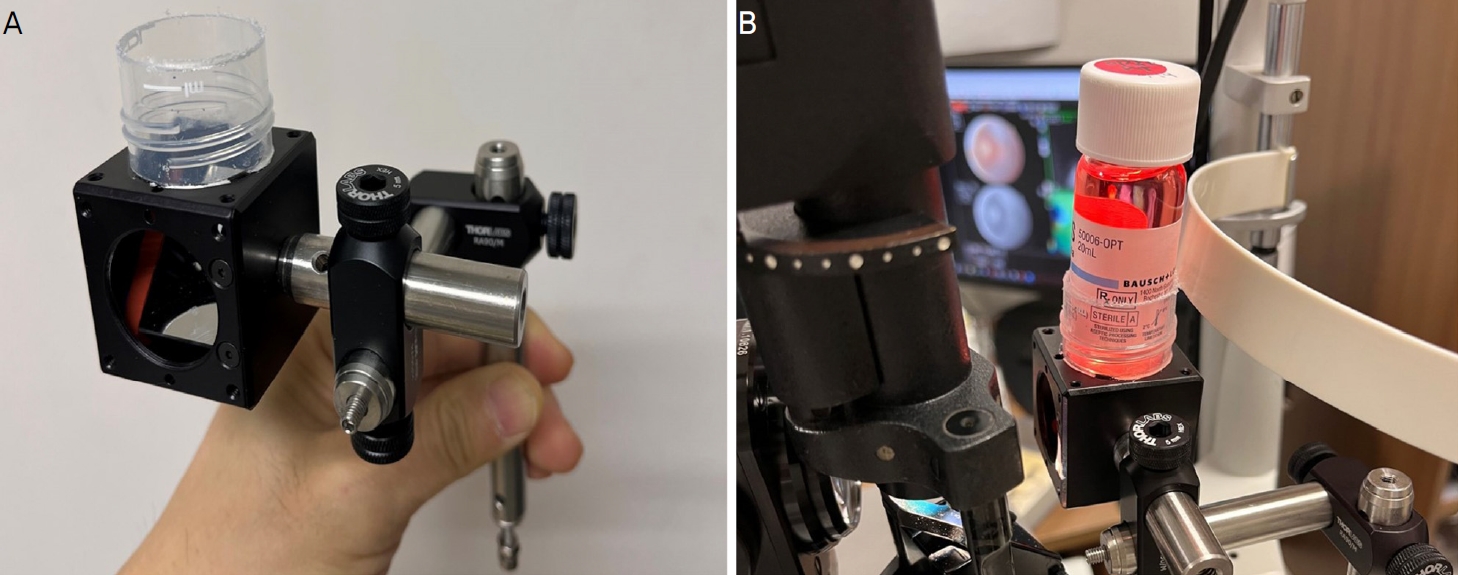
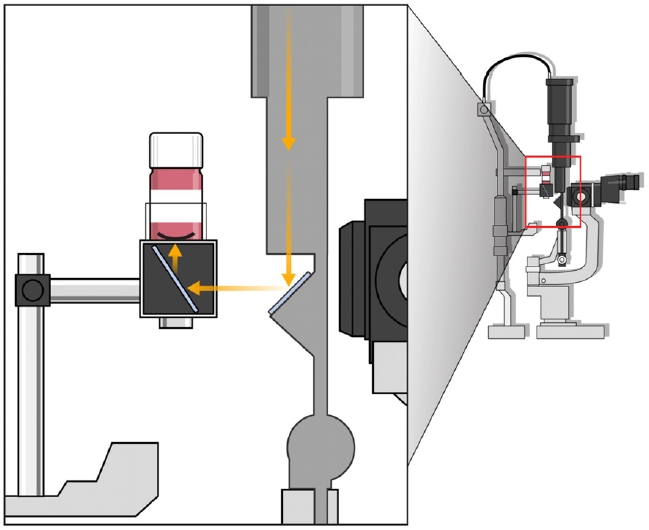
Ļ│ĀņĢłļÉ£ ņןņ╣śļŖö ņäĖ Ļ░Ćņ¦Ć ņŻ╝ņÜö ļČĆļČäņ£╝ļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņ׳ļŗż. ņ▓½ ļ▓łņ¦ĖļĪ£, ļ│┤ņĪ┤ņĢĪ ļ│æņØä Ļ│ĀņĀĢĒĢĀ ņłś ņ׳ļŖö ĒöīļØ╝ņŖżĒŗ▒ ĒÖĆļŹöĻ░Ć ņ׳ļŗż. ĒöīļØ╝ņŖżĒŗ▒ ĒÖĆļŹöļŖö ņ¦üĻ▓Į 30 mm, ĻĖĖņØ┤ 116 mmņØś ĒöīļØ╝ņŖżĒŗ▒ ņøÉņŗ¼Ļ┤Ć ĒŖ£ļĖī(SPL 50 mL conical tube, SPL Life Sciences, Pocheon, Korea)ņØś ņ£äņ¬Į 25 mmļź╝ ņלļØ╝ļé┤ņ¢┤ ņé¼ņÜ®ĒĢśņśĆļŗż. ĒÖĆļŹö ļ░öļĪ£ ņĢäļלņŚÉļŖö ļé┤ļČĆņŚÉ Ļ▒░ņÜĖņØ┤ ņןņ░®ļÉ£ ĒüÉļĖī(30 mm Cage Cube-Mounted UV-Enhanced Aluminum Turning Mirror; CCM1-F01/M, Thorlabs, Newton, NJ, USA)Ļ░Ć ņ׳ņ£╝ļ®░, ĒüÉļĖī ņĢäļלņ¬Įņ£╝ļĪ£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś Ēä▒ļ░øņ╣©ņŚÉ Ļ│ĀņĀĢĒĢĀ ņłś ņ׳ļŖö Ļ▒░ņ╣śļīĆĻ░Ć ņ׳ļŗż(Fig. 2A). Fig. 2BļŖö Ļ│ĀņĢłļÉ£ ņןņ╣śļź╝ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņŚÉ ņäżņ╣śĒĢ£ ļ¬©ņŖĄņØ┤ļŗż. Fig. 3ņØś ļ¬©ņŗØļÅäņŚÉņä£ņ▓śļ¤╝ Ļ│ĀņĢłļÉ£ ņןņ╣śņŚÉ ņ×ģņé¼ļÉ£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś ļ╣öņØĆ ĒüÉļĖī ļé┤ņØś Ļ▒░ņÜĖņŚÉ ņØśĒĢ┤ ļ░śņé¼ļÉśņ¢┤ ļ│┤ņĪ┤ņĢĪ ļé┤ņØś Ļ░üļ¦ēņŚÉ ņ×ģņé¼ĒĢ£ļŗż. ņØ┤ļź╝ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ļŗż.
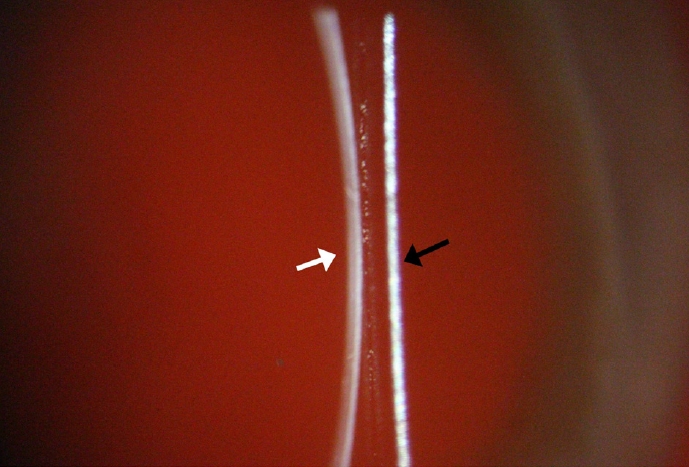
ļ©╝ņĀĆ, Ļ░üļ¦ēņØś ļé┤Ēö╝Ļ░Ć ļ│┤ņĪ┤ņĢĪ ļ│æņØś ņ£äņ¬Įņ£╝ļĪ£ Ē¢źĒĢśļÅäļĪØ ĒĢ£ ļŗżņØī ļ│┤ņĪ┤ņĢĪ ļ│æņØä Ļ│ĀņĢłļÉ£ ņןņ╣śņØś ĒöīļØ╝ņŖżĒŗ▒ ĒÖĆļŹöņŚÉ ņןņ░®ĒĢśļ®┤, Ļ▓Ćņé¼ņ×ÉļŖö ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś ņŖ¼ļ”┐ļ╣öņØś Ļ░üļÅäļź╝ ņĪ░ņĀłĒĢśĻ│Ā ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØä ņĢ×ļÆżļĪ£ ņøĆņ¦üņŚ¼ņä£ Ļ░üļ¦ēņŚÉ ņ┤łņĀÉņØä ļ¦×ņČś ļÆż, ņĀäņĢłļČĆ ņé¼ņ¦äņØä ņ┤¼ņśüĒĢśņśĆļŗż. ņäĖĻĘ╣ļō▒ņØś ļäōņØĆ ļ╣öņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļ│æņØä 360┬░ ļÅīļĀżĻ░Ćļ®┤ņä£ Ļ│Ąļ¦ē ļ│ĆņŚ░ļČĆļź╝ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Į ļ╣öņØś ļäłļ╣äļź╝ ņżäņŚ¼ņä£ Ļ░üļ¦ēņØś ļæÉĻ╗śļź╝ ĒÖĢņØĖĒĢśņśĆļŗż. ņ×ģņé¼Ļ░üņØä Ļ▒░ņØś 0┬░ļĪ£ ĒĢśļ®┤ Ļ░üļ¦ēņØä Ēł¼Ļ│╝ĒĢ£ ļ╣øņØĆ ļ│┤ņĪ┤ņĢĪ ļ│æņØś ĒØ░ņāē ļÜ£Ļ╗æņŚÉņä£ ļ░śņé¼ĒĢśņŚ¼ ņŚŁņĪ░ļ¬ģļ▓ĢĻ│╝ Ļ░ÖņØĆ ĒÜ©Ļ│╝ļź╝ Ļ░¢Ļ▓ī ļÉ£ļŗż. ņØ┤ļź╝ ĒåĄĒĢ┤ Ļ░üļ¦ēņāüĒö╝ņäĖĒżļź╝ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ļŹ░ņŖżļ®öļ¦ē ņŻ╝ļ”äņØ┤ ņ׳ļŖö ļČĆļČäņŚÉ ļīĆĒĢ┤ņä£ Ļ▓Įļ®┤ļ░śņé¼ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļé┤Ēö╝ņäĖĒżļź╝ ņ┤¼ņśüĒĢśņśĆļŗż.
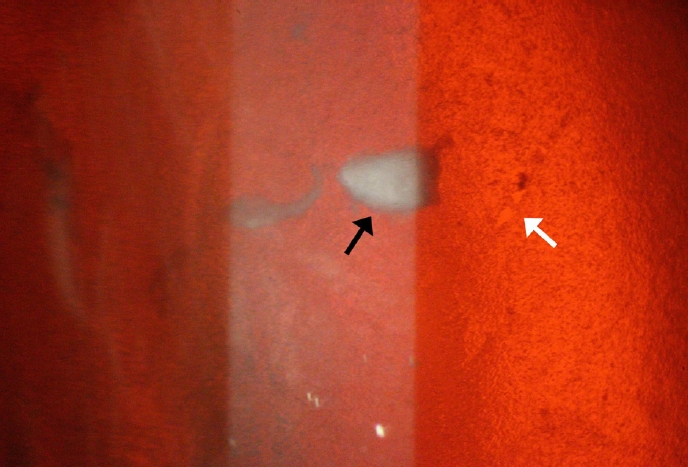
ļŗżņØīņ£╝ļĪ£, Ļ░üļ¦ēņØś ļé┤Ēö╝Ļ░Ć ļ│┤ņĪ┤ņĢĪ ļ│æņØś ļ░öļŗź ņ¬Įņ£╝ļĪ£ Ē¢źĒĢśļÅäļĪØ ĒĢ£ ļŗżņØī ļ│æņØä ņןņ╣śņŚÉ Ļ│ĀņĀĢĒĢ£ ņāüĒā£ņŚÉņä£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ ĒżļÅäļ¦ē ņĪ░ņ¦üņØ┤ ņל ļ░Ģļ”¼ļÉśņŚłļŖöņ¦Ć ĒÖĢņØĖĒĢśĻ│Ā, Ļ▓Įļ®┤ļ░śņé¼ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļé┤Ēö╝ņäĖĒżļź╝ Ļ┤Ćņ░░ĒĢśņśĆļŗż.
Ļ│ĀņĢłļÉ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŚ¼ņØśļÅäņä▒ļ¬©ļ│æņøÉņŚÉņä£ ĒåĄņāüņĀüņØĖ ņ¦äļŻīņŚÉ ņé¼ņÜ®ļÉśļŖö Ļ▓Įļ®┤Ēśäļ»ĖĻ▓Į(CellChek 20 Specular Microscope, Konan Medical, Irvine, CA, USA)ņØä ĒåĄĒĢ£ ĻĖ░ņ”ØĻ░üļ¦ēņØś ļé┤Ēö╝ņäĖĒż ņ┤¼ņśüņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░, ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼(Topcon DRI OCT Triton Swept source OCT, Topcon, Tokyo, Japan)ļź╝ ņŗżņŗ£ĒĢśņŚ¼ Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢ┤ ļ│┤ņĢśļŗż(Fig. 4).
Ļ▓░ Ļ│╝
ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼
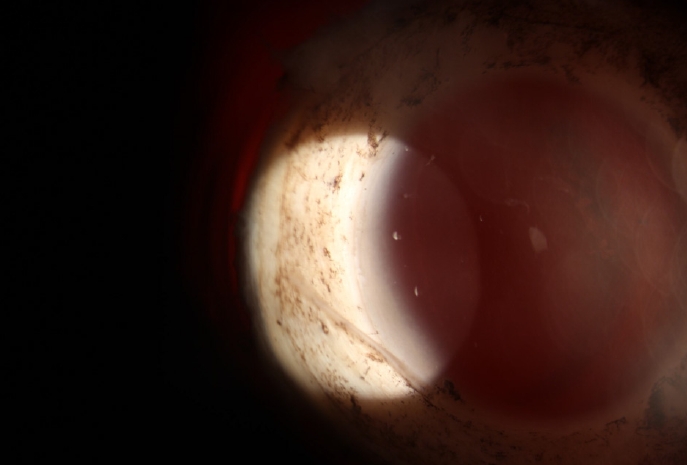
Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżĻ░Ć ņ£äļź╝ Ē¢źĒĢśļÅäļĪØ ĒĢ£ ņāüĒā£ņŚÉņä£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś ļäōņØĆ ļ╣öņ£╝ļĪ£ ĻĖ░ņ”ØĻ░üļ¦ēņØś Ļ░Ćņןņ×Éļ”¼ļź╝ ĒÖĢņØĖĒĢśņśĆļŗż. 52ņäĖ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉņä£ ļé©ņĢäņ׳ļŖö Ļ│Ąļ¦ēņØś ĒÅŁņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłņ£╝ļ®░ Ļ▓░ļ¦ē ļ░Ģļ”¼Ļ░Ć ļČłņÖäņĀäĒĢśļŗżļŖö Ļ▓āņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 5). ĻĄ░ļéĀĻ░£ļéś ļģĖņØĖĒÖś ļō▒ņØś Ļ░üļ¦ē ņŻ╝ļ│ĆļČĆ ļ│æļ│ĆņØ┤ ņŚåļŗżļŖö Ļ▓āļÅä ņĢī ņłś ņ׳ņŚłļŗż. ļ│┤ņĪ┤ņĢĪ ļ│æņØä 360┬░ ļÅīļ”¼ļ®┤ ĻĖ░ņ”ØĻ░üļ¦ēņØś Ļ│Ąļ¦ē ļ│ĆņŚ░ļČĆņØś ĒÅŁĻ│╝ Ļ▓░ļ¦ē ļ░Ģļ”¼ ņāüĒā£ļź╝ 360┬░ ņĀäņ▓┤ņĀüņ£╝ļĪ£ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Supplementary Video 1). ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś ņ¢ćņØĆ ļ╣öņ£╝ļĪ£ ņĀĆļ░░ņ£© ļ░Å Ļ│Āļ░░ņ£©ņØś Ļ░üļ¦ē ļŗ©ļ®┤ ņØ┤ļ»Ėņ¦Ćļź╝ ņ¢╗ņ¢┤, Ļ░üļ¦ēņŗżņ¦łņØś ņĀäļ░śņĀüņØĖ Ēł¼ļ¬ģļÅä, ļīĆļץņĀüņØĖ Ļ░üļ¦ēņØś ļæÉĻ╗śļź╝ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 6).
21ņäĖ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉņä£ ņŚŁņĪ░ļ¬ģļ▓ĢņØä ņØ┤ņÜ®ĒĢśņśĆņØä ļĢī ļé┤Ēö╝ņäĖĒżņĖĄņØĆ Ļ┤Ćņ░░ĒĢĀ ņłś ņŚåņŚłĻ│Ā, ņāüĒö╝ņŚÉ ļČÖņ¢┤ņ׳ļŖö Ļ│Ąļ¦ēņĪ░Ļ░üĻ│╝ ņāüĒö╝ņäĖĒżĻ░Ć ņś©ņĀäĒĢśĻ▓ī ļČÖņ¢┤ņ׳ņ¦Ć ņĢŖņĢä ļČłĻĘĀņ¦łĒĢśĻ▓ī ļ│┤ņØ┤ļŖö ļČĆļČäņŚÉņä£ Ļ░üļ¦ēņāüĒö╝ņØś Ļ▓░ņåÉņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 7). Ļ▓Įļ®┤ļ░śņé¼ļ▓ĢņŚÉņä£ļŖö ļŹ░ņŖżļ®öļ¦ē ņŻ╝ļ”äņØ┤ ņ׳ļŖö ļČĆņ£äņŚÉņä£ļŖö Ļ░ĢĒĢ£ ļ░śņé¼ ļÆżļĪ£ ļé┤Ēö╝ņäĖĒżņĖĄņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 8, Supplementary Video 2).
21ņäĖ ĻĖ░ņ”ØĻ░üļ¦ēņØś ļé┤Ēö╝Ļ░Ć ļ│æņØś ļ░öļŗź ņ¬Įņ£╝ļĪ£ Ē¢źĒĢśļÅäļĪØ ļåōņŚ¼ņ׳ļŖö ņāüĒā£ņŚÉņä£ļŖö ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś ļäōņØĆ ļ╣öņ£╝ļĪ£ Ļ░üĻ│Ąļ¦ē ņĀłĒÄĖņŚÉ ĒżļÅäļ¦ē ņĪ░ņ¦üņØ┤ ņל ļ░Ģļ”¼ļÉśņ¢┤ ņ׳ņØīņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 9). ĻĘĖļ”¼Ļ│Ā Ļ▓Įļ®┤ļ░śņé¼ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļé┤Ēö╝ņäĖĒżņĖĄņØä Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 10).
Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼(specular microscopy)
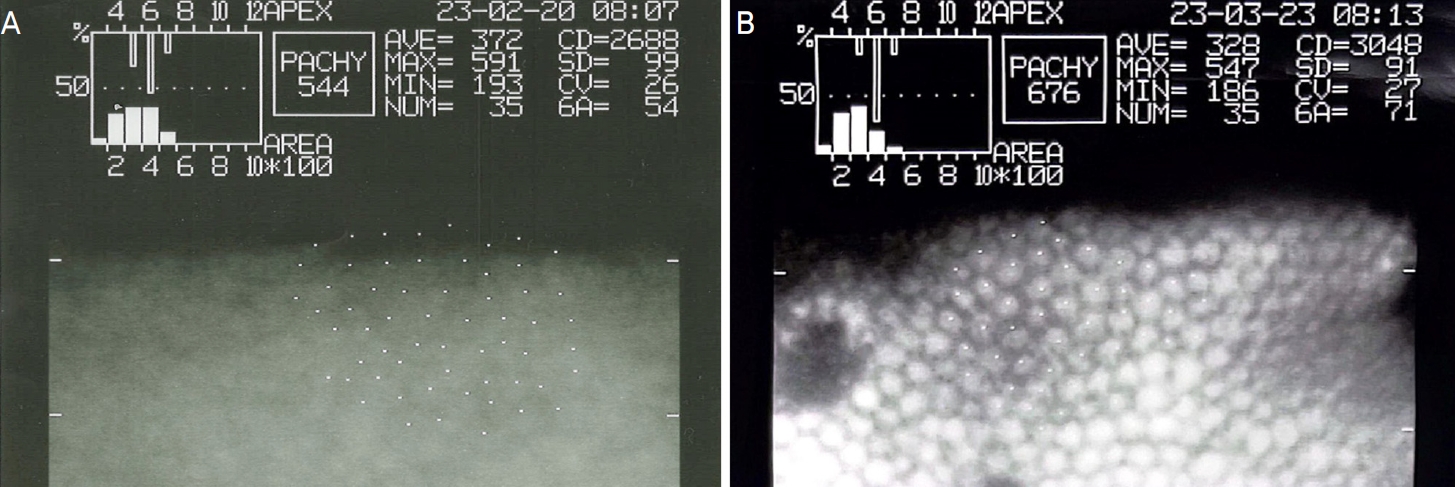
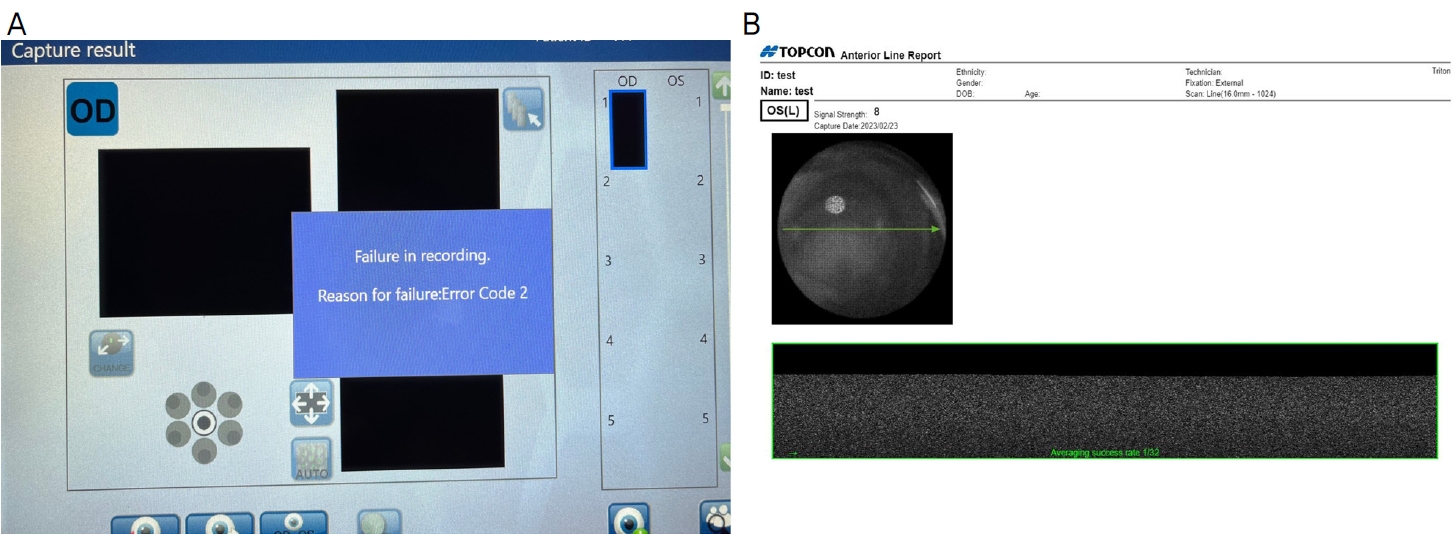
ņä£ņÜĖņä▒ļ¬©ļ│æņøÉ ņĢłņØĆĒ¢ēņŚÉņä£ ĻĖ░ņ”ØĻ░üļ¦ēņØś Ļ▓Ćņé¼ņŚÉ ņé¼ņÜ®ļÉśļŖö ĻĖ░ņ”ØĻ░üļ¦ēņÜ® Ļ▓Įļ®┤Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤Ļ▓©ņ׳ļŖö ļÅÖņØ╝ĒĢ£ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ļīĆĒĢśņŚ¼ ĻĖ░ņ”ØĻ░üļ¦ē 2ņĢł ļ¬©ļæÉņŚÉņä£ ļé┤Ēö╝ņäĖĒż ņ┤¼ņśüņØ┤ Ļ░ĆļŖźĒĢśņśĆņ£╝ļ®░, ļé┤Ēö╝ņäĖĒżņØś ļ░ĆļÅäņÖĆ ņäĖĒż ļ®┤ņĀüņØś ļ│ĆņØ┤Ļ│äņłś, ņäĖĒż ļ¬©ņ¢æņØś ļŗżĒśĢņä▒ ļō▒ņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. 52ņäĖ ĻĖ░ņ”ØĻ░üļ¦ēņØś Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļ░ĆļÅäļŖö 2,688/mm2 , 21ņäĖ ĻĖ░ņ”ØĻ░üļ¦ēņØś Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļ░ĆļÅäļŖö 3,048/mm2 ļĪ£ ņĖĪņĀĢļÉśņŚłļŗż(Fig. 11). ļ░śļ®┤, ņĀĆņ×ÉļōżņØ┤ Ļ│ĀņĢłĒĢ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŗ£Ē¢ēĒĢ£ ĒÖśņ×ÉņÜ® ļ╣äņĀæņ┤ēņŗØ Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņŚÉņä£ļŖö ĻĖ░ņ”ØĻ░üļ¦ē 2ņĢł ļ¬©ļæÉņŚÉņä£ ļé┤Ēö╝ņäĖĒż ņ┤¼ņśüņØ┤ ļČłĻ░ĆļŖźĒĢśņśĆļŗż(Fig. 12A).
ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼(anterior segment optical coherence tomography [OCT])
Ļ│ĀņĢłļÉ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ņŗ£Ē¢ēĒĢ£ ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼ņŚÉņä£ļÅä Ļ░üļ¦ēņØ┤ ņŗØļ│äļÉśņ¦Ć ņĢŖņĢä ĻĖ░ņ”ØĻ░üļ¦ē 2ņĢł ļ¬©ļæÉņŚÉņä£ Ļ░üļ¦ē ļŗ©ņĖĄņŚÉ ļīĆĒĢ£ ņ┤¼ņśüņØ┤ ļČłĻ░ĆļŖźĒĢśņśĆļŗż(Fig. 12B).
Ļ│Ā ņ░░
ņĢłņØĆĒ¢ēņŚÉņä£ļŖö ņłśņłĀ ņĀä ĻĖ░ņ”ØĻ░üļ¦ēņØś ņāüĒā£ļź╝ ĒīīņĢģĒĢśĻĖ░ ņ£äĒĢ┤ņä£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼, Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼, Ļ░üļ¦ēļæÉĻ╗ś ņĖĪņĀĢ ļō▒ņØä Ļ▓Ćņé¼ĒĢśĻ│Ā ņ׳ļŗż. ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļĪ£ļŖö Ļ░üļ¦ēņØś Ēś╝Ēāü ļ░Å ļČĆņóģ, ĻĖ░ņ¦łņ╣©ņ£ż, ņāüĒö╝Ļ▓░ņåÉ, ņŗĀņāØĒśłĻ┤Ć, ņØĄņāüĒÄĖ ļō▒ņØś ņĀäļ░śņĀüņØĖ Ļ░üļ¦ē ļ│æļ”¼ ņåīĻ▓¼ņŚÉ ļīĆĒĢ┤ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņ£╝ļ®░,5 Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļŖö ņØ┤ņŗØ Ļ░üļ¦ēņØś ņāØņĪ┤ņŚÉ Ļ░Ćņן ņżæņÜöĒĢ£ Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżņØś ĒśĢĒā£ņÖĆ ļ░ĆļÅäļź╝ ņĖĪņĀĢĒĢśļŖö ļŹ░ ĒĢäņłśņĀüņØĖ Ļ▓Ćņé¼ņØ┤ļŗż.6 ļśÉĒĢ£, Ļ░üļ¦ēļæÉĻ╗śļŖö Ļ░üļ¦ēļČĆņóģņØś ņŚ¼ļČĆļź╝ ĒīīņĢģĒĢśĻ│Ā Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżņØś ĻĖ░ļŖźņØä Ļ░äņĀæņĀüņ£╝ļĪ£ ņĢī ņłś ņ׳ļÅäļĪØ ĒĢśļŖö ņżæņÜöĒĢ£ Ļ▓Ćņé¼ņØ┤ļŗż.7
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤ĻĖ┤ ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ļīĆĒĢśņŚ¼ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśĻĖ░ ņ¢┤ļĀżņøĀļŹś ĒĢ£Ļ│äņĀÉņØä ĻĘ╣ļ│ĄĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ĻĖ░ņ”ØĻ░üļ¦ēĻ▓Ćņé¼ņÜ® ņןņ╣śļź╝ Ļ░£ļ░£ĒĢśņśĆņ£╝ļ®░, ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ē 2ņĢłņØä ļīĆņāüņ£╝ļĪ£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ Ļ│ĀņĢłļÉ£ ņןņ╣śņØś ņä▒ļŖźņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. ĻĖ░ņ”ØĻ░üļ¦ēņØ┤ ļŗ┤Ļ▓©ņ׳ļŖö ļ│┤ņĪ┤ņĢĪ ļ│æņØä ņןņ╣śņŚÉ Ļ│ĀņĀĢĒĢ£ ņāüĒā£ņŚÉņä£ ļ│æņØä ņ▓£ņ▓£Ē׳ ĒÜīņĀäņŗ£ņ╝£ Ļ│Ąļ¦ē ļ│ĆņŚ░ļČĆņÖĆ Ļ░üļ¦ēņ£żļČĆļź╝ 360┬░ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłļŗż. ļäōņØĆ ļ╣öņ£╝ļĪ£ ĻĖ░ņ”ØĻ░üļ¦ēņØä ņĀäļ░śņĀüņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśņŚ¼ Ļ▓░ļ¦ēĻ│╝ ĒżļÅäļ¦ē ņĪ░ņ¦üņØś ļ░Ģļ”¼Ļ░Ć ņל ļÉśņ¢┤ ņ׳ļŖöņ¦Ć ĒÖĢņØĖĒĢśĻ│Ā, ņóüņØĆ ļ╣öņ£╝ļĪ£ļŖö Ļ░üļ¦ē ļŗ©ļ®┤ņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. ņŚŁņĪ░ļ¬ģļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ Ļ░üļ¦ēņāüĒö╝ņäĖĒżļź╝ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłņ£╝ļ®░, Ļ▓Įļ®┤ļ░śņé¼ļ▓ĢņØä ĒåĄĒĢ┤ ļé┤Ēö╝ņäĖĒżņĖĄņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż.
ĻĖ░ņ”ØĻ░üļ¦ēņØś ļé┤Ēö╝ņäĖĒż ņāüĒā£ļŖö Ļ░üļ¦ēņØ┤ņŗØņłśņłĀņØś ņśłĒøäņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö Ļ░Ćņן ņżæņÜöĒĢ£ ņÜöņØĖ ņżæ ĒĢśļéśļĪ£ ņłĀ ņĀä ļé┤Ēö╝ņäĖĒżņØś ĒśĢĒā£ņÖĆ ļ░ĆļÅäĻ░Ć ņżæņÜöĒĢśļŗż.8 ņłśņ×ģ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśļŖö Ļ▓ĮņÜ░ņŚÉļŖö Ļ░üļ¦ēņØ┤ ļŗ┤ĻĖ┤ corneal viewing chamberļź╝ ņĢ×ļÆżļĪ£ ļÅīļĀżĻ░Ćļ®░ Ļ░üļ¦ēņØś ļé┤Ēö╝ļ®┤Ļ│╝ ņāüĒö╝ļ®┤ņØä ņŚ¼ļ¤¼ Ļ░üļÅäņŚÉņä£ ļÅÖņØ╝ĒĢśĻ▓ī ņל Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ Ļ│ĀņĢłļÉ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ Ļ▓Ćņé¼ļź╝ ņ¦äĒ¢ēĒĢśļŖö Ļ▓ĮņÜ░ Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļź╝ ņ£äļĪ£ Ē¢źĒĢśļÅäļĪØ ĒĢśĻ│Ā Ļ┤Ćņ░░ĒĢśņśĆņØä ļĢīļŖö ļŹ░ņŖżļ®öļ¦ē ņŻ╝ļ”äņØ┤ ņ׳ņ¢┤ ĻĄ┤Ļ│Īņ¦ä ļČĆļČäņŚÉņä£ļŖö Ļ▓Įļ®┤ļ░śņé¼ļ▓ĢņŚÉ ņØśĒĢ┤ Ļ░üļ¦ēņŗżņ¦ł ļÆżņØś ļé┤Ēö╝ņäĖĒżņĖĄņØä ļČĆļČäņĀüņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłļŗż. ļ░śļ®┤, Ļ░üļ¦ēļé┤Ēö╝Ļ░Ć ņĢäļלļĪ£ Ē¢źĒĢśļÅäļĪØ ĒĢśĻ│Ā Ļ┤Ćņ░░ĒĢśņśĆņØä ļĢīļŖö ļé┤Ēö╝ņäĖĒżņĖĄņØä ņ¦üņĀæ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłļŗż.
ņØ┤ļ▓łņŚÉ Ļ░£ļ░£ĒĢ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļé┤Ēö╝ņäĖĒżļ░ĆļÅäļź╝ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŗżļ®┤ Ļ░Ćņן ņØ┤ņāüņĀüņØ╝ Ļ▓āņØ┤ļŗż. ĻĘĖļ¤¼ļéś ĻĖ░ņ”ØĻ░üļ¦ēņÜ® Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮņØä ņØ┤ņÜ®ĒĢśļ®┤ ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ņ׳ļŖö ĻĖ░ņ”ØĻ░üļ¦ēņØś ļé┤Ēö╝ņäĖĒż ļ░ĆļÅäņÖĆ ĒśĢĒā£ļź╝ ņĖĪņĀĢĒĢĀ ņłś ņ׳ņŚłļŹś Ļ▓āņŚÉ ļ░śĒĢ┤, Ļ│ĀņĢłļÉ£ ņןņ╣śņŚÉ ļ│┤ņĪ┤ņĢĪ ļ│æņØä ņןņ░®ĒĢ£ ņāüĒā£ņŚÉņä£ ĒÖśņ×ÉņÜ® ņØ╝ļ░ś Ļ▓Įļ®┤Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆņØä ņŗ£ņŚÉļŖö ļé┤Ēö╝ņäĖĒżļź╝ ņĖĪņĀĢĒĢĀ ņłś ņŚåņŚłļŗż. ļ╣äņĀæņ┤ē Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮņØś ņ×æļÅÖ ņøÉļ”¼ļŖö Ļ░üļ¦ēņØś ņ×ģņé¼ļÉ£ ļ╣øņØś 0.02%Ļ░Ć ļé┤Ēö╝ņäĖĒżņĖĄņŚÉņä£ ļ░śņé¼ļÉśļŖöļŹ░ ņØ┤ļź╝ ņ┤¼ņśüĒĢśļŖö Ļ▓āņØ┤ļŗż.9 ņĢäļ¦łļÅä, ņØ┤ļ▓ł ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢĀ ļĢīļŖö Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮņØś ļ╣øņØ┤ ņןņ╣śņØś Ļ▒░ņÜĖņŚÉ ļ░śņé¼ļÉśņ¢┤ Ļ░üļ¦ēņ£╝ļĪ£ ņ×ģņé¼ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ļ╣øņØś ņ×æļÅÖ Ļ▓ĮļĪ£Ļ░Ć ļäłļ¼┤ ĻĖĖņ¢┤ņ¦Ćļ®┤ņä£ ļ░śņé¼ĒĢ£ ļ╣øņØä Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮņØ┤ ņØĖņŗØĒĢśņ¦Ć ļ¬╗ĒĢśņśĆĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ĻĖ░ņ”ØĻ░üļ¦ēņØś ļæÉĻ╗ś ņĖĪņĀĢņØĆ Ļ░üļ¦ēņØś ņØ┤ņŗØ Ļ░ĆļŖźņä▒ ļ░Å Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżņØś ĻĖ░ļŖźņØä Ļ░äņĀæņĀüņ£╝ļĪ£ ĒÖĢņØĖĒĢśļŖö ļŹ░ Ļ╝Ł ĒĢäņÜöĒĢśļŗż. ĻĖ░ņ”ØĻ░üļ¦ēņØś ļæÉĻ╗ś ņĖĪņĀĢņØĆ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Į, ņ┤łņØīĒīī ļśÉļŖö ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņ£╝ļĪ£ Ļ░ĆļŖźĒĢśļŗż. ĻĖ░ņ”ØĻ░üļ¦ēņØ┤ ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤ĻĖ┤ Ļ▓ĮņÜ░ņŚÉļŖö ņ┤łņØīĒīīļŖö ņé¼ņÜ®ĒĢĀ ņłś ņŚåļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ Ļ│ĀņĢłĒĢ£ ņןņ╣śņŚÉ ļ│┤ņĪ┤ņĢĪ ļ│æņØä Ļ│ĀņĀĢĒĢśĻ│Ā ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśņśĆņØä ļĢīļŖö ņĀĢņä▒ņĀüņ£╝ļĪ£ Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĢī ņłś ņ׳ņŚłļŗż. ļ¦īņĢĮ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØ┤ Ļ░ĆļŖźĒĢśņśĆļŗżļ®┤ Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĀĢļ¤ēņĀüņ£╝ļĪ£ ņĖĪņĀĢĒĢĀ ņłś ņ׳ņŚłņØä ĒģÉļŹ░ ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤ĻĖ┤ ĻĖ░ņ”ØĻ░üļ¦ē ņ┤¼ņśüņØĆ ņŗżĒī©ĒĢśņśĆļŗż. Ļ│ĀņĢłļÉ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśü Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆņØä ļĢī Ļ░üļ¦ēņØ┤ ņØĖņŗØļÉśņ¦Ć ņĢŖņĢśļŖöļŹ░, Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņÖĆ ļ¦łņ░¼Ļ░Ćņ¦ĆļĪ£ ļ╣øņØś ņ×æļÅÖ Ļ▓ĮļĪ£Ļ░Ć ĻĖĖņ¢┤ņĀĖņä£ ņĖĪņĀĢņŚÉ ņĀ£ĒĢ£ņØ┤ ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ņĀĆņ×ÉļōżņØĆ ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤ĻĖ┤ ĻĖ░ņ”ØĻ░üļ¦ēņØä ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ ņ┤¼ņśüĒĢ£ ņĀäņĢłļČĆ ņØ┤ļ»Ėņ¦Ćļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĀĢļ¤ēņĀüņ£╝ļĪ£ ņĖĪņĀĢĒĢśĻĖ░ ņ£äĒĢ£ ņŗ£ļÅäļź╝ ĒĢśņśĆļŗż. ļ│┤ņĪ┤ņĢĪ ļ│æ ļ░öļŗźņØś ļæÉĻ╗śļŖö ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼(Topcon DRI OCT Triton Swept source OCT, Topcon)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░, ļśÉĒĢ£ ļ│┤ņĪ┤ņĢĪ ļ│æņØä ĒīīņåÉņŗ£ņ╝£ ļ░öļŗźņØś ņŗżņĀ£ ļæÉĻ╗śļź╝ ļ▓äļŗłņ¢┤ ņ║śļ”¼ĒŹ╝ņŖżļĪ£ ļŗżņŗ£ ņĖĪņĀĢĒĢśņśĆļŗż. ĻĘĖ Ļ▓░Ļ│╝ ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢ£ ļ│┤ņĪ┤ņĢĪ ļ│æ ļ░öļŗźņØś ļæÉĻ╗śļŖö 953 ┬ĄmņśĆņ£╝ļ®░, ļ▓äļŗłņ¢┤ ņ║śļ”¼ĒŹ╝ņŖżļĪ£ ņĖĪņĀĢĒĢśņśĆ ļĢīļŖö 0.95 mm (950 ┬Ąm)ņśĆļŗż. ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Į ņ┤¼ņśü ņé¼ņ¦äņŚÉņä£ Ļ░üļ¦ē ļŗ©ļ®┤ņØś ļæÉĻ╗śņÖĆ ļ│┤ņĪ┤ņĢĪ ļ│æ ļ░öļŗźņØś ļŗ©ļ®┤ņØś ļæÉĻ╗śļź╝ Image J (NIH, Washington, USA)ļĪ£ ĒöĮņģĆ ņłśļĪ£ ņĖĪņĀĢĒĢśņŚ¼ ļ╣äļĪĆņŗØņØä ņØ┤ņÜ®ĒĢśņŚ¼ Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢśņśĆļŗż. ņØ┤ļĀćĻ▓ī ņĖĪņĀĢĒĢ£ 52ņäĖ ĻĖ░ņ”ØĻ░üļ¦ēņØś ļæÉĻ╗śļŖö 1,137.5 ┬ĄmļĪ£, ĻĖ░ņ”ØĻ░üļ¦ē Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņŚÉņä£ ņĖĪņĀĢļÉ£ ĻĖ░ņ”ØĻ░üļ¦ēņØś ļæÉĻ╗śņØĖ 544 ┬Ąmļ│┤ļŗż ņ¦Ćļéśņ╣śĻ▓ī Ēü░ Ļ░ÆņØä ļ│┤ņśĆļŗż. ņØ┤ļŖö ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś ļ╣öņØĆ ĒÅēĒ¢ēĻ┤æņäĀņØ┤ ņĢäļŗłļØ╝ ļ╣öņØ┤ ļ¬©ņśĆļŗżĻ░Ć ĒÄ┤ņ¦ĆļŖö ļ¬©ņ¢æņ£╝ļĪ£, ļ│┤ņĪ┤ņĢĪ ļ│æ ļ░öļŗźņŚÉ ļ╣öņØ┤ ņ┤łņĀÉņØä ļ¦║ņ£╝ļ®┤ ļ│┤ņĪ┤ņĢĪ ļ│æ ļ░öļŗźĻ│╝ Ļ▒░ļ”¼Ļ░Ć ļ¢©ņ¢┤ņĀĖ ņ׳ļŖö Ļ░üļ¦ēņŚÉņä£ļŖö Ēø©ņö¼ ĒŹ╝ņĀĖ ņ׳ļŖö ļ╣öņØ┤ ņ¦ĆļéśĻ░ĆĻĖ░ ļĢīļ¼ĖņØ┤ļ®░, ņØ┤ļ¤¼ĒĢ£ ļ░®ļ▓Ģņ£╝ļĪ£ļŖö ņĀĢļ¤ēņĀüņ£╝ļĪ£ ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢśļŖö Ļ▓āņØĆ ļČłĻ░ĆļŖźĒĢśļŗż. ļŗżļźĖ ļ░®ļ▓Ģņ£╝ļĪ£ļŖö ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗ś ņĖĪņĀĢņØä ņ£äĒĢ┤ņä£ Scheimpflug ņ╣┤ļ®öļØ╝ ļ░®ņŗØņØś Ļ░üļ¦ēņ¦ĆĒśĢļÅä Ļ▓Ćņé¼Ļ│ä(Pentacam [Oculus, Wetzlar, Germany], Galilei dual Scheimpflug system [Ziemer Ophthalmic Systems AG, Port, Switzerland])ļź╝ ņØ┤ņÜ®ĒĢ┤ļ│╝ ņłśļÅä ņ׳ļŗż. ņØ┤ļŖö ņČöĒøä ņŚ░ĻĄ¼ņŚÉņä£ ņŗ£ļÅäĒĢ┤ļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
ņØ┤ņĀäņŚÉļÅä ĒĢ┤ņÖĖņŚÉņä£ļŖö Ļ░üļ¦ē ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ĻĖ░ņ”ØĻ░üļ¦ēņØ┤ ļŗ┤ĻĖ┤ ņāüĒā£ļĪ£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņŚÉ Ļ│ĀņĀĢĒĢśņŚ¼ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢĀ ņłś ņ׳ļŖö ņןņ╣śĻ░Ć Ļ░£ļ░£ļÉ£ ņĀüņØ┤ ņ׳ļŗż.10 ĻĘĖĻ░Ć Ļ░£ļ░£ĒĢ£ ņןņ╣śļŖö ļ│┤ņĪ┤ņĢĪ ļ│æņØä ļü╝ņøī ļäŻņØä ņłś ņ׳ļŖö ļ¦üņØ┤ ļŗ¼ļĀżņ׳ļŖö ĒÖ®ļÅÖ ļ¦ēļīĆņÖĆ ņłśņ¦ü ļ░Å ĒÜīņĀäņØä Ļ░ĆļŖźĒĢśĻ▓ī ĒĢśļŖö Ēü┤ļשĒöä ļ░Å ļéśļ╣äļéśņé¼ ĻĘĖļ”¼Ļ│Ā 45┬░ Ļ░üļÅäļĪ£ ļČĆņ░®ļÉ£ Ļ▒░ņÜĖļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņ׳ļŗż. Ļ▒░ņÜĖņŚÉ ļ░śņé¼ļÉ£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņØś ļ╣öņØĆ ļ│┤ņĪ┤ņĢĪ ļ│æņØś ļ░öļŗźņ£╝ļĪ£ ņ×ģņé¼ĒĢśņŚ¼ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ļīĆĒĢ£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼Ļ░Ć Ļ░ĆļŖźĒĢśĻ▓ī ĒĢśņśĆļŗż.10 ĒĢ┤ņÖĖņŚÉņä£ ņé¼ņÜ®ĒĢśļŖö corneal viewing chamberļŖö ņ£äņÖĆ ņĢäļלĻ░Ć Ēł¼ļ¬ģĒĢ£ ĒöīļØ╝ņŖżĒŗ▒ ņ░Įņ£╝ļĪ£ ļÉśņ¢┤ ņ׳ņ£╝ļ®░, Ļ░üļ¦ēņØä ļé┤Ēö╝ņäĖĒżĻ░Ć ņ£äļĪ£ Ļ░ĆļÅäļĪØ chamber ņĢłņŚÉ Ļ│ĀņĀĢĒĢśļÅäļĪØ ļÉśņ¢┤ ņ׳ļŗż. ļö░ļØ╝ņä£, ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ ĻĖ░ņ”ØĻ░üļ¦ēņØś ļé┤Ēö╝ļ®┤ņØ┤ļéś ņāüĒö╝ļ®┤ņØä ņל Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņ£╝ļ®░, ĻĖ░ņ”ØĻ░üļ¦ēņÜ® Ļ▓Įļ®┤Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļ░ĆļÅäļź╝ ņĖĪņĀĢĒĢśļ®░, ņĀäņĢłļČĆ ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼ļĪ£ ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŗż.11 ĻĄŁļé┤ņŚÉļŖö ņØ┤ņÖĆ Ļ░ÖņØĆ corneal viewing chamberļź╝ ĻĄ¼ĒĢĀ ņłś ņŚåņ¢┤ņä£, ņĀĆņ×ÉļōżņØĆ Ļ░üļ¦ē ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤ĻĖ┤ ĻĖ░ņ”ØĻ░üļ¦ēņØä ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ ņēĮĻ▓ī Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ļŖö ņןņ╣śļź╝ Ļ│ĀņĢłĒĢ┤ ļ│┤ņĢśļŗż. ņÜ░ļ”¼ļéśļØ╝ņŚÉņä£ļŖö ļīĆļČĆļČä Ļ░üļ¦ē ļ▓äĒŖĖļŗØ Ēøä ļ│┤ņĪ┤ņĢĪ ļ│æņŚÉ ļŗ┤Ļ░Ćņä£ ļ│┤Ļ┤ĆĒĢśļŖöļŹ░, ņĀĆņ×ÉļōżņØ┤ Ļ│ĀņĢłĒĢ£ ņןņ╣ś ņŚåņØ┤ļŖö ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮņŚÉņä£ ĻĖ░ņ”ØĻ░üļ¦ēņØä Ļ┤Ćņ░░ĒĢĀ ņłś ņŚåĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļ¦īņ£╝ļĪ£ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ļīĆĒĢ┤ ļ¦ÄņØĆ ņĀĢļ│┤ļź╝ ņ¢╗ĻĖ░ņŚÉļŖö ņ¢┤ļĀżņøĀņ£╝ļ®░ Ļ▒░ņÜĖņØ┤ ņäżņ╣śļÉśņ¢┤ ņ׳ļŖö ĒüÉļĖī ļé┤ļČĆļĪ£ ļ╣øņØ┤ ņ×ģņé¼ļÉśņ¢┤ņĢ╝ ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Į ļ╣öņØś ņ×ģņé¼Ļ░üļÅäĻ░Ć ņĀ£ĒĢ£ņĀüņØ┤ļØ╝ļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż. ĒĢśņ¦Ćļ¦ī, Ļ░üļ¦ēņØś ļīĆļץņĀüņØĖ ļæÉĻ╗ś, Ļ▓░ļ¦ē ļ░Å ĒżļÅäļ¦ē ļ░Ģļ”¼ ņāüĒā£, ņŚŁņĪ░ļ¬ģļ▓ĢĻ│╝ Ļ▓Įļ®┤ļ░śņé¼ļ▓ĢņØä ĒåĄĒĢ┤ Ļ░üļ¦ēņāüĒö╝ņÖĆ ļé┤Ēö╝ļź╝ ņ¢┤ļŖÉ ņĀĢļÅä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż.
ņÜ░ļ”¼ļéśļØ╝ļÅä ĒĢ┤ņÖĖ ņĢłņØĆĒ¢ēņ▓śļ¤╝ corneal viewing chamberļź╝ ņé¼ņÜ®ĒĢ£ļŗżļ®┤ ņóŗĻ▓Āņ¦Ćļ¦ī, ĒśäņŗżņĀüņ£╝ļĪ£ ņØ┤ļź╝ ņłśņ×ģĒĢśļŖö ņŚģņ▓┤Ļ░Ć ņŚåņ¢┤ņä£ ņé¼ņÜ®ĒĢśĻĖ░ ņ¢┤ļĀĄļŗż. ļīĆņĢłņ£╝ļĪ£ļŖö corneal viewing chamberņŚÉ ļ│┤Ļ┤ĆļÉ£ ņłśņ×ģĻ░üļ¦ēņØä ņé¼ņÜ®ĒĢ£ ļŗżņØī ņØ┤ viewing chamberļź╝ ņäĖņ▓Ö ļ░Å ethylene oxide gas ņåīļÅģņØä ĒĢ£ ļŗżņØī ļ│┤Ļ┤ĆĒĢśņśĆļŗżĻ░Ć ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņØ┤ ņāØĻĖ░ļ®┤ ņØ┤ņÜ®ĒĢśļŖö ļ░®ļ▓ĢļÅä ņ׳ļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ņĀĆņ×ÉļōżņØ┤ Ļ░£ļ░£ĒĢ£ ņāłļĪ£ņÜ┤ ņןņ╣śļĪ£ ļ│┤ņĪ┤ņĢĪņŚÉ ļŗ┤ĻĖ┤ ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņØä ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓Įņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłļŗżļŖö Ļ▓āņØä ņåīĻ░£ĒĢśļŖö ļŹ░ ņŻ╝ņĢłņĀÉņØä ļæö ņŚ░ĻĄ¼ļĪ£, ļ¦ÄņØĆ ņłśņØś ĻĖ░ņ”ØĻ░üļ¦ēņØä ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ņŗ£ņ╝£ ĒåĄĻ│ä ļČäņäØņØä ĒĢśņ¦ĆļŖö ņĢŖņĢśļŗż. ņČöĒøä Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļ░ĆļÅäļéś ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļÅäļĪØ ņןņ╣śļź╝ Ļ░£ņäĀĒĢĀ ņłś ņ׳ļŗżļ®┤ ļ¦ÄņØĆ ņłśņØś ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ļīĆĒĢ┤ņä£ ņĀĢļ¤ē ļČäņäØ ņśłņĀĢņØ┤ļŗż.
ņĀĆņ×ÉļōżņØ┤ Ļ│ĀņĢłĒĢ£ ĻĖ░ņ”ØĻ░üļ¦ēĻ▓Ćņé¼ņÜ® ņןņ╣śļŖö ņäĖĻ│ä ņĄ£ņ┤łļŖö ņĢäļŗłņ¦Ćļ¦ī, ņÜ░ļ”¼ļéśļØ╝ņŚÉņä£ļŖö ņĄ£ņ┤łļĪ£ Ļ░£ļ░£ļÉ£ ņןņ╣śņØ┤ļŗż. Ļ│ĀņĢłļÉ£ ņןņ╣śļŖö ņĀ£ņ×æņØ┤ļéś ņäżņ╣śĻ░Ć ņ¢┤ļĀĄņ¦Ć ņĢŖņ£╝ļ®░, ĻĄŁļé┤ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ļīĆĒĢ£ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ņēĮĻ▓ī ĒĢĀ ņłś ņ׳Ļ▓ī ĒĢ£ļŗż. ļ╣äļĪØ Ļ│ĀņĢłļÉ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļé┤Ēö╝ņäĖĒżļ░ĆļÅäļéś Ļ░üļ¦ēļæÉĻ╗śļź╝ ņĀĢļ¤ēņĀüņ£╝ļĪ£ ņĖĪņĀĢĒĢśņ¦ĆļŖö ļ¬╗ĒĢśņśĆņ£╝ļéś, ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ Ļ░üļ¦ēļé┤Ēö╝ļéś ļæÉĻ╗śņŚÉ ļīĆĒĢ£ ņĀĢņä▒ņĀüņØĖ ĒÅēĻ░ĆĻ░Ć Ļ░ĆļŖźĒĢśļ®░, ņ£ĪņĢłņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśļŖö Ļ▓āļ│┤ļŗż Ēø©ņö¼ ņäĖļ░ĆĒĢśĻ│Ā ņĀĢĒÖĢĒĢ£ ĒÅēĻ░ĆĻ░Ć Ļ░ĆļŖźĒĢśņśĆļŗż. Ļ░üļ¦ēņØ┤ņŗØņłśņłĀ ņĀä ņłĀņ×ÉĻ░Ć Ļ│ĀņĢłļÉ£ ņןņ╣śļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ĻĖ░ņ”ØĻ░üļ¦ēņŚÉ ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢ£ļŗżļ®┤ ĻĖ░ņ”ØĻ░üļ¦ēņØä ĒÅēĻ░ĆĒĢśļŖö ļŹ░ Ēü░ ļÅäņøĆņØ┤ ļÉĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Supplement1
Supplement1 Print
Print






