 |
 |
| J Korean Ophthalmol Soc > Volume 64(8); 2023 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņ×äņāü Ļ▓ĮĻ│╝ņŚÉ ļīĆĒĢ┤ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢśņśĆļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
Ļ░£ļ░®Ļ░ü ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀņØä ņŗ£Ē¢ēļ░øĻ│Ā 1ļģä ņØ┤ņāü Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢ£ ĒÖśņ×Éļź╝ ĒøäĒ¢źņĀü ļČäņäØņØä ĒĢśņśĆļŗż. Advanced groupņØĆ ņłĀ ņĀä ņŗ£ņĢ╝Ļ▓Ćņé¼ņāü mean deviation (MD) Ļ░Æ -12 dB ļ»Ėļ¦īņ£╝ļĪ£ ņĀĢņØśĒĢśņśĆĻ│Ā, mild to moderateĻĄ░(MDŌēź-12 dB)ņØä ļīĆņĪ░ĻĄ░ņ£╝ļĪ£ ņäżņĀĢĒĢśņśĆļŗż. ņłĀ Ēøä 2ļģäĻ░äņØś ņĢłņĢĢ ļ│ĆĒÖöļź╝ ņĀĢļ¤ēņĀüņ£╝ļĪ£ ĒÖĢņØĖĒĢśņśĆĻ│Ā, ņłĀ Ēøä ņŗ£ļĀź, ņŗ£ņĢ╝ ņ¦ĆĒæ£(MD, pattern standard deviation) ļģ╣ļé┤ņן ņĢłņĢĮ Ļ░£ņłśļź╝ ĒĢ©Ļ╗ś ļČäņäØĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
Advanced group 87ļ¬ģ, mild to moderate group 109ļ¬ģņØ┤ ļČäņäØņŚÉ ĒżĒĢ©ļÉśņŚłļŗż. ņłĀ 1ņŻ╝ ĒøäļČĆĒä░ 24Ļ░£ņøöĻ╣īņ¦Ć ļæÉ ĻĄ░ ļ¬©ļæÉ ņłĀ ņĀä ļīĆļ╣ä Ļ░ÉņåīļÉ£ ņĢłņĢĢņØä ļ│┤ņśĆļŗż(all p<0.05). ņłĀ Ēøä 1ņØ╝ņ¦Ė ĻĖēĻ▓®ĒĢ£ ņĢłņĢĢņāüņŖ╣ņØś ļ╣łļÅäļŖö ļæÉ ĻĄ░ņŚÉņä£ ļ╣äņŖĘĒĢśņśĆĻ│Ā, ņłĀ Ēøä 2ļģä ļÅÖņĢł ļæÉ ĻĄ░ Ļ░ä ĒÅēĻĘĀ ņĢłņĢĢņØĆ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż. ņłĀ Ēøä 1ļģä ņŗ£ņĀÉņŚÉņä£ ļæÉ ĻĄ░ ļ¬©ļæÉ ņłĀ ņĀä ļīĆļ╣ä ņ£ĀņØśĒĢ£ ņŗ£ļĀź ņāüņŖ╣ņØä ļ│┤ņśĆņ£╝ļ®░, ņŗ£ņĢ╝Ļ▓Ćņé¼ ņ¦ĆĒæ£ļŖö Ļ░üĻ░ü ņłĀ ņĀä ļīĆļ╣ä ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż. ļģ╣ļé┤ņן ņĢłņĢĮ ņłśļÅä Ļ░ÉņåīĒĢśņśĆņ£╝ļéś, advancedĻĄ░ņŚÉņä£ļ¦ī ņ£ĀņØśņä▒ņØä ļ│┤ņśĆļŗż.
Ļ▓░ļĪĀ
ļ│Ė ņŚ░ĻĄ¼ļź╝ ĒåĄĒĢśņŚ¼ ļ¦ÉĻĖ░ ļģ╣ļé┤ņןĻĄ░ņØĆ ņ┤łĻĖ░ ļ░Å ņżæĻĖ░ ļģ╣ļé┤ņןĻ│╝ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņ£Āņé¼ĒĢ£ ņĢłņĢĢ ļ░Å ņŗ£ņĢ╝ ļ│ĆĒÖö, ņŗ£ļĀź Ē¢źņāü ļ░Å ņĢłņĢĢņĢĮ Ļ░£ņłśĻ░ÉņåīĻ░Ć ĒÖĢņØĖļÉśņŚłļŗż. ņØ┤ļŖö ļ¦ÉĻĖ░ ļģ╣ļé┤ņןņŚÉņä£ņØś ļ░▒ļé┤ņןņłśņłĀņØ┤ ļŗżļźĖ ļģ╣ļé┤ņןĻĄ░Ļ│╝ ļ╣äņŖĘĒĢ£ ņ×äņāü ĒÜ©Ļ│╝ ļ░Å Ļ▓ĮĻ│╝ļź╝ ļ│┤ņŚ¼ņżīņØä ņŗ£ņé¼ĒĢ£ļŗż.
ABSTRACT
Methods
A retrospective chart review of open-angle glaucoma patients who underwent cataract surgery and were followed-up for 1 year was conducted. Advanced glaucoma was defined as a mean deviation (MD) < -12 dB on the preoperative visual field test. A group with mild-to-moderate glaucoma (MD Ōēź -12 dB) served as the control group. Changes in intraocular pressure (IOP) at 1, 3, 6, and 12 months, and in the postoperative visual acuity (VA) as well as in the visual field indices (MD and the pattern standard deviation), and the number of antiglaucoma medications were compared.
Results
Eighty-seven eyes (87 patients) of the advanced group and 109 eyes (109 patients) of the mild-to-moderate group were finally included. From 1 week to 24 months postoperatively, both groups evidenced IOP decreases compared to the preoperative values (both p < 0.05). The IOP spike prevalence was similar in the two groups (11% vs. 13%, p = 0.199). The mean IOP difference between the two groups was not significant at months 1, 3, 6, 12, or 24 postoperatively (all p > 0.05). Both groups evidenced VA improvements at 1 year postoperatively and the visual field (VF) indices did not differ from those before surgery. The numbers of antiglaucoma medications used decreased after surgery, but the decrease was significant only in the advanced glaucoma group (p = 0.030).
Conclusions
The advanced and mild-to-moderate glaucoma groups evidenced similar IOP and VF changes after cataract surgery. The VA improved and the number of antiglaucoma medications decreased. Our findings suggest that cataract surgery for patients with advanced glaucoma may afford similar clinical outcomes compared to other less severe glaucoma groups.
ļģ╣ļé┤ņןņØĆ ĒŖ╣ņ¦ĢņĀüņØĖ ņŗ£ņĢ╝Ļ▓░ņåÉņØä ņĢ╝ĻĖ░ĒĢśļŖö ļ╣äĻ░ĆņŚŁņĀüņØĖ ņŗ£ņŗĀĻ▓Į ņåÉņāüņØ┤ ļÅÖļ░śļÉśļŖö ņ¦łĒÖśņ£╝ļĪ£ņä£, ņĢłņĢĢ ņĪ░ņĀłņØä ĒåĄĒĢ┤ ņ¦äĒ¢ēņØä ņ¢ĄņĀ£ĒĢśļŖö Ļ▓āņØ┤ ļģ╣ļé┤ņן Ļ┤Ćļ”¼ņØś ĻĘ╝Ļ░äņØ┤ ļÉśĻ│Ā ņ׳ļŗż.1 ņŗ£ņĢ╝ļź╝ ļ│┤ņĪ┤ĒĢśņŚ¼ ņĀüņĀłĒĢ£ ņŗ£ĻĖ░ļŖź ņāüĒā£ļź╝ ņ£Āņ¦ĆĒĢśļŖö Ļ▓āņØ┤ ļ¬®Ēæ£ņØ┤ļ®░, ņØ┤ļź╝ ņ£äĒĢ┤ ņĀÉņĢł ņĢłņĢĢĒĢśĻ░ĢņĀ£, ļĀłņØ┤ņĀĆ ņ╣śļŻī, ņłśņłĀņĀü ņ╣śļŻīļōżņØä ļŗ©Ļ│äņĀüņ£╝ļĪ£ ņĀüņÜ®ĒĢ┤ļ│╝ ņłś ņ׳ļŗż.2
ļģ╣ļé┤ņןĻ│╝ ļŹöļČłņ¢┤ ļ░▒ļé┤ņןņØĆ ļģĖĒÖöņŚÉ ļö░ļØ╝ ņ£Āļ│æļźĀņØ┤ ņ”ØĻ░ĆĒĢśļ®░, ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉĻ▓īņä£ ļ░▒ļé┤ņןņØ┤ ļÅÖļ░śļÉ£ Ļ▓ĮņÜ░Ļ░Ć ņĀüņ¦Ć ņĢŖļŗż. ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀņØĆ ņżæņŗ¼ ņŗ£ļĀźņØä Ē¢źņāüņŗ£Ēé¼ ņłś ņ׳Ļ│Ā, ņĢäņÜĖļ¤¼ ņĢłņĢĢ ņĖĪļ®┤ņŚÉņä£ļÅä ļÅäņøĆņØ┤ ļÉĀ ņłś ņ׳ļŗż.3 ņŚ¼ļ¤¼ ņŚ░ĻĄ¼ļōżņŚÉņä£ ĒśäļīĆņĀü ļ░▒ļé┤ņןņłśņłĀņØĆ ļŗ©ĻĖ░Ļ░ä Ēś╣ņØĆ ņןĻĖ░Ļ░äņØś ņĢłņĢĢ ĒĢśĻ░Ģ ĒÜ©Ļ│╝ļź╝ ļ│┤ņØ┤ļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż.4,5 ĒŖ╣Ē׳, ĻĖēņä▒ ļ░Å ļ¦īņä▒ĒÅÉņćäĻ░üļģ╣ļé┤ņןņŚÉņä£ ņ£ĀņØśĒĢ£ ņĢłņĢĢĒĢśĻ░ĢņØä ļ│┤ņØ┤ļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŖöļŹ░6,7 ņØ┤ļŖö ļ░▒ļé┤ņןņłśņłĀņØä ĒåĄĒĢ┤ ļæÉĻ║╝ņøīņ¦ä ņłśņĀĢņ▓┤ļź╝ ņĀ£Ļ▒░ĒĢśĻ│Ā ņ¢ćņØĆ ņØĖĻ│ĄņłśņĀĢņ▓┤Ļ░Ć ņ£äņ╣śĒĢ©ņ£╝ļĪ£ņŹ© ļ░®ņłśņ£ĀņČ£ļĪ£ ĒÅÉņćäĻ░Ć Ļ░£ņäĀļÉśņ¢┤ņ¦ĆļŖö ĒÜ©Ļ│╝ļĪ£ ĒĢ┤ņäØļÉ£ļŗż.8,9
ĒĢśņ¦Ćļ¦ī ĒÅÉņćäĻ░üļģ╣ļé┤ņןņŚÉ ļ╣äĒĢ┤ Ļ░£ļ░®Ļ░üļģ╣ļé┤ņןņŚÉņä£ņØś ļ░▒ļé┤ņןņłśņłĀņØ┤ ņĢłņĢĢĒĢśĻ░Ģ ļ░Å ļģ╣ļé┤ņןņŚÉ ļ»Ėņ╣śļŖö ĒÜ©Ļ│╝ļŖö ņāüļīĆņĀüņ£╝ļĪ£ ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖļŗż. ņØ┤ņĀä ņŚ░ĻĄ¼ņŚÉņä£ Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן ĒÖśņ×ÉļōżņŚÉĻ▓īļÅä ļ░▒ļé┤ņןņłśņłĀ ņ¦äĒ¢ē Ēøä ņĢłņĢĢĒĢśĻ░ĢņØś ĒÜ©Ļ│╝ņŚÉ ļīĆĒĢ┤ņä£ ļŗżņ¢æĒĢ£ Ļ▓░Ļ│╝ ļ░Å ņśłĒøäļź╝ ļ│┤ņØ┤Ļ│Ā ņ׳ļŗż.10 ĒŖ╣Ē׳ Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן ņżæ ļ¦ÉĻĖ░ ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ļŖö ņ×äņāüņĀüņ£╝ļĪ£ ļ░▒ļé┤ņןņłśņłĀņØś ņŗ£Ē¢ēņØ┤ ņŗ£ļĀź ļ░Å ņŗ£ņĢ╝ ĒÜīļ│ĄņŚÉ ĻĖ░ņŚ¼ĒĢśļŖö ĒÜ©Ļ│╝ļź╝ ĒīÉļŗ©ĒĢśĻĖ░Ļ░Ć ņēĮņ¦Ć ņĢŖļŗż. ņĢäņÜĖļ¤¼, ņåÉņāüļÉ£ ņŗ£ņŗĀĻ▓Į ņāüĒā£ļĪ£ ņØĖĒĢ┤ ļ░▒ļé┤ņןņłśņłĀ Ļ│╝ņĀĢ ļ░Å ņłĀ Ēøä ņĢłņĢĢ ņāüņŖ╣ ņÜöņåīļŖö ņ×äņāüņØśņŚÉĻ▓īļŖö Ēü░ ļČĆļŗ┤ņØ┤ ļÉĀ ņłś ņ׳ļŗż.10
ņØ┤ļ¤░ ļ░░Ļ▓ĮņŚÉņä£ ļ│Ė ņŚ░ĻĄ¼ļŖö ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×É ņżæ Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņ×äņāü ņ¢æņāüņŚÉ ļīĆĒĢ┤ ļČäņäØĒĢ┤ ļ│┤ņĢśļŗż. ņłśņłĀ Ēøä ņŗ£ļĀź ļ░Å ņŗ£ņĢ╝ņØś ļ│ĆĒÖö ņ¢æņāüĻ│╝ ņĢłņĢĢņØś ļ│ĆļÅÖ ņ¢æņāüņØä ĒÖĢņØĖĒĢśņśĆĻ│Ā ņŚ░Ļ┤ĆļÉ£ ņØĖņ×ÉņŚÉ ļīĆĒĢ┤ ĒĢ©Ļ╗ś ļČäņäØĒĢśņśĆļŗż.
2015ļģäļČĆĒä░ 2020ļģäĻ╣īņ¦Ć ļŗ©ņØ╝ĻĖ░Ļ┤ĆņØś ņāüĻĖēņóģĒĢ®ļ│æņøÉ ļģ╣ļé┤ņן Ēü┤ļ”¼ļŗēņŚÉ ļé┤ņøÉĒĢśņŚ¼ Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן ņ¦äļŗ©ņØä ļ░øĻ│Ā ļ░▒ļé┤ņןņłśņłĀ(ņ┤łņØīĒīīņ£ĀĒÖöņłĀ ļ░Å Ēøäļ░® ņØĖĻ│ĄņłśņĀĢņ▓┤ņéĮņ×ģņłĀ)ņØä ņŗ£Ē¢ēļ░øņØĆ 196ļ¬ģ 196ņĢłņØä ņł£ņ░©ņĀüņ£╝ļĪ£ ņŚ░ĻĄ¼ ļīĆņāüņ×ÉņŚÉ ĒżĒĢ©ĒĢśņśĆļŗż. ļīĆņāüņ×ÉļōżņØś ņØśļ¼┤ĻĖ░ļĪØ ļ░Å ņĢłĻ│╝ņĀü Ļ▓Ćņé¼ Ļ▓░Ļ│╝ļź╝ ĒøäĒ¢źņĀüņ£╝ļĪ£ ņĪ░ņé¼ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĒŚ¼ņŗ▒ĒéżņäĀņ¢ĖņØä ņżĆņłśĒĢśņŚ¼ ņ¦äĒ¢ēļÉśņŚłņ£╝ļ®░, ņ×äņāüņŗ£ĒŚśņŗ¼ņé¼ņ£äņøÉĒÜīņØś Ļ▓ĆĒåĀ ļ░Å ņŖ╣ņØĖņØä ļ░øņĢśļŗż(IRB ņŖ╣ņØĖļ▓łĒśĖ: 2021-01-025).
ņŚ░ĻĄ¼ ļīĆņāüņ×ÉņØś ĒżĒĢ© ĻĖ░ņżĆņØĆ (1) Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן, (2) ļ░▒ļé┤ņן ņłśņłĀ Ēøä 1ļģä ņØ┤ņāüņØś Ļ▓ĮĻ│╝ Ļ┤Ćņ░░, (3) ņłśņłĀ ņĀäĒøä ņŗĀļó░ņä▒ ņ׳ļŖö 2Ļ░£ ņØ┤ņāüņØś ņŗ£ņĢ╝Ļ▓Ćņé¼Ļ░Ć ņĪ┤ņ×¼ĒĢśļŖö Ļ▓ĮņÜ░, (4) ņĢĮļ¼╝ļĪ£ ņĪ░ņĀłļÉśļŖö ņĢłņĢĢņØä ļ│┤ņØ┤ļŖö Ļ▓ĮņÜ░(preoperative intraocular pressure[IOP] < 21 mmHg under medication)ļĪ£ ņĀĢĒĢśņśĆļŗż. ļŗżļ¦ī, (1) ņĀäļ░®Ļ░üĻ▓ĮĻ▓Ćņé¼ņÖĆ ņŻ╝ļ│ĆļČĆ ņĀäļ░®Ļ╣ŖņØ┤ ĒÅēĻ░Ćņāü(Van Herick method grade 0-2) ĒÅÉņćäĻ░ü ņØśņ”Ø(occludable angle), (2) ļ░▒ļé┤ņןņłśņłĀ ņØ┤ņÖĖņŚÉ ņĢłĻĄ¼ ļé┤ ņłśņłĀ ĻĖ░ņÖĢļĀźņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░, (3) ļģ╣ļé┤ņן ņØ┤ņÖĖņØś ņŗ£ņĢ╝ņåÉņāüņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŖö ļ¦Øļ¦ē ņ¦łĒÖśņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░, (4) ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņłśņ╣śĻ░Ć -6.0ļööņśĄĒä░(diopters, D) ļ»Ėļ¦īņØ┤Ļ▒░ļéś +3.0 D ņ┤łĻ│╝ĒĢ£ Ļ▓ĮņÜ░, (5) ņĢłņČĢņןņØ┤ 22 mm ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░, (6) ņŗ£ņŗĀĻ▓Į ņ░Įļ░▒ ļ░Å ņŗ£ņĢ╝Ļ▓Ćņé¼ņŚÉ ņśüĒ¢źņØä ņżä ņłś ņ׳ļŖö ļćīļ│æļ│ĆņØ┤ ņĪ┤ņ×¼ĒĢśļŖö Ļ▓ĮņÜ░, (7) Ļ▒░ņ¦ōļ╣äļŖśņ”ØĒøäĻĄ░ņØä ņĀ£ņÖĖĒĢ£ ņØ┤ņ░©ņä▒ ļģ╣ļé┤ņן(ņŚ╝ņ”Øņä▒, ņŗĀņāØĒśłĻ┤Ć, ņŖżĒģīļĪ£ņØ┤ļō£ ņ£Āļ░£)ņØ┤ ļÅÖļ░śļÉ£ Ļ▓ĮņÜ░, (8) ĻĖēņä▒ĒÅÉņćäĻ░üļģ╣ļé┤ņן ļ░£ņ×æ Ēś╣ņØĆ ĒÖŹņ▒äļĀłņØ┤ņĀĆņĀłĻ░£ņłĀ ļō▒ņØś Ļ│╝Ļ▒░ļĀźņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ņØś ĒÖśņ×ÉļōżņØĆ ņĀ£ņÖĖĒĢśņśĆļŗż.
ņłśņłĀ Ēøä 1ņØ╝, 1ņŻ╝ņØ╝, 1, 3, 6, 12, 24Ļ░£ņøö ņŗ£ņĀÉņŚÉņä£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ņØä ĒĢśņśĆļŗż. ļ¦ż ļ░®ļ¼Ė ņŗ£ļ¦łļŗż ņŗ£ļĀź ļ░Å ņĢłņĢĢĻ▓Ćņé¼, ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼, ĻĄ┤ņĀłĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņłśņłĀ ņĀä ņĢłņĢĢņØĆ ņłĀ ņĀä 2ļ▓łņØś ņÖĖļל ļ░®ļ¼ĖņŚÉņä£ ņĖĪņĀĢļÉ£ ņĢłņĢĢņØś ĒÅēĻĘĀĻ░Æņ£╝ļĪ£ ĒĢśņśĆļŗż. ņĢłņĢĢņØĆ Ļ│©ļō£ļ¦īņĢĢĒÅēņĢłņĢĢĻ│ä(Goldmann applanation tonometer) ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢśņśĆļŗż. ĻĖēĻ▓®ĒĢ£ ņĢłņĢĢņāüņŖ╣(IOP spike)ņØĆ ņłĀ Ēøä 3Ļ░£ņøö ņØ┤ļé┤ņŚÉ 1) ņĢłņĢĢņØ┤ 21 mmHg ņ┤łĻ│╝ĒĢ£ ļĢī ņłĀ ņĀä ņĢłņĢĢ ļīĆļ╣ä 50% ņØ┤ņāüņØś ņāüņŖ╣ņØĖ Ļ▓ĮņÜ░, 2) ņłĀ ņĀä ļīĆļ╣ä 10 mmHg ņØ┤ņāüņØś ņĢłņĢĢņāüņŖ╣, 3) ņĢłņĢĢņØ┤ 30 mmHgņØä ņ┤łĻ│╝ĒĢ£ Ļ▓ĮņÜ░ ņżæ ĒĢ£ Ļ░Ćņ¦ĆņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö Ļ▓ĮņÜ░ļĪ£ ņĀĢņØśĒĢśņśĆļŗż.11,12 Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░ä ņżæ ņĢłņĢĢņØ┤ 21 mmHg ņØ┤ņāü ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņĖĪņĀĢļÉ£ Ļ▓ĮņÜ░ ņ×äņāüņØśņØś ĒīÉļŗ© ĒĢśņŚÉ ļģ╣ļé┤ņן ņĢłņĢĮņØä ņČöĻ░ĆņĀüņ£╝ļĪ£ ņĀÉņĢłĒĢśļÅäļĪØ ĒĢśņśĆļŗż. ĒĢ£ĒÄĖ ņłĀ Ēøä ņØ╝ņŗ£ņĀü ņĢłņĢĢņāüņŖ╣ ņØ┤Ēøä ņĢłņĢĢņØ┤ ņĢłņĀĢĒÖöļÉ£ Ļ▓ĮņÜ░ņŚÉļŖö ņĢłņĢĢņĢĮ Ļ░£ņłśļź╝ ņżäņØ┤Ļ│Āņ×É ĒĢśņśĆļŗż. ņłĀ ņĀä ļģ╣ļé┤ņןņĢĮņØś Ļ░£ņłśļŖö ņłĀ ņĀä ņĄ£ņóģ ņÖĖļל ļé┤ņøÉ ņŗ£ ņé¼ņÜ®ĒĢśļŖö ņĢłņĢĢņĢĮ Ļ░£ņłśļĪ£ ĒĢśņśĆĻ│Ā, ņłĀ Ēøä ņĢłņĢĢņĢĮ Ļ░£ņłśļŖö ņłĀ Ēøä 6Ļ░£ņøö ņŗ£ņĀÉņŚÉ ņé¼ņÜ®ĒĢśĻ│Ā ņ׳ļŖö ņĢłņĢĢĒĢśĻ░ĢņĀ£ņØś Ļ░£ņłśļĪ£ ņĀĢĒĢśņśĆļŗż.
ņŗ£ļĀźņØĆ Snellen ņ░©ĒŖĖļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░, ņĢłņĢĢ ņĖĪņĀĢņØĆ Ļ│©ļō£ļ¦īņĢĢĒÅēņĢłņĢĢĻ│äļĪ£ 2ĒÜī ņĖĪņĀĢĒĢśņŚ¼ ĒÅēĻĘĀĻ░ÆņØä ņé¼ņÜ®ĒĢśņśĆļŗż. ļ░▒ļé┤ņןņłśņłĀ ņĀäĒøäņØś ņŗ£ņĢ╝Ļ▓Ćņé¼ņØś mean deviation (MD) ļ░Å pattern standard deviation (PSD) Ļ░ÆņØä ļČäņäØĒĢśņśĆļŗż. ņłĀ ņĀä ļ░▒ļé┤ņןņØś ņżæņ”ØļÅäļŖö Lens Opacities Classification System IIIļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ĒÅēĻ░ĆĒĢśņśĆļŗż.13 ļ░▒ļé┤ņןņØś ņżæņ”ØļÅäļŖö ĒĢĄĻ▓ĮĒÖö ņĀĢļÅäļź╝ ĻĖ░ņżĆņ£╝ļĪ£ 3ļŗ©Ļ│äļĪ£ ļČäļźśĒĢśņśĆļŗż.14 ņŗ£ņĢ╝Ļ▓Ćņé¼ļŖö ĒŚśĒöäļ”¼ņ×ÉļÅÖņŗ£ņĢ╝Ļ│ä(Humphrey┬« visual field analyzer 750, Carl Zeiss Meditec Inc., Dublin, CA, USA)ņØś Central 24-2 SITA-standard strategyļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņ×ÉļÅÖĻĄ┤ņĀłĻ▓Ćņé¼ĻĖ░(HRK-8000A, Huvitz, Anyang, Korea)ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ĻĄ¼ļ®┤ļĀīņ”łļīĆņØæņłśņ╣śļź╝ ņĖĪņĀĢĒĢśņśĆĻ│Ā, ņĢłņČĢņןņØĆ IOL master┬« 500 (Carl Zeiss Meditec AG, Jena, Germany)ņØä ņé¼ņÜ®ĒĢśņśĆļŗż. ņłśņłĀ ņĀäĒøä ļ¦Øļ¦ē ņāüĒā£ļŖö ĒīīņןĻ░Ćļ│Ćļŗ©ņĖĄņ┤¼ņśüĻĖ░ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļČäņäØĒĢśņśĆļŗż(swept-source optical coherence tomography; DRI OCT Triton┬«, Topcon, Tokyo, Japan).
ļ░▒ļé┤ņן ņ┤łņØīĒīīņ£ĀĒÖöņłĀ ļ░Å ņØĖĻ│ĄņłśņĀĢņ▓┤ņéĮņ×ģņłĀņØĆ ļŗżņØīĻ│╝ Ļ░ÖņØĆ ļ░®ņŗØņ£╝ļĪ£ ņłśĒ¢ēļÉśņŚłļŗż. Ļ▓░ļ¦ē ļ░Å Ēģīļģ╝ĒĢś lidocaine ļ¦łņĘ© Ēøä 2.8 mm Ēł¼ļ¬ģĻ░üļ¦ēņĀłĻ░£ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ĻĄ¼ļČĆļ¤¼ņ¦ä 27-gauge ļ░öļŖśņØä ņé¼ņÜ®ĒĢśņŚ¼ ņŚ░ņåŹņĀüņØĖ Ļ│ĪņäĀ ņłśņĀĢņ▓┤ļéŁ ņøÉĒśĢņĀłĻ░£ņłĀ Ēøä Ēæ£ņżĆ ņłśņĀĢņ▓┤ņ£ĀĒÖöņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ļ░▒ļé┤ņן ņĀ£Ļ▒░ Ēøä ņØĖĻ│ĄņłśņĀĢņ▓┤(Tecnis ZCB00 IOL, Abbot Medical Optics, Abbott Park, IL, USA)ļź╝ Ļ░üļ¦ēņĀłĻ░£ņ░ĮņØä ĒåĄĒĢ┤ ņłśņĀĢņ▓┤ļéŁņŚÉ ņéĮņ×ģĒĢśņśĆļŗż. Irrigation-aspirationņØĆ ņĄ£ņåī 30ņ┤ł ļÅÖņĢł ņłśĒ¢ēĒĢśņśĆņ£╝ļ®░, ņØĖĻ│ĄņłśņĀĢņ▓┤ ļÆżņ¬Įņ£╝ļĪ£ ļ│┤ņØ┤ļŖö ļ¬©ļōĀ ņĀÉĒāäļ¼╝ņ¦łņØś ļ░®ņČ£ņØä ņ┤ēņ¦äĒĢśĻĖ░ ņØĖĻ│ĄņłśņĀĢņ▓┤ļź╝ ļČĆļō£ļ¤ĮĻ▓ī ĒØöļōżļ®░ ņĄ£ļīĆĒĢ£ ņĀ£Ļ▒░ĒĢśņśĆļŗż. ņĀäļ░®ņØĆ balanced saline solution (BSS)ļĪ£ ņ×¼Ļ▒┤ĒĢśņśĆĻ│Ā, Ļ░üļ¦ē ņāüņ▓śņÖĆ ņĖĪļ®┤ ĒżĒŖĖļŖö BSSļĪ£ ņłśĒÖöĒĢśņŚ¼ ļ¦łļ¼┤ļ”¼ĒĢśņśĆļŗż. ļ¬©ļōĀ ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀ Ēøä levokacin 0.5% Ēś╣ņØĆ 1.5% (Cravit┬«, Santen Pharmaceutical, Osaka, Japan)ņÖĆ fluorometholone 0.1%(Flumetholone┬«, Santen Pharmaceutical)ļź╝ ņĢĮ 4ņŻ╝Ļ░ä 6ņŗ£Ļ░ä Ļ░äĻ▓®ņ£╝ļĪ£ ĒĢśļŻ© 4ņ░©ļĪĆ ņĀÉņĢłĒĢśļÅäļĪØ ĒĢśņśĆļŗż. ļ¬©ļōĀ ļīĆņāü ĒÖśņ×ÉļŖö ņłśņłĀĻĖ░ļĪØņ¦Ćļź╝ ļČäņäØĒĢśņŚ¼ ļ░▒ļé┤ņןņłśņłĀ Ļ│╝ņĀĢņŚÉņä£ ĒÖĢņØĖļÉśĻ▒░ļéś ļ░£ņāØļÉ£ ĒĢ®ļ│æņ”Ø(ĒøäļéŁĒīīņŚ┤, ņä¼ļ¬©ņ▓┤ņåīļīĆ ņĢĮĒÖö Ēś╣ņØĆ ĒĢ┤ļ”¼, ņ£Āļ”¼ņ▓┤ĒāłņČ£) ņŚ¼ļČĆļź╝ ņĪ░ņé¼ĒĢśņśĆļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĀäņ▓┤ ļīĆņāüĻĄ░ņØä ļģ╣ļé┤ņןņØś ņĀĢļÅäņŚÉ ļö░ļØ╝ ļæÉ ĻĘĖļŻ╣ņ£╝ļĪ£ ļéśļłäņŚłļŗż. ļ░▒ļé┤ņןņłśņłĀņØä ņŗ£Ē¢ēĒĢśĻĖ░ ņĄ£ņåī 6Ļ░£ņøö ņØ┤ņĀä ņŗ£Ē¢ēļÉ£ ņŗ£ņĢ╝Ļ▓Ćņé¼ Ļ▓░Ļ│╝ļź╝ ĻĖ░ņżĆņ£╝ļĪ£ ĒĢśņŚ¼ MDĻ░ÆņØ┤ -12 dB ņØ┤ņāüņØĖ mild to moderateĻĄ░, -12 dB ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░ļź╝ advancedĻĄ░ņ£╝ļĪ£ ļéśļłäņŚłļŗż. ņØ┤ļĢī ņŗ£ņĢ╝Ļ▓Ćņé¼ļŖö ņŗĀļó░ļÅä ņ׳ļŖö 2ĒÜī ņØ┤ņāüņØś ļ░śļ│ĄļÉ£ ņŗ£ņĢ╝Ļ▓Ćņé¼ņŚÉņä£ ĻĄ¼ņĪ░ņĀü ņåÉņāü(ņŗ£ņŗĀĻ▓Įņ£ĀļæÉ Ēś╣ņØĆ ļ¦Øļ¦ēņŗĀĻ▓Įņä¼ņ£ĀņĖĄ)Ļ│╝ ņāüņØæĒĢśļŖö ņŗ£ņĢ╝Ļ▓░ņåÉņØä ļ│┤ņØ┤ļŖö Ļ▓āņØä ņ▒äĒāØĒĢśņśĆļŗż. ņäĖļČĆņĀüņ£╝ļĪ£ ņ¢æņĢłņŚÉ ļ¬©ļæÉ ļģ╣ļé┤ņןņØ┤ ņØ┤ĒÖśļÉ£ Ļ▓ĮņÜ░, MDĻ░ÆņØä ĻĖ░ņżĆņ£╝ļĪ£ ļģ╣ļé┤ņןņä▒ ņåÉņāüņØ┤ ļŹö ņŗ¼ĒĢ£ ļłłņØä ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ĒĢśņśĆļŗż. ņśłļź╝ ļōżņ¢┤, ņÜ░ņĢł ļ¦ÉĻĖ░ļģ╣ļé┤ņן, ņóīņĢł ņżæļō▒ļÅä ļģ╣ļé┤ņןņØĖ Ļ▓ĮņÜ░ ņÜ░ņĢłņØä ĻĖ░ņżĆņ£╝ļĪ£ ļ¦ÉĻĖ░ļģ╣ļé┤ņןņ£╝ļĪ£ ļČäļźśĒĢśņśĆļŗż.
ĒåĄĻ│ä ļČäņäØņØĆ SPSS ĒöäļĪ£ĻĘĖļש(IBM SPSS Statistics for Windows, Version 22.0, IBM Corp., Armonk, NY, USA)ņØä ĒåĄĒĢśņŚ¼ ņ¦äĒ¢ēĒĢśņśĆļŗż. ņłĀ Ēøä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŗ£ņĀÉņØś ņŗ£ļĀźĻ│╝ ņĢłņĢĢņØä Ļ░üĻ░ü ņłĀ ņĀä ņłśņ╣śņÖĆ ļ╣äĻĄÉĒĢśņŚ¼, ĻĘĖ ĒÅēĻĘĀĻ░ÆņØś ņ░©ņØ┤(mean difference) ļź╝ ļČäņäØņŚÉ ĒÖ£ņÜ®ĒĢśņśĆļŗż. ļæÉ ĻĘĖļŻ╣ Ļ░äņØś ļ╣äĻĄÉ ļČäņäØņŚÉ ņŚ░ņåŹļ│ĆņłśļŖö T-test, Mann-Whitney U testļź╝, ļ╣äņŚ░ņåŹ ļ│ĆņłśļŖö chi-square testļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ļČäņäØĒĢśņśĆļŗż. ņØ┤ ļČäņäØņØä ĒåĄĒĢśņŚ¼ ņ£ĀņØśņłśņżĆņØ┤ 0.05 ļ»Ėļ¦ī(p<0.05)ņØ┤ļ®┤ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņĀĢņØśĒĢśņśĆļŗż.
ņĀäņ▓┤ ļīĆņāüĻĄ░ 196ņĢł 196ļ¬ģ ņżæņŚÉņä£, mild-moderateĻĄ░ņØĆ 109ņĢł, advancedĻĄ░ 87ņĢłņ£╝ļĪ£ ļČäļźśļÉśņŚłļŗż. Mild to moderateĻĄ░ņŚÉ ļ╣äĒĢ┤ advancedĻĄ░ņØś ĒÅēĻĘĀ ņŚ░ļĀ╣ņØ┤ ļŹö ļåÆņĢśĻ│Ā(75.0 ┬▒ 10.7ņäĖ vs. 69.6 ┬▒ 10.4ņäĖ, p<0.001), ļé©ņä▒ ļ╣äņ£©ņØ┤ ļŹö ļ¦ÄņĢśņ£╝ļ®░(60% vs. 33%, p<0.001), ļ░▒ļé┤ņןņØś ĒĢĄĻ▓ĮĒÖö ņĀĢļÅäĻ░Ć ļŹö ņŗ¼ĒĢśņśĆļŗż(1.37 ┬▒ 0.61 vs. 1.18 ┬▒ 0.45, p=0.014) (Table 1).
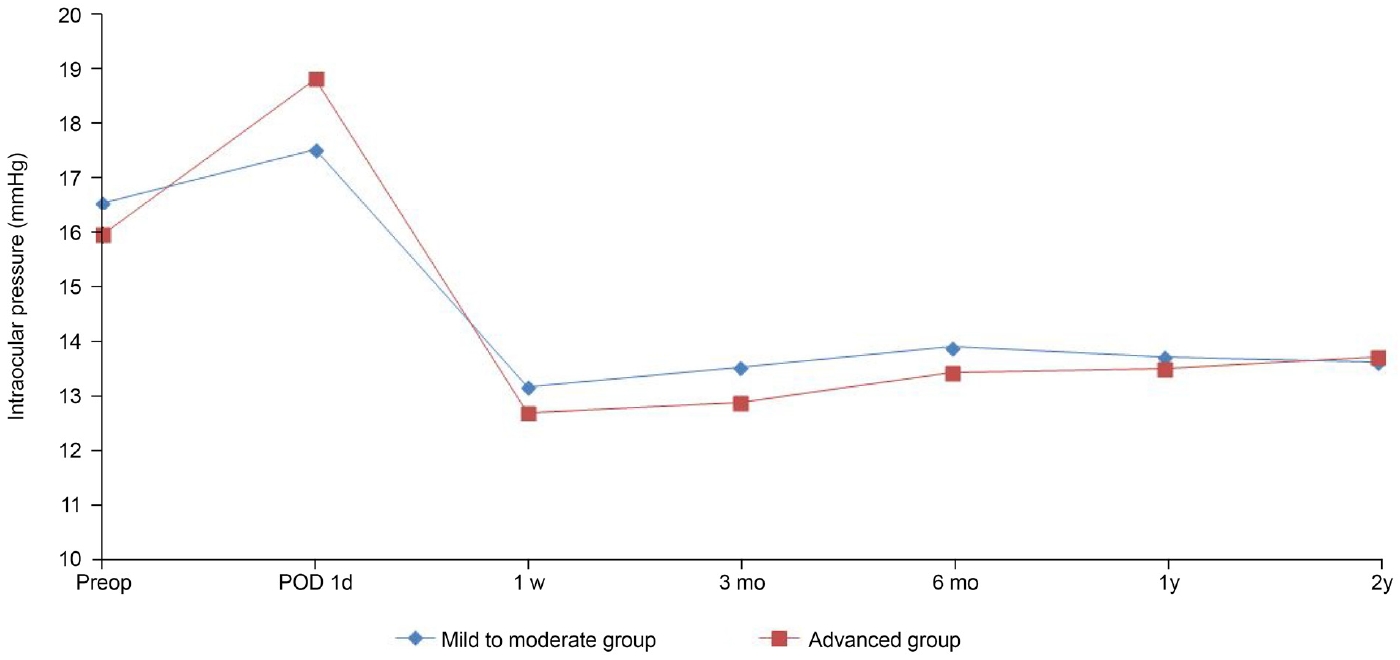
ļ░▒ļé┤ņןņłśņłĀ ņĀä ļ░Å ņłĀ Ēøä ņĢłņĢĢņØś ļ│ĆĒÖö ņ¢æņāüņØĆ Fig. 1ņŚÉ ļÅäņŗØĒÖöĒĢśņśĆļŗż. Mild to moderateĻĄ░Ļ│╝ advancedĻĄ░ņŚÉņä£ ņłĀ Ēøä 1Ļ░£ņøö, 3Ļ░£ņøö, 6Ļ░£ņøö, 12Ļ░£ņøö, 24Ļ░£ņøöņ¦Ė ņĢłņĢĢņØĆ Ļ░üĻ░ü 13.64 vs. 13.42 mmHg, 13.60 vs. 12.87 mmHg, 14.29 vs. 13.42 mmHg, 13.94 vs. 13.51 mmHg, 13.89 vs. 13.71 mmHgļĪ£ ļ¬©ļōĀ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņŗ£ņĀÉņŚÉņä£ ļæÉ ĻĄ░ Ļ░äņØś ĒÅēĻĘĀ ņĢłņĢĢņØĆ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż(all p>0.05) (Table 2).
Ļ░ü ĻĘĖļŻ╣ļ│äļĪ£ ņłĀ ņĀä ņĢłņĢĢ ļīĆļ╣ä ņłĀ Ēøä ņĢłņĢĢ ļ│ĆĒÖöļź╝ ņĀĢļ¤ēņĀüņ£╝ļĪ£ ļČäņäØĒĢśņśĆļŗż(Table 3). ņłĀ Ēøä 1ņØ╝ņ¦Ė ļæÉ ĻĄ░ ļ¬©ļæÉņŚÉņä£ ņłĀ ņĀäņŚÉ ļ╣äĒĢ┤ ņĢłņĢĢņØ┤ ņāüņŖ╣ĒĢśņśĆņ£╝ļéś advancedĻĄ░ņŚÉņä£ļ¦ī ĒåĄĻ│äĒĢÖņĀü ņ£ĀņØśņä▒ņØä ļ│┤ņśĆļŗż(mean difference = 2.43 mmHg, p=0.018). ņłĀ Ēøä 1ņŻ╝ņŚÉļŖö mild to moderateĻĄ░Ļ│╝ advancedĻĄ░ Ļ░üĻ░ü ņłĀ ņĀäņŚÉ ļ╣äĒĢ┤ ņĢłņĢĢņØ┤ Ļ░ÉņåīĒĢśņśĆņ£╝ļ®░(mean difference = -2.87 and -3.00 mmHg, both p=0.001), ņØ┤Ēøä 1, 3, 6, 12, 24Ļ░£ņøöņØś Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ļÅÖņĢł ļæÉ ĻĄ░ ļ¬©ļæÉ Ļ░ÉņåīļÉ£ ņĢłņĢĢņØ┤ ņ£Āņ¦ĆļÉśņŚłļŗż(all p<0.05).
ļ░▒ļé┤ņןņłśņłĀ Ēøä ņŗ£ļĀź ļ│ĆĒÖöļŖö ņłĀ ņĀäĻ│╝ ņłĀ Ēøä 1ļģä ņŗ£ņĀÉņŚÉņä£ņØś ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØś ņ░©ņØ┤ļź╝ ĒåĄĒĢ┤ ļČäņäØĒĢśņśĆļŗż(Table 4). Mild to moderateĻĄ░ņØĆ ņłĀ ņĀä 0.47 ┬▒ 0.29ņŚÉņä£ ņłĀ Ēøä 0.86 ┬▒ 0.26ņ£╝ļĪ£ advancedĻĄ░ņØĆ ņłĀ ņĀä 0.39 ┬▒ 0.26ņŚÉņä£ 0.77 ┬▒ 0.25ļĪ£ ļæÉ ĻĄ░ ļ¬©ļæÉ ņ£ĀņØśĒĢ£ ņŗ£ļĀź Ē¢źņāüņØä ļ│┤ņśĆļŗż(both p<0.001). ņŗ£ņĢ╝ ņ¦ĆĒæ£ļÅä ņłĀ ņĀäĻ│╝ ņłĀ Ēøä 1ļģä ņŗ£ņĀÉņØś Ļ▓Ćņé¼Ļ░ÆņØä ļ╣äĻĄÉĒĢśņśĆļŗż. ļ░▒ļé┤ņןņłśņłĀ ņĀäĒøä ņŗ£ņĢ╝ ņ¦ĆĒæ£ ļ│ĆĒÖöļ¤ēņØĆ mild to moderateĻĄ░ 0.42 dB(ņłĀ ņĀä -10.07 dB; ņłĀ Ēøä -9.65 dB), advancedĻĄ░ -0.40 dB(ņłĀ ņĀä -18.32 dB; ņłĀ Ēøä -19.22 dB)ļĪ£ ļæÉ ĻĄ░ ļ¬©ļæÉ ņłĀ ņĀä ļīĆļ╣ä ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦ĆļŖö ņĢŖņĢśļŗż(p=0.768 and 0.561) (Table 5). ņĢäņÜĖļ¤¼, PSD ļ│ĆĒÖöļ¤ēļÅä mild to moderateĻĄ░ 0.38 dB, advancedĻĄ░ņØĆ 0.40 dBļĪ£ ļæÉ ĻĄ░ ļ¬©ļæÉ ņłĀ Ēøä ļÜ£ļĀĘĒĢ£ ļ│ĆĒÖöļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż(p=0.576 and 0.536). ļ░▒ļé┤ņןņłśņłĀ ņĀäĒøä ļģ╣ļé┤ņן ņĢłņĢĮ ņłśļŖö mild to moderateĻĄ░(0.95 ┬▒ 0.84Ļ░£ vs. 0.85 ┬▒ 0.80Ļ░£)Ļ│╝ advancedĻĄ░(1.57 ┬▒ 0.70Ļ░£ vs. 1.34 ┬▒ 0.67Ļ░£) ļ¬©ļæÉ Ļ░ÉņåīĒĢśņśĆņ£╝ļéś, advancedĻĄ░ņŚÉņä£ļ¦ī ĒåĄĻ│äņĀü ņ£ĀņØśņä▒ņØä ļ│┤ņśĆļŗż(p=0.030) (Table 6).
ļ░▒ļé┤ņןņłśņłĀ ņżæ Ēś╣ņØĆ ņłśņłĀ ņ¦üĒøä ĒĢ®ļ│æņ”ØņØś ļ╣łļÅä ļ░Å ņŚ░Ļ┤Ć ņØĖņ×Éļź╝ ļČäņäØĒĢśņśĆļŗż(Table 7). Mild to moderateĻĄ░Ļ│╝ advanced ĻĄ░ Ļ░äņØś ņłĀ ņĀä Ļ▒░ņ¦ōļ╣äļŖśņ”ØĒøäĻĄ░ņØś ļČäĒżļŖö ņ░©ņØ┤Ļ░Ć ņŚåņŚłņ£╝ļ®░(1.83% vs. 1.15%, p=0.698), ļ░▒ļé┤ņןņłśņłĀ ņżæ ņ£ĀņØśĒĢ£ ĒĢ®ļ│æņ”Ø(ņä¼ļ¬©ņ▓┤ņåīļīĆ ņåÉņāü, ĒøäļéŁĒīīņŚ┤, ņ£Āļ”¼ņ▓┤ņĀłņĀ£ņłĀ ņŗ£Ē¢ē)ņØś ļ╣łļÅä ņŚŁņŗ£ ļ╣äņŖĘĒĢ£ ņ¢æņāüņØä ļ│┤ņśĆļŗż(7.34% vs. 9.20%, p=0.637). ļśÉĒĢ£ ņłśņłĀ ņ¦üĒøä ĻĖēĻ▓®ĒĢ£ ņĢłņĢĢņāüņŖ╣ņØś ļ╣äņ£©ņØĆ mild to moderate ĻĄ░ 11.01%, advancedĻĄ░ņØĆ 12.64%ļĪ£ advancedĻĄ░ņŚÉņä£ ļŗżņåī ļ¦ÄņĢśņ£╝ļéś ņ£ĀņØśĒĢśņ¦ĆļŖö ņĢŖņĢśļŗż(p=0.200).
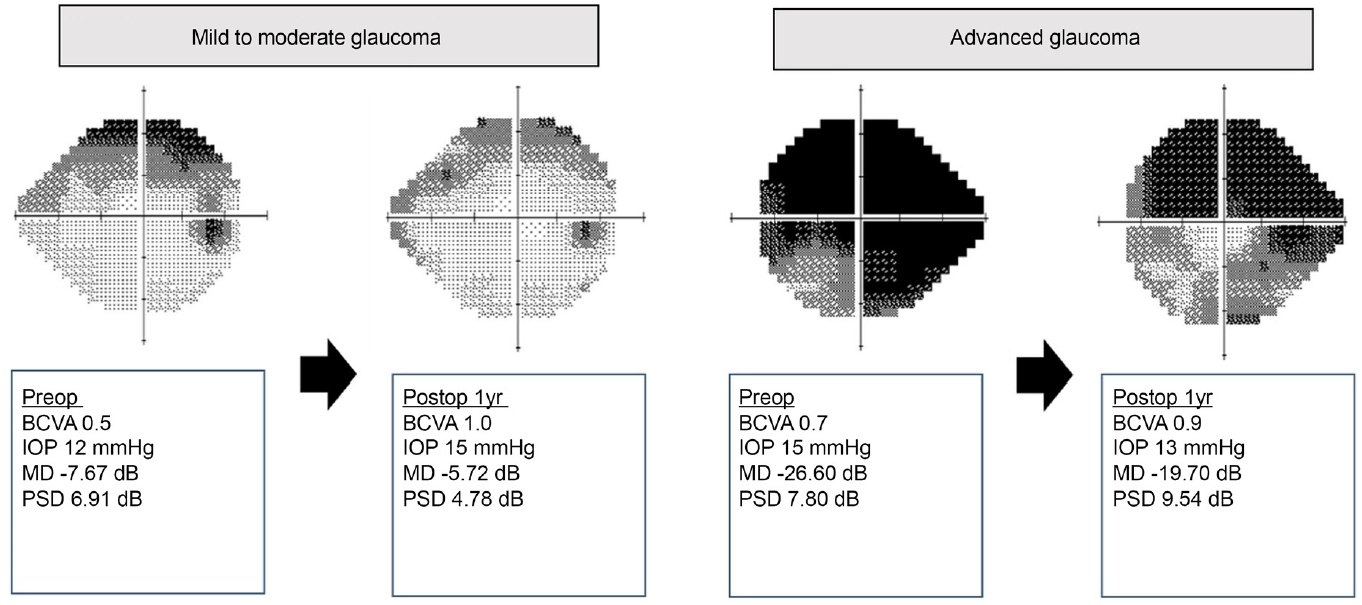
Fig. 2ļŖö mild to moderateĻĄ░Ļ│╝ advancedĻĄ░ņŚÉ ļīĆĒĢ£ Ļ░üĻ░üņØś ļīĆĒæ£ ņ”ØļĪĆņØ┤ļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ļ¦ÉĻĖ░ ļģ╣ļé┤ņן(advanced glaucoma group)ņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņ×äņāü Ļ▓ĮĻ│╝ļź╝ ņ┤łĻĖ░ ļ░Å ņżæĻĖ░ ļģ╣ļé┤ņן(mild to moderate glaucoma group)Ļ│╝ ļ╣äĻĄÉ ļČäņäØĒĢ£ ņŚ░ĻĄ¼ņØ┤ļŗż. ņłĀ Ēøä ļæÉ ĻĄ░ ļ¬©ļæÉ ņłĀ ņĀä ļīĆļ╣ä ņןĻĖ░ņĀüņØĖ ņĢłņĢĢ Ļ░Éņåīļź╝ ļ│┤ņśĆņ£╝ļ®░, ļæÉ ĻĄ░ Ļ░ä ņ£Āņé¼ĒĢ£ ņĢłņĢĢ ļ│ĆļÅÖ ņ¢æņāüņØä ļ│┤ņśĆļŗż. ņĢäņÜĖļ¤¼ ļæÉ ĻĄ░ņŚÉņä£ Ļ░üĻ░ü ņłĀ Ēøä ņ£ĀņØśĒĢ£ ņŗ£ļĀź Ļ░£ņäĀņØä ļ│┤ņśĆņ£╝ļ®░, ņłĀ Ēøä ņŗ£ņĢ╝ ņĢģĒÖöļÅä Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļŖö ļ¦ÉĻĖ░ ļģ╣ļé┤ņןņŚÉņä£ņØś ļ░▒ļé┤ņןņłśņłĀņØ┤ ņ┤łĻĖ░ ļ░Å ņżæĻĖ░ ļģ╣ļé┤ņןĻ│╝ ļ╣äņŖĘĒĢ£ ņ×äņāü ĒÜ©Ļ│╝ ļ░Å Ļ▓ĮĻ│╝ļź╝ ļ│┤ņŚ¼ņżīņØä ņŗ£ņé¼ĒĢ£ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ mild-moderateĻĄ░Ļ│╝ advancedĻĄ░ ļ¬©ļæÉ ņłśņłĀ Ēøä 1ņØ╝ņ¦Ė ņĢłņĢĢņØ┤ ņāüņŖ╣ĒĢśņśĆņ£╝ļ®░, 1ņŻ╝ ĒøäļČĆĒä░ļŖö ņłĀ ņĀä ļīĆļ╣ä ņĢłņĢĢņØ┤ Ļ░ÉņåīĒĢśņśĆļŗż. ņłĀ Ēøä 1ņØ╝ņ¦Ė ņĢłņĢĢņāüņŖ╣ņØĆ ņĀäļ░® ņŚ╝ņ”Øļ░śņØæĻ│╝ ļé©ņĢäņ׳ļŖö ņĀÉĒāäļ¼╝ņ¦łņØś ņśüĒ¢źņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. ņäĖļČĆņĀüņ£╝ļĪ£ ņłĀ Ēøä 1ņØ╝ņ¦Ė ņĢłņĢĢņāüņŖ╣ņØ┤ advancedĻĄ░ņŚÉņä£ļ¦ī ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśņä▒ņØä ļ│┤ņśĆļŖöļŹ░, ņØ┤ļŖö ņłĀ ņĀä mild to moderateĻĄ░ņŚÉ ļ╣äĒĢ┤ advancedĻĄ░ņŚÉņä£ ļ│┤ļŗż ļ¦ÄņØĆ ļģ╣ļé┤ņן ņĢĮņĀ£ļź╝ ņé¼ņÜ®ĒĢśņśĆļŹś ņĀÉņØä ņØ┤ņ£ĀļĪ£ ņāØĻ░üĒĢ┤ļ│╝ ņłś ņ׳ļŗż. ļģ╣ļé┤ņן ņĢĮņĀ£ņØś Ļ░£ņłśĻ░Ć ņ”ØĻ░ĆĒĢĀņłśļĪØ ņĢĮņĀ£ņŚÉ ĒżĒĢ©ļÉ£ ļ│┤ņĪ┤ņĀ£(benzalkonium chloride, BAK)ņØś ļåŹļÅäĻ░Ć ņ”ØĻ░ĆĒĢśņŚ¼ ņŚ╝ņ”Øļ░śņØæņØ┤ ņ”ØĻ░ĆļÉĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņØ┤ļŗż.
ļśÉĒĢ£ ļæÉ ĻĄ░ ļ¬©ļæÉ ņłĀ Ēøä ņØ╝ņŻ╝ņØ╝ ņŗ£ņĀÉņŚÉ ņłĀ ņĀä ļīĆļ╣ä ņĢłņĢĢņØ┤ Ļ░ÉņåīĒĢ£ ņ¢æņāüņØä ļ│┤ņśĆļŗż. ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀņØ┤ ņĢłņĢĢĒĢśĻ░ĢņØä ņØ╝ņ£╝ĒéżļŖö ĻĖ░ņĀäņ£╝ļĪ£ ļ░®ņłśņ£ĀņČ£ ĻĖ░ļŖź(outflow facility)ņØ┤ ņ”ØĻ░ĆļÉ£ ņĀÉņØä Ļ│ĀļĀżĒĢ┤ļ│╝ ņłś ņ׳ļŗż. Meyer et al11ņØś ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤, Ļ░ÉņåīļÉ£ ņä¼ņ£ĀņŻ╝ņØś ļ░®ņłśņ£ĀņČ£ ĻĖ░ļŖźņØĆ ņłśņĀĢņ▓┤ņ£ĀĒÖöņłĀļĪ£ Ļ░£ņäĀļÉĀ ņłś ņ׳ļŗżĻ│Ā ĒĢśņśĆļŗż. ņØ┤ņÖĖņŚÉ ņē┤ļשĻ┤ĆņØś ĒÖĢņן, ņłĀ Ēøä ĒöäļĪ£ņŖżĒāĆĻĖĆļ×Ćļöś F2ņØś ļ░░ņČ£ļĪ£ ņØĖĒĢ£ ļ░®ņłśņØś Ļ│Ąļ¦ē ĒżļÅäļ¦ē ņ£ĀņČ£ ņ”ØĻ░Ćļź╝ ņČöļĪĀĒĢ┤ļ│╝ ņłś ņ׳ļŗż. ĒöäļĪ£ņŖżĒāĆĻĖĆļ×ĆļöśņØś ļ░®ņČ£ļĪ£ ļ░®ņłśņØś ņ£ĀņČ£ņØś ĒÜ©Ļ│╝Ļ░Ć ņ”ØļīĆļÉśĻ│Ā ļśÉĒĢ£ ņāüļīĆņĀüņØĖ ļÅÖĻ│Ąņ░©ļŗ©ņØä ļ░®ņ¦ĆĒĢśņŚ¼ ņĢłņĢĢņØś ĒĢśĻ░ĢņØä ņ£Āļ░£ĒĢ£ļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.12,15 ļśÉĒĢ£ Zamani et al16ņØĆ ņĀäļ░® ņłśņĀĢņ▓┤ļéŁņØ┤ ņłĀ ĒøäņŚÉ ņĪ░ĻĖł ļŹö Ēøäļ░®ņ£╝ļĪ£ ņ£äņ╣śĒĢśļ®┤ņä£ ņä¼ļ¬©ņ▓┤ņåīļīĆĻ░Ć ņä¼ļ¬©ņ▓┤ ļ░Å Ļ│Ąļ¦ēļÅīĻĖ░ ņ¬Įņ£╝ļĪ£ Ēøäļ░® ļŗ╣Ļ╣ĆņØ┤ ņ”ØĻ░ĆĒĢśĻ▓ī ļÉśļ®┤ņä£ ņĢłņĢĢņØś ĒĢśĻ░ĢņØä ņ£ĀļÅäĒĢ£ļŗżĻ│Ā ļ│┤ņĢśļŗż.
Ļ░£ļ░®Ļ░üļģ╣ļé┤ņןņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņĢłņĢĢĒĢśĻ░ĢņØĆ ņŚ¼ļ¤¼ ņŚ░ĻĄ¼ļōżņØä ĒåĄĒĢ┤ņä£ ĒÖĢņØĖļÉśņŚłĻ│Ā,14,17 ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļÅä ņØ┤ņÖĆ ņ£Āņé¼ĒĢ£ ņĢłņĢĢ ļ│ĆĒÖö ņ¢æņāüņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż. ĒĢśņ¦Ćļ¦ī ĒāĆ ņŚ░ĻĄ¼ņŚÉ ļ╣äĒĢ┤ ņןĻĖ░Ļ░ä ņĢłņĢĢĒĢśĻ░ĢņØ┤ ņ£Āņ¦ĆļÉśņŚłļŖöļŹ░, ņłĀ Ēøä 2ļģä ņŗ£ņĀÉņŚÉņä£ļÅä ņłĀ ņĀä ļīĆļ╣ä ņĢłņĢĢņØ┤ ņ£ĀņØśĒĢśĻ▓ī ļé«ņØĆ ņĀÉņØĆ ĒŖ╣ņ¦ĢņĀüņØ┤ļŗż. ņØ┤ļŖö ļ¦ÉĻĖ░ ļģ╣ļé┤ņןņØś ĒŖ╣ņä▒ņ£╝ļĪ£ ņĀüĻĘ╣ņĀüņØĖ ņĢłņĢĢĒĢśĻ░ĢņĀ£ ņé¼ņÜ®ņØ┤ ņØ┤ļŻ©ņ¢┤ņĀĖ ņĢłņĢĢĒĢśĻ░ĢņØ┤ ņ£Āņ¦ĆļÉśņŚłņØä ņłś ņ׳ļŗż. ņĢäņÜĖļ¤¼ Ļ│ĀļĀ╣ ņ¦æļŗ©ņØĖ ļ│Ė caseņŚÉņä£ ļ╣äĻĄÉņĀü ņóüņØĆ ņĀäļ░®Ļ░ü ĒÖśņ×ÉĻ░Ć ļŗżņłś ĒżĒĢ©ļÉśņŚłņØä Ļ░ĆļŖźņä▒ņØä Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņÖĆ ļ╣äņŖĘĒĢśĻ▓ī ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×ÉļōżņØä ļīĆņāüņ£╝ļĪ£ ļ░▒ļé┤ņןņłśņłĀ ĒøäņØś ņ×äņāü Ļ▓ĮĻ│╝ļź╝ ļ░£Ēæ£ĒĢ£ ņŚ░ĻĄ¼ļōżņŚÉņä£, Altmeyer et al17ņØĆ ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×É 12ņĢłņØä ļīĆņāüņ£╝ļĪ£ ļ░▒ļé┤ņןņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, ņłĀ Ēøä ņØśļ»Ė ņ׳ļŖö ņŗ£ļĀź ĒśĖņĀä ļ░Å ņĢłņĢĢĒĢśĻ░Ģ(ĒÅēĻĘĀ 4.4 mmHg Ļ░Éņåī)ņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. ņĢäņÜĖļ¤¼ ņłĀ ņĀä 1.5Ļ░£ņŚÉņä£ ņłĀ Ēøä 0.8Ļ░£ļĪ£ ļģ╣ļé┤ņן ņĢłņĢĮ Ļ░£ņłśĻ░Ć Ļ░ÉņåīĒĢśņśĆĻ│Ā, ļ░▒ļé┤ņןņłśņłĀĻ│╝ ņŚ░Ļ┤ĆļÉ£ ņŗ¼Ļ░üĒĢ£ ĒĢ®ļ│æņ”ØņØ┤ ņŚåņØīņØä ļ░£Ēæ£ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņØś ļ¦ÉĻĖ░ ļģ╣ļé┤ņןĻĄ░ņŚÉņä£ļÅä ņłĀ ņĀäņŚÉ ļ╣äĒĢ┤ ņłĀ Ēøä ĒåĄĻ│äĒĢÖņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņŗ£ļĀź ĒśĖņĀä ļ░Å ņĢłņĢĢĒĢśĻ░Ģ ĒÜ©Ļ│╝ļź╝ ļ│┤ņśĆļŗż.
ĒŖ╣ņ¦ĢņĀüņ£╝ļĪ£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņŗ£ņĢ╝Ļ▓Ćņé¼ņāü MDļéś PSDĻ░ÆņØ┤ ņłĀ ņĀäņŚÉ ļ╣äĒĢ┤ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż. ĒĢ£ĒÄĖ Altmeyer et al17ņØś ņŚ░ĻĄ¼ņŚÉņä£ļŖö MDĻ░ÆņØ┤ ņłĀ ņĀä -27.5 dBņŚÉņä£ -26.4 dBļĪ£ Ļ▓Įļ»ĖĒĢśņ¦Ćļ¦ī ĒśĖņĀäļÉśņŚłĻ│Ā, ļŗżļźĖ ņŚ░ĻĄ¼ņŚÉņä£ļÅä ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀ Ēøä MDĻ░ÆņØ┤ ņłĀ ņĀäļ│┤ļŗż ĒśĖņĀäņØä ļ│┤ņśĆļŗż.18-21 ņØ┤ņÖĆ ņ£Āņé¼ĒĢśĻ▓ī ļ¦ÉĻĖ░ Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן(mean MD<-17.0 dB) ĒÖśņ×ÉļōżņØä ļīĆņāüņ£╝ļĪ£ ĒĢ£ Stewart et al22ņØś ņŚ░ĻĄ¼ņŚÉņä£ļÅä ļ░▒ļé┤ņןņłśņłĀ Ēøä MD ļ░Å PSDĻ░ÆņŚÉ Ēü░ ņ░©ņØ┤ ņŚåļŗżĻ│Ā ĒĢśņśĆļŗż. ļ░śļ®┤ņŚÉ, Chen and Budenz23ņØś ņŚ░ĻĄ¼ņŚÉņä£ļŖö Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן ĒÖśņ×ÉļōżņØś ļ░▒ļé┤ņןņłśņłĀ Ēøä ņŗ£ņĢ╝ņØś ļ│ĆĒÖöņŚÉ ļīĆĒĢśņŚ¼ Ļ▓ĮļÅä ļ░Å ņżæņ”ØļÅä ļģ╣ļé┤ņן ĒÖśņ×É(MD>-21.0dB)ļŖö MDĻ░ÆņØś ĒśĖņĀäņØ┤ Ēü¼ņ¦Ćļ¦ī(ļ│ĆĒÖöļ¤ē: 4.9 ┬▒ 3.1 dB) ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×É(MD<-21.0 dB)ļŖö Ēü░ ļ│ĆĒÖöĻ░Ć ņŚåļŗżĻ│Ā ĒĢśņśĆļŗż(ļ│ĆĒÖöļ¤ē: -2.4 ┬▒ 3.5 dB). ņóģĒĢ®ĒĢ┤ļ│┤ļ®┤, ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×ÉĻĄ░ņŚÉņä£ļÅä ļģ╣ļé┤ņןņØś ņżæļō▒ļÅä ļ░Å ĒÖśņ×ÉĻĄ░ņØś ĒŖ╣ņä▒ņŚÉ ļö░ļØ╝ņä£ ņłĀ Ēøä ņŗ£ņĢ╝ ļ│ĆĒÖöĻ░Ć ļŗżņ¢æĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņØ╝ ņłś ņ׳ļŗż. ņČöĒøä ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×Éļź╝ ņäĖļČĆ ļČäļźśĒĢśņŚ¼ ļ░▒ļé┤ņןņłśņłĀņØś ņśüĒ¢źņØä ļČäņäØĒĢśļŖö ņČöĻ░ĆņĀüņØĖ ņŚ░ĻĄ¼Ļ░Ć ļ│┤ņÖäļÉśņ¢┤ņĢ╝ ĒĢĀ Ļ▓āņØ┤ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņżæļō▒ļÅä ļģ╣ļé┤ņןĻĄ░(0.95 ┬▒ 0.84Ļ░£ vs. 0.85 ┬▒ 0.80Ļ░£)Ļ│╝ļŖö ļŗ¼ļ”¼ ļ¦ÉĻĖ░ ļģ╣ļé┤ņןĻĄ░ņŚÉņä£ ļģ╣ļé┤ņן ņĢłņĢĮ Ļ░£ņłśĻ░Ć ņ£ĀņØśĒĢśĻ▓ī Ļ░ÉņåīĒĢśņśĆļŗż(1.57 ┬▒ 0.70Ļ░£ vs. 1.34 ┬▒ 0.67Ļ░£). ņČöĻ░ĆņĀüņØĖ ļČäņäØ ļ░Å Ļ│Āņ░░ņØ┤ ĒĢäņÜöĒĢśĻ▓Āņ£╝ļéś ļ¦ÉĻĖ░ ļģ╣ļé┤ņןĻĄ░ņŚÉņä£ ņāüļīĆņĀüņ£╝ļĪ£ ņłĀ ņĀä ņĢłņĢĮ Ļ░£ņłśĻ░Ć ļ¦ÄĻĖ░ņŚÉ ņłĀ Ēøä Ļ░£ņłśņØś Ļ░ÉņåīĻ░Ć ņ£ĀņØśĒĢśĻ▓ī ļéśĒāĆļé¼ņØä Ļ░ĆļŖźņä▒ņØä ņāØĻ░üĒĢ┤ ļ│╝ ņłś ņ׳ļŗż. ĒĢśņ¦Ćļ¦ī ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļ¦ÉĻĖ░ ļģ╣ļé┤ņןĻĄ░ņØś ņןĻĖ░ņĀüņØĖ ņĢłņĢĢļÅä ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉ£ ņĀÉņØĆ, ņĢłņĢĢņĢĮ Ļ░£ņłś Ļ░Éņåī ĒÜ©Ļ│╝Ļ░Ć ļŹöņÜ▒ ņØśļ»Ė ņ׳ļŖö ņĀÉņØä ņŗ£ņé¼ĒĢ£ļŗż. ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ļģ╣ļé┤ņן ļ¦ÄņØĆ ņĢłņĢĮ ņé¼ņÜ®ņØĆ ņĢĮņĀ£ ļČĆņ×æņÜ®ņ£╝ļĪ£ ņØĖĒĢ£ ļČłĒÄĖĻ░ÉņØä ļåÆņØ┤Ļ│Ā, ņéČņØś ņ¦łņØä ņĀĆĒĢśņŗ£ĒéżĻĖ░ņŚÉ,1 ņĢłņĢĮ Ļ░£ņłś Ļ░ÉņåīļŖö ņł£ĻĖ░ļŖź ņĖĪļ®┤ņŚÉņä£ ņżæņÜöĒĢ£ Ļ▓░Ļ│╝ļĪ£ ļ│╝ ņłś ņ׳ļŗż.
ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉĻ▓īņä£ ļ░▒ļé┤ņןņłśņłĀ ņŗ£, ņłĀ Ēøä ĻĖēĻ▓®ĒĢ£ ņĢłņĢĢņāüņŖ╣ņØĆ ņ×äņāüņĀüņ£╝ļĪ£ Ēü░ ņ£äĒŚś ņÜöņåīĻ░Ć ļÉĀ ņłś ņ׳ļŗż. ņØ┤ļ¤¼ĒĢ£ ņĢłņĢĢņāüņŖ╣ņØĆ ņØ╝ņŗ£ņĀüņØ┤ņ¦Ćļ¦ī, ņØ┤ļ»Ė ļģ╣ļé┤ņןņä▒ ņŗ£ņŗĀĻ▓Į ņåÉņāüņØ┤ ņŗ¼ĒĢ£ ĒÖśņ×ÉņŚÉņä£ļŖö ļ╣äĻ░ĆņŚŁņĀüņØĖ ņŗ£ļĀź ļ░Å ņżæņŗ¼ ņŗ£ņĢ╝ ņāüņŗżņØä ņ┤łļלĒĢĀ ņłś ņ׳ļŗż.22,24 Yasutani et al25ņØś ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ░▒ļé┤ņןņłśņłĀ ļŗżņØī ļéĀ 30 mmHg ņØ┤ņāüņ£╝ļĪ£ ņś¼ļØ╝Ļ░ä IOP spikeņØś ļ╣äņ£©ņØ┤ ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉĻ▓ī 13%ļĪ£, ņĀĢņāü ļīĆņĪ░ĻĄ░ņŚÉ ļ╣äĒĢśņŚ¼ ļåÆņØĆ ņ¢æņāüņØä ĒÖĢņØĖĒĢśņśĆĻ│Ā, Slabaugh et al26ņØĆ 17%ņØś ļģ╣ļé┤ņן ĒÖśņ×ÉĻ░Ć ņłĀ ņĀäņŚÉ ļ╣äĒĢ┤ 50% ņØ┤ņāüņØś ņĢłņĢĢņāüņŖ╣ ļ╣äņ£©ņØä ļ│┤ņśĆļŗżĻ│Ā ļ░£Ēæ£ĒĢśņśĆļŗż. ĒĢśņ¦Ćļ¦ī ņ¢ĖĻĖēļÉ£ ņŚ░ĻĄ¼ļōżņŚÉņä£ IOP spikeļŖö ļģ╣ļé┤ņן ņĢłņĢĮņ£╝ļĪ£ ņĪ░ņĀłļÉśļŖö Ļ▓āņØ┤ ļīĆļČĆļČäņØ┤ņŚłĻ│Ā, ņ¦ĆņåŹ ņŗ£Ļ░äņØ┤ ĻĖĖņ¦Ć ņĢŖņØīņØä ĒÖĢņØĖĒĢśņśĆļŗż. ĒŖ╣Ē׳, ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö mild to moderateĻĄ░Ļ│╝ advancedĻĄ░ ņé¼ņØ┤ņŚÉ ņłśņłĀ ņ¦üĒøä IOP spikeņØś ļ╣äņ£©ņØĆ ĒåĄĻ│äĒĢÖņĀüņ£╝ļĪ£ ņ£ĀņØśļ»ĖĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż. ņØ┤ļź╝ ĒåĄĒĢ┤, ļ¦ÉĻĖ░ ļģ╣ļé┤ņן ĻĄ░ņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņĢłņĢĢ ļ│ĆĒÖöņŚÉ ņŻ╝ņØśļź╝ ĻĖ░ņÜĖņØ┤ļ®┤, ņłĀ Ēøä ĻĖēĻ▓®ĒĢ£ ņĢłņĢĢņāüņŖ╣ņØś ņ£äĒŚśļÅäĻ░Ć ņŗ¼Ļ░üĒĢśņ¦ĆļŖö ņĢŖņØä Ļ▓āņ£╝ļĪ£ ņČöļĪĀĒĢ┤ ļ│╝ ņłś ņ׳ļŗż.
ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļź╝ ĒĢ┤ņäØĒĢśĻ│Ā ņ×äņāüņĀüņ£╝ļĪ£ ņĀüņÜ®ĒĢśļŖö ļŹ░ ņ׳ņ¢┤ ļ¬ć Ļ░Ćņ¦Ć ņŻ╝ņØśĻ░Ć ņÜöĻĄ¼ļÉ£ļŗż. ņ▓½ņ¦Ė, ĒøäĒ¢źņĀü ļ░®ļ▓Ģņ£╝ļĪ£ ļŗ©ņØ╝ĻĖ░Ļ┤ĆņŚÉņä£ ņŚ░ĻĄ¼ļź╝ ņłśĒ¢ēĒĢśņśĆĻĖ░ņŚÉ ņäĀĒāØ ĒÄĖĒ¢ź ņśżļźś(selection bias)ņØś Ļ░ĆļŖźņä▒ņØ┤ ņĪ┤ņ×¼ĒĢ£ļŗż. ļæśņ¦Ė, ņĀäņ▓┤ ļīĆņāüĻĄ░ņØś ņĀäļ░® Ļ│äņĖĪņ╣śņŚÉ ļīĆĒĢ£ ĒÅēĻ░ĆĻ░Ć Ļ▓░ņŚ¼ļÉśņ¢┤ ņ׳ļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö Ļ░£ļ░®Ļ░üļģ╣ļé┤ņן ĒÖśņ×Éļ¦īņØä ĒżĒĢ©ĒĢśņśĆņ£╝ļéś, ņĀäļ░®Ļ░üņØś Ļ░£ļ░® ņĀĢļÅäņŚÉ ļö░ļØ╝ ņĢłņĢĢĒĢśĻ░Ģ ņĀĢļÅäĻ░Ć ņśüĒ¢źņØä ļ░øņØä ņłś ņ׳ņØä Ļ▓āņ£╝ļĪ£ ļ│┤ņŚ¼ņ¦äļŗż.27 ļśÉĒĢ£ ļ░▒ļé┤ņןņłśņłĀņØĆ ļģ╣ļé┤ņן ņĀäļ¼ĖņØśņØĖ 2ņØĖņØś ņłĀņ×ÉņŚÉ ņØśĒĢśņŚ¼ ļÅÖņØ╝ĒĢ£ ņłśņłĀ ĻĖ░ĻĄ¼ ļ░Å ņØĖĻ│ĄņłśņĀĢņ▓┤ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņłśĒ¢ēļÉśņŚłņ£╝ļéś, ņłĀ ņ×ÉņØś ņłÖļĀ©ļÅäņŚÉ ļö░ļØ╝ ņłĀņ×É Ļ░äņØś ņłśņłĀ ņŗ£Ļ░äņØ┤ļéś ĒĢ®ļ│æņ”Ø ļ░£ņāØ ļ╣łļÅäņŚÉ ņ░©ņØ┤Ļ░Ć ņ׳ņØä ņłś ņ׳ļŗż. ļüØņ£╝ļĪ£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļ¦ÉĻĖ░ ļģ╣ļé┤ņןņØĆ ņŗ£ņĢ╝Ļ▓Ćņé¼ ĻĖ░ņżĆņ£╝ļĪ£ -12 dB ņØ┤ĒĢśļĪ£ ņĀĢņØśĒĢśņśĆņ¦Ćļ¦ī, ņØ┤ ņżæ ņŗżņĀ£ļĪ£ terminal stage (<-20 dB)ņŚÉ ĒĢ┤ļŗ╣ļÉśļŖö ņŗ¼Ļ░üĒĢ£ ļģ╣ļé┤ņן ņāüĒā£ļŖö ņØ╝ļČĆņŚÉ ļČłĻ│╝ĒĢśļŗż. ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ╣äĻ░ĆņŚŁņĀüņØĖ ņżæņŗ¼ ņŗ£ļĀź ņåīņŗż(wipe out Ēśäņāü)Ļ│╝ ņŗ¼Ļ░üĒĢ£ ĒĢ®ļ│æņ”Ø ļ╣łļÅäļź╝ ļČäņäØĒĢśĻĖ░ņŚÉļŖö ĒĢ£Ļ│äĻ░Ć ņ׳ļŗż. ĻĘĖļ¤¼ļ»ĆļĪ£ ļ│Ė ņŚ░ĻĄ¼ļź╝ terminal stageņØś ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ņ×äņāüņŚÉ ņĀüņÜ®ĒĢĀ ļĢīņŚÉļŖö Ļ░üļ│äĒĢ£ ņŻ╝ņØśĻ░Ć ņÜöĻĄ¼ļÉ£ļŗż.
ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ ļ¦ÉĻĖ░ ļģ╣ļé┤ņןņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀņØĆ Ļ▓ĮļÅä ļ░Å ņżæļō▒ļÅä ļģ╣ļé┤ņןĻĄ░Ļ│╝ ļ╣äĻĄÉĒĢśņśĆņØä ļĢī ņŗ£ļĀź Ļ░£ņäĀ ļ░Å ņĢłņĢĢĒĢśĻ░ĢņØś ĒÜ©Ļ│╝ ņĖĪļ®┤ņŚÉņä£ ņ£Āņé¼ĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż. ņĢäņÜĖļ¤¼, ņŗ£ņĢ╝ ņĢģĒÖö ļ░Å ĒĢ®ļ│æņ”Ø ļ░£ņāØ ņĖĪļ®┤ņŚÉņä£ļÅä ņŚ┤ļō▒ĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢä, ņĢłņĀäņä▒ ņĖĪļ®┤ņŚÉņä£ļÅä ļ╣äĻĄÉņĀü ņ£äĒŚśĒĢśņ¦Ć ņĢŖņØīņØä ĒÖĢņØĖĒĢśņśĆļŗż. ņ×äņāüņĀü ņ£äĒŚśļÅäļź╝ Ļ│ĀļĀżĒĢśļ®░ ņĢłņĢĢ ļ│ĆĒÖöņŚÉ ĒŖ╣Ē׳ ņŻ╝ņ£äļź╝ ĻĖ░ņÜĖņØ┤ļŖö Ļ░ĆņÜ┤ļŹ░, ļ¦ÉĻĖ░ ļģ╣ļé┤ņןĻĄ░ņŚÉņä£ļÅä ņŗ£ļĀź ĒśĖņĀäņØä ņ£äĒĢ┤ ļ░▒ļé┤ņן ņłśņłĀņØä ņČ®ļČäĒ׳ Ļ│ĀļĀżĒĢ┤ļ│╝ ņłś ņ׳Ļ▓Āļŗż. ņČöĒøä ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļź╝ ļ│┤ņÖäĒĢśĻ│Ā ņØ╝ļ░śĒÖöĒĢśĻĖ░ ņ£äĒĢ┤ ņäĖļČĆ ļČäņäØ ļ░Å ļŗżĻĖ░Ļ┤Ć ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢśļŗżĻ│Ā ĒīÉļŗ©ļÉ£ļŗż.
Figure┬Ā1.
Serial changes of mean IOP * at each time point. Preop = preoperative; POD = postoperative day; d = day; mo = month; y = year; IOP = intraocular pressure. * No difference in IOP between the mild to moderate and advanced groups at all time points (all Ps > 0.05).
Figure┬Ā2.
Representative cases of a mild to moderate and advanced glaucoma group after cataract surgery. Preop = preoperative; BCVA = best corrected visual acuity; IOP = intraocular pressure; MD = mean deviation; PSD = pattern standard deviation; Postop = postoperative; yr = year.
Table┬Ā1.
Demographics and clinical characteristics of each group of mild to moderate and advanced glaucoma group
| Characteristics | Mild to moderate glaucoma | Advanced glaucoma | p-value | |
|---|---|---|---|---|
| Number of eyes | 109 | 87 | ||
| Age (years) | 69.6 ┬▒ 10.4 | 75.0 ┬▒ 10.7 | <0.001 | |
| Sex, M/F | 37/72 | 53/34 | <0.001 | |
| Type of glaucoma | 0.111 | |||
| NTG | 56 (51) | 55 (63) | ||
| POAG | 12 (11) | 16 (18) | ||
| PXFG | 2 (2) | 1 (1) | ||
| Other | 39 (36) | 15 (17) | ||
| Systemic disease | ||||
| Hypertension | 61 (55) | 49 (56) | 0.780 | |
| Diabetes mellitus | 31 (28) | 26 (29) | 0.874 | |
| Spherical equivalent | 0.00 ┬▒ 3.46 | 0.39 ┬▒ 2.03 | 0.503 | |
| Axial length | 23.43 ┬▒ 1.35 | 23.32 ┬▒ 1.03 | 0.145 | |
| Central corneal thickness | 549.12 ┬▒ 64.28 | 536.53 ┬▒ 34.12 | 0.202 | |
| Lens status (LOCS)* | 1.18 ┬▒ 0.45 | 1.37 ┬▒ 0.61 | 0.014 | |
| preop BCVA | 0.47 ┬▒ 0.29 | 0.39 ┬▒ 0.26 | 0.067 | |
| preop IOP (mmHg) | 16.50 ┬▒ 8.33 | 16.41 ┬▒ 6.41 | 0.930 | |
| Number of glaucoma medications | 0.95 ┬▒ 0.84 | 1.57 ┬▒ 0.70 | <0.001 | |
| Prostaglandin analogues, % | 42.2 (46/109) | 92.0 (80/87) | <0.001 | |
| ╬▓-blockers, % | 44.0 (48/109) | 62.0 (54/87) | 0.012 | |
| CAIs, % | 29.3 (32/109) | 55.1 (48/87) | <0.001 | |
| ╬▒-adrenergics, % | 16.5 (18/109) | 1.0 (27/87) | 0.016 | |
| preop VF, MD (dB) | -10.07 ┬▒ 6.97 | -18.32 ┬▒ 7.75 | <0.001 | |
| preop VF, PSD (dB) | 6.00 ┬▒ 3.57 | 6.89 ┬▒ 3.29 | 0.127 | |
| Duration of follow up (months) | 17.64 ┬▒ 7.44 | 34.80 ┬▒ 39.6 | ||
Data are presented as mean ┬▒ standard deviation or number (%) unless otherwise indicated.
M/F = male/female; NTG = normal tension glaucoma; POAG = primary open angle glaucoma; PXFG = pseudoexfoliation glaucoma; LOCS = Lens Opacity Classification System; BCVA = best corrected visual acuity; IOP = intraocular pressure; CAIs = carbonic anhydrase inhibitors; VF = visual field; MD = mean deviation; PSD = pattern standard deviation.
Table┬Ā2.
Comparison of IOP changes in mild-moderate vs. advanced glaucoma group
| Mild to moderate glaucoma (mmHg) | Advanced glaucoma (mmHg) | p-value* | |
|---|---|---|---|
| Preop | 16.50 ┬▒ 8.33 | 16.41 ┬▒ 6.41 | 0.930 |
| POD 1 | 17.76 ┬▒ 6.93 | 18.84 ┬▒ 6.94 | 0.485 |
| 1 month | 13.64 ┬▒ 4.05 | 13.42 ┬▒ 3.76 | 0.441 |
| 3 months | 13.60 ┬▒ 3.64 | 12.87 ┬▒ 3.32 | 0.793 |
| 6 months | 14.29 ┬▒ 4.18 | 13.42 ┬▒ 2.81 | 0.707 |
| 1 year | 13.94 ┬▒ 3.11 | 13.51 ┬▒ 2.69 | 0.784 |
| 2 years | 13.89 ┬▒ 2.65 | 13.71 ┬▒ 2.90 | 0.401 |
Table┬Ā3.
Comparison of IOP differences from preoperative value
|
Mild to moderate glaucoma (mmHg) |
Advanced glaucoma (mmHg) |
|||||
|---|---|---|---|---|---|---|
| Mean IOP | Mean diff.* | p-valueŌĆĀ | Mean IOP | Mean diff.* | p-valueŌĆĀ | |
| Preop | 16.50 ┬▒ 8.33 | 16.41 ┬▒ 6.41 | ||||
| POD 1 | 17.76 ┬▒ 6.93 | +0.98 | 0.221 | 18.84 ┬▒ 6.94 | +2.43 | 0.018 |
| 1 month | 13.64 ┬▒ 4.05 | -2.87 | 0.001 | 13.42 ┬▒ 3.76 | -3.00 | 0.001 |
| 3 months | 13.60 ┬▒ 3.64 | -2.91 | <0.001 | 12.87 ┬▒ 3.32 | -3.54 | <0.001 |
| 6 months | 14.29 ┬▒ 4.18 | -2.21 | 0.012 | 13.42 ┬▒ 2.81 | -2.99 | <0.001 |
| 1 year | 13.94 ┬▒ 3.11 | -2.57 | 0.003 | 13.51 ┬▒ 2.69 | -2.91 | <0.001 |
| 2 years | 13.89 ┬▒ 2.65 | -2.62 | 0.004 | 13.71 ┬▒ 2.90 | -2.70 | 0.001 |
Table┬Ā4.
Comparison of BCVA in mild to moderate vs. advanced glaucoma group
|
Mild to moderate glaucoma |
Advanced glaucoma |
|||
|---|---|---|---|---|
| Preop | POD 1 year | Preop | POD 1 year | |
| BCVA | 0.47 ┬▒ 0.29 | 0.86 ┬▒ 0.26 | 0.39 ┬▒ 0.26 | 0.77 ┬▒ 0.25 |
| Mean diff.* | 0.390 | 0.380 | ||
| p-valueŌĆĀ | <0.001 | <0.001 | ||
Table┬Ā5.
Changes of MD and PSD value in visual filed test after postoperative 1 year
|
Mild to moderate glaucoma |
Advanced glaucoma |
|||
|---|---|---|---|---|
| Preop | POD 1 year | Preop | POD 1 year | |
| MD | -10.07 ┬▒ 6.97 | -9.65 ┬▒ 8.12 | -18.32 ┬▒ 7.75 | -19.22 ┬▒ 8.32 |
| Mean diff.* | 0.420 | -0.400 | ||
| p-valueŌĆĀ | 0.768 | 0.561 | ||
| PSD | 6.00 ┬▒ 3.57 | 6.38 ┬▒ 3.73 | 6.89 ┬▒ 3.29 | 7.29 ┬▒ 03.29 |
| Mean diff.* | 0.380 | 0.400 | ||
| p-valueŌĆĀ | 0.576 | 0.536 | ||
Table┬Ā6.
Changes of the number of antiglaucoma medications at postoperative 1 year
|
Mild to moderate glaucoma |
Advanced glaucoma |
|||
|---|---|---|---|---|
| Preop | POD 1 year | Preop | POD 1 year | |
| Number of antiglaucoma medications | 0.95 ┬▒ 0.84 | 0.85 ┬▒ 0.80 | 1.57 ┬▒ 0.70 | 1.34 ┬▒ 0.67 |
| Mean diff.* | -0.100 | -0.220 | ||
| p-valueŌĆĀ | 0.366 | 0.030 | ||
Table┬Ā7.
Comparison of cataract surgery-related complications and associated factors
| Mild to moderate glaucoma | Advanced glaucoma | p-value | |
|---|---|---|---|
| Pseudoexfoliation | 2 (1.83) | 1 (1.15) | 0.698 |
| Intraoperative complications* | 8 (7.34) | 8 (9.20) | 0.637 |
| IOP spike rateŌĆĀ | 12 (11.01) | 11 (12.64) | 0.200 |
REFERENCES
1) Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311:1901-11.



2) Musch DC, Lichter PR, Guire KE, Standardi CL. The collaborative initial glaucoma treatment study: study design, methods, and baseline characteristics of enrolled patients. Ophthalmology 1999;106:653-62.


3) Friedman DS, Jampel HD, Lubomski LH, et al. Surgical strategies for coexisting glaucoma and cataract: an evidence-based update. Ophthalmology 2002;109:1902-13.


4) Mansberger SL, Gorden MO, Jampel H, et al. Reduction in intraocular pressure after cataract extraction. Ophthalmology 2012;119:1826-31.


5) Samuelson TW, Katz LJ, Wells JM, et al. Randomized evaluation of the trabecular mico-bypass stent with phacoemulsification in patients with glaucoma and cataract. Ophthalmology 2011;118:459-67.


6) Liu CJ, Cheng CY, Ko YC, Lau LI. Determinants of long-term intraocular pressure after phacoemulsification in primary angle-closure glaucoma. J Glaucoma 2011;20:566-70.


7) Lam DS, Leung DY, Tham CC, et al. Randomized trial of early phacoemulsification versus peripheral iridotomy to prevent intraocular pressure rise after acute primary angle closure. Ophthalmology 2008;115:1134-40.


8) Nonaka A, Kondo T, Kikuchi M, et al. Angle widening and alteration of ciliary process configuration after cataract surgery for primary angle closure. Ophthalmology 2006;113:437-41.


9) Jacobi PC, Dietlein TS, L├╝ke C, et al. Primary phacoemulsification and intraocular lens implantation for acute angle-closure glaucoma Historical image. Ophthalmology 2002;109:1597-603.


10) Chen PP, Lin SC, Junk AK, et al. The effect of phacoemulsification on intraocular pressure in glaucoma patients: a report by the American Academy of Ophthalmology. Ophthalmology 2015;122:1294-307.


11) Meyer MA, Savitt ML, Kopitas E. The effect of phacoemulsification on aqueous outflow facility. Ophthalmology 1997;104:1221-7.


12) Greve EL, Wagemans MJ. Extracapsular cataract extraction in primary open angle glaucoma. In: Greve EL, ed. Surgical management of coexisting glaucoma and cataract, 1st ed. Asterdam: Kugler publications, 1987;51-7.
13) Kim YN, Kang JH, Kim JS, Lee JH. Correlation between retinal nerve fiber layer thickness and visual field in normal tension glaucoma. J Korean Ophthalmol Soc 2005;46:1532-9.
15) Greve EL, Wagemans MJ. Reduction of intraocular pressure after extracapsular cataract extraction with posterior chamber intraocular lens implantation in patients with narrow angle. In: Greve EL, ed. Surgical management of coexisting glaucoma and cataract, 1st ed. Asterdam: Kugler publications, 1987;59-64.
16) Zamani M, Feghhi M, Azarkish A. Early changes in intraocular pressure following phacoemulsification. J Ophthalmic Vis Res 2013;8:25-31.


17) Altmeyer M, Wirbelauer C, H├żberle H, Pham DT. Cataract surgery in patients with end-stage glaucoma. Klin Monatsbl Augenheilkd 2006;223:297-302.


18) Hayashi K, Hayashi H, Nakao F, Hayashi F. Influence of cataract surgery on automated perimetry in patients with glaucoma. Am J Ophthalmol 2001;132:41-6.


19) Lam BL, Alward WL, Kolder HE. Effect of cataract on automated perimetry. Ophthalmology 1991;98:1066-70.


20) Smith SD, Katz J, Quigley HA. Effect of cataract extraction on the results of automated perimetry in glaucoma. Arch Ophthalmol 1997;115:1515-9.


21) Carrillo MM, Artes PH, Nicolela MT, et al. Effect of cataract extraction on the visual fields of patients with glaucoma. Arch Ophthalmol 2005;123:929-32.


22) Stewart WC, Rogers GM, Crinkley CM, Carlson AN. Effect of cataract extraction on automated fields in chronic open-angle glaucoma. Arch Ophthalmol 1995;113:875-9.


23) Chen PP, Budenz DL. The effects of cataract extraction on the visual field of eyes with chronic open-angle glaucoma. Am J Ophthalmol 1998;125:325-33.


24) Handa J, Henry JC, Krupin T, Keates E. Extracapsular cataract extraction with posterior chamber lens implantation in patients with glaucoma. Arch Ophthalmol 1987;105:765-9.


25) Yasutani H, Hayashi K, Hayashi H, Hayashi F. Intraocular pressure rise after phacoemulsification surgery in glaucoma patients. J Cataract Refract Surg 2004;30:1219-24.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 709 View
- 56 Download
- Related articles
-
Research on the Quality of Life of Glaucoma Patients.2014 December;55(12)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



