 |
 |
| J Korean Ophthalmol Soc > Volume 64(4); 2023 > Article |
|
국문초록
목적
Anterion®으로 측정한 안구 생체계측과 Lenstar LS900®, Essilor AKR 750®, PacScan300A®로 측정한 안구계측을 비교하여 Anterion®의 유용성을 알아보고자 하였다.
대상과 방법
환자 47명, 86안을 선정하여 Anterion®, Lenstar®로 안축장, 수정체두께, 중심각막두께, 전방깊이, 각막곡률, AKR 750®으로 각막곡률, PacScan 300A®로 안축장을 측정 후, 차이값과 상관관계를 확인했으며, 급내상관계수와 Bland-Altman plot으로 일치도를 분석하였다.
결과
Anterion®, Lenstar®로 측정한 안축장, 수정체두께, 중심각막두께, 전방깊이, 각막윤부직경은 -0.02 ± 0.08, 0.08 ± 0.13, -2.66 ± 11.12, 0.05 ± 0.12, 0.08 ± 0.26으로 유의미한 차이를 보였다. Anterion®과 Lenstar®로 측정한 평균 각막굴절력은 -0.08 ± 0.47로 유의미한 차이를 보인 반면, AKR 750®와 비교했을 때는 차이가 없었다. Anterion®의 측정값은 다른 기기의 측정값과 피어슨 상관계수를 검증했을 때 강한 양의 상관관계를 보였고 급내상관계수, Bland-Altman plot에서 높은 일치도를 보였다.
ABSTRACT
Purpose
We compared optical biometric measurements made using new swept-source optical-coherence tomography, low-coherence reflectometry, autokeratometry, and A-scan biometry.
Methods
In total, 86 eyes of 47 patients were included. Axial length, lens thickness, central corneal thickness, anterior chamber depth, and corneal curvature were measured using the Anterion® (Heidelberg Engineering, inc., Heidelberg, Germany) and Lenstar LS 900® (Haag-Streit AG, Koeniz, Switzerland) platforms. Corneal curvature and axial length were measured using the Essilor AKR 750® (Essilor instruments, France, Charenton-le-Pont) and PacScan 300A® (Sonomed Inc., Chicago, IL, USA) platforms, respectively. The evaluated biometric parameters were compared and verified; intraclass correlation coefficients and Bland-Altman plots were used to analyze statistical agreement.
Results
The differences between the Anterion® and Lenstar LS 900® platforms in terms of axial length, lens thickness, central corneal thickness, anterior chamber depth, and white-to-white diameter were -0.02 ± 0.08, 0.08 ± 0.13, -2.66 ± 11.12, 0.05 ± 0.12, and 0.08 ± 0.26, respectively. All values were statistically significant. The mean corneal curvature between Anterion® and Lenstar LS 900® had a statistically significant difference of -0.08 ± 0.47, while the difference between the Anterion® and AKR 750® platforms was not significant. Biometric parameters measured using an Anterion® and other devices showed a strong positive correlation when assessed using Pearson’s correlation analysis; there was good agreement between the results when analyzed using intraclass correlation coefficients and Bland-Altman plots.
Conclusions
Optical biometric measurements made using the Anterion® platform were not significantly different from those obtained using other devices, but there were significant differences compared to the Lenstar LS 900® platform. Since these significant differences could influence decision making during intraocular lens selection for cataract surgery, the values are clinically useful for reference.
안축장과 각막곡률, 전방깊이, 수정체두께는 백내장수술에서 정확한 인공수정체를 선택하는 데 고려해야 할 중요한 요소이다.1,2 Olsen3은 백내장수술 후 목표하는 굴절값이 다른 이유를 안축장(54%), 각막곡률(8%), 전방깊이(38%)의 부정확한 측정을 보고한 바 있다. 정확한 각막곡률 측정은 각막굴절수술 시 우수한 시력 결과를 결정 짓게 되며, 수술 후 경과 관찰 시 합병증 발생의 진행을 확인하기 위해 필요하다. 중심각막두께는 각막굴절교정수술에서 술 전에 필수적으로 측정해야 하며, 안압을 측정할 때 영향을 미치므로, 녹내장을 비롯한 다양한 질환에서 고려해야 할 계측이다.4-7 각막윤부직경 역시 후방유수정체 안내렌즈삽입술에서 인공수정체의 크기를 결정하는 섬모체고랑거리를 임상적으로 유추할 수 있는 중요한 계측이다.8
안과적 질환의 진단과 치료를 위해서는 정확한 안구 생체 계측이 필요하고 이를 위해 다양한 기기가 이용되고 있다. 대표적으로 A-scan을 이용한 안축장 측정,9 자동굴절검사기(autorefractor & keratometer), 각막지형도(tophography) 등을 이용한 각막곡률의 측정이 있으며, 부분결합간섭기계(partial-coherence interferometry), 저간섭성반사계(low-coherence reflectometry)를 이용한 안구 생체계측 역시 많이 사용되고 있다.10 최근에는 파장가변 빛간섭단층촬영기(swept-source optical-coherence tomography)를 이용하여 더욱 정확하게 계측을 할 수 있도록 노력이 이루어지고 있다.
Anterion®(Heidelberg Engineering, inc., Heidelberg, Germany)은 새로운 고해상도 파장가변 방식의 빛간섭단층촬영 기기로서, 14.0 mm의 깊이, 16.5 mm의 폭, 14-32 mm의 안축장을 1,300 nm의 긴 파장의 광원으로 측정하며, 전면 각막표면부터 후면 수정체표면을 포함하는 자세한 구조적 이미지를 재현할 수 있다.11
국내에서는 Kim et al12이 파장가변 빛간섭단층촬영기(Anterion®)와 부분결합간섭기계(IOL Master 500®, Zeiss, Oberkochen, Germany)로 측정한 안축장과 각막곡률의 일치도를 비교하였고, Oh et al13은 파장가변 빛간섭단층촬영기(Anterion® and Casia2®, Tomey, Nagoya, Japan) 두 기기와 부분결합간섭기계(IOL Master 700®)로 측정한 안축장, 각막곡률, 수정체두께, 중심각막두께, 전방깊이를 비교하였다. Anterion®은 다양한 안구 생체계측치를 한번에 측정할 수 있는 유용한 기기로 알려져 있으나, 아직은 한국인을 대상으로 한 Anterion®과 다른 다양한 기존 생체계측 기기들과 비교를 한 연구가 부족한 실정이다. 이에 본 연구에서는 Anterion®로 측정한 안구 생체계측과 저간섭성반사계(Lenstar LS 900®, Haag-Streit AG, Koeniz, Switzerland), A-Scan(PacScan 300A®, Sonomed Inc., Chicago, IL, USA) 자동굴절검사기(Essilor AKR 750®, Essilor instruments, Charentonle-Pont, France)로 측정한 안구 생체계측치의 차이, 상관성, 일치도를 평가하여 Anterion®의 임상에서의 유용성을 확인해보고자 하였다.
본 연구는 헬싱키선언(Declaration of Helsinki)을 준수하였고, 본원 연구윤리심의위원회(Institutional Review Board)의 승인을 받았으며(승인 번호: 116286-202206-HR-01) 2021년 3월에 본원 안과 외래에 내원한 환자 47명, 86안을 무작위로 선정하였다. 대상자들 중 백내장수술 예정 환자는 15명이었고, 백내장수술을 통해 인공수정체를 삽입하거나 굴절교정수술, 각막이식을 시행한 환자들은 제외하였다. 또한 백내장수술을 하지 않았더라도 유리체출혈, 유리체혼탁, 각막혼탁, 과숙백내장 등이 있어 빛이 안저까지 통과하지 못해 부정확한 계측이 되는 환자들과, 군날개, 원추각막 등 각막곡률에 영향을 미칠 수 있는 질환을 가진 환자들 역시 제외하였다.
Anterion®, Lenstar LS900®으로 안축장, 각막곡률의 편평한 축과 가파른 축, 평균 각막굴절률, 수정체두께, 중심각막두께, 전방깊이, 각막윤부직경을 측정하였다. Essilor AKR 750 ®으로 각막곡률의 편평한 축과 가파른 축을 측정하였고 PacScan 300A®로 안축장을 측정하였다.
분석은 Statistical Package for Social Sciences version 22.0 (IBM Corp., Armonk, NY, USA)를 사용하였다. Anterion®, Lenstar LS900®으로 측정한 계측값들과 Anterion®, Essilor AKR 750®으로 측정한 계측값들의 차이는 paired-t test로 비교하였다. Anterion®, PacScan 300A®로 측정한 안축장의 차이값과 Lenstar LS900®, PacScan 300A®로 측정한 안축장의 차이값은 Wilcoxon signed-rank test with Bonferroni’s correction를 통해 비교하였다. 모든 계측값들은 상관관계 평가를 위해 피어슨 상관계수(Pearson correlation coefficient)를 계산하였고 0.1 이상 0.3 미만은 약한 양적 상관관계, 0.3 이상 0.7 미만은 뚜렷한 양적 상관관계, 0.7 이상이면 강한 양적 상관관계로 분류하였다. 또한 모든 계측값들의 급내상관계수(intraclass correlation coefficient)를 이차원변량 모델(단일 측정)로 계산하였고 0.4 미만은 좋지 않음(poor), 0.4 이상 0.6 미만은 보통(fair), 0.6 이상 0.75 미만은 좋음(good), 0.75 이상은 매우 좋음(excellent)으로 분류하였다. Bland-Altman plot을 그려 일치도를 평가하였다. p-value가 0.05 미만인 경우 통계적 유의성이 있는 것으로 하였다.
본 연구의 대상자 47명의 평균 연령은 62.55 ± 13.00세(40-87세)였으며 남자는 26명(55.3%), 여자는 21명(44.7%)이었다.
Anterion®, Lenstar LS900®, PacScan 300A®로 측정한 안축장의 평균은 각각 23.65 ± 2.88 mm, 23.92 ± 0.95 mm, 23.78 ± 0.93 mm였다. Anterion®과 Lenstar LS900®으로 측정한 안축장의 차이값은 -0.02 ± 0.08 mm로 두 군 간에 유의한 차이를 보였다(p=0.04). Anterion®과 PacScan 300A®, Lenstar LS900®과 PacScan 300A®로 측정한 안축장의 값은 각각 0.00 ± 0.08, 0.04 ± 0.09였으나 두 군 간의 의미 있는 차이를 보이지 않았다(p>0.05, Table 1).
Anterion®, Lenstar LS900®으로 측정한 수정체두께는 각각 4.66 ± 0.41 mm, 4.58 ± 0.43 mm, 중심각막두께는 542.12 ± 32.75 µm, 544.71 ± 34.46 µm, 전방깊이는 3.22 ± 0.41 mm, 3.21 ± 0.34 mm, 각막윤부직경은 11.77 ± 0.45 mm, 11.85 ± 0.46 mm였다. Anterion®, Lenstar LS900®으로 측정한 차이값은 수정체두께가 0.08 ± 0.13 mm, 중심각막두께가 -2.66 ± 11.12 µm, 전방깊이가 0.05 ± 0.12 mm, 각막윤부직경이 0.08 ± 0.26 mm였으며 모두 두 군 간의 유의한 차이를 보였다(p<0.001, p=0.04, p=0.001, p=0.01, Table 2).
Anterion®, Lenstar LS900®, Essilor AKR 750®으로 측정한 각막곡률은 각각 평평한 축 43.03 ± 1.39 diopters (D), 43.13 ± 1.40 D, 42.88 ± 1.43 D, 가파른 축 44.01 ± 1.39 D, 44.14 ± 1.45 D, 44.03 ± 1.52 D, 평균 각막굴절력 43.52 ± 1.35 D, 43.65 ± 1.40 D, 43.46 ± 1.42 D였다(Table 3). Anterion®과 Lenstar LS900®의 편평한 축, 가파른 축, 평균 각막굴절력의 차이값은 -0.09 ± 0.36 D, -0.12 ± 0.35 D, -0.10 ± 0.29 D로 두 군 간에 유의한 차이를 보였다(p=0.02, p=0.002, p=0.02). Anterion®과 Essilor AKR 750®, Lenstar LS900®과 Essilor AKR 750®으로 측정한 각막곡률의 차이는 편평한 축이 각각 -0.04 ± 0.52 D, 0.04 ± 0.59 D, 가파른 축 -0.11 ± 0.53 D, -0.05 ± 0.59 D, 평균 각막굴절력이 -0.08 ± 0.47 D, -0.02 ± 0.54 D였으나 유의하지 않았다(p>0.05, Table 3).
상관관계 분석에서 안축장의 피어슨 상관계수는 Anterion®과 Lenstar LS900®에서 0.977, Anterion®과 PacScan 300A®에서 0.997, Lenstar LS900®과 PacScan 300A®에서 0.994로 모두 강한 양의 상관관계를 보였다(p<0.001, Table 4).
Anterion®과 Lenstar LS900®으로 측정한 수정체두께, 중심각막두께, 전방깊이, 각막윤부직경의 피어슨 상관계수는 각각 0.947, 0.947, 0.934, 0.842였으며 모두 강한 양의 상관관계를 보였다(p<0.001, Table 5).
Anterion®, Lenstar LS900®으로 측정한 편평한 축, 가파른 축, 평균 각막굴절력의 피어슨 상관계수는 각각 0.968, 0.971, 0.977이었으며, Anterion®, Essilor AKR 750®으로 측정한 편평한 축, 가파른 축, 평균 각막굴절력의 피어슨 상관계수는 각각 0.932, 0.937, 0.943이었으며, Lenstar LS900®, Essilor AKR 750®로 측정한 편평한 축, 가파른 축, 평균 각막굴절력의 피어슨 상관계수는 각각 0.911, 0.922, 0.924였고 모두 강한 양의 상관관계를 보였다(p<0.001, Table 6).
Anterion®, Lenstar LS900®으로 측정한 안축장의 급내상관계수는 0.998, Anterion®, PacScan 300A®의 경우는 0.997, Lenstar LS900®, PacScan300A®는 0.998이었으며 모두 매우 좋음(excellent)으로, 높은 일치도를 보였다(p<0.001, Table 4).
Anterion®와 Lenstar LS900®으로 측정한 수정체두께, 중심각막두께, 전방깊이, 각막윤부직경의 급내상관계수는 각각 0.964, 0.971, 0.961, 0.908이었으며 모두 매우 좋음(excellent)으로 높은 일치도를 보였다(p<0.001, Table 5).
Anterion®, Lenstar LS900®으로 측정한 편평한 축, 가파른 축, 평균 각막굴절력의 급내상관계수는 각각 0.983, 0.983, 0.987이었으며, Anterion®, Essilor AKR 750®으로 측정한 편평한 축, 가파른 축, 평균 각막굴절력의 급내상관계수는 각각 0.965, 0.965, 0.970이었으며, Lenstar LS900®, Essilor AKR 750®으로 측정한 편평한 축, 가파른 축, 평균 각막굴절력의 급내상관계수는 각각 0.953, 0.959, 0.961이었고 모두 매우 좋음(excellent)으로 높은 일치도를 보였다(p<0.001, Table 6).
Bland-Altman plot을 이용한 일치도 분석에서 95% limits of agreement (LoA) 구간은 Anterion®와 Lenstar LS900®으로 측정한 안축장은 0.13 to -0.17 mm, Lenstar LS900®와 PacScan 300A®는 0.15 to -0.22 mm, Lenstar LS900®과 PacScan 300A®는 0.16 to -0.16 mm였다(Fig. 1). Anterion®과 Lenstar LS900®으로 측정한 전방깊이, 수정체두께, 중심각막두께, 각막윤부직경의 LoA는 0.30 to -0.19 mm, 0.34 to -0.19 mm, 19.13 to -24.45 mm, 0.43 to -0.58 mm였다(Fig. 2). Anterion®과 Lenstar LS900®으로 측정한 편평한 축의 LoA 구간은 0.60 to -0.79 mm, Lenstar LS900®과 Essilor AKR 750®은 0.98 to -1.05 mm, Lenstar LS900®과 Essilor AKR 750®은 0.98 to -1.09 mm였다(Fig. 3). Anterion®과 Lenstar LS900®으로 측정한 가파른 축의 LoA 구간은 0.56 to -0.81 mm, Lenstar LS900®과 Essilor AKR 750®은 0.93 to -1.16 mm, Lenstar LS900®과 Essilor AKR 750®은 1.10 to -1.20 mm였다(Fig. 4).
Fişuş et al14은 최초로 Anterion®과 IOL Master 700®으로 측정한 안축장, 각막곡률, 수정체두께, 중심각막두께, 전방 깊이를 비교하여 기기 간에 높은 연관성을 확인하였다. Ruíz-Mesa et al15은 Anterion®으로 안축장, 각막곡률, 동공 직경, 중심각막두께, 전방깊이, 전방 용적 등을 반복해서 측정하였을 때 좋은 재현성을 보였다는 것을 보고하였다.
국내에서는 Kim et al12이 Anterion®과 IOL Master 500®으로 측정한 안축장과 각막곡률이 높은 일치도를 보였음을 보고하였다. 또한 Oh et al13은 Anterion®, Casia2®두 기기와 부분 결합간섭기계를 측정한 안축장, 각막곡률, 수정체두께, 중심각막두께, 전방깊이를 비교하였고 전체 각막곡률을 제외한 다른 계측들은 높은 일치도가 확인되었다.
본 연구에서도 각 기기 간의 안구 생체계측치는 앞서 언급한 기존 연구들12-15처럼 모두 강한 양의 상관관계를 보였고 급내상관계수와 Bland-Altman plot에서도 높은 일치도를 보였다. 그러나 Anterion®과 Lenstar LS900®으로 측정한 안축장 수정체두께, 중심각막두께, 전방깊이, 각막윤부직경, 각막곡률의 값은 통계적으로 의미 있는 차이를 보였다.
안축장과 각막곡률은 백내장수술에서 인공수정체의 도수를 결정하는 아주 중요한 계측이므로 Anterion®이 백내장수술 전 렌즈를 결정하는 기존 기기를 대체할 수 있을지 판단하기 위해서는 Anterion®과 기존 기기의 안축장, 각막곡률의 차이값에 대한 고찰이 필요할 것으로 생각된다.
Eibschitz-Tsimhoni et al 16 은 안축장이 0 mm에서 0.05 mm 차이날 때 백내장수술 후 0.1 D 이하의 굴절 오류가 발생한다고 보고하였다. 본 연구에서 Anterion®, Lenstar LS900® 안축장의 차이값은 0.02 ± 0.08 mm로 Anterion®이 더 작게 측정되었고 그로 인한 안축장의 차이값으로 인한 백내장수술 후 오차 역시 0.1 D 이하로 예측해 볼 수 있다.
Anterion®과 PacScan 300A®, Lenstar LS900®과 PacScan 300A®로 측정한 안축장의 피어슨 상관계수는 각각 0.997, 0.994로 아주 강한 양의 상관관계를 보였고(Table 4), 차이값은 -0.00 ± 0.08, -0.04 ± 0.09 mm였으나 통계적으로 유의한 차이가 없었다(Table 1). Anterion®과 Lenstar LS900®으로 계측한 안축장의 피어슨 상관계수는 0.997로 아주 강한 양의 상관관계를 보였지만, 차이값은 -0.02 ± 0.08로 두 군 간에 유의미한 차이를 보였다. PacScan 300A®와 Lenstar LS900®으로 측정한 안축장의 차이는 0.04 ± 0.09 mm로 Anterion®과 Lenstar LS900®의 안축장 차이값 -0.02 ± 0.08 mm에 비해 큰 수치가 확인되었지만, 통계적으로는 PacScan 300A®와 Lenstar LS900®의 계측값 차이가 없는 것으로 확인되었다(Table 1). 이는 PacScan 300A®를 측정한 대상군이 Anterion®과 Lenstar LS900®의 대상군보다 작아 PacScan 300A®을 포함한 계측의 차이값을 비교할 때 다른 통계적 방법이 적용되었기 때문에 나타난 결과로 생각되며, 본 연구에서 PacScan 300A®와 Anterion®, Lenstar LS900®으로 측정한 안축장의 차이값에 대한 결과는 임상에서 일반적으로 적용하기는 한계가 있을 것으로 생각된다.
본 연구에서 Anterion®, Lenstar LS900®으로 계측한 편평한 축, 가파른 축, 평균 각막굴절력의 차이값은 -0.09 ± 0.36 D, -0.12 ± 0.35 D, -0.10 ± 0.30 D로 두 군 간에 유의한 차이를 보였고, Anterion®과 Lenstar LS900®, Lenstar LS900®과 AKR 750®에서의 각막곡률에는 의미 있는 차이를 보이지 않았다(Table 3). 각막곡률의 측정은 Anterion®의 경우 3 mm 범위에 65 방사형 스캔을 통해 얻어지고, Lenstar LS900®은 1.65 mm의 안쪽 원과 2.3 mm의 바깥 원 2개 원에 각각 16개씩 나눠진, 32개의 광원을 각막에 조사하여 측정하고,17 AKR 750®은 3 mm zone의 각막곡률을 측정해서 얻어지게 된다. 이처럼 각막곡률은 기기마다 측정하는 기준 및 방법이 다르기 때문에 본 연구 결과의 기기 간의 측정치 차이를 통계적으로 큰 의미를 부여하기는 어려울 것으로 생각된다.
그러나 각 기기 간의 상관계수가 0.9 이상으로 강한 양의 상관관계를 보였고, 매우 좋은(excellent) 급내상관계수가 확인되었으므로 임상적으로 기기 간의 참고 수치로 활용하는 것은 고려해 볼 수 있다. 또한 각 기기 간의 각막곡률의 차이가 평균적으로 0.1 D 이내로 측정되었다는 점으로 보았을 때, Eibschitz-Tsimhoni et al 16 이 각막곡률이 1 D 차이가 발생할 때 0.8에서 1.3 D의 차이가 있을 수 있음을 보고하였던 것을 고려하면, 백내장수술 시 인공수정체 도수 선정에 있어서 큰 차이를 보이지 않을 것으로 생각된다.
그러나 본 연구에서 안축장과 각막곡률의 차이값에 따른 인공수정체의 도수 차이 값이 작을 것으로 예측되었더라도, 백내장수술에서 인공수정체를 결정할 때는 안축장, 각막곡률, 전방깊이를 동시에 고려해야 된다는 사실은 간과해서는 안 된다. 실제로 Song et al18은 Anterion®과 IOL Master 700을 비교한 연구에서 계측값들이 높은 일치도를 보였고, 차이값은 안축장 0.01 ± 0.01 mm, 전방깊이 0.07 ± 0.01 mm, 평평한 축 -0.14 ± 0.01 mm, 가파른 축 -0.10 ± 0.04 mm로 본 연구처럼 작은 차이가 있었음을 보고하였다. 그럼에도 불구하고 SRK/T, Haigis, Barrett Universal II, Holladay 1으로 계산한 굴절이상 예측값과 수술 후 굴절이상값과 비교하였을 때, 두 기기 간의 차이가 있었고, Anterion®이 IOL Master 700®보다 나은 결과를 보이지 못하였으며, 대체할 수 없다고 판단하였다. 그렇기 때문에 Anterion®은 백내장수술 시 참고 수치로 활용은 가능할지라도, 아직은 Lenstar®를 대체할 수 있다고 판단할 수는 없으며, Anterion®과 Lenstar®로 측정한 수술 전 굴절이상 예측값과 수술 후 굴절이상값을 비교하여 Anterion®의 유용성을 평가하는 연구 역시 추가로 필요할 것으로 생각된다.
Ehlers et al7은 각막두께가 520 µm일 때 10 µm 마다 0.7 mmHg 차이를 보인다고 보고하였다. 본 연구에서 Anterion®과 Lenstar LS900®으로 측정한 중심각막두께의 차이값은 -2.66 ± 11.12 µm으로 유의미한 차이를 보였지만(Table 2) 이는 임상적으로 고려하면 안압에 큰 차이를 발생하지 않을 것으로 생각된다.
안내렌즈삽입술에 렌즈 크기를 결정할 때, 제조사(STAAR Surgical AG, Switzerland)는 Lenstar®로 각막윤부직경을 측정할 경우, 0.4 mm보다 작은 값에 비례하여 크기를 결정하도록 권고하고 있으며, 크기를 결정 짓는 측정값이 경계에 있을 때는 전방깊이 3.4 mm를 기준으로 안내렌즈 크기를 고려하도록 하고 있다. 후방유수정체 안내렌즈삽입술에서 렌즈는 보통 12.1 mm, 12.6 mm, 13.2 mm, 13.7 mm 네 가지 크기를 사용하는데, 본 연구에서 측정한 Anterion®, Lenstar® 각막윤부직경의 차이값은 0.08 ± 0.26 mm, 전방깊이는 0.05 ± 0.12 mm로(Table 2), 렌즈 크기 단위에 비해 작은 수치의 차이가 있었다. 그러나 각막윤부직경의 측정값이 기준치의 경계값으로 측정되거나, 전방깊이가 3.4 mm 경계로 측정될 경우에는 측정값의 차이가 렌즈의 크기에 영향을 미칠 수 있으므로 임상적으로 다른 결과를 만들 수 있다.
본 연구는 대상이 47명, 86안으로 적고, 연령대가 특정되지 않고 다양했으며, 오직 한국인으로만 대상으로 연구가 진행되었으며, 대상자들이 안축장 및 각막곡률에 영향을 미칠 수 있는 질환 외에 다른 질환은 고려하지 않고 무작위로 선정되었으며, 백내장수술의 활용에 주로 초점을 맞췄기 때문에 다른 질환에 대한 Anterion®의 유용성 평가가 부족한 것이 한계점으로 존재한다. 따라서 본 연구의 제한점을 보안한 질환별, 연령별, 대규모 연구가 필요할 것으로 생각된다.
결론적으로 Anterion®은 기존 기기들과 비교했을 때 차이의 절대값은 크지 않으나, Lenstar®의 경우 통계적으로 유의한 차이를 보인 지표들이 있었다. 백내장수술에서 인공수정체를 결정하는 등 임상 적용 시 기존 기기와 다른 결과를 만들 수 있기 때문에 주의할 필요가 있다.
Figure 1.
Bland-Altman plots for mean axial length obtained using Anterion®, Lenstar LS900® and PacScan 300A®. (A) Agreements of axial length in Anterion® and Lengstar LS900®. (B) Agreements of axial length in Anterion® and PacScan 300A®. (C) Agreements of axial of length in Lenstar LS900® and PacScan 300A®. SD = standard deviation.
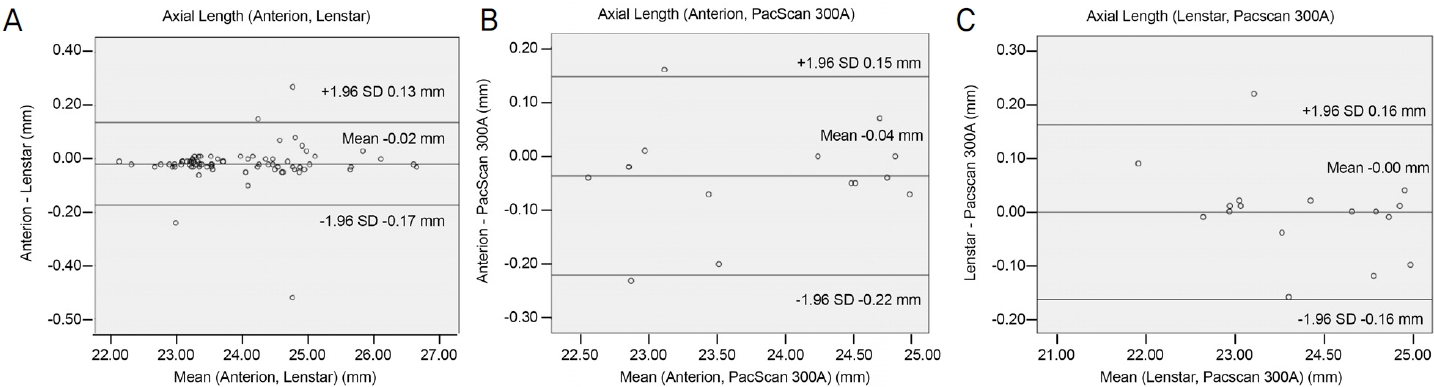
Figure 2.
Bland-Altman plots for mean ocular biometry in Anterion® and Lengstar LS900®. (A) Agreements of anterior chamber depth in Anterion® and Lengstar LS900®. (B) Agreements of lens thickness in Anterion® and Lengstar LS900®. (C) Agreements of white to white in Lenstar LS900® and Lengstar LS900®. SD = standard deviation.
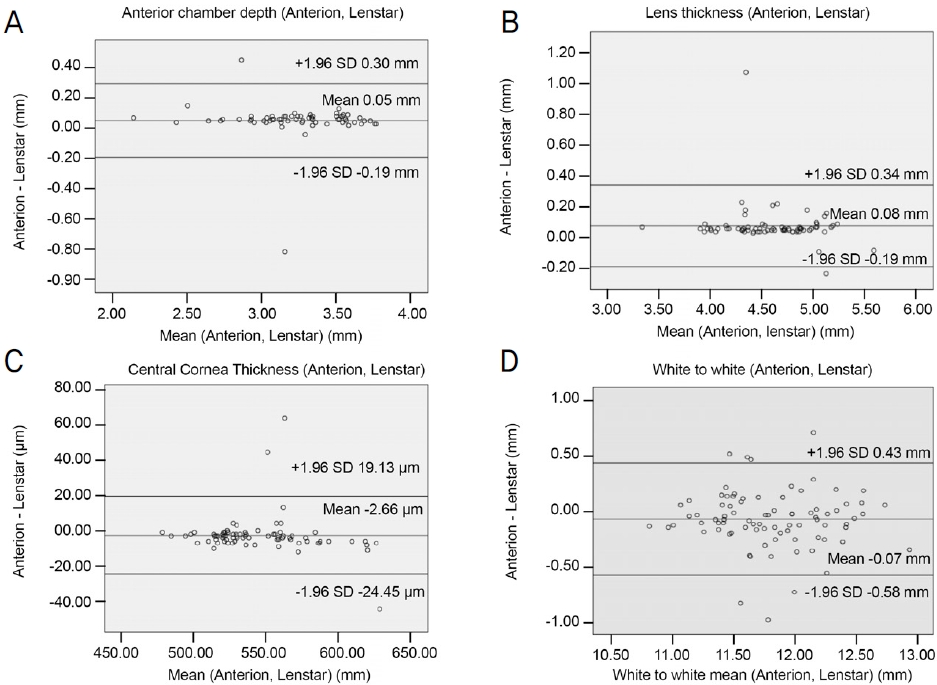
Figure 3.
Bland-Altman plots for mean in flat keratometry mesurements Anterion®, Lengstar LS900®, and Essilor AKR 750®. (A) Agreements of anterior flat keratometry mesurements in Anterion® and Lengstar LS900®. (B) Agreements of anterior flat keratometry mesurements in Anterion® and Essilor AKR 750®. (C) Agreements of anterior flat keratometry mesurements in Lenstar LS900® and Essilor AKR 750®. SD = standard deviation; D = diopters.
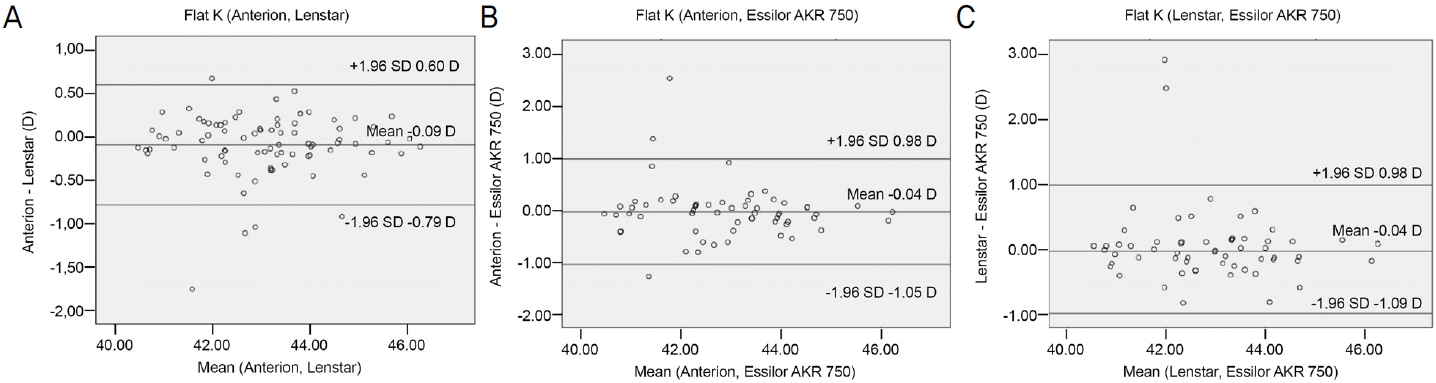
Figure 4.
Bland-Altman plots for mean in steep keratometry mesurements Anterion®, Lengstar LS900®, and Essilor AKR 750®. (A) Agreements of anterior steep keratometry mesurements in Anterion® and Lengstar LS900®. (B) Agreements of anterior steep keratometry mesurements in Anterion® and Essilor AKR 750®. (C) Agreements of anterior steep keratometry mesurements in Lenstar LS900® and Essilor AKR 750®. SD = standard deviation; D = diopters.
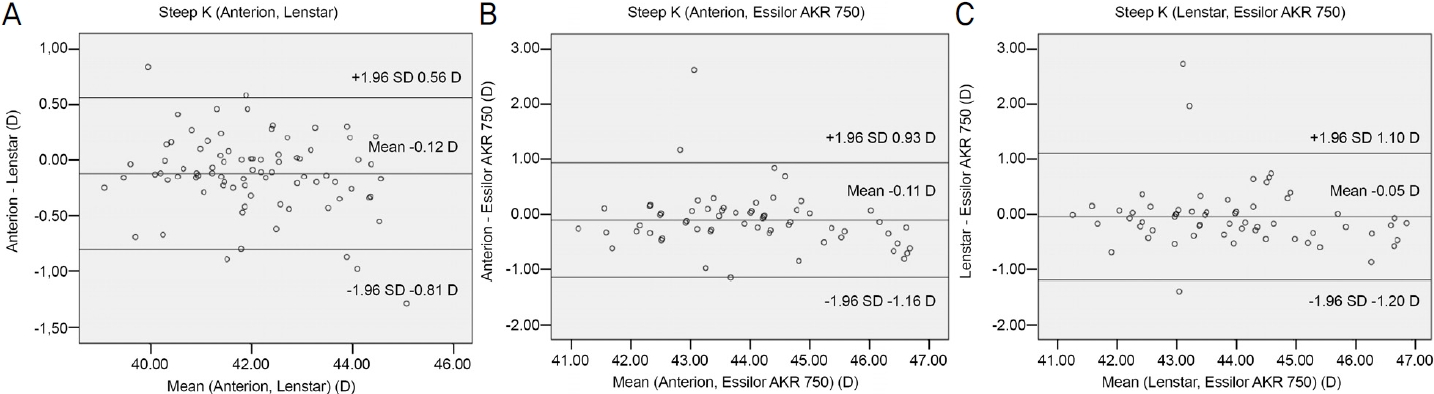
Table 1.
Comparison of axial length between swept-source optical-coherence tomography (Anterion®), low-coherence reflectometry (Lenstar LS900®) and A-Scan (PacScan 300A®)
| Anterion® (n=86) | Lenstar® (n=82) | PacScan 300A® (n=18) |
Anterion® vs. Lenstar® |
Anterion® vs. PacScan 300A® |
Lenstar® vs. PacScan 300A® |
||||
|---|---|---|---|---|---|---|---|---|---|
| Difference | p-value* | Difference | p-value† | Difference | p-value† | ||||
| Axial length (mm) | 23.65 ± 2.88 (22.08 to 26.61) | 23.92 ± 0.95 (21.96 to 26.64) | 23.78 ± 0.93 (21.87 to 25.03) | -0.02 ± 0.08 (-0.52 to 0.27) | p=0.04 | 0.00 ± 0.08 (-0.23 to 0.16) | p=0.09 | 0.04 ± 0.09 (-0.16 to 0.22) | p=0.90 |
Table 2.
Comparison of ocular parameters between swept-source optical-coherence tomography (Anterion®), low-coherence reflectometry (Lenstar LS900®), A-Scan (PacScan 300A®)
| Anterion® (n=86) | Lenstar® (n=82) |
Anterion® vs. Lenstar® |
||
|---|---|---|---|---|
| Difference | p-value* | |||
| Lens thickness (mm) | 4.66 ± 0.41 (3.37 to 5.55) | 4.58 ± 0.43 (3.30 to 5.63) | 0.08 ± 0.13 (-0.23 to 1.07) | p<0.001 |
| Central corneal thickness (µm) | 542.12 ± 32.75 (478 to 622) | 544.71 ± 34.46 (479 to 650) | -2.66 ± 11.12 (-44.00 to -63.00) | p=0.04 |
| Anterior chamber depth (mm) | 3.22 ± 0.41 (1.98 to 4.27) | 3.21 ± 0.34 (2.11 to 3.75) | 0.05 ± 0.12 (-0.81 to 0.45) | p=0.001 |
| White to white (mm) | 11.77 ± 0.45 (10.75 to 12.77) | 11.85 ± 0.46 (10.89 to 13.12) | 0.08 ± 0.26 (-0.98 to 0.70) | p=0.01 |
Table 3.
Comparison of keratometry measurements between swept-source optical coherence tomography (Anterion®), low-coherence reflectometry (Lenstar LS900®) and autokeratometer (Essilor AKR 750®)
| Anterion® (n=86) | Lenstar® (n=82) | Essilor AKR 750® (n=18) |
Anterion® vs. Lenstar® |
Anterion® vs. Essilor AKR 750® |
Lenstar® vs. Essilor AKR 750® |
||||
|---|---|---|---|---|---|---|---|---|---|
| Difference | p-value* | Difference | p-value* | Difference | p-value* | ||||
| Flat K (D) | 43.03 ± 1.39 (40.42 to 46.21) | 43.13 ± 1.40 (40.54 to 46.32) | 42.88 ± 1.43 (40.5 to 46.25) | -0.09 ± 0.36 (-1.76 to 0.68) | p=0.02 | -0.04 ± 0.52 (-1.29 to 2.54) | p=0.59 | 0.04 ± 0.59 (-0.84 to 2.92) | p=0.59 |
| Steep K (D) | 44.01 ± 1.39 (40.98 to 46.59) | 44.14 ± 1.45 (41.23 to 47.73) | 44.03 ± 1.52 (41.25 to 47.00) | -0.12 ± 0.35 (-1.28 to 0.84) | p=0.002 | -0.11 ± 0.53 (-1.16 to 2.62) | p=0.10 | -0.05 ± 0.59 (-1.40 to 2.73) | p=0.50 |
| Average corneal refractive power (D) | 43.52 ± 1.35 (40.81 to 46.29) | 43.65 ± 1.40 (41.01 to 46.85) | 43.46 ± 1.42 (41.00 to 46.63) | -0.10 ± 0.29 (-0.96 to 0.58) | p=0.02 | -0.08 ± 0.47 (-0.93 to 2.56) | p=0.16 | -0.02 ± 0.54 (-1.00 to 2.82) | p=0.76 |
Table 4.
Pearson correlation coefficient and intraclass correlation coefficient of axial length between swept-source optical coherence tomography (Anterion®), low-coherence reflectometry (Lenstar LS900®) and A-Scan (PacScan 300A®)
Table 5.
Pearson correlation coefficient and intraclass correlation coefficient of ocular parameters between swept-source optical coherence tomography (Anterion®), low-coherence reflectometry (Lenstar LS900®)
Table 6.
Pearson correlation of keratometry measurements between swept-source optical-coherence tomography (Anterion®), low-coherence reflectometry (Lenstar LS900®) and autokeratometer (Essilor AKR 750®)
REFERENCES
1) Holladay JT, Prager TC, Ruiz RS, et al. Improving the predictability of intraocular lens power calculation. Arch Ophthalmol 1986;104:539-41.

2) Mamalis N. Complications of foldable intraocular lenses requiring explanation or secondary intervention-1998 survey. J Cataract Refract Surg 2000;26:766-72.

3) Olsen T. Sources of error in intraocular lens power calculation. J Cataract Refract Surg 1992;18:125-9.


4) Villaseñor RA, Santos VR, Cox KC, et al. Comparison of ultrasonic corneal thickness measurements before and during surgery in the prospective evaluation of radial keratotomy (PERK) study. Ophthalmology 1986;93:327-30.


6) Bechmann M, Thiel MJ, Neubauer AS, et al. Central corneal thickness measurement with a retinal optical coherence tomography device versus standard ultrasonic pachymetry. Cornea 2001;20:50-4.


7) Ehlers N, Bramsen T, Sperling S. Applanaton tonometry and central corneal thickness. Acta Ophthalmol (Copenh) 1975;53:34-43.

8) Rosen E, Gore C. Staar collamer posterior chamber phakic intraocular lens to correct myopia and hyperopia. J Cataract Refract Surg 1998;24:596-606.


9) Rose LT, Moshegov CN. Comparison of the Zeiss IOL Master and applanation A-scan ultrasound: biometry for intraocular lens calculation. Clin Exp Ophthalmol 2003;31:121-4.


10) Buckhurst PJ, Wolffsohn JS, Shah S, et al. A new optical low coherence reflectometry device for ocular biometry in cataract patients. Br J Ophthalmol 2009;93:949-53.


11) Choe GS, Kim KY. Comparison of anterior segment measurements between Scheimpflug-placido camera and new swept-source optical coherence tomography. J Korean Ophthalmol 2022;63:10-9.


12) Kim KY, Choi GS, Kang MS, Kim US. Comparison study of the axial length measured using the new swept-source optical coherence tomography ANTERION and the partial coherence interferometry IOL Master. PLoS One 2020;15:e0244590.



13) Oh R, OH JY, Choi HJ, et al. Comparison of ocular biometric measurements in patients with cataract using three swept-source optical coherence tomography devices. BMC Ophthalmol 2021;21:62.




14) Fişuş AD, Hirnschall ND, Findl O. Comparison of 2 swept-source optical coherence tomography-based biometry devices. J Cataract Refrac Surg 2021;47:87-92.

15) Ruíz-Mesa R, Aguilar-Córcoles S, Montés-Micó R, Tañá-Rivero P. Ocular biometric repeatablity using a new high-resolution swept-source optical coherence tomographer. Expert Rev Med Devices 2020;17:591-7.

16) Eibschitz-Tsimhoni M, Tsimhoni O, Archer SM, Del Monte MA. Effect of axial length and keratometry measurement error on intraocular lens implant power prediction formulas in pediatric patients. J AAPOS 2008;12:173-6.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




