인공수정체 공막봉합고정술과 무봉합공막고정술(야마네 기법)에서 굴절력 예측의 정확성
The Refractive Outcomes of Sutured and Sutureless Scleral Fixation (the Yamane Technique)
Article information
Abstract
목적
인공수정체 공막봉합고정술과 비교하여 무봉합공막고정술(야마네 기법)에서 술 전 예상한 굴절력과 술 후 측정한 굴절력의 정확성을 알아보고자 한다.
대상과 방법
본원에서 인공수정체 탈구 또는 수정체떨림으로 인공수정체 공막봉합고정술(20안) 또는 무봉합공막고정술(12안)을 시행받은 환자들을 대상으로 의무기록을 후향적으로 분석하였다. 수술 전 예측구면렌즈대응치는 IOL master® (Zeiss, Carl Zeiss Meditec, Jena, Germany) 측정값과 A-scan biometry (AL-100; Tomey, Nagoya, Japan) 초음파로 측정한 안축장에 각막형태검사로 측정한 각막곡률반경값을 대응하여 계산하였다. 수술 후 1개월째 구면렌즈대응치는 자동굴절각막곡률계를 이용하여 측정하였고, 수술 전 예측구면 렌즈대응치와 술 후 1개월째 구면렌즈대응치의 일치 정도를 비교 분석하였다.
결과
술 전 인공수정체 공막봉합고정술을 시행한 군의 예측구면렌즈대응치는 -0.158 ± 0.577 diopters (D) (A-scan), -0.143 ± 0.617 D (IOL master®)로 1개월째 구면렌즈대응치 -0.400 ± 0.923 D와 각각의 일치도를 비교한 상관계수는 유의하게 나타나지 않았다(p=0.903, 0.563). 반면 무봉합공막고정술을 시행한 군의 예측구면렌즈대응치는 -0.340 ± 0.368 D (A-scan), -0.183 ± 0.251 D (IOL master®)로 1개월째 구면렌즈대응치 -0.313 ± 1.129 D와 각각 유의한 상관관계를 보였다(p=0.038, 0.005).
결론
무봉합공막고정술군에서 술 전 목표로 한 굴절력과 술 후 측정된 굴절력이 유의하게 일치되는 상관관계를 보였다. 삽입된 인공수정체 도수의 굴절력 예측에 있어서 무봉합공막고정술이 공막봉합고정술과 비교하여 그 정확성이 떨어지지 않으면서, 안전하게 시행 가능한 수술 방법임을 확인할 수 있었다.
Trans Abstract
Purpose
To evaluate the pre- and post-operative refractive powers of patients undergoing sutured and sutureless scleral fixation (the latter: the Yamane technique).
Methods
Patients who had undergone sutured or sutureless scleral fixation to treat intraocular lens (IOL) dislocation or phacodonesis at Dong-A University Hospital from January 2017 to December 2021 were retrospectively investigated. The preoperatively predicted spherical equivalents (derived using the radii of corneal curvature) were measured via optical coherence topography and the axial lengths were determined using an IOL master ® (Zeiss, Carl Zeiss Meditec, Jena, Germany) device and A-scan biometry (AL-100; Tomey, Nagoya, Japan) ultrasound. The spherical equivalent was measured 1 month after surgery employing an automatic refractive keratometer. The extent of agreement between the predicted and actual spherical equivalents were compared between the sutured and sutureless scleral fixation groups.
Results
The sutured scleral fixation group included 20 eyes and the sutureless group 12 eyes. The preoperatively predicted spherical equivalent of the sutured group was -0.158 ± 0.577 diopters (D) on A-scan (Tomey) ultrasound and -0.143 ± 0.617 D employing the IOL master ® (Carl Zeiss Meditec); both correlated poorly with the postoperatively measured spherical equivalent of -0.400 ± 0.923 D (p = 0.903, 0.563). However, the predicted spherical equivalent of the group undergoing sutureless fixation was -0.340 ± 0.368 D on A-scan ultrasound and -0.183 ± 0.251 D using the IOL master ® (Carl Zeiss Meditec); both correlated significantly with the postoperatively measured spherical equivalent of -0.313 ± 1.129 D (p = 0.038, 0.005).
Conclusions
The preoperatively predicted refractive power correlated significantly with the postoperative refractive power after sutureless but not sutured scleral fixation. Sutureless fixation was safe and the postoperative refractive power was comparable to that of sutured fixation.
수정체떨림, 인공수정체이탈 등과 같이 수정체낭의 지지가 충분하지 않아서 인공수정체를 수정체낭에 삽입하지 못하는 경우 앞방인공수정체삽입술, 홍채봉합후방인공수정체 삽입술 또는 공막봉합술을 통한 이차 인공수정체삽입술 등의 방법을 이용한 인공수정체 삽입이 가능하다[1]. 공막봉합술을 통해 인공수정체를 고정하는 방법은 크게 두 가지가 있으며 바늘을 공막의 안쪽에서 바깥쪽으로 통과시키는 방법(ab interno)과 바깥쪽에서 안쪽으로 통과시키는 방법(ab externo)이 있다[2,3].
각각의 방법들은 수정체낭의 지지가 충분하지 않을 경우 이차적으로 인공수정체 삽입을 가능하게 하지만 각 술기들의 단점과 발생 가능한 합병증을 고려하지 않을 수 없다. 앞방인공수정체삽입술의 경우 각막내피세포 소실 및 주변 홍채앞유착으로 인한 녹내장 발생 가능성이 높다. 홍채봉합후방인공수정체삽입술은 봉합사 절단, 수술 중 출혈, 포도막염으로 인한 포도막염녹내장앞방출혈증후군(uveitis-glaucoma-hyphema syndrome), 인공수정체로 인한 동공 확장의 방해와 같은 합병증이 발생할 수 있으며 인공수정체 공막봉합술의 경우 봉합사 노출, 인공수정체중심이탈 및 기울어짐, 급성낭포황반부종 등의 합병증이 발생할 수 있다[4-7].
기존의 봉합사를 사용하여 인공수정체를 삽입하는 방법과는 달리 봉합사를 사용하지 않고 공막터널을 통하여 인공수정체를 공막에 고정하는 여러 방법들이 시도되었고[8-11] 그중 최근 Yamane et al [12]은 두 개의 30게이지 바늘을 이용하여 만든 공막터널로 인공수정체의 양쪽 지지부를 동시에 통과시켜 공막에 봉합사 없이 인공수정체를 고정하는 방법을 소개하였다. 이 방법은 술기 과정이 기존의 다른 방법들과 비교하여 간단하고 술 후 내피세포 소실의 정도도 적었으며, 상대적으로 다른 합병증의 발생률도 낮게 나타나는 결과를 보였다[12].
이차 인공수정체를 삽입하는 여러 술기들을 시행함에 있어 발생 가능한 합병증뿐 아니라 술 후 시력 및 굴절력 또한 고려해야 하는 중요한 요소 중의 하나이다. 인공수정체를 수정체낭내에 삽입하는 경우와 달리 공막에 고정하는 경우 인공수정체가 고정된 위치에 따라 술 후 굴절값이 변하게 되며 인공수정체 낭내 삽입술에 적용된 공식을 대입시 오차가 발생하여 보정을 필요로 한다[13]. 하지만 인공수정체 공막봉합고정술의 술 후 굴절력 예측에 관한 연구들은 있으나 무봉합공막고정술(야마네 기법)에서 정확한 술후 굴절력 예측과 인공수정체 도수 결정에 대한 정보는 제한적이다[14-16]. 본 연구는 인공수정체 공막봉합고정술과 비교하여 무봉합공막고정술(야마네 기법)에서 술 전 예상한 굴절력과 술 후 측정한 굴절력의 일치 정도를 확인하고, 이를 통하여 술 전 인공수정체 도수 결정의 정확도를 높이는 데 도움을 주고자 한다.
대상과 방법
2017년 1월에서 2021년 12월까지 본원에서 인공수정체 탈구 또는 수정체떨림으로 인공수정체 공막봉합고정술 또는 무봉합공막고정술(야마네 기법)을 시행받은 환자들을 대상으로 의무기록지를 후향적으로 분석하였다. 안 외상 또는 이전에 유리체절제술 병력이 있는 환자, 시력에 영향을 주는 황반부 병력이 있는 환자는 제외하였다. 본 연구는 헬싱키선언을 준수하였으며, 본원 연구윤리위원회의 승인을 받아 진행하였다(IRB 승인 번호: DAUHIRB-22-064).
수술 전과 수술 1개월째 세극등현미경, 안압, 최대교정시력 검사를 시행하였다. 시력은 decimal 시력표를 이용하여 측정된 값을 logarithm of the minimal angle resolution (logMAR) 값으로 변환하여 분석하였다. 안축장 측정은 초음파를 이용한 A-scan biometry (AL-100; Tomey, Nagoya, Japan)와 IOL master ® (Zeiss, Carl Zeiss Meditec, Jena, Germany)를 사용하여 각각 측정하였고 각막곡률은 각막형태검사(Oculus keratography 5M, G4; OCULUS Optikgeräte GmbH, Wetzlar, Germany)로 측정하였다.
술 전 목표로 한 굴절값은 안축장 길이가 22.4-24.5 mm인 경우는 SRK II, >24.5 mm 또는 <22.4 mm인 경우는 SRK-T 공식을 사용하여 A-scan (Tomey)과 IOL master ® (Carl Zeiss Meditec)로 측정하였다. 술 후 구면렌즈대응치는 자동굴절각막곡률계(PRK-8000; POTEC, Daejeon, Korea)를 이용하여 측정하여 술 전 목표로 한 굴절값과 일치 정도를 확인하였다.
수술은 한 명의 술자에 의해 전신 마취 하에 시행되었다. 25게이지 또는 27게이지 3-공막절개창을 통하여 유리체절제술을 시행하였고, Sensar 3-피스 인공수정체(Sensar ® , AR40e; AMO, Santa Ana, CA, USA)를 사용하였다. 수정체안의 경우 수정체유화술 또는 유리체절제침을 이용한 평면부수정체절제술로 수정체를 제거하였다. 기존의 탈구된 인공수정체가 있는 경우는 탈구된 인공수정체를 앞방으로 이동시켜 Fine straight Stitch Scissors (E3340, Storz Instrument Co., St Louis, MO, USA)로 자른 후 12시 방향 3 mm 각막절개 부위를 통해 제거하였다.
인공수정체 공막봉합고정술의 경우 12시와 6시 방향에 각막가장자리에서 2 mm 떨어진 곳을 각각 표시한 후 26게이지 주사 바늘을 표시된 지점에서 섬모체고랑을 통해 안구 내측으로 통과시켜 반대편(6시 방향)에서 통과시킨 10-0 프롤렌(polypropylene; Ethicon LLC., San Lorenzo, Puerto Rico, USA) 봉합사를 주사 바늘 구멍으로 넣어 12시 방향에서 빼내었다. 10-0 프롤렌 봉합사를 안구 내에서 갈고리로 걸어 상측 각막절개 부위를 통하여 꺼낸 뒤 잘랐다. 인젝터에 인공수정체를 장착 후 밀어내어 나온 앞쪽의 인공 수정체지지부의 끝에서 1.5 mm 떨어진 부위에 자른 봉합사로 매듭을 지어 고정하였다. 이후 인젝터를 통해 매듭이 지어지지 않은 반대편 지지부를 제외하고 인공수정체를 앞방으로 삽입하고, 각막절개 밖에 나와있는 인공수정체지지부 끝을 마찬가지로 봉합사로 묶은 뒤 앞방에 위치시키고 봉합사를 공막에 고정하였다.
무봉합공막고정술(야마네 기법)의 경우는 우선 12시 방향에 3 mm 각막절개를 만든 후 각막절개와 수직을 이루는 3시와 9시 방향에 각각 각막 가장자리에서 2 mm 떨어진 지점을 표시하였다. 인젝터를 사용하여 인공수정체지지부 한쪽과 광학부를 앞방으로 밀어넣은 후, 끝을 45도 구부려 놓은 26게이지 바늘로 공막터널을 2 mm 길이로 만들어 미리 표시된 지점에서 바늘 끝이 섬모체고랑을 통과하여 안구 내에 위치하게 하였다. 앞방에 위치한 지지부 한쪽을 27게이지 맥스그립 포셉(Grieshaber MaxGrip Forceps; Alcon Laboratories, Inc., TX, USA)으로 잡아 26게이지 바늘 내강으로 밀어넣은 후 바늘을 지지부와 함께 바깥으로 빼냈다. 다른 한쪽 지지부도 동일한 방법으로 26게이지 바늘을 이용하여 공막터널을 통해 외부로 빼낸 뒤 공막터널을 통해 나온 각각의 지지부 끝을 단극전기소작기(Accu-Temp Cautery; Beaver-Visitec international Inc, Waltham, MA, USA)로 열을 가하여 지름이 약 0.3 mm 정도 되는 타원형으로 만들어 공막터널쪽으로 밀어 넣어 고정시켰다.
두 군 간의 술 전 검사값 및 술 후 시력 변화는 Fisher’s exact test와 Mann-Whitney U test를 사용하여 비교하였다. 수술 전 예상된 굴절력값과 술 후 굴절력값의 차이를 측정하였고, 술 전과 술 후 굴절력의 일치 정도를 Bland Altman analysis를 통하여 분석하였다. 또한 Pearson correlation coefficient로 수술 전후 각각 군에서의 변수 간 관련성을 분석하였다. 통계 분석은 SPSS statistics v 18.0 for Window (IBM Corp., Armonk, NY, USA)를 이용하였고, p값이 0.05 미만일 경우를 통계학적으로 유의한 것으로 정의하였다.
결 과
인공수정체 공막봉합고정술군 20명(20안), 무봉합공막고정술(야마네 기법)군 12명(12안)이 포함되었다. 두 군 간의 평균 연령, 남녀 성비에서 유의한 차이는 없었다(Table 1). 술 전 A-scan (Tomey)과 IOL master ® (Carl Zeiss Meditec)로 각각 측정한 평균 안축장의 길이는 공막봉합고정술군이 24.547 ± 2.347 mm (A-scan), 24.633 ± 2.351 mm (IOL master ® )였으며, 무봉합공막고정술(야마네 기법)군이 23.913 ± 1.491 mm (A-scan), 23.982 ± 1.502 mm (IOL master ® )로 두 군 간의 유의한 차이를 보이지 않았다(p-value=0.387, 0.366, Mann-Whitney U test) (Table 1). 술 전 평균 시력은 공막봉합고정술군이 0.564 ± 0.657 logMAR, 무봉합공막고정술(야마네 기법)군이 0.566 ± 0.682 logMAR로 두 군 간의 유의한 차이는 없었다(p-value=0.863, Mann-Whitney U test) (Table 1). 술 전 목표로 한 구면렌즈대응치는 공막봉합고정술군이 -0.158 ± 0.577 D (A-scan), -0.143 ± 0.617 D (IOL master ® )였으며, 무봉합공막고정술(야마네 기법)군이 -0.340 ± 0.368 D (A-scan), -0.183 ± 0.251 D (IOL master ® )로 두 군 간의 유의한 차이를 보이지 않았다(p-value=0.076, 0182, Mann-Whitney U test) (Table 1). 삽입된 인공수정체의 평균 굴절력은 공막봉합고정술군이 17.675 ± 5.171 D, 무봉합공막고정술(야마네 기법)군이 18.440 ± 3.431 D로 이 또한 두 군 간에 유의한 차이는 없었다(p-value=0.454, Mann-Whitney U test) (Table 1).
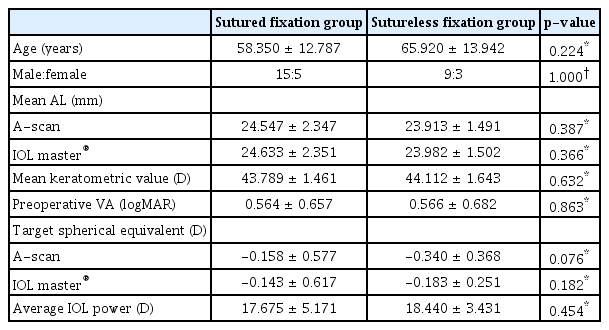
Preoperative baseline characteristics in the sutured and sutureless (Yamane) scleral fixation groups
술 후 두 군에서 모두 평균 시력이 유의하게 호전되는 결과를 보였다(p-vaule=0.037, 0.013, Wilcoxon singed rank test). 술 전 목표로 한 굴절값과 술 후 1달째 측정된 구면렌즈대응치의 평균을 비교한 결과 공막봉합고정술군의 경우 A-scan (Tomey)으로 측정된 술 전 목표구면렌즈대응치는 -0.158 ± 0.577 D로 술 후 1달째 -0.400 ± 0.923 D와 비교하여 유의한 차이를 보이지 않았으며(p-value=0.305, Wilcoxon singed rank test), IOL master ® (Carl Zeiss Meditec)로 측정된 목표구면렌즈대응치 또한 술 전 -0.143 ± 0.617 D에서 술 후 측정된 구면렌즈대응치 평균인 -0.400 ± 0.923 D와 통계적으로 유의한 차이가 없었다(p-value=0.185, Wilcoxon singed rank test) (Table 2). 무봉합공막고정술(야마네 기법)군에서 A-scan (Tomey)으로 측정된 술 전 목표구면렌즈대응치 -0.340 ± 0.368 D와 술 후 1달째 구면렌즈대응치 -0.313 ± 1.129 D 또한 유의한 차이를 보이지 않았으며(p-value=0.666, Wilcoxon singed rank test), IOL master ® (Carl Zeiss Meditec)로 측정된 목표구면렌즈대응치도 술 전 -0.183 ± 0.251 D에서 술 후 측정된 구면렌즈대응치 평균인 -0.313 ± 1.129 D와 유의한 차이가 없었다(p-value=0.937, Wilcoxon singed rank test) (Table 2). 술 전 목표구면렌즈 대응치와 술 후 1달째 구면렌즈대응치의 차이 값은 공막봉합고정술군에서 -0.243 ± 1.074 D (A-scan), -0.257 ± 1.037 D (IOL master ® )로 20안 중 13안(65.0%; A-scan), 15안(75.0%; IOL master ® )에서 술 전과 술 후 구면렌즈대응치 차이값의 절대치가 1.00 D를 넘지 않았다(Table 2). 무봉합공막고정술(야마네 기법)군의 경우 술 전과 술 후 구면렌즈대응치 차이 값은 0.028 ± 0.953 D (A-scan), -0.257 ± 1.037 D (IOL master ® )로 총 12안 중 8안(66.7%; A-scan), 9안(75.0%; IOL master ® )에서 차이값의 절대치가 1.00 D를 넘지 않았다(Table 2, Fig. 1).
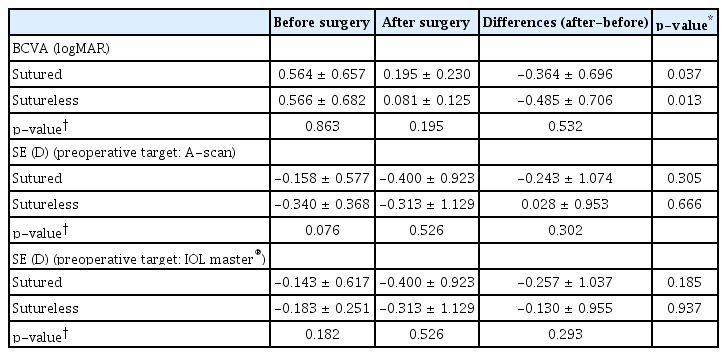
Comparison of visual acuity and spherical equivalent before and after surgery between the sutured and sutureless (Yamane) scleral fixation groups
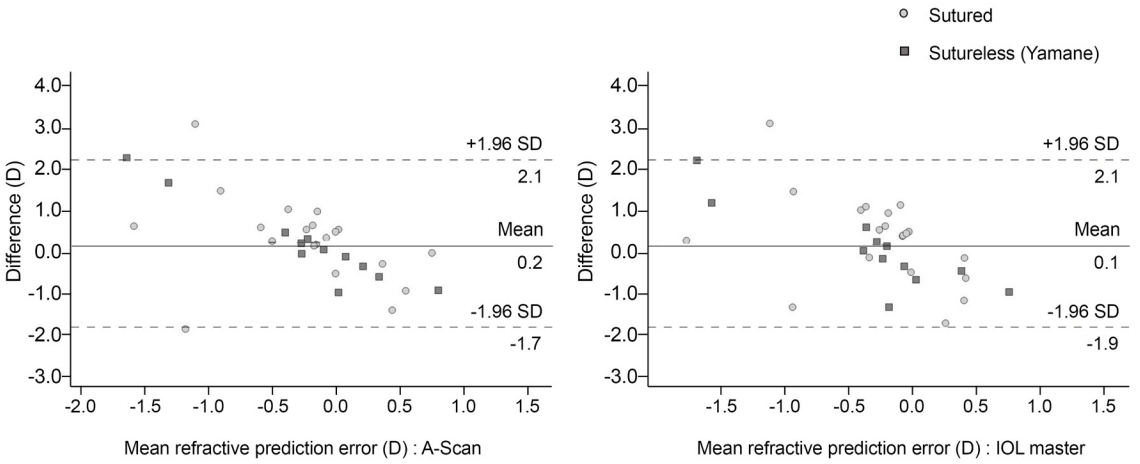
Bland-Altman plot for the comparison of estimated spherical equivalent to the reference refractive prediction error (A-scan and IOL master®) for sutured and sutureless (Yamane) scleral fixation groups. SD = standard deviation; D = diopter.
A-scan (Tomey) 및 IOL master ® (Carl Zeiss Meditec)로 측정된 예측구면렌즈대응치와 술 후 1개월째 측정된 구면렌즈대응치의 일치도를 비교한 결과, 공막봉합고정술군에서 r=0.029 (A-scan), 0.137 (IOL master ® ), 무봉합공막고정술(야마네 기법)군에서 r=0.604 (A-scan), 0.749 (IOL master ® ) (Pearson correlation coefficient)로 무봉합공막고정술(야마네 기법)군이 공막봉합고정술군에 비하여 1에 근접한 상관 계수를 보였다(Fig. 2). 또한 무봉합공막고정술(야마네 기법)군에서만 술 전과 술 후 구면렌즈대응치가 통계적으로 유의한 상관관계를 나타냈다(p-value=0.038 [A-scan], 0.005 [IOL master ® ], Pearson correlation coefficient) (Fig. 2).
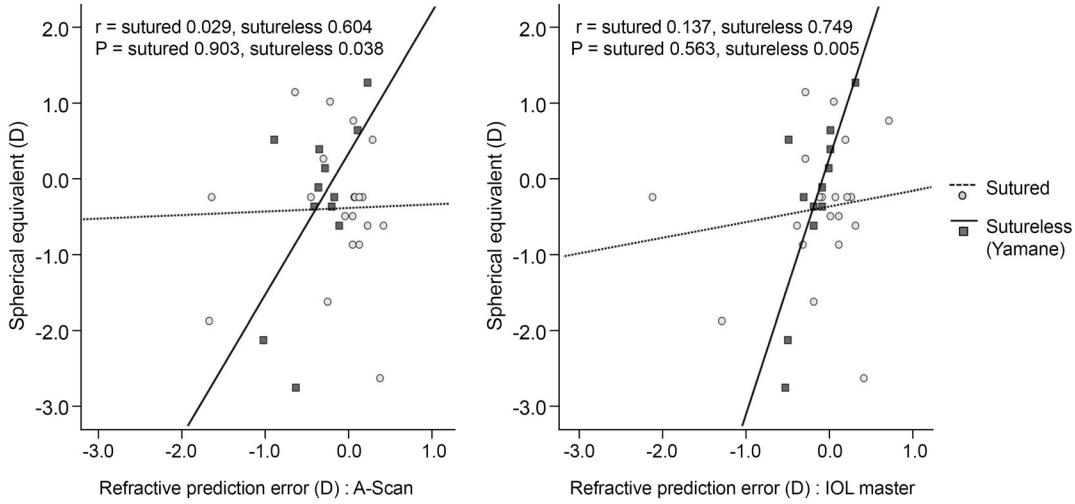
Comparison of correlation coefficient between preoperative refractive prediction error and postoperative spherical equivalent within sutured and sutureless (Yamane) scleral fixation groups. D = diopter.
술 후 공막봉합고정술군 중 2안에서 인공수정체광학부의 동공물림이 확인되었으며, 무봉합공막고정술(야마네 기법)군에서는 술 후 합병증 관찰되지 않았다.
고 찰
인공수정체삽입술을 시행함에 있어 여러 요인들을 고려해야 하는데, 그중에서도 술 전 예측한 구면렌즈대응치가 술 후 실제로 확인된 구면렌즈대응치와 얼마나 정확히 일치하는지의 여부는 환자의 시력 예후를 결정하는 데 있어 중요한 요인으로 고려된다. 수정체낭내 인공수정체삽입술의 경우 술 후 목표 굴절력을 예상하여 삽입하고자 하는 인공수정체의 도수를 결정하게 되는데 정확한 인공수정체 도수 결정을 위하여 다양한 공식들을 사용한다. 임상에서 사용되는 공식들에는 Hoffer Q, Holladay I/II, SRK II, SRK/T 등이 있으며, 안축장의 길이에 따라 굴절 예측률이 높은 공식을 선택하여 삽입할 인공수정체의 도수를 결정한다[17,18]. 각 계산 공식들은 효과적인 도수 결정을 위한 상수(constant)를 사용하는데, 이 상수들은 A-상수, anterior chamber depth 상수 그리고 술자에 의해 결정되는 상수들(surgical factors)이며, 각각의 인공수정체 종류에 따른 최적화된 상수를 적용한다[18]. 이러한 공식들과 상수는 수정체낭내 인공수정체 삽입을 위한 도수 결정에서는 비교적 정확한 예측률을 보여주지만 공막에 인공수정체를 고정하는 경우 굴절력 예측의 정확성이 떨어지며, 인공수정체 공막고정술에서 삽입할 인공수정체의 도수 결정을 위한 차별화된 공식도 없다. 또한 인공수정체를 공막에 고정하는 여러 방법들에 대한 발표들은 있으나[7,19,20] 수술 후 굴절 결과에 대해서는 최근에 드물게 보고되고 있다[21-23].
수술 후 목표로 하는 굴절 상태를 얻기 위해서는 정확한 생체 계측을 토대로 도수를 결정하게 되지만 그럼에도 불구하고 수술 후 목표치와 1 D 이상의 오차를 보이는 빈도가 10% 이상이라는 보고가 많으며 수술 후 시간이 지나면서 앞방이 깊어져 인공수정체가 수술 직후보다 뒤쪽으로 이동하여 원시화되는 경향이 있어 일반적으로 목표 굴절값보다 약간 근시 쪽으로 도수를 선택하라는 보고들이 있다[24]. 또한 인공수정체를 수정체낭내에 위치시키지 못하고 섬모체고랑에 위치시켜야 할 경우 도수를 1 D 정도 낮춰야한다고 보고하였다[25-27].
하지만 공막고정술에서의 인공수정체 도수에 대한 이러한 정보들은 제한적이며 공막고정술 시행 후 굴절 결과가 예상한 것과 다르게 오차가 종종 발생하게 되는데 이러한 오차들은 수술 과정에서 유발될 수 있다. 인공수정체 공막고정술에서 공막터널의 위치가 전-후방으로 이동(anterior-posterior placement)하게 되면 인공수정체 양쪽 지지부의 장력이 증가하면서 수정체 광학부의 앞방 이동을 유발하여 근시화를 일으킬 수 있다[28]. 공막터널을 만들기 위한 바늘의 진입 각도가 너무 커지는 경우 광학부의 위치가 예상보다 후방 쪽으로 이동하거나 광학부가 기울어지게 되면서 원시화를 일으키거나 난시를 유발하게 된다[28].
무봉합공막고정술(야마네 기법)은 기존의 공막봉합고정술과 비교하여 술기가 간단하여 수술 시간을 단축시키면서 안전하게 인공수정체를 공막에 고정할 수 있는 방법이다. 본 연구에서는 술 전 목표로 하는 구면렌즈대응치와 술 후 실제로 측정된 구면렌즈대응치의 일치 정도를 무봉합공막고정술(야마네 기법)군과 공막봉합고정술군에서 비교 분석해 보았다. 그 결과 공막봉합고정술군의 경우 A-scan (Tomey)으로 예측한 술 전 구면렌즈대응치와 술 후 구면렌즈대응치의 차이는 -0.243 ± 1.074 D, IOL master ® (Carl Zeiss Meditec)의 경우 -0.257 ± 1.037 D, 무봉합공막고정술(야마네 기법)군에서는 A-scan (Tomey)의 경우 술 전과 술 후 구면 렌즈대응치의 차이가 0.028 ± 0.953 D, IOL master ® (Carl Zeiss Meditec)로는 -0.130 ± 0.955 D로 두 방법 모두에서 술 전 예상한 구면렌즈대응치가 술 후 실제로 측정된 구면렌즈대응치와 통계적으로 유의한 차이를 보이지 않았으며 (Table 2), Bland-Altman plot (Fig. 2)에서 무봉합공막고정술(야마네 기법)군과 공막봉합고정술군 모두에서 술 전과 술 후 구면렌즈대응치 차이값이 비교적 평균을 중심으로 모여 있는 결과를 보였고, 이를 통해 무봉합공막고정술(야마네 기법)이 공막봉합고정술과 비교하여 술 후 구면렌즈 대응치 예측에 있어서 일치도가 떨어지지 않음을 확인할 수 있었다.
또한 본 연구에서 무봉합공막고정술(야마네 기법)군에 포함된 총 12안 중 8안(66.7%; A-scan), 9안(75.0%; IOL master ® )에서 술 전과 술 후 구면렌즈대응치 차이값의 절대치가 1.00 D를 넘지 않아 공막봉합고정술군과 비교하여(65.0%; A-scan, 75.0%; IOL master ® ) 1 D 이하의 굴절 오차를 보이는 환자의 비율이 높거나 동일하게 나타나는 결과를 보였다.
술 후 1개월째 측정된 구면렌즈대응치의 일치도를 비교한 상관분석에는 무봉합공막고정술(야마네 기법)군이 공막봉합고정술군에 비하여 상관계수(r)값이 A-scan (Tomey)과 IOL master ® (Carl Zeiss Meditec) 모두에서 0.604, 0.749로 공막봉합고정술군에서의 상관계수(r)값인 0.029, 0.137보다 높은 결과를 보여주었으며, 상관계수가 1과 가까울수록 두 변수 간의 관련성이 높아지는 것을 고려하면 무봉합공막고정술(야마네 기법)군이 공막봉합고정술군과 비교하였을 때 삽입한 인공수정체의 술 후 굴절력 예측에 있어서 정확성이 높게 나타나는 결과를 확인할 수 있었다.
본 연구는 무봉합공막고정술(야마네 기법)의 술 후 굴절력에 관한 기존 연구들[29,30]과는 달리 한 명의 술자가 동일한 인공수정체(Sensar 3-피스)를 사용함으로써 술 후 굴절력에 영향을 미칠 수 있는 변수들을 어느 정도 통제할 수 있었다. 수정체낭내 인공수정체삽입 시 사용되는 공식으로 무봉합공막고정술(야마네 기법)에 삽입할 도수를 결정하였으며, 안축장 길이에 따라 SRK II 또는 SRK/T 공식에 A 상수는 A-scan (Tomey)에서는 118.40, IOL master ® (Carl Zeiss Meditec)에서는 118.70을 사용하였다.
무봉합공막고정술(야마네 기법)에서 차별화된 도수 결정을 위한 공식이 없으므로 기존의 공식을 대입하여 인공수정체 도수를 결정했으며, 실제로 측정된 술 전과 술 후 구면렌즈대응치의 차이값을 분석한 결과 술 전 목표로 한 A-scan (Tomey) 구면렌즈대응치보다 +0.028 D 원시화, IOL master ® (Carl Zeiss Meditec) 구면렌즈대응치보다 -0.130 D 근시화되는 경향을 보였으나 오차 범위가 크지 않았고 비교적 술 전과 술 후 굴절력의 일치도가 높은 결과를 보였다. 굴절력 예측에 있어서도 공막봉합고정술군과 비교한 결과 무봉합공막고정술(야마네 기법)을 시행한 경우에서 굴절력 예측의 정확도가 떨어지지 않음을 확인할 수 있었다.
본 연구에서 무봉합공막고정술(야마네 기법)군이 공막봉합고정술군과 비교하여 대등하거나 높은 굴절력 예측 결과를 보였다. 공막봉합고정술의 경우 인공수정체 양쪽 지지부를 봉합사로 고정하는 과정에서 장력이 일정하게 작용하지 않을 경우 수정체 광학부가 전후로 이동하게 되면서 근시화 또는 원시화를 유발할 수 있는데[28], 무봉합공막고정술(야마네 기법)에서는 인공수정체지지부 끝을 타원형(flange)으로 만든 후 공막터널쪽으로 밀어넣는 방법으로 인공수정체를 고정시켜 인공수정체의 위치 이동이나 기울어짐 발생을 예방할 수 있고, 이로 인해 술 후 굴절력 변화에 영향을 적게 주었을 것으로 생각된다.
이전 연구에서는 무봉합공막고정술(야마네 기법) 시 술 후 원시화되는 경향이 있어 목표 굴절값보다 0.50에서 0.75 D 정도 근시 쪽으로 도수를 선택하라고 권고하였으나[30] 본 연구에서는 정시안을 목표로 도수를 결정하였고, 66.7% (A-scan), 75.0% (IOL master ® )에서 1 D 이하의 굴절 오차를 기대할 수 있었다. 술 후 실제로 측정된 굴절력 또한 근시화나 원시화되지 않고 목표로 한 도수에 근접함을 알 수 있었으나, 상기 결과는 본 연구에 포함된 환자 수가 적었던 점을 고려하여 해석되어야 한다.
본 연구는 술 후 굴절력에 영향을 미치는 앞방깊이, 인공수정체의 위치 등에 대한 객관적인 검사가 이루어지지 않은 한계점이 존재한다. 무봉합공막고정술(야마네 기법)에서 인공수정체의 위치는 각막 윤부로부터 공막터널의 거리, 인공수정체지지부 끝을 전기 소작하는 정도에 영향을 받을 수 있으며 이러한 부분들의 추가적인 고려가 필요하다. 또한 후향적 연구로 전체 대상자 수가 적고 술 후 경과 관찰기간이 한 달로 짧았으므로 추후 더 많은 환자를 대상으로 하는 전향적 연구가 필요할 것으로 사료된다.
Notes
Conflicts of Interest
The authors have no conflicts to disclose.
References
Biography
이재훈 / Jae Hun Lee
동아대학교 의과대학 안과학교실
Department of Ophthalmology, Dong-A University College of Medicine
