 |
 |
| J Korean Ophthalmol Soc > Volume 63(6); 2022 > Article |
|
국문초록
증례요약
(증례 1) 우안 폐쇄각녹내장이 있는 76세 여자 환자에서 아메드밸브삽입술을 시행하였다. 각막부전을 우려하여 아메드밸브 튜브를 섬모체고랑 내에 위치시켰다. 술 후 8일째, 얕은 전방과 안압상승으로 수술적 홍채절제술을 시행하였다. 술 후 3주째 안압상승 및 전방소실로 유리체절제술을 시행하였고, 반복적 안압상승이 있어 아메드밸브 튜브를 유리체강 내로 재위치 시킨 후 안압이 조절되었다. (증례 2) 거짓비늘녹내장이 있는 93세 여자 환자에게 좌안 아메드밸브삽입술 시행 후 5일째 안압상승 및 전방소실, 전방 내 수정체 피질과 탈출된 유리체가 관찰되었다. 전방세척과 수술적 홍채절제술을 시행했으나 술 후 1개월 안압 재상승 및 전방소실로 앞유리체절제술을 시행하였다.
ABSTRACT
Case summary
(Case 1) A 76-year-old female with angle closure glaucoma in the right eye underwent Ahmed valve implantation. To reduce the risk of corneal endothelial failure, the tube tip was located in the sulcus. Eight days after surgery, surgical iridectomy was performed due to intraocular pressure elevation and a shallow anterior chamber. Three weeks later, vitrectomy was performed due to intraocular pressure elevation with a shallow anterior chamber. Recurrent intraocular pressure elevation was resolved after tip reposition into the vitreous cavity. (Case 2) A 93-year-old female with pseudoexfoliation glaucoma underwent Ahmed valve implantation in the left eye. Five days after surgery, the intraocular pressure increased with a shallow anterior chamber; the remnant cortex and prolapsed vitreous body were present in the anterior chamber. She underwent anterior chamber washing and surgical iridectomy; however, the increase in intraocular pressure with a shallow anterior chamber worsened after 1 month; thus, anterior vitrectomy was performed.
Conclusions
Malignant glaucoma after Ahmed valve implantation is considered very rare. However, if risk factors such as short axial length, zonular weakness, old age, or female gender are present, as in these cases, there may be an increased risk of malignant glaucoma developing after Ahmed valve implantation.
악성녹내장이라는 용어는 기존의 녹내장 치료에 잘 반응하지 않고, 빠르게 진행하여 실명까지 이를 수 있게 하는 공격적인 녹내장을 묘사하기 위해 1869년 von Graefe [1]가 제시했다. 악성녹내장은 전형적으로 일차폐쇄각녹내장을 가진 환자에서 수술적 치료를 시행했을 때 드물게 나타나는 녹내장의 한 형태이며, 맥락막상강출혈 또는 맥락막삼출 등 망막의 병변은 없으며 홍채 절개창이 적절하게 개방되어 있지만 매우 얕거나 소실된 전방과 더불어 안압이 올라가는 특징을 지닌다[2]. 특히 백내장수술이 수술 과정에 포함된 경우 발병률이 높으며, 녹내장수술 중에서는 섬유주절제술을 시행하였을 때가 Seton valve, ExPress shunt 등[3]의 방수유출장치를 삽입하였을 때보다 악성녹내장 발병률이 높은 것으로 보고된 바 있다. 아메드밸브삽입술 후 악성녹내장이 발생한 사례는 매우 드물며, 아메드밸브삽입술 재수술 이후 발생한 국외보고 1예와 고령의 거짓비늘증후군에서 아메드밸브삽입술 이후에 발생한 국내 환자보고 1예가 있다[4,5]. 이에 저자들은 아메드밸브삽입술 단독 시행 후 악성녹내장이 발생한 2예를 경험하였기에 이를 보고하고자 한다.
76세 여자 환자에게 폐쇄각녹내장으로 우안 아메드밸브삽입술을 시행하였다. 5년 전 양안 백내장수술을 시행하였으며 인공수정체는 후낭에 위치하고 있었으며 섬모체소대의 약화는 뚜렷하지 않았다. 술 전 우안 최대교정시력은 0.5이고 골드만압평안압계로 측정한 안압은 18 mmHg였다. 우안 안축장은 20.83 mm, 술 전 측정한 각막내피세포밀도는 1,244 cells/mm2였다. 수술은 아메드밸브의 개방성을 확인 후 술 후 저안압을 방지하기 위해 1가닥의 4-0 Nylon을 튜브 안으로 넣은 상태에서 튜브를 8-0 Vicryl로 결찰하고 이후 nylon을 제거하였다. 전방에 1.6% hyaluronic acid/4.0% chondroitin sulfate (Discovisc®; Alcon Laboratories, Inc., Fort Worth, TX, USA)를 채운 뒤 튜브를 삽입하였고 결막 봉합 전 저안압 및 얕은 전방을 방지하기 위해 전방 내에 점탄물질(Discovisc®, Alcon Laboratories, Inc.)을 채워 넣었다. 각막부전 위험을 최소화하기 위해 아메드밸브 튜브를 섬모체고랑 내에 위치시켰다. 술 후 1일째 우안 안압은 15 mmHg로 측정되었으며 전방은 깊게 유지되었다. 술 후 8일째 우안 시력 안전수지 30 cm, 안압 36 mmHg, 얕은 전방이 관찰되며 홍채가 튜브 끝을 막고 있는 것이 의심되었다. 동공 차단 녹내장을 배제하기 위해 넓은 수술적 홍채절제술을 시행 후 절제된 홍채 내로 튜브를 통과시켜 전방에 위치시켰다(Fig. 1). 다음날 우안 안압 12 mmHg로 측정되었으며 전방 소실되어 전방 내 점탄물질(Discovisc®; Alcon Laboratories, Inc.)을 주입하였다. 수술적 홍채절제술 시행 1주 후 우안 통증, 각막부종과 함께 안압이 31 mmHg로 상승하였으며 얕은 전방이 관찰되었다. 초음파검사상 맥락막상강출혈이나 맥락막삼출 등의 특이 소견은 보이지 않았다(Fig. 2). 1% atropine sulfate (Isopto® Atropine; Alcon Laboratories, Inc.) 하루 2회, 1% predisolone acetate (PredForte®; Allergan Inc., Irvine, CA, USA) 하루 4회 점안과 더불어 dorzolamide hydrochloride/timolol maleate (Cosopt®; Merck & Co, Inc., Kenilworth, NJ, USA) 하루 2회 점안, brimonidine tartrate (Alphagan®-P; Allergan Inc.) 하루 3회 점안 및 Travoprost (Travatan®, Alcon Inc., Camberley, UK) 하루 1회 점안하였음에도 불구하고 안압이 37 mmHg로 측정되어 악성녹내장 진단하에 우안 유리체절제술을 시행하였다. 술 후 1일째 안압은 13 mmHg 소견을 보였고 전방은 잘 유지되었다. 유리체절제술 1년 후, 우안 시력은 안전수동, 안압은 25 mmHg, 각막내피세포밀도 790 cells/mm2로 측정되었으며 아메드밸브 튜브 끝이 홍채에 막혀있었다. 이에 아메드밸브 튜브를 섬모체 평면부를 통해 유리체강 내에 재위치 시켰으며 아메드밸브 튜브 재위치술 후 5개월째 우안 교정시력 0.2, 안압 12 mmHg, 각막내피세포밀도 875 cells/mm2로 측정되었으며 전방은 깊게 유지되었다(Fig. 3).
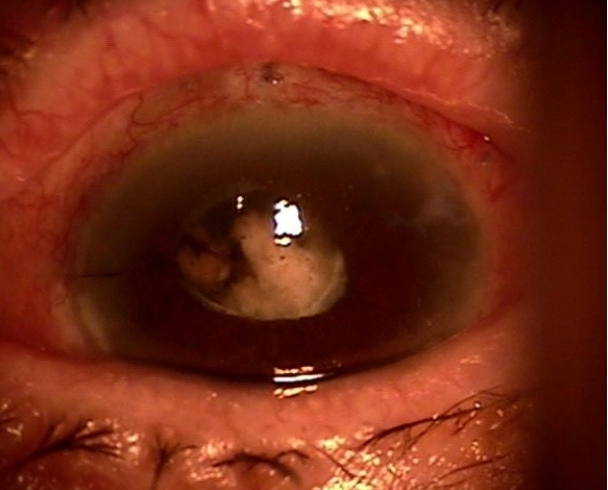
93세 여자 환자가 거짓비늘녹내장으로 좌안 아메드밸브 삽입술을 시행하였다. 술자 및 수술 방법은 증례 1과 동일하며 아메드밸브의 튜브는 전방 내로 위치시켰다. 9년 전 우안 섬유주절제술 및 양안 백내장수술을 시행한 기왕력이 있으며, 좌안 인공수정체는 후낭에 삽입되어 있었고 후낭 파열은 관찰되지 않았다. 인공수정체떨림이 관찰되었다. 술 전 좌안 최대교정시력은 0.1, 골드만압평안압계로 측정한 안압은 30 mmHg, 안축장은 22.0 mm로 측정되었다. 술 후 1일째 좌안 최대교정시력 안전수동, 안압 5 mmHg로 측정되었고 얕은 전방이 관찰되었다. 술 후 5일째 전방은 여전히 얕었고 안압은 22 mmHg로 상승한 소견을 보였으며, 술 전 및 술 중 보이지 않던 인공수정체 아래쪽으로 남아있던 피질과 유리체 일부의 탈출이 관찰되었다(Fig. 4). 1% atropine sulfate (Alcon Laboratories, Inc.)을 하루 2회 점안 및 전방 내 점탄물질(Discovisc®; Alcon Laboratories, Inc.)을 주입 시행하며 경과관찰 중 술 후 7일째 안압이 41 mmHg로 측정되었고 전방은 소실되었다. 초음파검사 상 특이 소견은 관찰되지 않았으며 악성녹내장이 의심되었으나 튜브 끝의 개통이 확인되지 않고 동공차단녹내장의 가능성을 배제 하기 위해 우선적으로 좌안 전방세척과 수술적 홍채절제술을 시행하였다. 이후 경과 관찰 시 안압은 Cosopt® (Merck & Co, Inc., Kenilworth, NJ, USA), Alphagan® (Allergan Inc., Irvine, CA, USA), Travatan® (Alcon Inc., Camberley, UK)으로 최대 약물 치료를 하면서 20 mmHg 전후로 유지가 되었으며 전방은 지속적으로 중심각막두께 1.5배 정도로 얕게 유지되었다. 홍채절제술 시행 한 달 후 안압이 다시 31 mmHg로 상승하며 중심부 및 주변부 전방 모두 소실되어 앞유리체절제술을 시행하여 전방 내로 탈출한 피질과 유리체를 제거하였다. 다음날 안압은 12 mmHg로 감소하였으며 전방 깊이 또한 중심각막두께 3배로 호전되었다. 1년 후, 좌안 최종시력은 광각으로 안압상승은 없었고 전방도 깊게 유지되었다.
악성녹내장은 기존에 전방각폐쇄가 있는 눈에서 녹내장 수술을 받은 후 주로 나타나며 2-4%의 빈도를 보인다고 알려져 있다[6]. 그러나 레이저수술이나 다른 안과적 수술을 받은 경우에도 나타날 수 있으며 이전에 수술받지 않은 눈에서도 외상, 염증, 축동제의 사용으로 인해 유발되거나 특별한 원인 없이도 나타난다는 보고가 있다[7]. 수술 후 발생하는 시기는 수시간 내에서 수년 내로 다양하다[2]. 악성녹내장은 발생 기전에 따라 섬모체차단녹내장(ciliary block glaucoma), 방수흐름이상증후군(aqueous misdirection), 섬모체수정체 녹내장(ciliolenticular glaucoma), 섬모유리체차단 녹내장(ciliovitreal block glaucoma) 등의 여러 가지 용어로도 불리운다[8]. 무수정체안, 인공수정체안, 수정체안에서 모두 나타날 수 있으며 기전은 공통적으로 방수가 정상적인 유출 경로를 따라가지 않고 유리체 쪽으로 역류하면서, 후방 압력이 올라가고 앞유리체면이 앞쪽으로 이동하여 수정체나 홍채를 전방으로 밀어 이차적인 전방각폐쇄를 일으키는 것이다. 이에 따라 방수는 전방으로 계속 빠져나가지 못하는 악순환이 발생하게 되며 안압이 상승하게 되는 것이 악성녹내장의 기전으로 생각되고 있다[9].
악성녹내장의 일차적 약물적 치료는 방수생성 억제를 위한 안압하강제제와 유리체용적을 줄이는 고삼투압제를 사용하며, 섬모체 소대를 긴장시켜 렌즈-홍채 평면을 후방으로 이동시켜 섬모체-렌즈, 섬모체-유리체 차단을 해소할 목적으로 조절마비제를 사용한다. 내과적 치료에 반응이 없는 경우 수술적 치료를 고려하게 되며 비정상 방수의 흐름의 차단을 풀어주는 것을 목적으로 한다. 레이저홍채절개술은 동공차단 기전의 감별 및 해소를 위해 일차적으로 시행될 수 있으며 이전 홍채절개 부위의 개통성이 의심된다면 주변부 홍채절제술을 실시하여 후방에서 전방으로의 통로를 만들어줄 수 있다. 유리체 내 갇힌 방수의 배출을 위해 후방 공막절개술 및 vitreous tapping, Nd:Yag 레이저 후낭절개술, 평면부 유리체절제술을 시행할 수 있으며 최근에는 평면부 유리체절제술이 많이 사용되고 있다. 인공수정체 안에서는 앞유리체절제술과 동반한 홍채절제술-유리체절제술-소대절제술(iridectomy-hyaloidotomy-zonulectomy) 또한 높은 성공률을 보인다고 알려져 있다[2,10].
악성녹내장의 위험인자로는 원시, 소안구, 전방각폐쇄의 병력, 고원홍채, 술 중 기침이나 스트레스로 인해 협조가 잘 안되는 경우, 심한 백내장, 거짓비늘증후군, 섬모체소대 약화, 술 후 좁은 전방각 등이 있다[3,8]. 아시아인에서 더 흔하게 발생하는데 그 이유로는 상대적으로 짧은 안축장과 그로 인해 좁은 전방각을 가질 소인이 높은 것으로 유추되고 있다[11]. 악성녹내장이 발병하는 평균 나이는 70대이며 여성의 비율이 더 높은 것으로 알려져 있다[3,12]. 녹내장수술 중에서는 심부공막절제술(deep sclerectomy), i-stent 등의 비관통수술(nonpenetrating surgery)에 비해 섬유주절제술, Ex-press shunt 삽입 같은 관통수술(penetrating surgery)을 시행하였을 때 2.3%의 환자에서 악성녹내장이 나타나 위험인자로 볼 수 있으며 홍채각막각이 좁을수록 악성녹내장 발생 위험이 3배 증가하는 것으로 나타났다[3].
이에 비해 아메드밸브삽입술은 관통수술임에도 불구하고 악성녹내장이 술 후 합병증으로 발생하는 경우는 드문 것으로 알려져 있으며 증례보고도 드물다. 아메드밸브삽입술을 시행 시 악성녹내장이 발생한 증례는 인공수정체안에서 2예, 백내장수술과 동시에 시행한 안에서 1예 보고되었다[4,5,13]. 아메드밸브삽입술 후 장기 결과를 추적한 연구에서도 악성녹내장이나 방수이상흐름증후군이 포함된 경우는 드물어 대략적인 빈도를 알기 어려우나, Wishart et al [14]의 연구에서는 일시적 튜브 결찰과 가스를 채운 그룹은 51안 중 4안에서 방수이상흐름증후군이 나타났고, 튜브 결찰과 가스 사용이 없었던 그룹에서는 36수정체안 중 1안에서 방수이상흐름증후군이 나타났다고 보고하였다. 앞선 증례들에서 악성녹내장의 치료는 주변부홍채절제술과 함께 평면부 유리체절제술 또는 앞유리체절제술과 유리체-소대절제술 (hyaloido-zonulectomy)을 통해 이루어졌다. 그러나 Baerveldt 방수 유출 장치의 경우에는 단독으로 삽입술을 시행하였을 때 섬유주절제술과 결과를 비교한 the tube versus trabeculectomy (TVT) study에서 초기 술 후 합병증에서 악성녹내장의 빈도가 각각 3%, 1%로 더 높은 것으로 보고된 바 있다[15]. 같은 방수 유출 장치이나 아메드장치는 밸브를 가지고 있어 상대적으로 밸브가 없는 Baerveldt나 다른 녹내장 수술에 비해 술 후 급격한 저안압, 좁은 전방각이 나타나는 경우가 더 적다고 기존 연구에서 알려져 있으며[16], 이러한 부분에 의해 술 후 모양체와 수정체의 접촉의 가능성이 낮아 악성녹내장의 위험인자를 감소시키는 것으로 여겨진다.
본 증례에서는 아메드밸브삽입술 단독으로 시행한 녹내장 환자에서 술 후 발생한 악성녹내장 2예를 경험하였다. 두 증례 모두 고령의 여성이었고, 안축장이 짧았으며 한 증례는 거짓비늘증후군로 인한 섬모체소대해리와 유리체탈출의 위험인자를 가지고 있었다. 고령과 거짓비늘녹내장은 공통적으로 섬모체소대의 약화를 가져올 수 있고 짧은 안축장으로 술 후 모양체유리체 차단이 보다 쉽게 일어나 악성녹내장으로 진행한 것으로 보인다. 본 증례같이 악성녹 내장의 여러 위험인자가 공존하는 경우에는 아메드밸브삽입술에서 드물게 발생하는 합병증인 악성녹내장의 가능성을 염두에 두어 수술 후 급격한 안압하강이 일어나지 않게 튜브의 매듭 등을 조절해야 하며 술 후 전방의 변화를 주의 깊게 살펴야 한다. 그리고 안압하강제와 조절마비제로 즉시 약물치료를 시행해야 하며 효과가 없을 시, 조기에 유리체절제술 등의 수술적 치료법을 고려하는 것이 필요하다. 악성녹내장으로 전방이 소실되는 과정과 이차적인 수술을 거치면서 추후 각막부전의 위험성이 커지는데, 증례 1에서처럼 섬모체평면부를 통해 튜브재위치술을 시행하는 것도 장기적으로 각막내피세포밀도 감소를 최소화할 수 있는 방법이 될 수 있다.
결론적으로, 아메드밸브삽입술 후 악성녹내장이 생기는 경우는 비교적 드물다. 하지만 안축장이 짧거나, 섬모체소대가 약하거나, 고령 혹은 여성 등 위험요소를 가지고 있는 경우 아메드밸브삽입술 후 악성녹내장 발생 가능성이 높아질 수 있어 주의를 요한다.
Figure 1.
Intraoperative images of surgical iridectomy. (A) Iris blocking the tube tip was removed by large surgical iridectomy and (B) the tube tip was repositioned into the anterior chamber through iridectomy site.
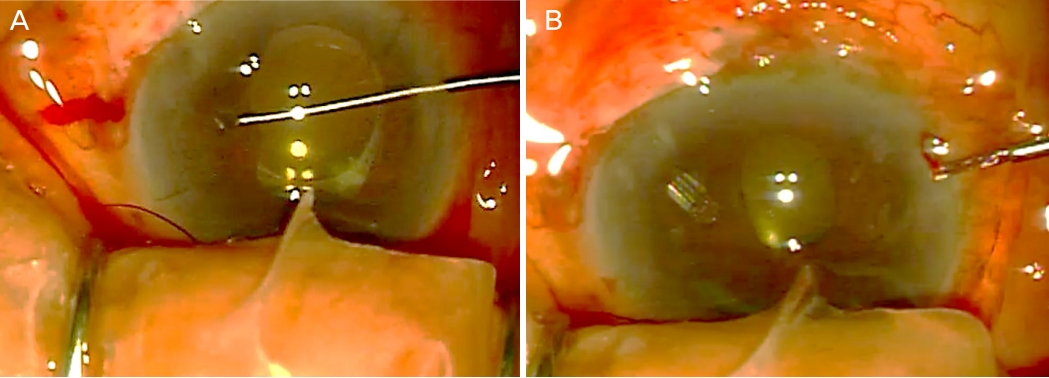
Figure 2.
Ocular ultrasonography. There were no signs of suprachoroidal hemorrhage or choroidal effusion present in posterior part of eye. OD = oculus dexter.
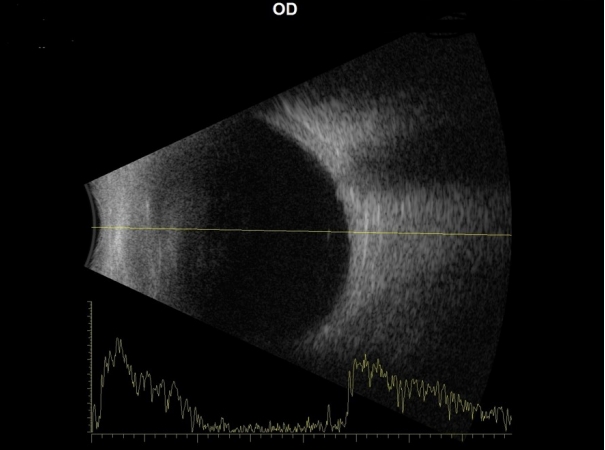
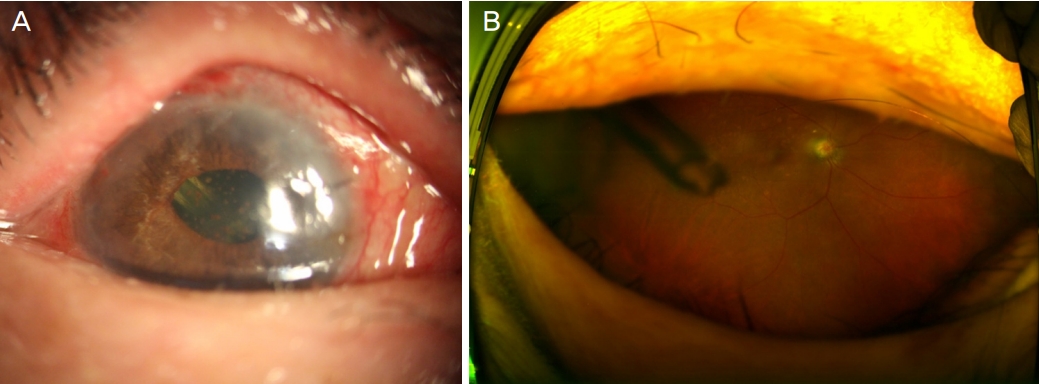
Figure 3.
Right eye 5 months after tube reposition into the vitreous cavity through pars plana. Tube tip was repositioned to avoid corneal decompensation. Slit lamp examination (A) showed clear cornea with deep anterior chamber, and ultra-widefield fundus photograph (B) showed tube position and patency.
REFERENCES
1) von Graefe A. Beltrage zur patholoogie and therapie des glaucomas. Albrecht von Graefe. Arch Ophthalmol 1869;15:article 108.
2) Foreman-Larkin J, Netland PA, Salim S. Clinical management of malignant glaucoma. J Ophthalmol 2015;2015:283707.




3) Krix-Jachym K, Żarnowski T, Rękas M. Risk factors of malignant glaucoma occurrence after glaucoma surgery. J Ophthalmol 2017;2017:9616738.




4) Lee SY, Bae HW, Kim CY. Evaluating anterior segment structure using anterior segment optical coherence tomography in malignant glaucoma after Ahmed valve implantation. Med case rep study protoc 2020;1:e0006.

5) Martínez-de-la-Casa JM, García-Feijoó J, Castillo A, et al. Malignant glaucoma following combined Ahmed valve implant and phacoemulsification surgery for chronic angle-closure glaucoma. Arch Soc Esp Oftalmol 2005;80:667-70.

6) Byrnes GA, Leen MM, Wong TP, Benson WE. Vitrectomy for ciliary block (malignant) glaucoma. Ophthalmology 1995;102:1308-11.


7) Schwartz AL, Anderson DR. Malignant glaucoma" in an eye with no antecedent operation or miotics. Arch Ophthalmol 1975;93:379-81.


8) Grzybowski A, Kanclerz P. Acute and chronic fluid misdirection syndrome: pathophysiology and treatment. Graefes Arch Clin Exp Ophthalmol 2018;256:135-54.




9) Balekudaru S, Choudhari NS, Rewri P, et al. Surgical management of malignant glaucoma: a retrospective analysis of fifty eight eyes. Eye (Lond) 2017;31:947-55.




11) Varma DK, Belovay GW, Tam DY, Ahmed II. Malignant glaucoma after cataract surgery. J Cataract Refract Surg 2014;40:1843-9.


12) Dave P, Senthil S, Rao HL, Garudadri CS. Treatment outcomes in malignant glaucoma. Ophthalmology 2013;120:984-90.


13) Bitrian E, Caprioli J. Pars plana anterior vitrectomy, hyaloido-zonulectomy, and iridectomy for aqueous humor misdirection. Am J Ophthalmol 2010 150:82-7. e1.


14) Wishart PK, Choudhary A, Wong D. Ahmed glaucoma valves in refractory glaucoma: a 7-year audit. Br J Ophthalmol 2010;94:1174-9.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 1,672 View
- 77 Download
- Related articles
-
Two Cases of Cataract after COVID-19 mRNA Vaccine Injection2022 December;63(12)
Surgical Treatment for Tube Erosion after Ahmed Valve Implantation.2016 March;57(3)
A Case of Malignant Glaucoma in a Vitrectomized Eye.2015 April;56(4)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



