샤임플러그-플라시도원반 방식 사진기와 새로운 파장가변 빛간섭단층촬영계의 전안부 계측치 비교
Comparison of Anterior Segment Measurements between Scheimpflug-Placido Camera and New Swept-source Optical Coherence Tomography
Article information
Abstract
목적
샤임플러그-플라시도원반 혼합방식의 전안부 사진기(SIRIUS® [Costruzione Strumenti Oftalmici, Florence, Italy])와 새로운 파장가변 빛간섭단층촬영계(ANTERION® [Heidelberg Engineering Inc., Heidelberg, Germany])을 이용하여 전안부 계측치를 비교해 보고자 하였다.
대상과 방법
총 74명, 101안을 대상으로 SIRIUS®와 ANTERION®으로 측정한 전안부 계측치를 분석하였다. 두 장비로 측정한 중심각막두께, 전방깊이, 각막곡률값, J0, J45 성분, 각막윤부직경을 비교하였다.
결과
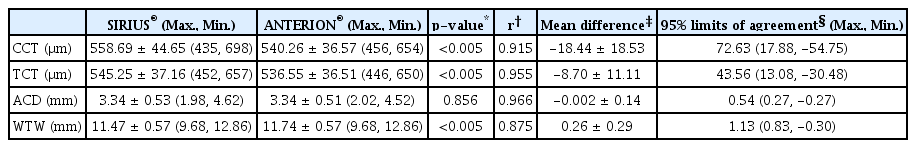
SIRIUS®와 ANTERION®으로 측정한 중심각막두께는 각각 558.69 ± 44.65 및 540.26 ± 36.57 μm였고 통계적으로 유의한 차이와(p<0.005), 높은 상관관계를 보였다(r=0.915). 전방깊이는 각각 3.34 ± 0.53 및 3.34 ± 0.51 mm (p=0.856)로 측정되었고 높은 상관관계를 보였다(r=0.966). 두 장비로 측정한 각막윤부직경(p<0.005, r=0.875), 평균각막곡률값(p=0.017, r=0.967) 및 J0 성분(p<0.005, r=0.933)은 모두 유의한 차이를 보였고 높은 상관관계를 보였다.
결론
SIRIUS®와 ANTERION®으로 측정한 전방깊이는 유의한 차이를 보이지 않았으나 중심각막두께, 각막윤부직경, 각막곡률값, J0 성분은 유의한 차이를 보여 두 장비는 임상에서 상호호환이 어려울 것으로 생각한다.
Trans Abstract
Purpose
We compared anterior segment measurements obtained using a Scheimpflug-Placido topographer (SIRIUS®, Costruzione Strumenti Oftalmici, Florence, Italy) and a new anterior module for a swept-source optical coherence tomography system (ANTERION®, Heidelberg Engineering Inc., Heidelberg, Germany).
Methods
Anterior segment measurements were evaluated in 74 eyes of 101 patients with the two devices. Central corneal thickness (CCT), anterior chamber depth (ACD), corneal refractive power (K), J0 (Jackson cross-cylinder with axes at 180° and 90°), J45 vector (Jackson cross-cylinder with axes at 45° and 135°), and white-to-white corneal diameter (WTW) measurements obtained using the SIRIUS® system and the new anterior segment module of ANTERION® were compared.
Results
The mean CCTs measured by SIRIUS® and ANTERION® were 558.69 ± 44.65 and 540.26 ± 36.57 μm, respectively. The difference was statistically significant (p < 0.005), and there were high correlations between the two methods (r = 0.915, p < 0.001). The mean ACD measurements were 3.34 ± 0.53 and 3.34 ± 0.51 mm (p = 0.856), respectively, for SIRIUS® and ANTERION®. The measurements were strongly correlated (r = 0.966, p < 0.001). The measurements of WTW, total mean K, and J0 obtained with the two systems differed significantly (p < 0.005, p = 0.017, and p < 0.005, respectively), with high correlations between the two systems (r = 0.875, r = 0.967, and r = 0.933, respectively; all p < 0.001).
Conclusions
There were significant differences in measurements of K, CCT, WTW, and J0 between the two devices. Agreement analysis suggests that SIRIUS® and ANTERION® should not be used interchangeably.
전안부의 생체계측은 각막질환, 녹내장, 굴절이상과 더불어 여러 안과질환들을 평가하고 백내장수술 등에 필요한 정보 제공에 있어서 매우 중요하기 때문에 정확한 생체계 측은 여러 안과질환의 정확한 진단 및 치료에 필수적이다[1,2]. 중심각막두께(central corneal thickness), 전방깊이(anterior chamber depth), 각막굴절력의 측정은 백내장수술 시 인공수정체 삽입 도수의 계산, 수술 방법의 결정에 있어서 중요한 지표가 된다[3]. 중심각막두께와 각막굴절력은 시력교정 수술 시 수술 방법의 결정 및 각막확장증 위험인자 파악에 사용된다[4,5]. 전안부의 생체계측은 다양한 장비에 의해 측정되는데 주사 세극등(slit-scanning tomography), 회전 샤임플러그 카메라(rotating Scheimpflug camera), 전안부빛간섭단층촬영계(anterior segment optical coherence tomography) 등이 있다[6]. 이 중 SIRIUS® (Costruzione Strumenti Oftalmici, Florence, Italy)는 360°로 회전하는 샤임플러그 카메라와 플래시도 디스크가 결합된 방식으로 두 개의 카메라가 있고, 중심부 카메라가 측정안의 주시를 담당하고, 두 번째 카메라가 측정하는 거리를 조절하는 방식이다. 샤임플러그 안구계측기는 전면각막곡률계와 더불어 후면각막곡률계도 측정할 수 있어 정확한 각막곡률값을 구할 수 있다[7]. ANTERION® (Heidelberg Engineering Inc., Heidelberg, Germany)은 새로운 고해상도 파장가변 방식의 빛간섭단층촬영 기기로써 1,300 nm의 긴 파장의 광원으로 14.0 mm의 깊이와 16.5 mm의 폭으로 촬영할 수 있고 14-32 mm의 안축장을 측정할 수 있으며 빛간섭단층촬영 이미지와 전면 각막 표면부터 후면 수정체 표면까지 자세한 구조적 이미지 정보를 제공할 수 있다[8,9].
이전 연구에서 SIRIUS®는 기존에 높은 재현성이 증명된 Pentacam® HR과[10] Galilei와[11] 비슷한 정도의 재현성이 확인되었고, 이를 바탕으로 SIRIUS®로 측정된 전안부 계측치는 여러 임상 상황에 적용할 수 있는 신뢰도를 가지고 있다고 알려져 있다[7]. 본 연구는 기존의 SIRIUS®와 새로운 전안부 계측기인 ANTERION®을 이용하여 중심각막두께, 전방깊이, 각막윤부직경, 각막곡률값의 비교분석을 통해 새롭게 소개된 ANTERION®의 임상적 신뢰도 및 SIRIUS®와 ANTERION®의 임상적 상호호환성에 대해 평가하고자 한다.
대상과 방법
2020년 3월부터 2020년 9월까지 본원에 내원한 74명 101안의 의무기록을 후향적으로 분석하였다. 본 연구는 김안과병원 윤리위원회승인(승인 번호: 2021-07-004)을 받았으며, 모든 연구 절차는 헬싱키선언의 가이드라인을 따랐다. 전안부 계측 시 측정값에 영향을 줄 수 이는 안과적 수술력, 외상, 그리고 백내장과 굴절이상을 제외한 다른 안과질환이 있는 경우는 제외하였다. 또한 최대교정시력이 0.8 이상인 환자들에서 측정한 경우만 연구에 포함하였다. 모든 환자들에게 동일한 검사자가 SIRIUS®와 ANTERION®을 이용하여 중심각막두께, 전방깊이, 각막윤부직경, 각막곡률값을 측정하였다. 검사 전 환자들에게 머리를 정확히 고정하도록 하였고, 눈을 깜빡이게 하여 눈물이 각막표면에 균일하게 도포되도록 하였다. 검사는 SIRIUS®, ANTERION®의 순서로 진행하였고, 각 검사마다 10분간의 휴식 시간을 거친 후에 검사를 시행하였다. SIRIUS®은 모든 측정치 검토 과정에서 “ok”를 보이는 측정치만 연구 대상에 포함시켰고, ANTERION®인 경우에는 “pass”의 경우에만 연구 대상에 포함시켰다.
SIRIUS®는 샤임플러그 카메라와 플래시도 디스크가 결합되어 있는 장비이며 중심부의 카메라는 측정안의 주시를 담당하고, 두 번째 카메라는 적절한 측정 거리를 적절하게 조절하는 역할을 한다[7]. ANTERION®은 1,300 nm의 파장을 이용하여 10 µm 이하의 해상도, 14 mm의 촬영 깊이, 16.5 mm까지의 측방향의 안구 B-scan 초음파 영상을 제공하여 준다. 또한, 깊은 투과력을 지닌 긴 파장의 광원으로 이용하여 수정체 후면까지 전안부 전체를 분석하고, 측면 촬영을 통해 전안부 각 부분의 단면 영상을 얻을 수 있다. 이 장비는 측면 촬영용 파장가변 빛간섭단층촬영기와 적외선 카메라 두 가지의 영상기법을 사용하여 촬영하고[8], 각막 정보는 65개의 방사형 B-scan 이미지에서 측정되고 최대 8.0 mm의 직경에서 분석된다[12].
중심각막두께는 각막 중앙의 각막상피에서 각막내피까지의 거리로, SIRIUS®에서는 35,632개의 각막 전면과 30,000개의 각막 후면 지점들의 정보를 이용하여 각막두께 지도(pachymetry map)를 재구성하여 측정하고[13], ANTERION®에서는 전면 각막 정점으로부터 전면과 후면 각막 표면 사이의 수직거리를 측정한다[14]. 전방깊이는 각막 중앙의 각막 내피의 정점에서 수정체 전낭 표면의 정점까지의 거리로 정의하였고 SIRIUS®에서는 광축(optical axis)을 따라 측정하고[15], ANTERION®에서는 시축(visual axis)을 따라 각막의 후면 중심에서부터 수정체 전면 중심까지의 거리인 방 수 깊이(aqueous depth)를 측정한 후 중심각막두께를 합하여 도출한다[14]. 각막굴절력(SimK-flat, steep, posterior K, total mean K)은 전면과 후면의 각막굴절력을 측정하여 분석하였고, SIRIUS®에서는 플래시도 디스크가 22개의 플래시도랑 각막지형측정기가 각막의 25개 방사형 영역을 촬영하여 전면각막굴절력의 경우 1.3375의 각막굴절상수, 후면각막굴절력의 경우 1.376의 각막굴절상수와 1.336의 방수굴절상수를 이용하여 계산된다[7]. ANTERION®에서는 총 65개의 방사형 이미지에서 측정하며 전면각막굴절력의 경우 1.3375의 각막굴절상수, 후면각막굴절력의 경우 1.376의 각막굴절상수와 1.336의 방수굴절상수를 이용하여 도출되었다[14]. 각막윤부직경의 경우 SIRIUS®에서는 촬영된 전안부 이미지에서 측정하였고[16], ANTERION®에서는 비측과 이측의 각막윤부 사이의 거리를 적외선카메라의 이미지상에서 측정하였다[17].
각막굴절력의 크기와 축에 대한 평가를 위해 파워벡터법을 이용하여 비교하였다. 파워벡터법에서 J0 성분은 잭슨의 크로스실린더에서 0°와 90° 경선의 굴절력에 의해 결정되고, J45 성분은 45°와 135° 경선의 굴절력에 의해 결정된다. 각 성분의 분석은 다음과 같은 공식을 사용하였다: J0 = (-cylinder/2) × cos 2α, J45 = (-cylinder/2) × sin 2α. J0 성분의 절대값이 J45 성분의 절대값보다 크고 양수이면 직난시로, 음수이면 도난시로 분류하고, J45 성분이 J0 성분보다 크면 사난시로 분류할 수 있다[18]. 또한 두 장비 간에 난시의 차이는 double-angle plot을 이용하여 비교하였다.
통계학적 분석은 SPSS 18.0 version (IBM Corp., Armonk, NY, USA)를 이용하였고, paired t-test를 이용하여 두 장비의 측정값 차이의 통계적 유의성을 평가하였다. 또한 Bland and Altman plots을 이용하여 두 장비 간의 일치도를 평가하였으며 Pearson correlation을 이용하여 측정 방식 간의 상관계수를 구하였고 통계적 유의한 차이가 있음은 p-value가 0.05 이하인 경우로 판단하였다.
결 과
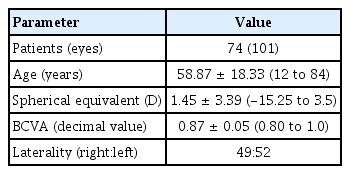
전체 환자수는 74명, 총 101안에서 본 연구가 진행되었고, 대상자들의 나이는 12세에서 84세로 평균 58.87 ± 18.33세, 현성굴절검사상 평균 구면 도수 대응치는 1.45 ± 3.39 D, 최대교정시력은 0.87 ± 0.05 (decimal value)였다(Table 1). SIRIUS®와 ANTERION®으로 측정한 중심각막두께는 각각 558.69 ± 44.65 μm, 540.26 ± 36.57 μm로 통계적으로 유의한 차이를 보였고(p<0.005), 높은 상관관계를 보였다(r=0.915, p<0.001) (Table 2). Bland-Altman plots 일치도 분석 결과 SIRIUS®와 ANTERION®의 95% 일치도 한계는 -54.75 to 17.88 μm였다(Fig. 1). 가장 얇은 부분 각막 두께는 SIRIUS®에서 545.25 ± 37.16 μm, ANTERION®에서 536.55 ± 36.51 μm로 측정되었으며, 통계적으로 유의한 차이를 보였고(p<0.005), 높은 상관관계를 보였다(r=0.955, p<0.001) (Table 2). Bland-Altman plots 일치도 분석 결과 SIRIUS®와 ANTERION®의 95% 일치도 한계는 -30.48 to 13.08 μm였다(Fig. 1).
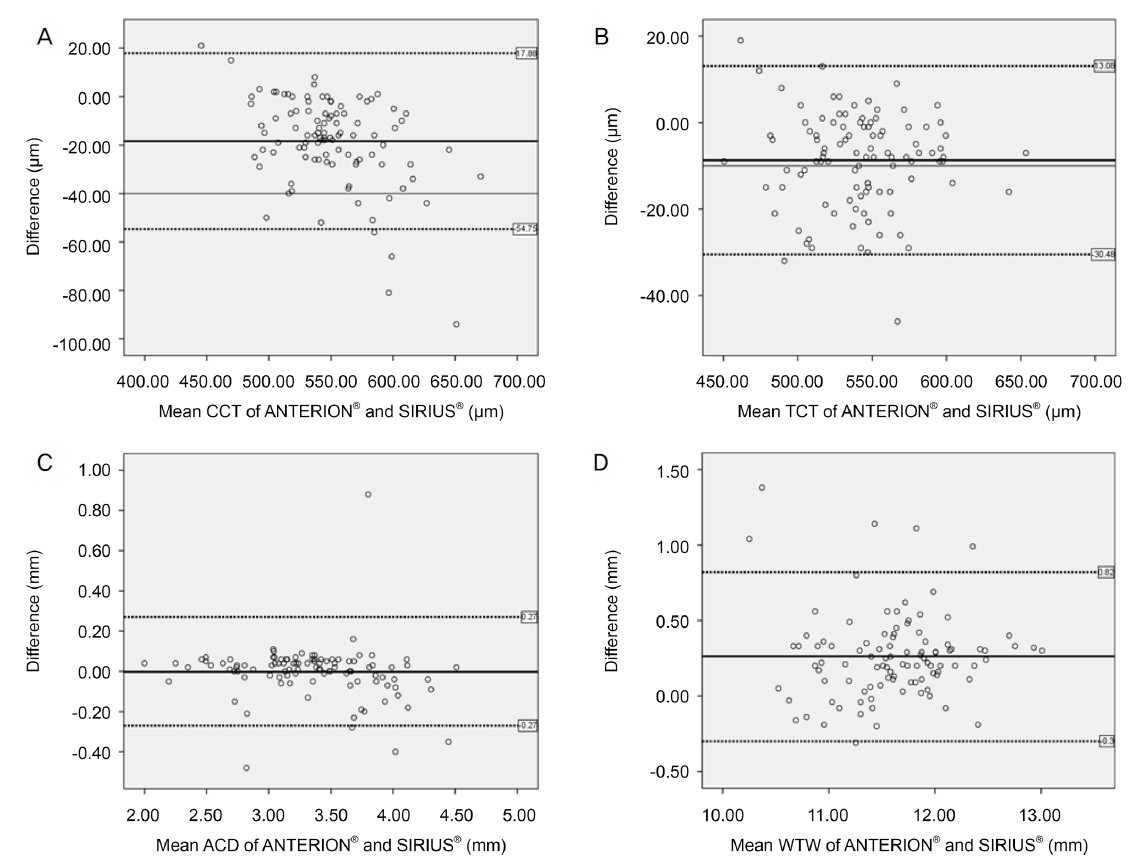
Bland Altman plots of ANTERION® and SIRIUS® in anterior segment parameters. (A) Central corneal thickness (CCT). (B) Thinnest corneal thickness (TCT). (C) Anterior chamber depth (ACD). (D) White to white (WTW). The solid line shows the mean difference (bias). Upper and lower dashed lines imply 95% limits of agreement.
SIRIUS®와 ANTERION®으로 측정한 전방깊이는 각각 3.34 ± 0.53 mm, 3.34 ± 0.51 mm로 측정되었고 통계적으로 유의한 차이를 보이지 않았고(p=0.856), 높은 상관관계를 보였다(r=0.966, p<0.001) (Table 2). Bland-Altman plots 일치도 분석 결과 SIRIUS®와 ANTERION®의 95% 일치도 한계는 -0.27 to 0.27 mm였다(Fig. 1). 각막윤부직경은 각각 11.47 ± 0.57 mm, 11.74 ± 0.57 mm로 통계적으로 장비 간에 유의한 차이를 보였고(p<0.005), 높은 상관관계를 보였다(r=0.875, p<0.001) (Table 2). Bland-Altman plots 일치도 분석 결과 SIRIUS®와 ANTERION®의 95% 일치도 한계는 -0.30 to 0.83 mm였다(Fig. 1).
SIRIUS®를 이용하여 측정한 전면 각막굴절력은 각각 43.37 ± 1.77 diopters (D) (SimK1), 44.39 ± 1.80 D (SimK2)로 측정되었고, ANTERION®은 각각 43.36 ± 1.77 D (SimK1), 44.55 ± 1.82 D (SimK2)로 높은 상관관계를 보였다(r=0.975, p<0.001; r=0,979, p<0.001). SimK1에서는 두 기기 간 통계적으로 유의한 차이를 보이지 않았으나 (p=0.624), SimK2에서는 통계적으로 유의한 차이를 보였다(p<0.005) (Table 3). SimK1과 SimK2의 두 기기 간 95% 일치도 한계는 각각 -0.80 to 0.76 D, -0.57 to 0.89 D였다(Fig. 2A, B). 후면 각막굴절력은 SIRIUS®에서 -6.20 ± 0.30 D (PostK1), -6.56 ± 0.34 D (PostK2), ANTERION®에서 -6.10 ± 0.27 D (PostK1), -6.47 ± 0.32 D (PostK2)로 측정되었다. 후면 각막굴절력은 PostK1, PostK2 모두 통계적으로 두 기기 간 유의한 차이를 보였고(p<0.005), 높은 상관관계를 보였다(r=0.907, p<0.001; r=0.906, p<0.001). PostK1과 PostK2의 두 기기 간 95% 일치도 한계는 각각 -0.14 to 0.34 D, -0.19 to 0.37 D였다(Fig. 2C, D). 마지막으로 평균 전체 각막굴절력도 SIRIUS®와 ANTERION®에서 각각 43.49 ± 1.77 D, 43.38 ± 1.76 D로 측정되었고, 두 기기 간 통계적으로 유의한 차이를 보였고(p=0.017) 높은 상관 관계를 보였다(r=0.967, p<0.001) (Table 3). 평균 전체 각막굴절력의 두 기기 간 95% 일치도 한계는 -1.00 to 0.78 D였다(Fig. 2E).

Comparison of corneal refractive power (K) and Astigmatism components obtained using SIRIUS® and ANTERION®

Bland Altman plots of ANTERION® and SIRIUS® in keratometry. (A) Simulated keratometry 1 (SimK1). (B) Simulated keratometry 2 (SimK2). (C) Posterior keratometry 1 (PostK1). (D) Posterior keratometry 2 (PostK2). (E) Mean keratometry (Total Mean K). The solid line shows the mean difference (bias). Upper and lower dashed lines imply 95% limits of agreement. D = diopters.
파워벡터분석의 난시 성분인 J0은 SIRIUS®에서는 0.30 ± 0.67 D, ANTERION®에서는 0.15 ± 0.57 D로 나타났고, 두 장비 간 통계학적으로 유의한 차이를 보였고(p<0.005) 높은 상관관계를 보였다(r=0.933, p<0.001). 다른 난시 성분인 J45에서는 SIRIUS®에서는 0.06 ± 0.27, ANTERION®에서는 0.03 ± 0.22로 나타났고 두 장비 간 통계학적으로 유의한 차이를 보이지 않았으나(p=0.18) 양의 상관관계를 보였다(r=0.622, p<0.001) (Table 3).
고 찰
전안부의 정확한 생체계측은 굴절수술 및 백내장수술에서 중요한 정보를 제공하고, 원추 각막, 부정형 난시, 각막뒤틀림, 굴절수술 전 각막두께검사, 굴절수술 후 각막확장증 등의 진단과 각막교정술(orthokeratology) 및 경과 관찰에 필수적이다. 전안부의 계측을 위해 주로 사용되고 있는 기계로는 회전샤임플러그 카메라인 Pentacam® HR [10], Galilei [11], 샤임플러그-플래시도 원반 혼합방식의 전안부 사진기인 SIRIUS® [7] 등이 있다. 본 연구에서는 이전에 비교하여 평가했던 적이 없었던 SIRIUS®와 최근 새로 개발된 ANTERION®의 전안부 계측치를 비교분석해 보고자 하였다.
본 연구에서 전방깊이를 제외한 모든 전안부 측정값에서 ANTERION®과 SIRIUS® 간에 모두 통계적으로 유의한 차이를 보였다. 또한 두 장비 간의 일치도를 보았을 때 전방 깊이를 제외한 95% 일치도 한계에서 산점도는 대부분 오차범위 내에 존재하였으나 다소 산발적인 분포로 중심값에 모이지 않는 경향성을 보였다. 이전 연구에서 SIRIUS®와 동일한 샤임플러그 카메라 방식을 사용하는 Pentacam® HR 간에 전안부 계측치의 차이를 비교 분석하였는데, 측정값 차이의 이유 중 하나를 측정안의 정렬로 들었다[19]. 전안부 계측치 측정에 동일한 샤임플러그 방식을 사용했음에도 장비 간에 이동을 하면서 측정안의 정렬이 달라지거나 동공 중심에서 이탈되는 정도에 따라 전안부 계측 측정값이 달라질 수 있다고 하였다. 본 연구에서도 장비 간에 이동을 하면서 측정안의 정렬이 달라졌을 가능성이 있다. 또한 두 장비 사이에는 측정안의 정렬 방법에 차이가 있는데 ANTERION®은 빛간섭단층촬영기와 적외선 카메라 두 가지의 영상기법을 사용하는 반면, SIRIUS®는 두 개의 카메라로 측정안의 정렬과 측정거리를 조절하게 되는데 이러한 요인도 측정치의 차이를 가져왔을 수 있다.
전방깊이에 있어 두 장비 측정치에는 통계적으로 유의한 차이를 보이지 않았고(p=0.856), 두 기기 간의 95% 일치도도 -0.27 to 0.27 mm로 나타났다. 이는 이전 샤임플러그-플라시도원반 혼합방식 기기와 파장가변 빛간섭단층촬영계의 비교 연구와 상응하는 결과를 보였다. 이전에 듀얼샤임플러그-플라시도원반 혼합방식의 기기인 Galilei G4와 파장가변 빛간섭단층촬영계인 IOLMaster 700®을 비교한 연구에서 두 장비들 간의 전방깊이는 서로 대체 가능하다고 보고하였다[20,21]. 또한 이전에 시행된 IOLMaster 500과 SIRIUS®를 비교한 연구에서 전방깊이는 SIRIUS®에서 IOLMaster 500보다 더 깊게 측정되었으나 그 차이는 통계학적으로 유의하지 않는 차이라 보고하였고, 그 원인으로 IOLMaster 500은 전방깊이를 각막후면에서 수정체 전면까지 시축을 따라 측정하고 SIRIUS®는 광축을 따라 측정한다는 점을 언급하였다[15]. 본 연구에서 사용된 ANTERION®도 시축을 따라 전방깊이를 측정하고, SIRIUS®는 광축을 따라 전방깊이를 측정한다는 점에서 두 장비 간의 미세한 차이의 가능성도 생각해 볼 수 있었으나, 본 연구에서는 평균 차이(mean difference)가 0.002 ± 0.14 mm로 낮은 결과를 보여 ANTERION®과 SIRIUS®의 전방깊이의 측정값은 서로 대체 가능하다고 생각된다.
각막두께 측정에 있어 SIRIUS®는 각막 전면과 후면의 지점들의 정보를 이용하여 pachymetric map을 구성하는 방식이고, ANTERION®은 전면 각막 정점으로부터 후면 각막 사이의 수직 거리를 측정하는 방식으로 각막두께를 측정한다. 현재까지 ANTERION®과 SIRIUS®를 직접적으로 비교한 연구는 없었지만, 같은 샤임플러그-플라시도원반 혼합방식의 기기인 TMS-5와 파장가변 빛간섭단층촬영계인 CASIA를 비교한 연구에서도 본 연구에서와 같이 각 기기 간의 중심각막두께 측정값의 차이를 보고하였다[22]. 이 연구에서 중심각막두께와 가장 얇은 부분 각막두께는 TMS-5보다 CASIA에서 더 작게(8 μm) 측정되었다. 또한 SIRIUS®와 스펙트럼영역 빛간섭단층촬영계인 RTVue를 비교한 논문에서도 중심각막두께와 가장 얇은 부분 각막두께는 SIRIUS®보다 RTVue에서 10 μm 작게 측정되었다고 보고하였다[23]. Pentacam® HR과 CASIA를 비교한 논문에서도 두 장비 간 중심각막두께와 가장 얇은 부분 각막두께 차이는 Pentacam® HR보다 CASIA에서 15 μm 작게 측정되었다고 보고되었다[24]. 이러한 차이의 원인으로는 샤임플러그 방식과 빛간섭단층촬영 방식 간 측정 방법의 차이로 볼 수 있다. 샤임플러그 방식의 기기는 회전하는 카메라에 의해 얻어진 각막 전, 후면의 융기를 측정하는 지점을 기반으로 공기-눈물막 경계 면에서 각막 후면 표면 사이의 각막두께를 측정하였고[25] 빛간섭단층촬영계는 각막의 전면과 각막의 후면을 식별하여 측정된 거리를 중심각막두께로 변환하는 방식으로 각막두께값을 도출한다[26]. 빛간섭단층촬영계에 의해 식별된 각막 전면경계면은 실제 각막 전면 표면보다 약간 후방에 위치될 수 있다고 하였고, 이는 각막두께의 과소 측정으로 이어질 수 있다고 설명하였다[27].
두 장비 간의 각막곡률 측정값을 비교해보면 SimK1를 제외한 다른 각막곡률 측정값들에서 두 장비 간 통계적으로 유의한 차이를 보였다(p<0.005). 파장가변 방식의 빛간섭단층촬영 기기인 IOLMaster 700과 두 개의 샤임플러그 카메라와 플래시도 디스크가 결합된 방식인 Galilei G6을 이용하여 분석한 이전 연구에서 SimK1, SimK2, mean keratometry는 통계학적으로 유의미한 차이가 있다고 보고하였으며, 두 기기 간 평균 차이는 각각 0.08 ± 0.51 D, 0.15 ± 0.58 D, 0.11 ± 0.43 D로 95% 일치도 한계는 -0.91 to 1.08 D, -0.99 to 1.29 D, -0.73 to 0.95 D로 보고하였다[28]. 본 연구에서도 Bland-Altman plots 일치도 분석 결과 SimK1, SimK2, total mean K의 두 기기 간의 평균 차이는 -0.02 ± 0.39 D, 0.16 ± 0.37 D, -0.11 ± 0.46 D로 95% 일치도 범위는 -0.80 to 0.76 D, -0.57 to 0.89 D, -1.00 to 0.78 D로 도출되어 이전에 시행된 연구와 비슷한 결과를 보였다. 추가로 이전에 시행된 SIRIUS®와 IOLMaster 700을 비교한 연구에서의 SimK1, total mean K의 95% 일치도 범위(-0.28 to 0.37 D, -0.17 to 0.26 D)보다 본 연구에서의 SimK1, total mean K의 95% 일치도 범위(-0.80 to 0.76 D, -1.00 to 0.78 D)가 더 큰 범위를 보였다[27]. 이 연구에서도 IOLMaster 700의 각막곡률값이 SIRIUS®의 값보다 통계학적으로 높게 측정되었다고 보고하였다. 차이의 원인으로 SIRIUS®에서는 35,632개의 각막 전면 지점을 샤임플러그 이미징과 플래시도 기반의 topography를 혼합하여 측정하여 각막곡률값을 도출하는 방식을 사용하였고, IOLMaster 700에서는 전면 각막 표면으로부터 18개의 지점을 측정하여 각막곡률값을 도출한 방식을 사용하였다는 점을 언급하며 두 장비 간의 측정 방식이 각막곡률값의 차이를 유발하였다고 설명하였다. 본 연구에서도 두 기기 모두 같은 각막굴절상수 및 방수굴절상수를 사용하나, SIRIUS®에서는 35,632개의 각막 전면 지점을 측정하여 3 mm 중심각막곡률을 계산하였고, ANTERION®에서는 총 65개의 방사형 이미지를 측정하여 3 mm 중심각막곡률값을 계산하는 방식의 차이가 두 장비 간 각막곡률값의 통계학적으로 유의미한 차이를 유발하였다고 생각해 볼 수 있다. 또한 플래시도 기반의 원리를 이용하여 전면각막굴절률을 측정할 경우 안구건조증과 같은 안구표면 상태에 파장가변 빛간섭단층촬영장비에 비해 영향도 더 받을 것으로 생각된다. 백내장수술 시 부정확한 인공수정체 계산 오류의 원인 중 하나는 각막곡률의 부정확한 측정으로 알려져 있고[29], 각막곡률값의 0.5 D의 오차는 ±1.17 D의 인공수정체 도수 차이를 가져올 수 있다고 하였다[30]. 본 연구에서 SIRIUS®와 ANTERION®의 total mean K의 평균 차이는 -0.11 ± 0.46 D로 나타나 두 장비 간 통계학적으로 유의미한 차이를 보이지 않았다 하더라도 인공수정체 도수 계산 시 두 장비 간에 약 1.0 D의 인공수정체 도수 오차가 날 수 있음을 고려해야 할 것이다.
백내장수술에서 정확한 각막난시의 측정은 필수적이며, 특히 토릭 인공수정체를 이용한 난시의 교정 시 각막난시값과 난시 축 측정의 일관성은 필수적이다. 난시는 난시 축과 난시 도수로 표기되어야 하고, 이를 효과적으로 표현하기 위해 임상에서는 구면원주 표기법을 사용한다. 그러나 난시축이 일치하지 않는 경우, 굴절력 계산이 어렵다. 이 문제를 보완하기 위해서 난시를 파워벡터법으로 변환하여 분석할 수 있으며, 이는 구면원주 표기법으로 표현한 계측치와 좋은 일치를 볼 수 있다[9]. 본 연구에서 파워벡터법에서의 난시 성분인 J0와 J45을 이용해 SIRIUS®와 ANTERION® 간의 난시축과 난시 크기를 통계적으로 비교하였다. 두 장비 간 J0은 두 장비 간의 통계적으로 유의한 차이를 보였고, J45는 두 장비 간의 통계적으로 유의한 차이를 보이지 않았다. J0은 ANTERION®보다 SIRIUS®에서 0.15 ± 0.25 D 더 크게 나타났고, J45 성분에서는 ANTERION®보다 SIRIUS®에서 0.03 ± 0.22 D 더 크게 나타났다. 다른 연구에서 Pentacam® HR과 IOLMaster 700 간에 J0은 통계적으로 유의한 차이를 보였고, J45은 통계적으로 유의한 차이를 보이지 않았다. 두 장비 간 평균 차이는 J0에서 0.33 ± 0.09 D, J45에서 -0.011 ± 0.10 D로 나타나 이러한 결과를 바탕으로 Pentacam® HR과 IOLMaster 700의 J0는 임상적으로 상호 호환하기 힘들 것이라고 하였다[31]. 본 연구도 이와 유사한 결과를 보였으며 SIRIUS®와 ANTERION®의 J0 결과는 임상적으로 상호호환하기 어려울 것이다.
Fig. 3은 두 장비로 측정한 전면난시와 후면난시를 double angle plot에 도식화한 것으로, 전면난시에서는 SIRIUS®보다 ANTERION®에서 더 큰 범위의 분포를 보였고(blue ellipse), 이는 ANTERION®에서 전면난시 측정 시 높은 변동성을 의미한다. 그러나 후면난시에서는 SIRIUS®보다 ANTERION®에서 더 작은 영역을 보였고, 이는 ANTERION®에서 후면 난시 측정 시 낮은 변동성을 의미한다. 후면난시에서는 깊은 투과력을 지닌 파장가변 빛간섭단층촬영을 한 경우가 후면난시 측정에 유리할 수 있다고 생각한다.
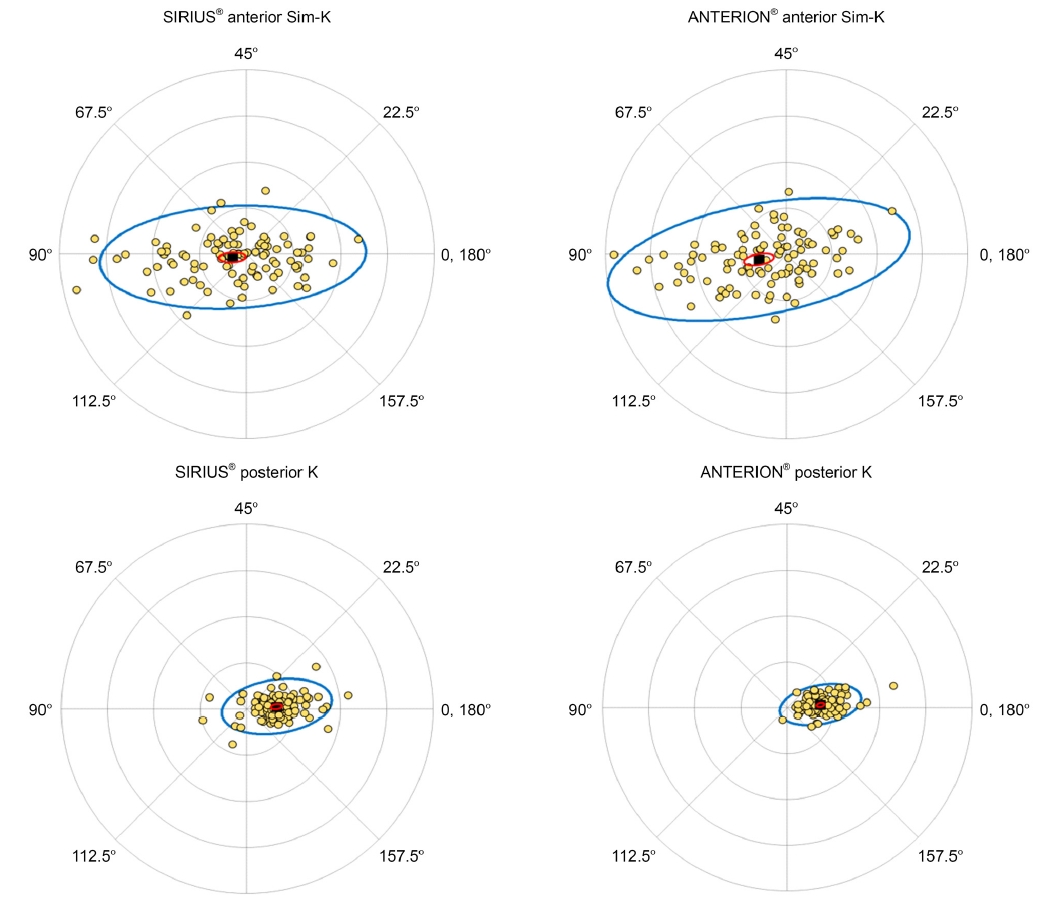
Anterior and posterior astigmatism using double angle plot between ANTERION® and SIRIUS®. Sim-K = simulated keratometry.
본 연구에서 SIRIUS®와 ANTERION® 간 각막윤부직경의 평균 차이는 0.26 ± 0.29 mm였으며, 95% 일치도 범위는 1.13 (-0.30 to 0.83)으로 나타났다. 이전에 ANTERION®, IOLMaster 700, Pentacam® HR, Cassini 간의 각막윤부직경을 비교한 연구에서 ANTERION®과 Pentacam® HR는 임상적으로 상호호환 가능하나, IOLMaster 700과 Pentacam® HR은 상호호환이 가능하지 않다고 보고하였다[32]. 이 연구에서 IOLMaster 700과 Pentacam® HR의 평균차는 0.277 ± 0.143 mm, 95% 일치도 범위는 -0.004 to 0.559로 보고하였으며, 유수정체 인공수정체(implantable collamer lens) 크기가 0.5 mm의 범위로 변한다는 점을 언급하며 각막윤부직경의 차이가 0.5 mm 이상인 경우는 임상적으로 의미 있는 변화이기 때문에 IOLMaster 700과 Pentacam® HR의 각막윤부직경의 측정값은 임상적으로 상호호환이 가능하지 않다고 하였다[32]. 본 연구에서도 SIRIUS®와 ANTERION® 간의 95% 일치도 범위가 0.5 mm보다 큰 결과를 보여 두 장비 간의 각막윤부직경 결과는 임상적으로 상호호환하기 어려울 것이다.
본 연구의 제한점으로 백내장이 있는 환자를 포함하였기에 측정 시 오차를 유발할 수 있는 변수가 된다는 점이다. 하지만 최대교정시력 0.8 이상인 환자를 연구 대상으로 하였고 측정값의 고유 신뢰도를 확인하고 분석하였기에 그 오차를 최소화하였을 것으로 생각한다. 또한, 각 장비마다 여러 번의 측정을 통해 SIRIUS®와 ANTERION®의 반복성과 재현성을 평가하지 않았다. 새로운 장비의 신뢰도를 판단할 때 그 장비의 재현성을 측정하고, 높은 재현성이 확인되면 기존에 사용하던 장비와 비교하게 된다. 이전 연구에서 SIRIUS®는 기존에 높은 재현성이 증명된 Pentacam® HR과[10] Galilei와[11] 비슷한 정도의 재현성이 확인되었고, 이를 바탕으로 SIRIUS®로 측정된 전안부 계측치는 여러 임상 상황에 적용할 수 있는 신뢰도를 가지고 있다고 보고되었다[7]. ANTERION®은 최근 진행된 한 연구에서 기존에 높은 재현성이 증명된 MS-39 [33]와 비슷한 정도의 재현성이 확인되었고[14], 다른 연구에서도 ANTERION®의 높은 재현성을 증명하였다[8]. 본 연구에서는 한 번 측정한 계측치로 SIRIUS®와 ANTERION®을 비교하였는데 두 장비 모두 높은 재현성이 있어 측정값을 비교하는 데 문제는 없을 것으로 보인다.
이 연구는 샤임플러그-플라시도원반 혼합 방식의 전안부 사진기와 높은 투과력의 파장가변 빛간섭단층촬영 장비를 이용한 전안부 계측치 간에 국내 최초 비교 분석이라는 점에서 의의가 있겠다. 결론적으로 전방깊이 외에 다른 전안부 계측치에서 통계학적인 차이를 보여 임상적용 시에 SIRIUS®와 ANTERION®를 상호 대치하여 사용할 수 없을 것이라고 생각되고, 특히 굴절교정수술이나 백내장수술 시 두 장비 간의 차이를 고려해야 할 것으로 생각된다.
Notes
Conflict of Interest
The authors have no conflicts to disclose.
References
Biography
최곤수 / Gon Soo Choe
김안과병원
Kim’s Eye Hospital