 |
 |
| J Korean Ophthalmol Soc > Volume 62(12); 2021 > Article |
|
국문초록
대상과 방법
쇼그렌증후군 환자들 중 마이봄샘기능장애가 동반된 43명을 펄스광선조사 치료와 마이봄샘 압출을 함께 시행받은 복합 치료군(22명)과 마이봄샘 압출만 시행 받은 단독치료군(21명)으로 분류하였다. 치료는 3주 간격으로 총 3회에 걸쳐 시행되었으며 치료 종료 6주 후 한 번 더 내원하였다. 내원 시마다 안구표면질환지수, 형광 및 비침습눈물막파괴시간, 눈물띠 높이, 쉬르머검사, 안구표면 염색 점수, 마이봄샘 질 및 배출 점수, 마이봄 점수 평가를 시행하였으며 복합치료군에서는 추가적으로 눈물막지질층을 평가하였다.
결과
복합치료군에서 안구표면질환지수, 형광 및 비침습눈물막파괴 점수, 각막표면염색 점수, 마이봄 질 점수, 마이봄 점수와 눈물막지질층 등급은 치료 전에 비하여 통계적으로 유의한 호전을 보였고, 복합치료군과 단독치료군 모두에서 마이봄 배출 점수의 호전을 보였다(p<0.05). 결막표면염색 점수, 쉬르머검사, 눈물띠 높이는 두 치료군 모두 치료 전과 후의 차이를 보이지 않았다. 치료 종료 후 복합치료군이 단독치료군에 비하여 안구표면질환지수, 각막염색 점수, 마이봄 질 및 배출 점수는 유의하게 낮았고, 형광 눈물막파괴시간은 높게 나타났다(p<0.05).
ABSTRACT
Purpose
To investigate the efficacy of intense pulsed light (IPL) treatment in patients with meibomian gland dysfunction (MGD) associated with Sjögren’s syndrome.
Methods
This study included 43 patients with MGD and Sjögren’s syndrome. Patients received either IPL with meibomian gland expression (IPL/MGX) (n = 22) or MGX only (n = 21). Treatments were administered three times at a 3-week interval. Patients were followed up 6 weeks after the end of the treatment. Ocular Surface Disease Index (OSDI), tear film breakup time with fluorescein dye (FBUT), non-invasive tear breakup time, tear meniscus height (TMH), Schirmer test, SICCA ocular surface staining score, meibum quality score (MQS), and meibum expression score (MES) were evaluated at each visit. Meibomian gland dropouts (meiboscore) and tear film lipid layer grade were measured using keratography.
Results
OSDI, FBUT, corneal surface staining score, MQS, meiboscore, and tear film lipid layer grade improved after IPL/MGX treatment (p < 0.05). In both treatment groups, MES significantly improved (p < 0.01 and p < 0.05 for IPL/MGX and MGX groups, respectively). The Schirmer test score, conjunctival surface staining score, and TMH after treatment were not significantly different between the groups. After treatment, the IPL/MGX group had significantly lower OSDI, FBUT, corneal staining score, MQS, and MES, but higher FBUT, compared with the MGX group (p < 0.05).
쇼그렌증후군은 주로 여성에서 발생하는 자가면역성 질환의 일종으로 건성안, 구강건조증을 유발하는 흔한 원인이다[1-3]. 쇼그렌증후군은 침샘, 눈물샘 등의 외분비샘에 림프구가 축적되어 신경전달물질들의 방출이 방해되고, 눈물 분비세포와 눈물관상피세포의 기능장애를 유발하여 수성 눈물 생성이 줄어들고 건성안이 유발된다[4].
쇼그렌증후군 건성안은 수성 눈물 생성 부족뿐 아니라 눈물막 증발이 증가해서 발생하는 증발형 건성안이 동반되는 경우가 많다[4]. 쇼그렌증후군 건성안 환자들에서 마이봄질 및 배출 점수의 저하, 마이봄샘의 소실이 흔하게 나타난다는 것은 여러 연구들에서 확인된 바 있다[5-7]. 이전의 보고에 의하면, 결막의 상피는 쇼그렌증후군의 직접적인 면역학적인 타겟이 되어 마이봄샘 개구부 상피세포의 과각화가 발생하며 마이봄샘의 소실을 유발한다[8-11]. 또한 쇼그렌증후군 환자들에서 림프구의 침윤이 외분비샘 뿐만 아니라 피부의 피지선에도 침범하는 양상이 관찰되었다[6,7,12,13]. 이는 마이봄샘 또한 쇼그렌증후군의 표적 기관이 될 수 있음을 시사하며 쇼그렌증후군 건성안 환자들이 다른 건성안 환자들에서보다 더 심한 마이봄샘의 기능저하를 보이는 것을 뒷받침한다[6].
쇼그렌증후군을 동반한 건성안 환자들의 치료는 인공눈물, 안연고, 스테로이드, 싸이클로스포린A 등 수분결핍 건성안을 해결하기 위한 것들이 주를 이룬다[14]. 쇼그렌증후군에 의한 수분결핍 건성안이 있는 환자들에서 마이봄샘기능장애로 인한 지질층 부족이 발생하게 되면, 안구표면의 손상이 더욱 심하게 일어날 수 있어, 마이봄샘기능장애에 대한 적극적인 치료가 필요하다[15]. 이를 위해 눈꺼풀 위생 관리, 온찜질, 마이봄샘 압출(meibomian gland expression, MGX) 등을 시도할 수 있으나, 그 효과가 단기적이고 쇼그렌증후군으로 인한 심한 안구표면 손상과 환자의 건성안 증상은 호전되지 않는 경우가 많다[16-20].
최근 마이봄샘기능장애의 치료로 펄스광선조사(intense pulsed light, IPL) 치료가 새로운 대안으로 사용되며, 기존의 치료에 효과가 없는 마이봄샘기능장애에서도 그 효과가 입증되었다[16,17,21-25]. IPL 치료는 590-1,300 nm 정도의 파장의 광선을 10-15차례 정도 눈꺼풀 주위에 조사하여 선택적으로 눈꺼풀 표면의 혈관을 수축시켜 이상 혈관확장 및 홍반을 감소시킨다. 또한 박테리아 및 모낭충을 감소시키고 피부 표면 온도를 높여 비정상적인 마이봄을 녹여 액체화 할 수 있다[22,24,25]. IPL 치료를 시행받은 후 환자들의 눈물층 내 염증성 사이토카인(interleukin-17A, interleukin-6, prostaglandin E2)이 감소된다는 연구 결과도 있는데, 이러한 IPL 치료의 작용이 쇼그렌증후군과 관련된 건성안 및 마이봄샘 기능장애의 치료에 도움이 될 수 있을 거라고 판단하였다[16,21,22,24,26,27].
마이봄샘기능장애에 동반된 증발형 건성안에서 IPL 치료의 효과는 여러 연구들을 통하여 입증되었으나[16,17,21-25], 마이봄샘기능장애를 동반한 쇼그렌증후군 건성안 환자들을 대상으로 시행한 IPL 치료 효과에 대한 보고는 없었다. 본 연구에서는 마이봄샘기능장애가 동반된 쇼그렌증후군 환자들을 IPL과 MGX를 함께 시행한 복합치료군과 MGX만 시행한 단독치료군으로 나눠 눈물막 및 안구표면지표와 더불어 마이봄샘 지표들의 변화를 비교해 보고자 하였다.
2020년 7월부터 2020년 12월까지 전남대학교병원 안과에 내원한 쇼그렌증후군 환자 중 마이봄샘기능장애가 동반된 환자 43명, 85안을 대상으로 연구를 시행하였다. 본 임상시험은 헬싱키선언을 준수하였고, 전남대학교병원 생명의학 연구윤리심의위원회의 승인에 따라 진행되었다(승인번호: CNUH-2021-128). 각 환자들은 모두 자발적인 의사 하에 치료 방법에 대한 충분한 설명을 듣고 이해한 후 동의서를 작성하였다. 모든 대상자들의 성별, 나이, 안과적 질환의 유병 기간 및 종류, 전신질환의 유무, 수술 기왕력 등을 확인하였고 쇼그렌증후군은 2016년 발표된 American College of Rheumatology/European League Against Rheumatism의 분류기준을 토대로 진단하였다[28]. 마이봄샘기능장애는 2011년 International Workshop on Meibomian Gland Dysfunction에서 정의한 것을 기준으로 하였다[29].
대상자들을 IPL 치료와 MGX를 모두 시행 받은 IPL/MGX군(22명 43안)과 MGX만 시행 받은 MGX군(21명 42안)으로 무작위 배정하였다. 환자들은 모두 0.15% 히알루론산 눈물 약(New hyaluni 0.15%®, Taejoon Pharm Co. Ltd, Seoul, Korea), 0.05% 사이클로스포린 점안액(Cyporin N 0.05%®, Taejoon Pharm Co. Ltd, Seoul, Korea)을 사용 중이었고, 연구 기간 동안 점안액 치료를 유지하였다. 대상자 중 마이봄샘 기능장애에 대한 치료로 온찜질이나 티트리오일 등의 눈꺼풀 위생을 교육받은 환자들은 연구에서 제외하였다. 또한 치료 시작일 3개월 이내에 백내장수술, 눈꺼풀수술 등의 안과 수술을 시행 받거나, 안구의 감염성 질환을 앓았던자, 만성 콘택트렌즈 사용자인 경우, 다래끼 등 마이봄샘기능에 영향을 줄 수 있는 요인이 있는 경우, 치료 시작일 2주 이내에 녹내장 안약 등 건성안에 악영향을 줄 만한 안약을 점안하거나 전신 약제를 복용 중인 경우, 치료 시작일로부터 3개월 이내에 건성안 치료 약제를 변경한 경우도 연구 대상에서 제외하였다. 단안만 연구에 이용하였으며, 더 심한 각결막염색 점수를 보이는 쪽을 분석에 이용하였고, 양안이 같은 경우 우안을 분석하였다.
환자들에게 광과민성과 피부색에 따라 Fitzpatrick 피부 유형 분류를 시행하였고, Fitzpatrick 피부유형 5, 6형 환자들은 IPL 치료 시 피부의 색소침착이나 흉터 등의 부작용이 발생할 수 있으므로 IPL 치료를 시행하지 않았다[30]. IPL 치료 시행 전, 환자들이 화장을 하고 있을 경우, 화장을 지우도록 권고하였고, 눈꺼풀에 초음파용 젤을 바른 후 쟈거리드 플레이트(Jaeger lid plate, Suzhou Mingren Medical Equipment, Suzhou, China)를 결막낭에 위치시켜 각막과 공막을 보호하였다. IPL 치료는 M22® (Lumenis, Dreieich, Germany) 장비의 590 nm 필터를 이용하여 6 mm 원통형 사파이어쿨팁으로 조사를 시행하였으며 15 J/cm2의 출력으로 아래눈꺼풀에 8회, 위눈꺼풀에 3회 조사하였다[26].
MGX 치료는 프로파라카인 점안액(Paracaine, Hanmi Pharm, Seoul, Korea)으로 점안마취를 시행한 후 숙련된 각막 전문의(H.J.Y.)가 하안검 및 상안검의 내측, 중앙, 가측 부위를 마이봄샘 압출용 포셉(Arita forcep, Katena Products, Parsippany-Troy Hills, NJ, USA)을 이용하여 일정한 힘으로 누르며 시행하였다.
치료는 총 3회, 3주 간격으로 시행하였으며 세 번째 치료가 종료되고 6주 뒤 한 차례 더 경과 관찰을 시행하였다. 모든 대상 환자들에서 내원 시마다 시력, 안압, 안구표면질환지수(Ocular Surface Disease Index, OSDI), 쉬르머검사(Schirmer test)를 통해 증상 및 기본 눈물분비량을 평가하고 세극등현미경을 이용하여 형광 눈물막파괴시간(fluoresecein tear breakup time)을 측정한 이후, 플루레신과 리사민그린을 이용한 각막표면 및 결막표면염색검사를 시행하였고, 각 검사 사이에는 5분의 간격을 두었다. 마이봄샘기능을 평가하기 위하여 마이봄 질 점수(meibum quality score), 마이봄 배출 점수(meibum expression score), 눈꺼풀테의 이상 정도(lid margin abnormality score)를 평가한 후 케라토그라피(Keratograph 5M, Oculus Optikgerӓte GmbH, Wetzlar, Germany)를 이용하여 비침습눈물막파괴시간, 눈물띠높이, 마이봄 점수(Meiboscore)를 평가하였다. IPL/MGX군에서는 추가적으로 내원 시마다 눈물막지질층 등급(tear film lipid layer grade)을 확인하였다.
매 방문 시마다 OSDI 설문지를 이용하여 증상의 정도를 측정하였다. OSDI 설문지는 건성안 증상에 대한 질문 5가지, 시각 기능과 관련하여 일상생활에 지장을 받은 정도를 확인하는 질문 4가지, 그리고 환경적 요인에 의한 자극에 대한 질문 3가지로 구성되었다. 전체 OSDI 점수는 각 점수의 총합을 답변한 질문 수로 나누어 계산하였다[31].
눈물띠 높이는 케라토그라피를 이용하여 아래눈꺼풀 경계의 중심부에서 동공의 중심부로 수직의 가상선을 그어 소수점 두 번째 자리까지 밀리미터(mm) 단위로 측정하였다. 쉬르머검사는 점안마취 없이 쉬르머검사지(Eagle Vision, Memphis, TN, USA)를 하결막낭 이측 1/3 지점에 넣고 5분 후 눈물로 인해 젖은 부위의 길이를 mm 단위로 측정하였다.
형광 눈물막파괴시간은 세극등현미경의 코발트블루 광원을 통하여 1.0%로 희석한 플루오레신(fluorescein) 용액을 결막에 한 방울 점안한 후 대상자의 눈을 몇 차례 깜빡이게 한 뒤, 염색된 눈물막에서 형광염색의 결손이 관찰될 때까지의 시간을 소수점 1자리까지 초 단위로 3회 측정한 후, 그 평균값을 계산하였다. 비침습눈물막파괴시간 측정은 케라토그라피를 이용하였고, 적외선 빛을 통해 나타나는 플라시도 링이 일그러지는 시간을 모든 지점에서 관찰하여 마이어상이 처음 깨지는 시간들의 평균값을 소수점 2자리까지 초 단위로 측정하였다.
안구표면염색검사는 1.0% 플루오레신 용액 4 μL와 1.0% 리사민그린(lissamine green) 용액 4 μL를 혼합한 용액을 환자의 아래눈꺼풀에 점안하여 염색한 후 Sjögren’s International Collaborative Clinical Alliance 점수를 기준으로 표기하였다. 각막상피손상 정도의 평가는 플루오레신용액 염색 후 표층 점상각막미란이 없으면 0점, 1-5개가 있을 경우 1점, 6-30개가 관찰될 경우 2점, 30개를 초과하는 경우 3점으로 계산하였다. 여기에 플루오레신에 의한 판형태의 염색을 보이는 경우, 동공을 가리는 위치에서 염색이 보이는 경우, 1개 이상의 필라멘트가 관찰되는 경우에 각 1점을 더하여 최종 각막상피손상점수로 정했다. 결막상피손상의 정도는 리사민그린용액염색에서 점상병변의 개수에 따라 0-9개면 0점, 10-32개일 경우 1점, 33-100개면 2점, 100개가 넘는 점상병변이 보이면 3점으로 계산하였고, 이측과 비측 결막 염색 점수를 더하여 점수화하였다.
마이봄샘기능 평가(Meibomian gland involvement score)는 아래눈꺼풀 중심부의 5개 마이봄샘을 기준으로 하였다[29,32]. 마이봄 질 점수는 마이봄샘 압출용 포셉을 사용하여 눈꺼풀테를 지압하여 나오는 분비물의 양상에 따라 분비물이 맑은 액체일 경우 0점, 탁한 액체이면 1점, 탁하면서 입자양상을 띨 때 2점, 치약과 같은 양상일 때 3점으로 분류하였다. 마이봄 배출 점수는 분비물이 나오는 마이봄샘의 숫자에 따라 마이봄 배출 점수를 평가하였다. 모든 마이봄샘에서 분비물이 나오는 경우 0점, 3-4개의 마이봄샘에서 분비물이 나오면 1점, 1-2개의 마이봄샘에서 분비물이 나오는 경우 2점, 모든 마이봄샘에서 분비물이 배출되지 않는 경우를 3점으로 점수화하였다. 눈꺼풀테 이상의 경우, 눈꺼풀 경계에 불규칙성이 있거나 눈꺼풀 경계의 모세혈관 확장 혹은 마이봄샘 배출구 막힘 소견이 있는 경우를 각각 1점씩으로 더해서 총 0점부터 3점으로 평가하였다.
마이봄점수는 케라토그라피를 이용하여 마이봄샘을 촬영한 후 측정하였다. 마이봄샘의 소실이 없는 경우 0점, 소실이 전체 마이봄샘 면적의 1/3 미만일 경우 1점, 1/3 이상 2/3 미만의 소실이 있는 경우 2점, 2/3 이상의 소실이 있는 경우 3점으로 점수화하였다[32].
두 치료군 사이의 요소들을 비교하기 위하여 연속형 변수는 Mann Whitney U test를 이용하였고, 범주형 변수는 Fisher exact test를 이용하여 분석하였다. 각 군에서 치료 전과 치료 후의 변화를 비교하기 위하여 Wilcoxon signed rank test를 이용하였다. 마이봄샘 촬영을 통한 마이봄 점수를 평가할 때, 이미지 분석 프로그램인 Image J (Bethesda, MD, USA, http://imageJ.nih.gov)를 이용하였다. 모든 통계적 분석은 SPSS for Windows Ver 23.0 (IBM Corp., Armonk, NY, USA)를 이용하였으며, p-value가 0.05 미만인 경우를 통계적으로 유의하다고 판정하였다.
본 연구에 참여한 쇼그렌증후군 환자 43명 중 IPL/MGX군은 여자 22명, MGX군은 남자 1명, 여자 20명이었다. 대상자의 평균 나이는 IPL/MGX군에서 62.36 ± 10.59세, MGX군에서 평균 62.54 ± 9.20세였다(p=0.86). 치료 시작일 1년 전부터 3개월 이전 사이에 백내장 등의 안과적 수술 및 눈꺼풀수술 과거력이 있는 환자 수와 쇼그렌증후군 및 마이봄샘기능장애의 유병 기간은 두 군에서 차이가 없었다. IPL/MGX군에서 Fitzpatrick 피부 유형은 3형이 14명, 4형이 8명이었다(Table 1). 치료 전 OSDI, 형광 눈물막파괴시간, 비침습눈물막파괴시간, 눈물띠 높이, 쉬르머검사, 각막 및 결막염색 점수, 마이봄 질 및 배출 점수, 눈꺼풀테 이상 정도, 마이봄 점수는 두 군 간의 유의한 차이가 없었다(Table 2).
OSDI는 IPL/MGX군에서 치료 전 46.50 ± 22.08, 치료 종료 6주 후 39.26 ± 22.36으로 유의한 호전을 보였고(p=0.02), MGX군의 경우 치료 전 43.35 ± 19.99, 치료 후 42.39 ± 17.21로 유의한 변화 보이지 않았다(Fig. 1A). 치료 후 IPL/MGX군의 OSDI 점수는 MGX군에 비해 낮았다(p=0.04). OSDI의 호전이 관찰된 IPL/MGX군에서 OSDI 항목들을 세분화해서 치료 전과 치료가 종료된 이후의 점수를 비교해보았을 때, 안구 증상에 관한 항목은 치료 전 8.43 ± 5.50에서 치료 후 7.29 ± 4.78 (p=0.02), 시각 기능과 관련된 점수는 8.08 ± 3.60에서 치료 후 6.86 ± 3.77로 감소를 보였으나(p=0.04), 환경적 요인에 대한 점수는 치료 전 4.71 ± 4.15, 치료 후 5.43 ± 3.78로 차이가 없었다(p=0.24, Fig. 1B).
형광 눈물막파괴시간은 IPL/MGX군에서 치료 전 4.41 ± 1.37초였고 치료 후 4.91 ± 1.60초로 호전되었으며(p=0.03), MGX군에서는 치료 전 4.29 ± 1.27초, 치료가 종료된 뒤 3.95 ± 1.40초로 유의한 차이를 보이지 않았다. 치료 후 형광 눈물막파괴시간은 IPL/MGX군이 MGX군에 비하여 길게 나타났다(p=0.03, Fig. 2A). 비침습눈물막파괴시간은 IPL/MGX군에서 치료 전 8.26 ± 4.67초였으나 치료 후 8.80 ± 3.74초로 증가하였으며(p=0.01), MGX군에서는 치료 전 비침습눈물막파괴시간이 8.64 ± 4.11초였으나 치료 후 8.46 ± 4.10초로 유의한 차이 보이지 않았다(p=0.61). 치료 후 두 군 간의 비침습눈물막파괴시간은 유의한 차이를 보이지 않았다(p=0.08, Fig. 2B). 눈물띠 높이는 IPL/MGX군에서 치료 전 0.20 ± 0.08 mm, 치료 후 0.21 ± 0.07 mm (p=0.68), MGX군에서 치료 전 0.21 ± 0.10 mm, 치료 후 0.18 ± 0.09 mm였다(p=0.56, Fig. 2C). 쉬르머검사 수치는 치료 전 IPL/MGX군에서 5.23 ± 1.82 mm, MGX군에서 5.29 ± 1.79 mm였으며(p=0.95), 치료가 종료된 이후에도 각각 5.18 ± 1.56 mm, 5.09 ± 1.67 mm였다(p=0.18, Fig. 2D). 각막염색 점수는 IPL/MGX군에서 치료 시작 전 2.05 ± 1.40, 치료 후 1.23 ± 1.51로 호전되었고(p=0.02), MGX군은 치료 전 2.24 ± 1.95, 치료 후 2.00 ± 2.12로 유의한 차이가 없었다(Fig. 2E). 결막염색 점수는 치료 전 IPL/MGX군과 MGX군에서 각각 2.05 ± 1.93, 2.05 ± 1.69, 치료 이후 2.00 ± 1.62, 1.93 ± 1.44로 두 군에서 모두 호전을 보이지 않았다(Fig. 2F). 치료 이후의 각막염색 점수는 IPL/MGX군이 MGX군보다 낮았고(p=0.04), 결막염색 점수는 두 군 간 차이를 보이지 않았다(p=0.59).
마이봄 질 점수는 IPL/MGX군에서 치료 시작 전 1.46 ± 0.60, 치료 종료 후 1.00 ± 0.62로 치료 전과 비교하여 유의한 호전을 보였다(p<0.01, Fig. 3A). 마이봄 배출 점수 또한 치료 전에는 1.36 ± 0.58이었으나, 치료 종료 후 0.86 ± 0.64로 유의한 호전을 보였다(p<0.01, Fig. 3B). 눈꺼풀테 이상 정도의 경우, 치료 시작 전 1.64 ± 0.49, 치료 종료 후 1.16 ± 0.64였다(p=0.41, Fig. 3C). MGX군에서 치료 전 마이봄 질 점수와 눈꺼풀테 이상 정도는 각각 1.29 ± 0.85, 1.57 ± 0.74였으며, 치료 후에는 각각 1.48 ± 0,75, 1.62 ± 0.59로 호전을 보이지 않았다. 그러나 마이봄 배출 점수는 MGX군에서 치료 전 1.29 ± 0.90, 치료 종료 후 1.10 ± 0.75로 감소하였다(p=0.04). 마이봄샘의 소실의 호전은 마이봄샘 촬영을 통하여 확인할 수 있었고, Fig. 4와 같이 나타났다. 마이봄 점수는 IPL/MGX군에서는 치료 전 1.27 ± 0.70이나 치료 후 0.95 ± 0.79로 유의한 호전을 보였으며(p=0.02), MGX군에서는 치료 전 1.27 ± 0.94, 치료 후 1.00 ± 0.76으로 소실의 감소를 보이지 않았다(p=0.30, Fig. 3D).
눈물막지질층 등급은 적은 표본 수로 인하여 grade 0와 4는 관찰되지 않았고, 나머지 총 4가지 등급으로 평가가 이루어졌다. 치료 전 grade 1은 10안(45%), grade 2는 3안(14%), grade 3은 7안(32%), grade 5는 2안(9%)이었으며, 세 차례 IPL/MGX 치료를 받고 6주 후 다시 측정하였을 때는 각각 5안(23%), 5안(23%), 8안(36%), 4안(18%)으로 변화하였다(p=0.03, Fig. 5).
IPL 치료를 시행 받은 22명의 환자들 중 4명에서 레이저치료 직후 눈 주위 열감을 호소하였고, 1명은 레이저치료 직후 일시적 눈꺼풀부종을 호소하였다. 5명 모두에게 냉찜질을 20분 시행하였고, 이후 증상 호전을 보였다. 또한 경도의 안구통증을 호소한 환자가 3명이 있었으나, 치료 종료 후 이상 증상을 호소하지는 않았다.
건성안은 눈물막의 불안전성과 높은 눈물 삼투압 농도, 안구 표면 염증 및 손상, 그리고 신경감각계 이상 등의 여러 원인이 복합적으로 영향을 주어 발생하는 안구 표면질환을 뜻한다[4,36]. 건성안의 종류에는 크게 수분결핍형과 눈물증발형이 있으며 최근, 눈물증발형 건성안의 발생에 있어 마이봄샘기능의 중요성이 강조되고 있다[37]. 마이봄샘기능장애가 지속될 경우, 마이봄샘의 파괴, 눈물의 과도한 증발, 삼투압 및 염증의 증가로 이어져 눈물 지질층의 불안정성이 유발되어 안구표면의 손상을 유발할 수 있다[32,38]. 쇼그렌증후군은 수분 부족형 건성안을 유발하는 대표적인 질환이지만, 마이봄샘의 파괴가 동반되는 경우가 많으며 대개 쇼그렌증후군이 없는 건성안 환자들에 비해서 그 정도가 심하다[5-7].
IPL 치료는 수분결핍형과 눈물증발형 건성안 모두에서 치료 효과가 있다[17,21,23,25,39]. 건성안에 대한 IPL의 치료 효과에 대한 연구는 불응성 마이봄샘기능장애, 눈물증발형 건성안, 다른 기저질환이 없는 건성안 등 여러 환자군에 대하여 행해졌고, 대부분의 연구들에서 보조적인 건성안 치료 방법으로 사용 시 눈물막파괴시간, 쉬르머검사 및 주관적인 건성안 증상의 호전이 뚜렷했고, 마이봄샘 지표의 호전을 보이는 경우도 있었다[7,16,26,39].
비쇼그렌 건성안 환자들에 비해 쇼그렌증후군과 연관된 건성안 환자들은 각결막 염증 및 손상이 심할 뿐만 아니라 더 심한 마이봄샘기능저하를 동반하는 경우가 많은데, 지금까지 쇼그렌증후군 환자들을 대상으로 IPL 치료의 효과에 대해 살펴본 연구는 없었다. 따라서 본 연구에서는 쇼그렌증후군이 동반된 마이봄샘기능장애 환자들에서 IPL 치료 후 눈물막 및 안구표면지표, 마이봄샘 지표의 변화를 확인하고자 하였다. 그 결과, IPL 치료와 MGX를 함께 시행받은 환자에서 치료 전에 비하여 치료 후 OSDI, 형광 및 비침습눈물막파괴시간, 각막염색 점수, 눈물막 지질층 등급 등의 눈물막 및 안구표면지표와 마이봄 질 점수, 배출 점수 및 마이봄 점수 등 마이봄샘기능 평가에서 뚜렷한 호전이 나타났다. 치료 후 IPL/MGX군의 눈물막 및 안구표면지표, 마이봄샘기능 평가를 MGX군과 비교했을 때도 OSDI, 각막염색 점수, 마이봄 질 및 배출 점수가 낮게 나타났고, 형광 눈물막파괴시간은 높게 측정되었다.
OSDI는 IPL/MGX군에서 치료 후 감소하였으며, 특히 건성안의 안구 증상 및 시각 기능에 관련된 항목에서 호전을 보였다. 마이봄샘기능장애가 있는 건성안 환자에서 건성안 증상은 마이봄샘기능장애의 징후와 관련이 있고, 특히 마이봄 질 점수와 건성안의 증상 사이의 강한 상관관계가 있다[22,40,41]. 본 연구에서도 IPL/MGX군에서 마이봄 질 점수의 호전이 있었는데, 이러한 마이봄샘기능호전이 건조증 증상 호전과 연관이 있었을 것으로 보인다. 형광 및 비침습눈물막파괴시간, 각막염색점수의 유의한 호전이 있었던 것은, IPL 치료가 눈물층의 지질 성분 비율을 높이고, 눈꺼풀 염증을 호전시킨 것이 원인이 되었을 것으로 보인다[38,42].
IPL 치료의 건성안에 대한 영향을 살펴본 연구에서 Gil et al [43]은 건성안 환자에서 조절펄스광선조사(intense regulated pulse light) 치료 후 형광 눈물막파괴시간, 쉬르머검사, 안구표면염색점수 및 주관적인 건성안 증상이 호전되는 것을 확인하였다. 그러나 본 연구에서는 쉬르머검사의 호전이 관찰되지 않았는데, 이는 본 연구에서 쇼그렌증후군 환자들은 수년 이상의 사이클로스포린 안약과 인공누액 사용을 했음에도 증상 조절이 되지 않는 환자들을 대상으로 했다는 것이 영향을 주었을 것이고, IPL 치료의 항염증 효과가 눈물샘에까지 작용하지는 않았음을 시사해볼 수 있다.
마이봄 질 및 배출 점수는 IPL/MGX 복합치료군에서 치료를 시행 받은 이후 호전되었다. 마이봄 배출 점수는 MGX 단독치료군에서도 호전되었는데, 이는 기존의 연구에 부합하는 결과로 IPL 레이저에서 나온 열과 적외선의 영향으로 막혀있던 마이봄 지질의 액화가 촉진되어 마이봄샘에서 분비가 촉진되었을 것으로 생각된다[44].
마이봄 점수와 눈물막 지질층 등급은 IPL/MGX군에서만 유의한 개선이 있었다. 이는 마이봄샘 배출능이 좋아지면, 마이봄샘이 위축이 억제되고, 손상된 마이봄샘의 기능이 호전되기 때문일 것으로 생각된다[45,46]. IPL의 광조절(photomodulation) 효과가 광생체자극(photobiostimulatory) 효과를 내면서 동시에 상처 회복, 광회춘(photorejuvenation) 등의 세포 활성을 유발해 마이봄샘의 미세구조를 변화시켰을 수 있다[46-48].
본 연구에서는 쇼그렌증후군 환자에게서 동반된 마이봄샘 기능장애에 시행한 IPL/MGX 치료에 대해 OSDI, 형광 및 비침습눈물막파괴시간, 안구표면염색점수, 눈물막 지질층 등급 등의 눈물막 및 안구 표면지표와 마이봄샘기능 평가뿐만 아니라 마이봄샘 촬영을 통하여 마이봄샘의 구조적 변화를 함께 확인하였다는 점에서 그 의의가 있다. 그러나, 일반적으로 IPL 치료를 시행할 시 치료에 반응이 없는 환자에게는 몇 차례 더 치료를 시행하게 된다. 본 연구는 모든 환자들을 3회에서 치료 종료하였기 때문에 실제로 불응성 환자인지, 치료를 더 하면 호전 가능성이 있을지 판단이 어려웠고, 장기적인 부작용 또한 확인이 불가하였다. 또한, 이전에 안구건조증 치료를 위하여 사용하던 안약 점안을 유지하였으나, 안약의 효과가 완전히 배제되지는 않았기 때문에 편향(bias)이 있을 수 있었을 것으로 보인다. 또한 본 연구에서는 케라토그라피 등의 레이저 간섭계를 이용하여 눈물막 지질층의 등급을 정성적으로 평가하였으나 IPL/MGX 군에서만 눈물막 지질층에 대한 분석이 이루어졌다는 한계점이 있었다. 이에 추후 시행될 연구에서는 모든 환자들을 대상으로 눈물막 지질층에 대한 효과를 정량적으로 분석할 수 있는 Lipiview (Tearscience, Johnson & Johnson, New York, NY, USA) 등의 기계를 사용하는 것이 치료 효과를 평가하는 데에 도움이 될 것으로 사료된다. 이러한 점들을 보완하는 다기관 장기 임상 연구가 필요할 것이다.
본 연구에서 마이봄샘기능장애가 있는 쇼그렌증후군 환자에게 IPL 치료와 마이봄샘 압출을 함께 시행하는 것이 눈물막 및 안구표면지표의 호전뿐만 아니라 마이봄샘의 기능적, 구조적 개선에도 도움이 되었다. 따라서, 쇼그렌증후군 환자에게서 마이봄샘기능장애가 있을 경우 IPL 치료 및 마이봄샘 압출 복합 치료가 효과적인 보조적 치료법이 될 수 있을 것이다.
Figure 1.
Ocular surface disease index (OSDI) in study subjects. (A) Changes of OSDI score after treatments in the intense pulsed light (IPL)/meibomian gland expression (MGX) and MGX groups. (B) Changes of OSDI subgroup scores in the IPL/MGX group. *p < 0.05 compared with baseline values; †p < 0.05 compared between the IPL/MGX and MGX groups.
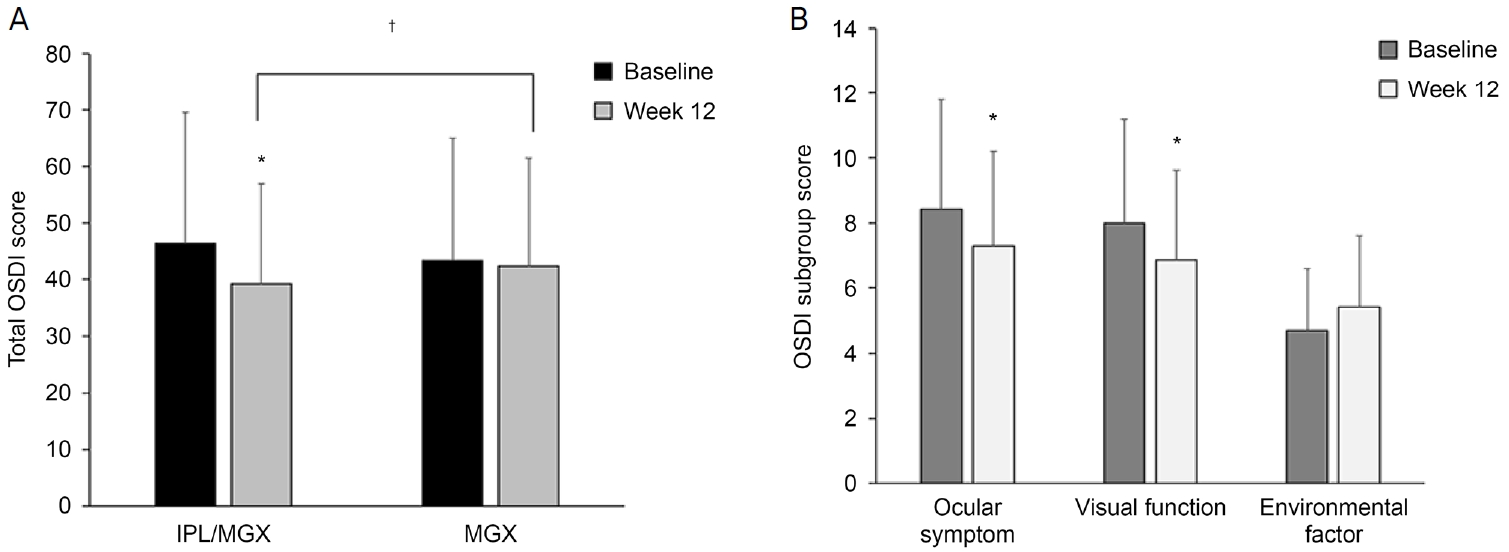
Figure 2.
Changes in clinical objective parameters of dry eye after treatments in the intense pulsed light (IPL)/meibomian gland expression (MGX) and MGX groups (A-F). FBUT = fluorescein tear film break up time; NIBUT = tear film noninvasive breakup time. *p < 0.05 compared with baseline values; †p < 0.05 compared between the IPL/MGX and MGX groups.

Figure 3.
Changes in meibomian gland involvement score after treatments in the intense pulsed light (IPL)/meibomian gland expression (MGX) and MGX groups (A-D). *p < 0.05, compared with baseline values; †p < 0.05 compared between the IPL/MGX and MGX groups.

Figure 4.
Representative meibographic images of a meibomian gland dysfunction patient. (A) Meibograpic image before intense pulsed light (IPL)/meibomian gland expression (MGX) treatment. (B) Meibographic image after IPL/MGX treatments.
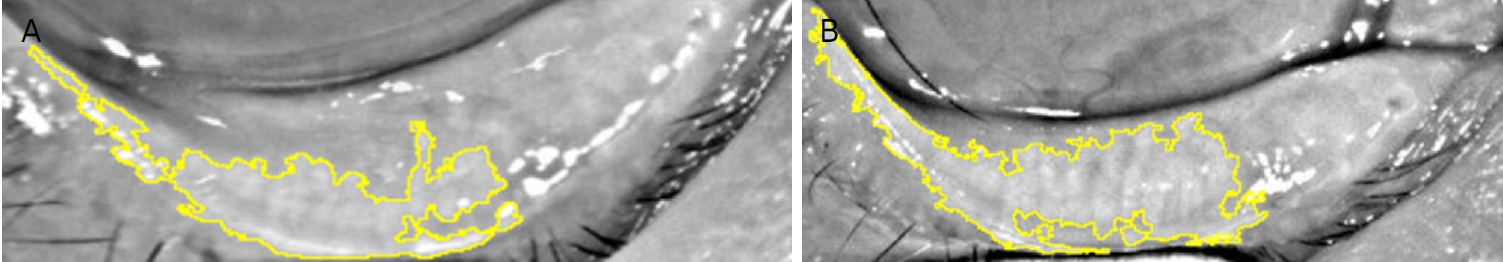
Figure 5.
Tear film lipid layer grading by keratograph. (A) Tear film lipid layer grade before and after treatment in the intense pulsed light/meibomian gland expression group. Data represent the percentage of eyes (n = 22). (B) Examples of improved tear film lipid layer grade, grade 1 (open meshwork) at baseline and grade 5 (color fringe) at the end of the follow up period. *p < 0.05, compared with baseline.

Table 1.
The characteristics of the study subjects in the IPL-MGX and MGX groups
| Characteristic | IPL/MGX group (n = 22) | MGX group (n = 21) | p-value |
|---|---|---|---|
| Age (years) | 62.36 ± 10.59 | 62.54 ± 9.20 | 0.86* |
| Sex (female/male) | 22/0 | 20/1 | |
| Fitzpatrick scale (III/IV) | 14/8 | - | - |
| Previous ocular surgery or blepharosurgery (%) | 32 | 24 | 0.56† |
| Duration of Sjögren’s syndrome (years) | 6.64 ± 3.19 | 7.00 ± 3.59 | 0.96* |
| Duration of MGD (years) | 3.50 ± 2.52 | 3.70 ± 1.30 | 0.44* |
Table 2.
Baseline clinical parameters of patients with meibomian gland dysfunction accompanied by Sjögren’s syndrome in the IPL-MGX and MGX groups
| IPL/MGX group (n = 22) | MGX group (n = 21) | p-value* | |
|---|---|---|---|
| Tear film and ocular surface parameters | |||
| OSDI (score) | 46.76 ± 22.08 | 43.35 ± 19.99 | 0.78 |
| FBUT (seconds) | 4.41 ± 1.37 | 4.29 ± 1.27 | 0.76 |
| NIBUT (seconds) | 8.26 ± 4.67 | 8.64 ± 4.11 | 0.36 |
| TMH (mm) | 0.20 ± 0.09 | 0.21 ± 0.13 | 0.90 |
| Schirmer test (mm) | 5.23 ± 1.82 | 5.29 ± 1.79 | 0.71 |
| Corneal staining score | 2.05 ± 1.40 | 2.24 ± 1.95 | 0.90 |
| Conjunctival staining score | 2.05 ± 1.93 | 2.06 ± 1.69 | 0.77 |
| Meibomian gland involvement score | |||
| Meibum quality (score) | 1.46 ± 0.60 | 1.29 ± 0.85 | 0.32 |
| MG expressibility (score) | 1.36 ± 0.58 | 1.29 ± 0.90 | 0.46 |
| Lid margin (score) | 1.64 ± 0.49 | 1.57 ± 0.7 | 0.86 |
| Meiboscore | 1.27 ± 0.94 | 1.27 ± 0.70 | 0.98 |
REFERENCES
1) Sullivan DA, Rocha EM, Aragona P, et al. TFOS DEWS II sex, gender, and hormones report. Ocul Surf 2017;15:284-333.


2) Shimazaki J. Definition and diagnostic criteria of dry eye disease: historical overview and future directions. Invest Ophthalmol Vis Sci 2018;59:DES7-12.


3) The definition and classification of dry eye disease: report of the Definition and Classification Subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf 2007;5:75-92.


4) Bron AJ, de Paiva CS, Chauhan SK, et al. TFOS DEWS II pathophysiology report. Ocul Surf 2017;15:438-510.


5) Shimazaki J, Goto E, Ono M, et al. Meibomian gland dysfunction in patients with Sjögren syndrome. Ophthalmology 1998;105:1485-8.


6) Kang YS, Lee HS, Li Y, et al. Manifestation of meibomian gland dysfunction in patients with Sjögren’s syndrome, non-Sjögren’s dry eye, and non-dry eye controls. Int Ophthalmol 2018;38:1161-7.


7) Epitropoulos AT, Goslin K, Bedi R, Blackie CA. Meibomian gland dysfunction patients with novel Sjögren’s syndrome biomarkers benefit significantly from a single vectored thermal pulsation procedure: a retrospective analysis. Clin Ophthalmol 2017;11:701-6.


8) Pflugfelder SC, Tseng SC, Sanabria O, et al. Evaluation of subjective assessments and objective diagnostic tests for diagnosing tear-film disorders known to cause ocular irritation. Cornea 1998;17:38-56.


9) Hikichi T, Yoshida A, Tsubota K. Lymphocytic infiltration of the conjunctiva and the salivary gland in Sjögren’s syndrome. Arch Ophthalmol 1993;111:21-2.


10) Jester JV, Rife L, Nii D, et al. In vivo biomicroscopy and photography of meibomian glands in a rabbit model of meibomian gland dysfunction. Invest Ophthalmol Vis Sci 1982;22:660-7.

11) Jester JV, Nicolaides N, Smith RE. Meibomian gland studies: histologic and ultrastructural investigations. Invest Ophthalmol Vis Sci 1981;20:537-47.

12) Hwang JH, Lee JH, Chung SH. Comparison of meibomian gland imaging findings and lipid layer thickness between primary sjögren syndrome and non-sjögren syndrome dry eyes. Ocul Immunol Inflamm 2020;28:182-7.


13) Bloch KJ, Buchanan WW, Wohl MJ, Bunim JJ. Sjögren’s syndrome: a clinical, pathological, and serological study of sixty-two cases. Medicine (Baltimore) 1965;44:187-231.


14) Akpek EK, Lindsley KB, Adyanthaya RS, et al. Treatment of Sjögren’s syndrome-associated dry eye an evidence-based review. Ophthalmology 2011;118:1242-52.


15) Fox RI. Sjögren’s syndrome: current therapies remain inadequate for a common disease. Expert Opin Investig Drugs 2000;9:2007-16.


16) Arita R, Fukuoka S, Morishige N. Therapeutic efficacy of intense pulsed light in patients with refractory meibomian gland dysfunction. Ocul Surf 2019;17:104-10.


17) Wladis EJ, Aakalu VK, Foster JA, et al. Intense pulsed light for meibomian gland disease: a report by the American Academy of Ophthalmology. Ophthalmology 2020;127:1227-33.


18) Thode AR, Latkany RA. Current and emerging therapeutic strategies for the treatment of meibomian gland dysfunction (MGD). Drugs 2015;75:1177-85.


19) Qiao J, Yan X. Emerging treatment options for meibomian gland dysfunction. Clin Ophthalmol 2013;7:1797-803.


20) Geerling G, Tauber J, Baudouin C, et al. The international workshop on meibomian gland dysfunction: report of the subcommittee on management and treatment of meibomian gland dysfunction. Invest Ophthalmol Vis Sci 2011;52:2050-64.



21) Tashbayev B, Yazdani M, Arita R, et al. Intense pulsed light treatment in meibomian gland dysfunction: a concise review. Ocul Surf 2020;18:583-94.


22) Vigo L, Giannaccare G, Sebastiani S, et al. Intense pulsed light for the treatment of dry eye owing to meibomian gland dysfunction. J Vis Exp 2019 Apr 1 doi: 10.3791/57811.

23) Xue AL, Wang MTM, Ormonde SE, Craig JP. Randomised double-masked placebo-controlled trial of the cumulative treatment efficacy profile of intense pulsed light therapy for meibomian gland dysfunction. Ocul Surf 2020 18:286-97. [E-pub].


24) Tang Y, Liu R, Tu P, et al. A retrospective study of treatment outcomes and prognostic factors of intense pulsed light therapy combined with meibomian gland expression in patients with meibomian gland dysfunction. Eye Contact Lens 2021;47:38-44.


25) Mejía LF, Gil JC, Jaramillo M. Intense pulsed light therapy: a promising complementary treatment for dry eye disease. Arch Soc Esp Oftalmol (Engl Ed) 2019;94:331-6.


26) Rong B, Tang Y, Tu P, et al. Intense pulsed light applied directly on eyelids combined with meibomian gland expression to treat meibomian gland dysfunction. Photomed Laser Surg 2018;36:326-32.


27) Liu R, Rong B, Tu P, et al. Analysis of cytokine levels in tears and clinical correlations after intense pulsed light treating meibomian gland dysfunction. Am J Ophthalmol 2017;183:81-90.


28) Shiboski CH, Shiboski SC, Seror R, et al. 2016 American College of Rheumatology/European League Against Rheumatism Classification Criteria for Primary Sjögren’s Syndrome: a consensus and data-driven methodology involving three international patient cohorts. Arthritis Rheumatol 2017;69:35-45.



29) Tomlinson A, Bron AJ, Korb DR, et al. The international workshop on meibomian gland dysfunction: report of the diagnosis subcommittee. Invest Ophthalmol Vis Sci 2011;52:2006-49.



30) Fitzpatrick TB. The validity and practicality of sun-reactive skin types I through VI. Arch Dermatol 1988;124:869-71.


31) Asiedu K, Kyei S, Mensah SN, et al. Ocular surface disease index (OSDI) versus the standard patient evaluation of eye dryness (SPEED): a study of a nonclinical sample. Cornea 2016;35:175-80.

32) Fu J, Chou Y, Hao R, et al. Evaluation of ocular surface impairment in meibomian gland dysfunction of varying severity using a comprehensive grading scale. Medicine (Baltimore) 2019;98:e16547.



33) Craig JP, Muntz A, Wang MTM, et al. Developing evidence-based guidance for the treatment of dry eye disease with artificial tear supplements: a six-month multicentre, double-masked randomised controlled trial. Ocul Surf 2021;20:62-9.


34) Guillon JP. Use of the tearscope plus and attachments in the routine examination of the marginal dry eye contact lens patient. Adv Exp Med Biol 1998;438:859-67.


35) Craig JP, Wang MT, Kim D, Lee JM. Exploring the predisposition of the Asian eye to development of dry eye. Ocul Surf 2016;14:385-92.


36) Tsubota K, Yokoi N, Watanabe H, et al. A new perspective on dry eye classification: proposal by the Asia Dry Eye Society. Eye Contact Lens 2020;46 Suppl 1:S2-13.


37) Viso E, Gude F, Rodríguez-Ares MT. The association of meibomian gland dysfunction and other common ocular diseases with dry eye: a population-based study in Spain. Cornea 2011;30:1-6.


38) Korb DR, Blackie CA. Meibomian gland diagnostic expressibility: correlation with dry eye symptoms and gland location. Cornea 2008;27:1142-7.


39) Gupta PK, Vora GK, Matossian C, et al. Outcomes of intense pulsed light therapy for treatment of evaporative dry eye disease. Can J Ophthalmol 2016;51:249-53.


40) Seo MH, Shin JY, Lee DH, Kim JH. Objective parameters associated with subjective symptom severity in dry eye syndrome patients. J Korean Ophthalmol Soc 2017;58:259-67.

41) Zengin N, Tol H, Gündüz K, et al. Meibomian gland dysfunction and tear film abnormalities in rosacea. Cornea 1995;14:144-6.


42) Nichols JJ, Nichols KK, Puent B, et al. Evaluation of tear film interference patterns and measures of tear break-up time. Optom Vis Sci 2002;79:363-9.


43) Gil TY, Bae GH, Kwag JY, et al. Effect of intense regulated pulse light on thickness of tear film lipid layer and dry eye syndrome. J Korean Ophthalmol Soc 2018;59:1103-7.

44) Lane SS, DuBiner HB, Epstein RJ, et al. A new system, the LipiFlow, for the treatment of meibomian gland dysfunction. Cornea 2012;31:396-404.


45) Yin Y, Gong L. Reversibility of gland dropout and significance of eyelid hygiene treatment in meibomian gland dysfunction. Cornea 2017;36:332-7.


46) Yin Y, Liu N, Gong L, Song N. Changes in the meibomian gland after exposure to intense pulsed light in meibomian gland dysfunction (MGD) patients. Curr Eye Res 2018;43:308-13.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




