 |
 |
| J Korean Ophthalmol Soc > Volume 62(11); 2021 > Article |
|
국문초록
대상과 방법
안과 질환이 없는 성인을 대상으로 촬영한 빛간섭단층촬영 및 빛간섭단층혈관조영술을 분석하였다. ‘Hole-in-the-card test’를 시행하여 주시안을 확인하였다. 시신경유두주위에 4.5 x 4.5 mm scan을 시행하여 시신경유두주위 관류밀도 및 플럭스 지수를 측정하였으며, 중심황반두께 및 신경절세포층 및 내망상층, 망막신경섬유층 두께 역시 측정하였다. 주시안과 비주시안의 빛간섭단층촬영, 빛간섭단층혈관조영술 측정값을 비교 분석하였다.
결과
42명 84안이 포함되었다. 대상군의 평균 나이는 27.3 ± 5.63세였으며, 주시안은 우안 28안(66.7%), 좌안이 14안(33.3%)이었다. 빛간섭단층촬영검사에서 주시안과 비주시안 간의 중심황반두께(260.00 ± 14.16 μm, 258.71 ± 15.18 μm, p=0.183), 신경절세포층 및 내망상층 복합체두께(82.02 ± 5.07 μm, 82.43 ± 5.60 μm, p=0.460), 망막신경섬유층 두께(99.36 ± 9.27 μm, 97.90 ± 9.46 μm, p=0.091)에 유의한 차이가 없었다. 또한, 빛간섭단층혈관조영술검사의 시신경 주위 표층모세혈관망의 관류 밀도(44.62 ± 5.25%, 45.60 ± 2.27%, p=0.221), 플럭스 지수(0.455 ± 0.020, 0.449 ± 0.028, p=0.060)에서도 통계적인 차이는 확인되지 않았다.
ABSTRACT
Purpose
To assess whether optical coherence tomography (OCT) measurements and peripapillary microvascular parameters measured via optical coherence tomography angiography (OCTA) were similar between the dominant and non-dominant eyes of normal subjects.
Methods
We retrospectively analyzed spectral domain OCT and OCTA data on healthy Koreans. The “hole-in-the-card” technique was used to determine ocular dominance. The perfusion density (PD) and flux index (FI) of the peripapillary 4.5 × 4.5-mm area were measured via OCTA. Central macular, peripapillary retinal nerve fiber layer, and macular ganglion cell-inner plexiform layer thicknesses were measured with the aid of spectral-domain OCT. The OCT and OCTA data of dominant and non-dominant eyes were compared.
Results
A total of 84 eyes of 42 healthy subjects were analyzed. The average age was 27.3 ± 5.63 years. Twenty-eight subjects (66.7%) were right eye-dominant and 14 (33.3%) left eye-dominant. None of the central macular (260.00 ± 14.16 μm, 258.71 ± 15.18 μm, p = 0.183), macular ganglion cell-inner plexiform layer (82.02 ± 5.07 μm, 82.43 ± 5.60 μm, p = 0.460), or peripapillary retinal nerve fiber layer thickness (99.36 ± 9.27 μm, 97.90 ± 9.46 μm, p = 0.091) differed between the eyes; neither did any OCTA-assessed microvascular parameter.
우세안이란 보는 것의 주요 기능을 수행하고 덜 우세한 눈의 도움을 받는 눈으로 정의될 수 있다. 다르게 말하면 두 눈은 동일한 힘으로 시각 인식에 영향을 미치지 않는다. 한쪽 눈이 다른 쪽 눈을 이끄는 눈을 우세안이라고 한다[1]. 같은 사지로부터 뇌로 받아들이는 신호와 뇌로부터 사지로 전달하는 신호는 뇌의 한쪽 반구와 관련되어 있다. 이와 대조적으로, 한쪽 눈에서 받아들인 신호는 양쪽 뇌에 모두 전달되고, 한쪽 눈의 외안근에 전달되는 신호는 뇌의 서로 다른 두 반구에서 나오는데, 이는 눈 움직임의 방향에 따라 결정된다[2]. 이런 연구 결과를 바탕으로, 우세안은 대뇌 편측성과는 관련이 없다고 보고되었다[3].
빛간섭단층촬영(optical coherence tomography, OCT)의 발달로 인하여 망막 및 시신경의 정량적 분석이 가능하게 되었고, 중심황반두께(central macular thickness, CMT), 망막신경절세포층-내망상층(ganglion cell-inner plexiform layer, GC-IPL), 시신경유두주위 망막신경섬유층(peripapillary retinal nerve fiver layer, pRNFL)의 측정값은 임상적으로 매우 유용하게 사용되고 있다. 우세안 여부가 망막 및 시신경에 해부학적으로 어떠한 영향을 미치는지에 대하여 과거 여러 연구가 진행되었고, 많은 연구들에서 우세안은 빛간섭단층촬영 측정값에 영향을 미치지 않는다고 보고하였다[4-7].
최근 도입된 빛간섭단층혈관조영술(optical coherence tomography angiography, OCTA)은 적혈구의 움직임을 분석하여 조영제 없이 망막 및 시신경 주변의 혈관을 분석할 수 있는 장비이며, 안과의 여러 분야에서 임상 및 연구에 활발하게 사용되고 있다. 빛간섭단층혈관조영술은 관류 밀도(perfusion density, PD) 및 플럭스 지수(flux index, FI)를 정량적으로 측정할 수 있는 장점이 있으며, 측정 영역의 3차원적인 분석도 가능하게 해준다. 과거 우세안 여부와 혈관 및 PD 등의 빛간섭단층혈관조영술 측정값이 어떠한 연관성이 있는지를 보고한 연구들은 있었지만, 아직 시신경 주변 혈관과 우세안과의 연관성을 분석한 연구는 보고된 바 없다. 이에 저자들은 전신적, 안과적으로 이상이 없는 정상인을 대상으로 본 연구를 진행하였으며, 우세안이 시신경 주변 혈관 빛간섭단층혈관조영술 측정값에 어떠한 영향을 미치는지를 알아보고자 하였다.
본 연구는 상업적 이해관계가 없으며, 임상연구심의위원회(Institutional Review Board, IRB)의 승인을 받아 진행하였고 헬싱키선언(Declaration of Helsinki)을 준수하였다(IRB 승인 번호: 2021-04-044). 2020년 3월부터 2021년 1월까지 안과 검진 및 검사를 목적으로 충남대학교병원 안과 망막클리닉에 처음 내원한 전신 질환 및 안과 질환 없는 정상인 42명 84안을 대상으로 후향적 연구를 시행하였다. 정상인은 굴절수술을 제외한 안과 수술력이 없고, 전안부 및 망막검사상 이상이 없으며 최대교정시력이 0.8 이상 교정되는 사람으로 정의하였다. 본 연구를 진행한 대상자들은 다른 어떠한 연구에도 포함되지 않았다.
본 연구에 포함된 모든 대상자들은 세극등현미경검사, 굴절검사, 안압검사, 안저검사, 안저촬영을 시행하였으며, 안압이 21 mmHg 이상인 경우, 전안부, 망막 및 시신경에 이상 소견이 발견된 경우는 모두 연구에서 제외하였다. 모든 대상군들은 Hole-in-the-card test를 시행하여 가운데 작은 구멍이 뚫린 카드를 환자가 양손으로 잡게 하고, 양안을 뜨고 정면 주시 상태에서 카드의 구멍을 통하여 먼 곳의 목표물을 주시하게 하였다. 그 상태에서 한쪽 눈을 교대로 감게 하여 어느 쪽이 우세안인지를 확인하였다. 5분 간격을 두고 2회 검사를 시행하여 결과가 일치하는 경우 최종적으로 우세안을 결정하였다. IOL Master® (IOL Master®, Carl Zeiss, Jena, Germany)를 이용하여 안축장 길이를 측정하였고, 모든 대상자들에게서 빛간섭단층촬영검사 및 빛간섭단층혈관조영술을 진행하였으며, 그 방법은 아래와 같다.
빛간섭단층촬영검사는 스펙트럼영역 빛간섭단층촬영기(Cirrus HD 5000, Carl Zeiss Meditec, Inc., Dublin, CA, USA)를 이용하여 Macular cube 512 × 128 scan을 시행하여 우세안과 비우세안 간의 중심황반두께, 황반부의 망막신경절세포층-내망상층 두께를 비교 분석하였다. 망막신경절세포층-내망상층 분석은 중심와를 중심으로 세로 방향 내부지름 1.0 mm, 외부지름 4.0 mm, 가로 방향 내부지름 1.2 mm, 외부지름 4.8 mm의 타원형 고리를 60°로 분할하여 상측, 상이측, 하이측, 하측, 하비측, 상비측의 여섯 영역으로 나누어 분석하였다. Optic disc cube 200 × 200 scan을 시행하여 시신경유두주위 망막신경섬유층의 평균 두께를 분석하였으며 하측, 상측, 비측, 이측 사분면으로 나누어 분석하였다.
빛간섭단층혈관조영술은 스펙트럼영역 빛간섭단층촬영기(Cirrus HD 5000, Carl Zeiss Meditec, Inc.)를 이용하여 4.5 × 4.5 mm2 scan을 시신경유두 주위에 시행하여 혈관조영 이미지를 얻었다. 빛간섭단층혈관조영술은 중심부 파장 길이 840 nm, 초당 70,000 A-scan의 속도, 대역폭 50 nm로 촬영되며, 각 volume에는 각 고정 위치에서 캡쳐된 두 개의 연속된 B-scan이 있는 350 × 350개의 A-scan이 포함된다. 모든 스캔은 내장된 소프트웨어(AngioPlex™, version 10.0)를 이용하여 자동으로 분석하였으며, PD와 FI를 측정하였다. PD는 단위 면적당 관류된 혈관의 총 면적을 의미한다. FI는 단위 면적당 관류된 혈관의 총 면적에 flow signal의 강도를 보정한 것으로, 단위 시간 동안 통과한 적혈구의 수에 대한 내용이 FI 안에 포함된다[8]. 모든 분석에는 신호 강도가 9 이상인 이미지를 사용하였으며 빛간섭단층촬영, 빛간섭단층혈관조영술 스캔 결과에서 영상의 질적 저하(segmentation error, motion artifact 등)가 관찰되는 경우 연구에서 모두 제외하였다.
통계분석은 statistical package R, version 3.5.0 (R Foundation for Statistical Computing, Vienna, Austria)과 SPSS statistical software for Windows, version 21.0 (IBM Corp., Armonk, NY, USA) 프로그램을 이용하였으며, paired t-test를 이용하여 양안의 다양한 측정값들을 비교 분석하였다. 또한 우세안의 방향에 따라 우안과 좌안 두 군으로 나누어 같은 지표들을 비교 분석하였다. Shapiro-Wilk test를 이용하여 정규성 검정을 시행하였으며, 정규 분포를 따르지 않는 경우 비모수 검정인 Wilcoxon signed rank test를 이용하여 분석하였다. p-value가 0.05 미만인 경우 유의한 차이가 있는 것으로 정의하였다. 빛간섭단층촬영 및 빛간섭단층혈관조영술의 측정 지표들이 우세안을 구분하는 정도를 분석하기 위해 area under the receiver operating characteristic curve (AUROC)를 이용하였다. AUROC >0.8인 경우 우세안을 구분하는 진단 가치가 있는 것으로 판단하였다.
연구 대상자 42명 중 남자가 22명(52.4%), 여자가 20명(47.6%)이었으며 평균 나이 27.3세(23-46세)였다. Hole-in-the-card test를 5분 간격으로 2회 시행하여 우세안의 방향이 다르게 나온 경우는 없었으며, 우안이 우세안인 대상군은 28명(66.7%), 좌안이 우세안인 대상군은 14명(33.3%)이었다. 우세안과 비우세안 사이의 최대교정시력, 구면대응치(spherical equivalent), 안압과 안축장에는 두 군 간의 차이가 없었다(Table 1).
우세안과 비우세안의 평균 황반두께는 각각 282.93 ± 13.51 μm, 280.76 ± 14.94 μm로 측정되었으며 통계적으로 유의한 차이는 없었다(p=0.076). 중심황반두께는 각각 260.00 ± 14.16 μm, 258.71 ± 15.18 μm였으며, 두 군 사이의 유의한 차이는 없었다(p=0.183). 신경절세포-내망상층의 평균 두께는 우세안과 비우세안 각각 82.02 ± 5.07 μm, 82.43 ± 5.60 μm로 측정되었으며 통계적으로 유의한 차이는 없었다(p=0.460). 신경절세포-내망상층을 여섯 영역으로 나누어 분석하였을 때에도 각 영역별로 두 군 간의 차이는 없었다(모두 p>0.05). 평균 망막신경섬유층 두께는 우세안과 비우세안이 각각 99.36 ± 9.27 μm, 97.90 ± 9.46 μm였으며 통계적으로 유의한 차이는 없었다(p=0.091). 또한 망막신경섬유층을 사분면으로 나누어 분석한 두께에도 유의한 차이가 없었다(모두 p>0.05, Table 2).
빛간섭단층혈관조영술을 이용하여 시신경유두주위 표층 모세혈관망을 분석한 결과 중심부에서 4.5 mm 영역의 평균 관류모세혈관 밀도(perfused capillary density)의 경우 우세안과 비우세안에서 각각 44.62 ± 5.25%, 45.60 ± 2.27%로 측정되었으며 유의한 차이는 없었다(p=0.221). 상측, 이측, 하측, 비측으로 나누어 분석하여도 유의한 차이는 확인되지 않았다(모두 p>0.05). 평균 FI 역시 중심부에서 4.5 mm 영역에서 우세안과 비우세안이 각각 0.455 ± 0.020, 0.449 ± 0.028로 측정되었으며 두 군 사이의 차이는 없었다(p=0.060). 상측, 이측, 하측, 비측으로 나누어 분석하였을 때에도 유의한 차이는 확인되지 않았다(모두 p>0.05, Table 3).
우세안의 방향에 따른 우세안과 비우세안 사이 측정치에 차이가 있는지 알아보기 위하여 우세안이 우안인 환자들과 우세안이 좌안인 환자들로 나누어 위와 동일한 방법으로 우세안과 비우세안의 빛간섭단층촬영과 시신경유두주위 빛간섭단층혈관조영 측정치를 비교하였다. 우세안의 방향에 관계없이 양안의 측정값은 유사한 경향을 보이고 있었으며(Fig. 1, 2), 모든 측정값에서 양안 사이에 유의한 차이는 확인되지 않았다(모두 p<0.05, Table 4). 양안의 빛간섭단층촬영과 빛간섭단층혈관조영 측정치를 이용하여 양안에서 우세안을 구분할 수 있는지를 AUROC 값을 이용하여 확인한 결과, 모든 변수에서 AUROC 0.6 이하로 낮은 구분력을 보이고 있었다(Fig. 3).
이번 연구를 통해, 우세안과 비우세안에서 중심황반, 신경절세포-내망상층, 그리고 망막신경섬유층 두께에 유의한 차이가 없음을 확인하였다. 빛간섭단층혈관조영술을 이용하여 시신경유두주위 표층모세혈관망을 분석한 결과 중심부에서 4.5 mm 영역의 평균 관류모세혈관 밀도, 평균 FI에도 유의한 차이가 없었으며, 우세안의 방향에 따라 대상군을 나누어 비교 분석한 결과에서도 양안은 비슷한 측정 결과를 보였다. 또한, 빛간섭단층촬영과 시신경유두주위 빛간섭단층혈관조영술 각각의 측정 지표들이 우세안과 비우세안을 구분할 수 있는지에 대하여 그 진단적 가치를 평가하기 위해서 AUROC 분석을 시행하였고, 측정 결과들 중 우세안을 구분할 수 있는 진단적 가치가 있는 지표는 찾지 못하였다.
일반적으로 양안을 포함한 인체의 장기들은 대칭성을 보이며, 질환이 발생할 때 그 대칭성은 어긋나게 된다. 양안은 각막, 망막 및 시신경에서도 역시 대칭적인 경향을 보이며, 질환이 발생하는 경우 양안의 대칭성은 사라지게 된다[9]. 이러한 대칭성에 우세안의 개념이 어떠한 영향을 미치는지에 대해서 이전부터 여러 연구가 진행되어 왔다. 우세안은 주시와 주의, 그리고 인지 시에 비우세안에 비해 우세안인 눈으로부터 시각 정보를 얻으려는 성향으로 정의된다[1,2,10]. 우세안은 몇몇 안과적 질환에서 의미 있는 영향을 미친다고 보고되었는데, 사시수술 결과에 영향을 준다는 연구 결과가 있었으며[11], 또한, 황반원공수술 결과에도 영향을 미친다는 보고가 있었다[12].
빛간섭단층촬영 및 빛간섭단층혈관조영 측정치가 우세안과 어떤 영향이 있는지에 대해서는 여러 연구가 있었다. Samarawickrama et al [13]에 따르면, 1,538명의 6살 아이들과 1,844명의 12살 아이들을 대상으로 빛간섭단층촬영을 통해 분석해보니, 우세안과 비우세안 사이에 황반두께, 망막신경섬유층 두께에 차이가 없다고 보고하였다. Cevher et al [14]의 보고에서도 황반부와 시신경유두 주위 망막신경섬유층의 두께는 우세안과 비우세안에서 유의한 차이가 없다고 확인하였다. Pekel et al [15] 및 Zhou et al [16]의 연구에서도 황반두께, 시신경-중심와 각도 및 중심와의 혈관 수가 우세안 결정에 중요한 요인이 아니라는 것을 보여주었고, 이는 황반은 건강한 젊은 성인의 우세안 결정에 영향을 미치지 않음을 보여준다. 이렇게 대부분의 연구들에서 우세안은 빛간섭단층촬영 측정값에 영향을 미치지 않는다고 보고하였지만, 황반부 신경절세포-내망상층의 평균, 하비측, 하측 분절의 두께가 우세안에서 유의하게 두꺼웠다고 보고한 연구도 있었다[17].
빛간섭단층혈관조영술을 이용한 양안의 대칭성 연구도 최근에 이루어지고 있는데, Liu et al [18]에 따르면, 망막중심 오목무혈관부위(foveal avascular zone, FAZ)와 중심황반두께 측정치의 좌우안 차이는 없었으나, 우안이 우세안인 경우 표층과 심층의 망막모세혈관망 및 맥락막모세혈관망의 밀도가 우안에서 더 높다고 보고하였고, 좌안이 우세안인 경우에는 표층과 심층의 망막모세혈관망 밀도는 좌안에서 높았으나, 맥락막모세혈관망의 밀도는 그렇지 않았다고 하였다. 우세안과 더 높은 혈관 밀도가 관련이 있을 것이라고 본 것이다. 이와는 반대로, 저자들이 최근에 보고한 연구에서는, 우세안과 비우세안 사이 빛간섭단층촬영 및 빛간섭단층혈관조영술의 측정값들에는 유의한 차이가 없었으며, 이는 우세안이 안구내 요인에 의해서 결정되는 것이 아닌 시피질의 발달과 연관된다는 것을 의미한다고 보고하였다[5].
이번 연구의 한계점으로는 몇 가지가 있는데, 첫 번째로 정상안 42명 84안으로 대상군의 수가 상대적으로 적다는 점이다. 목표 대상자 수를 G*Power version 3.1.9.2 sample size package (http://www.gpower.hhu.de/)를 이용하여 산출하면, α=0.05, power=95%, effect size=0.5로 하였을 때 적절한 대상군의 수는 45명으로 나오며, 본 연구의 대상군 수는 이보다 약간 적다. 두 번째로, 검사 순응도를 고려하고 또한 다양한 질환 가능성을 배제하려고 노력하였는데, 이로 인하여 대부분 젊은 대상군들이 연구에 포함되었다. 대상군들을 30세 미만(34명), 30세 이상(8명) 두 그룹으로 나누어 분석한 결과, 두 그룹에서 모두 우세안에 의한 영향을 발견하지 못하였으며(data not shown), 또한 우세안과 비우세안과의 측정값 차이는 나이와 유의한 상관관계를 보이지 않았다(average PD: r=0.094, p=0.554; average FI: r=-0.226, p=0.150). 본 연구 데이터를 고려하면 나이가 우세안에 미치는 영향은 크지 않을 것이라 추측되지만, 본 연구에 포함되지 않은 50대 이상에서는 우세안이 어떠한 영향을 미치는지에 대해서는 확인하지 못했다. 이를 보완하기 위하여 다양한 연령대가 포함된 다수의 대상군을 대상으로 한 연구가 필요할 것으로 생각한다. 마지막으로 표층 모세혈관망의 빛간섭단층혈관조영술 결과만을 비교하였기 때문에 심층 모세혈관망 결과를 확인하지 못하였다는 한계가 있다. 하지만, 아직까지 시신경유두주위 혈관 밀도와 우세안 사이에 연관성을 분석한 연구가 충분히 이루어지지 않았기에, 본 연구 결과는 우세안을 연구하는 독자들에게 도움이 될 것으로 생각한다.
이번 연구 결과, 지금까지의 대부분의 연구들에서와 마찬가지로 우세안은 빛간섭단층촬영 측정값에 영향을 미치지 않는다는 것을 확인하였고, 빛간섭단층혈관조영술 측정값에도 영향을 미치지 않음을 확인하였다. 위 결과는 우세안을 결정하는 요인이 안구 내 요인보다는 시피질을 포함한 중추신경계 요인에 의하여 결정될 가능성이 높음을 시사한다. 하지만 대부분의 시피질의 발달이 망막을 통한 시자극을 통하여 이뤄지기 때문에 우세안이 결정되는 데 있어서 안구의 영향을 완전히 배제할 수 없다. 추후 더 정밀하고 정교한 진단 방법들이 개발되면 추가적인 연구가 필요할 것으로 보이며, 조금 더 많은 수를 대상으로 한 연구가 필요할 것으로 생각된다.
Figure 1.
Comparison of right and left eye in central macular thickness (A), average ganglion cell-inner plexiform layer (GC-IPL) thickness (B), average retinal nerve fiber layer (RNFL) thickness (C), perfusion density (D), and flux index (E) when right eye is dominant eye.
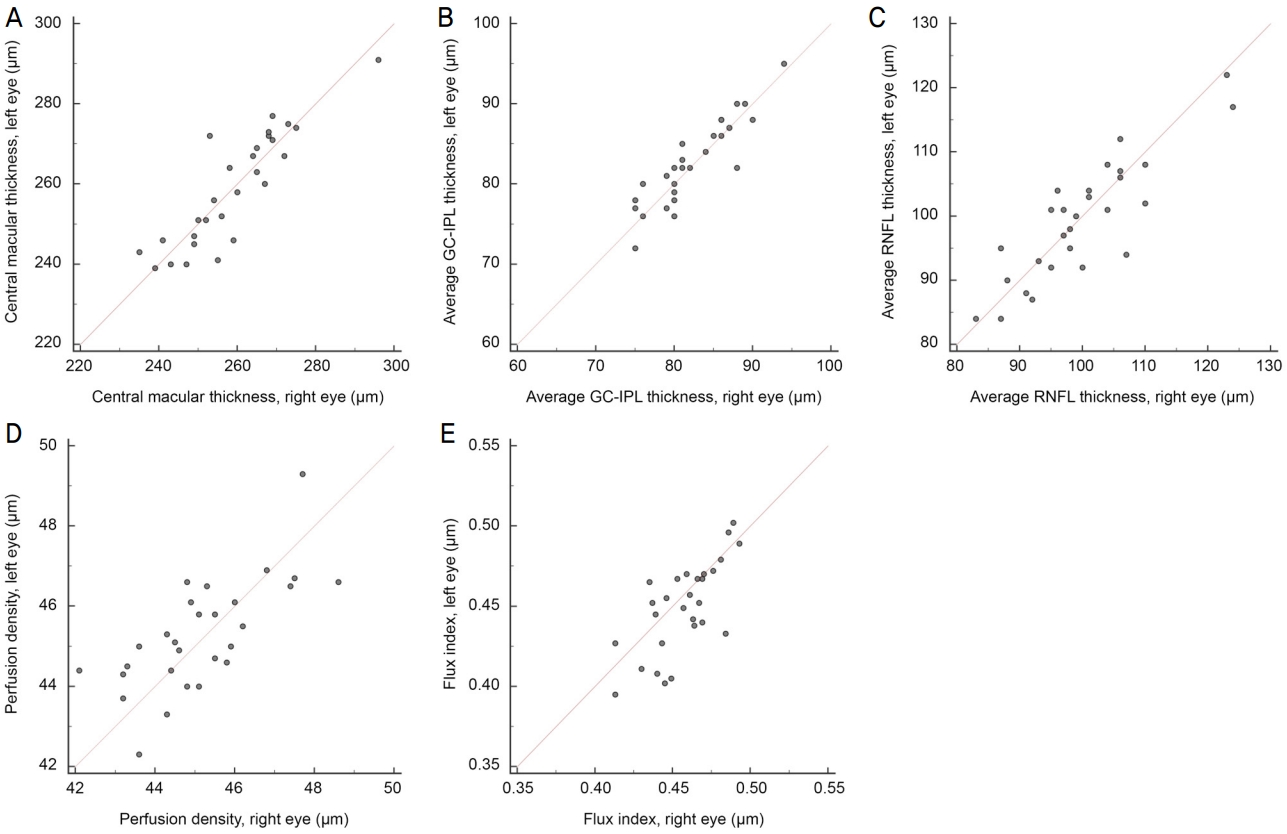
Figure 2.
Comparison of right and left eye central macular thickness (A), average ganglion cell-inner plexiform layer (GC-IPL) thickness (B), average retinal nerve fiber layer (RNFL) thickness (C), perfusion density (D), and flux index (E) when left eye is dominant eye.

Figure 3.
Area under the receiver operating characteristic curve of each parameter of optical coherence tomography (OCT) and peripapillary OCT angiography to differentiate the dominant eye. AUC = area under the curve; GC-IPL = ganglion cell-inner plexiform layer; RNFL = retinal nerve fiber layer.
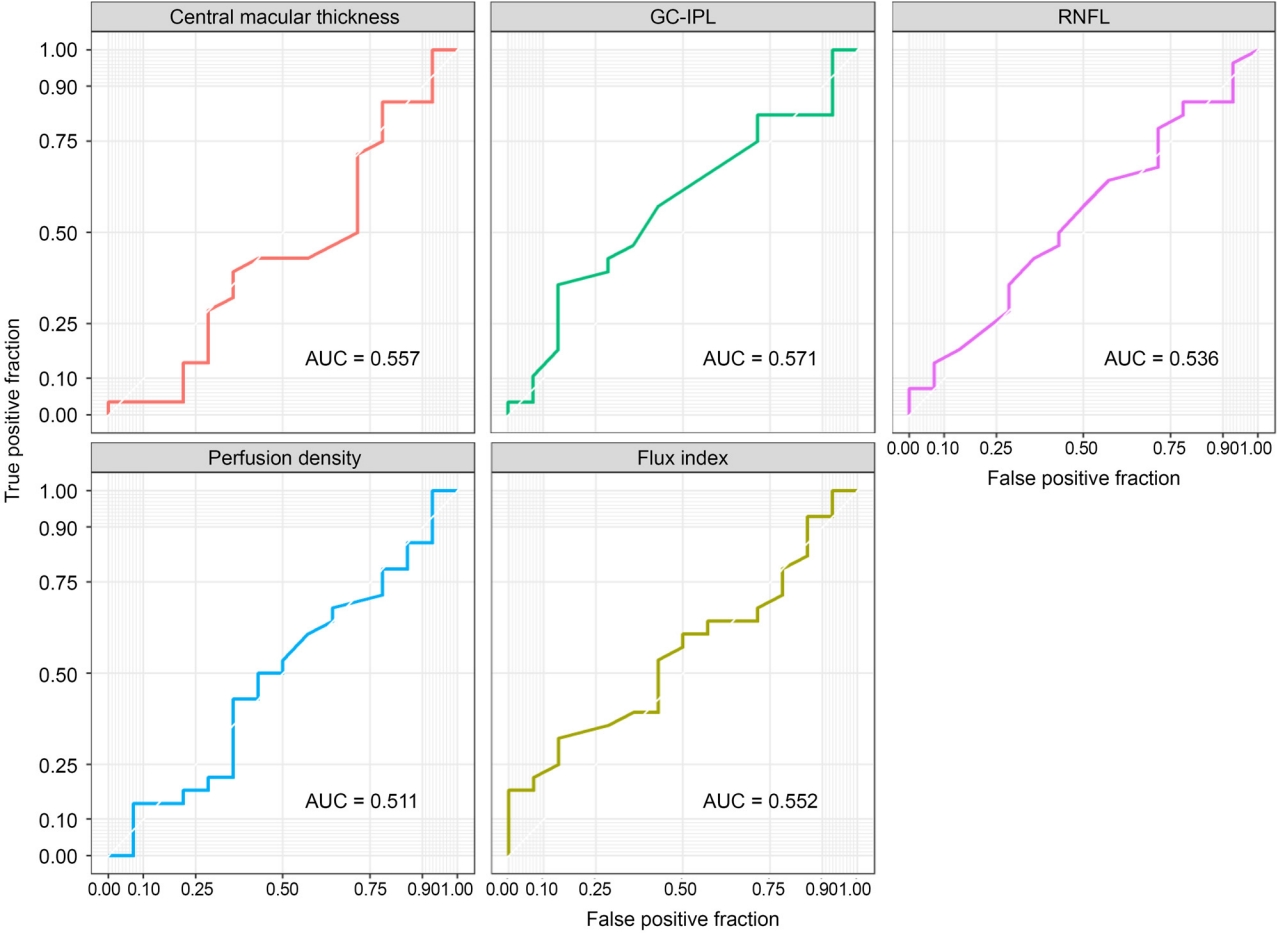
Table 1.
Demographics of patients
| Characteristic | Dominant eye | Non-dominant eye | p-value* |
|---|---|---|---|
| Visual acuity (logMAR) | 0.00 ± 0.01 | 0.00 ± 0.00 | 0.323 |
| Refractive error (diopters) | -2.86 ± 2.97 | -2.72 ± 3.01 | 0.473 |
| Intraocular pressure (mmHg) | 15.21 ± 3.76 | 14.95 ± 3.46 | 0.343 |
| Axial length (mm) | 25.61 ± 1.17 | 25.59 ± 1.19 | 0.824 |
Table 2.
Comparison of optical coherence tomography parameters between dominant and non-dominant eyes
| Variable (μm) | Dominant eye | Non-dominant eye | p-value* |
|---|---|---|---|
| Average macular thickness | 282.93 ± 13.51 | 280.76 ± 14.94 | 0.076 |
| Central macular thickness | 260.00 ± 14.16 | 258.71 ± 15.18 | 0.183 |
| pRNFL | |||
| Average | 99.36 ± 9.27 | 97.90 ± 9.46 | 0.091 |
| Inferior | 123.38 ± 18.43 | 123.14 ± 16.83 | 0.891 |
| Superior | 120.21 ± 16.17 | 119.38 ± 14.53 | 0.645 |
| Nasal | 65.64 ± 10.82 | 64.07 ± 11.06 | 0.356 |
| Temporal | 87.83 ± 18.92 | 85.31 ± 17.01 | 0.111 |
| mGC-IPL | |||
| Average | 82.02 ± 5.07 | 82.43 ± 5.60 | 0.460 |
| Superior | 82.50 ± 6.49 | 82.95 ± 7.66 | 0.677 |
| Supratemporal | 82.43 ± 5.28 | 82.86 ± 5.58 | 0.445 |
| Infratemporal | 82.38 ± 6.40 | 82.43 ± 5.89 | 0.920 |
| Inferior | 79.48 ± 5.83 | 79.26 ± 6.82 | 0.735 |
| Infranasal | 81.86 ± 5.47 | 83.07 ± 7.08 | 0.238 |
| Supranasal | 83.21 ± 7.08 | 83.21 ± 7.72 | 0.332 |
Table 3.
Comparison of optical coherence tomography angiography parameters of peripapillary superficial capillary plexus between dominant and non-dominant eyes
| Dominant eye | Non-dominant eye | p-value* | |
|---|---|---|---|
| Perfusion density (%) | |||
| Average | 44.62 ± 5.25 | 45.60 ± 2.27 | 0.221 |
| Superior | 44.02 ± 2.73 | 44.60 ± 2.81 | 0.264 |
| Temporal | 48.63 ± 2.12 | 48.94 ± 1.92 | 0.333 |
| Inferior | 44.74 ± 2.04 | 44.90 ± 2.12 | 0.634 |
| Nasal | 43.87 ± 4.13 | 44.05 ± 5.65 | 0.848 |
| Flux index | |||
| Average | 0.455 ± 0.020 | 0.449 ± 0.028 | 0.060 |
| Superior | 0.447 ± 0.021 | 0.440 ± 0.025 | 0.077 |
| Temporal | 0.462 ± 0.025 | 0.464 ± 0.034 | 0.673 |
| Inferior | 0.451 ± 0.018 | 0.450 ± 0.025 | 0.562 |
| Nasal | 0.461 ± 0.026 | 0.455 ± 0.026 | 0.077 |
Table 4.
Interocular comparison of optical coherence tomography and optical coherence tomography angiography parameters according to ocular dominance
|
Right ocular dominance (n = 28) |
Left ocular dominance (n = 14) |
|||||
|---|---|---|---|---|---|---|
| Right eye (dominant eye) | Left eye | p-value* | Right eye | Left eye (dominant eye) | p-value* | |
| CMT (μm) | 258.96 ± 13.10 | 258.93 ± 14.45 | 0.981 | 262.07 ± 16.41 | 259.29 ± 17.77 | 0.085 |
| Average mGC-IPL (μm) | 82.50 ± 5.07 | 83.36 ± 5.73 | 0.359 | 81.07 ± 5.12 | 80.57 ± 5.02 | 0.142 |
| Average pRNFL (μm) | 99.93 ± 9.73 | 99.46 ± 9.37 | 0.709 | 98.21 ± 8.51 | 96.79 ± 9.18 | 0.107 |
| Perfusion density (%) | ||||||
| Average | 45.14 ± 1.53 | 45.21 ± 1.37 | 0.648 | 43.59 ± 8.97 | 46.39 ± 3.37 | 0.132 |
| Superior | 43.33 ± 1.77 | 43.97 ± 1.37 | 0.108 | 45.40 ± 3.74 | 45.85 ± 3.92 | 0.754 |
| Temporal | 48.48 ± 1.81 | 48.81 ± 1.88 | 0.428 | 48.95 ± 2.69 | 49.19 ± 2.05 | 0.234 |
| Inferior | 44.69 ± 2.31 | 44.91 ± 1.96 | 0.494 | 44.83 ± 1.45 | 44.88 ± 2.48 | 0.754 |
| Nasal | 43.94 ± 3.10 | 43.38 ± 4.22 | 0.056 | 43.74 ± 5.81 | 45.39 ± 7.79 | 0.177 |
| Flux index | ||||||
| Average | 0.457 ± 0.021 | 0.449 ± 0.029 | 0.077 | 0.453 ± 0.019 | 0.448 ± 0.028 | 0.638 |
| Superior | 0.448 ± 0.021 | 0.442 ± 0.025 | 0.198 | 0.443 ± 0.019 | 0.436 ± 0.026 | 0.442 |
| Temporal | 0.461 ± 0.025 | 0.463 ± 0.035 | 0.758 | 0.464 ± 0.025 | 0.466 ± 0.033 | 0.706 |
| Inferior | 0.452 ± 0.019 | 0.447 ± 0.027 | 0.181 | 0.455 ± 0.021 | 0.449 ± 0.014 | 0.155 |
| Nasal | 0.462 ± 0.029 | 0.455 ± 0.032 | 0.103 | 0.461 ± 0.013 | 0.458 ± 0.020 | 0.423 |
REFERENCES
2) Mapp AP, Ono H, Barbeito R. What does the dominant eye dominate? A brief and somewhat contentious review. Percept Psychophys 2003;65:310-7.


4) Davey PG, Alvarez SD, Lee JY. Macular pigment optical density: repeatability, intereye correlation, and effect of ocular dominance. Clin Ophthalmol 2016;10:1671-8.



5) Kim KM, Lim HB, Shin YI, et al. Symmetry of optical coherence tomography angiography parameters between dominant and non-dominant eyes in healthy Koreans. J Korean Ophthalmol Soc 2020;61:1057-64.

6) Lee MS, Cho KJ, Cho WH, et al. Retinal nerve fiber layer thickness and optic disc parameters in dominant compared with non-dominant eyes. J Korean Ophthalmol Soc 2013;54:784-8.

7) Song YJ, Kim DH. Comparison of OCT parameters between the dominant and nondominant eye. J Korean Ophthalmol Soc 2014;55:1687-92.

8) Robbins CB, Grewal DS, Thompson AC, et al. Repeatability of peripapillary optical coherence tomography angiography parameters in older adults. J Vitreoretin Dis 2021;5:239-46.


9) Lee SY, Jeoung JW, Park KH, Kim DM. Macular ganglion cell imaging study: interocular symmetry of ganglion cell-inner plexiform layer thickness in normal healthy eyes. Am J Ophthalmol 2015 159:315-23. e2.


11) Jeoung JW, Lee MJ, Hwang JM. Bilateral lateral rectus recession versus unilateral recess-resect procedure for exotropia with a dominant eye. Am J Ophthalmol 2006;141:683-8.


12) Waheed K, Laidlaw DA. Disease laterality, eye dominance, and visual handicap in patients with unilateral full thickness macular holes. Br J Ophthalmol 2003;87:626-8.



13) Samarawickrama C, Wang JJ, Huynh SC, et al. Macular thickness, retinal thickness, and optic disk parameters in dominant compared with nondominant eyes. J AAPOS 2009;13:142-7.


14) Cevher S, Kocluk Y, Cetinkaya S, Sukgen EA. Macular thickness and retinal nerve fiber thickness analysis in ocular dominance. Rev Bras Oftalmol 2018;77:316-9.
15) Pekel G, Acer S, Ozbakis F, et al. Macular asymmetry analysis in sighting ocular dominance. Kaohsiung J Med Sci 2014;30:531-6.


16) Zhou M, Lu B, Zhao J, et al. Interocular symmetry of macular ganglion cell complex thickness in young chinese subjects. PLoS One 2016;11:e0159583.







 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




