 |
 |
| J Korean Ophthalmol Soc > Volume 62(9); 2021 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ņ”ØļĪĆņÜöņĢĮ
2Ļ░£ņøö ļé©ņĢäĻ░Ć ņČ£ņāØ ņŗ£ļČĆĒä░ ņ׳ņŚłļŹś ņÜ░ņĖĪ ņĢłņÖĆ ņóģĻ┤┤ļź╝ ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņśĆļŗż. ņĢłņÖĆ ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņŚÉņä£ ņÜ░ņĖĪ ņĢłņÖĆņØś ĒĢśļé┤ņĖĪņŚÉ ĻĘĀņØ╝ĒĢśĻ▓ī ņĪ░ņśüņ”ØĻ░ĢļÉśļŖö Ļ▓ĮĻ│äĻ░Ć ļ¬ģĒÖĢĒĢ£ ņóģņ¢æņØ┤ Ļ┤Ćņ░░ļÉśņŚłĻ│Ā, Ļ│©ļ»Ėļ×Ć ņåīĻ▓¼ņØĆ ņŚåņŚłļŗż. ņØ┤ņŚÉ Ļ▓░ļ¦ē Ļ▓Įņ£Ā ņĢłņÖĆņĀłĻ░£ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, ĒĢśņé¼ĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ ņĢłņÖĆņóģņ¢æņØä ĒÖĢņØĖĒĢ£ Ēøä ņĀłņĀ£ĒĢśņśĆļŗż. ņĪ░ņ¦üļ│æļ”¼Ļ▓Ćņé¼ Ļ▓░Ļ│╝ ņĮ£ļØ╝Ļ▓É ĻĖ░ņ¦ł ļé┤ņŚÉ ņāüĒö╝ņäĖĒżļĪ£ ĻĄ¼ņä▒ļÉ£ Ļ▒░ņ¦ōņāś ĻĄ¼ņĪ░(pseudo-glandular structure)ņÖĆ ņØ┤ļź╝ ļæśļ¤¼ņŗĖļŖö ļæÉĻ║╝ņÜ┤ ĻĖ░ņĀĆļ¦ē, ĻĖ░ņ¦ł ļé┤ņØś ņØ╝ļČĆ ņé¼ņóģĒśĢ ņäØĒÜīĒÖö(psammo-matous calcific foci)ņÖĆ Ļ┤Ćļé┤Ļ░ĢņØś ĒśĖņé░ņä▒ ļ¼╝ņ¦łņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż. ļ®┤ņŚŁņĪ░ņ¦üĒÖöĒĢÖĻ▓Ćņé¼ņāü S-100, ņé¼ņØ┤ĒåĀ ņ╝ĆļØ╝Ēŗ┤(cytokeratin) ņ¢æņä▒ ņåīĻ▓¼ņØä ļ│┤ņŚ¼ phakomatous choristomaļĪ£ ņ¦äļŗ©ĒĢśņśĆļŗż.
ABSTRACT
Purpose
We report a case of phakomatous choristoma presenting as an orbital tumor with involvement of the inferior oblique muscle.
Case summary
A 2-month-old male infant presented to our clinic with a right orbital mass that had been present since birth. Magnetic resonance imaging demonstrated a homogenous enhanced well-defined mass located in the inferomedial portion of the right orbit without bone erosion. By transconjunctival orbitotomy, the orbital tumor invading the inferior oblique muscle was identified and resected. Histopathology showed a thick basement membrane surrounding pseudoglandular structures embedded in a collagenous stroma, psammomatous calcific foci in the stroma, and eosinophilic material in the lumen. Immunohistochemical analysis showed positive staining for S-100 and cytokeratin. On histopathological evaluation, the tumor was diagnosed as phakomatous choristoma.
Conclusions
To our knowledge, this is the first report in South Korea of phakomatous choristoma of the orbit with involvement of the inferior oblique muscle. Although rare, phakomatous choristoma should be included in the differential diagnosis of tumors occurring on the inferomedial side of the orbit.
Phakomatous choristomaļŖö 1971ļģä Zimmerman [1]ņØ┤ ņ▓śņØī ĻĖ░ņłĀĒĢ£ ņłśņĀĢņ▓┤ ĻĖ░ņøÉņØś ĒؼĻĘĆĒĢ£ ņóģņ¢æņØ┤ļŗż. ņØ┤ ņóģņ¢æņØĆ ļ¦żņÜ░ ļō£ļ¼╝Ļ▓ī ļ░£ņāØĒĢśĻ│Ā, ņØ╝ļ░śņĀüņ£╝ļĪ£ ņ£ĀĒö╝ļéŁņóģ ļśÉļŖö ĻĖ░ĒāĆ ļČĆņåŹĻĖ░ ņóģņ¢æņ£╝ļĪ£ ņśżņØĖļÉ£ļŗż. Ēśäņ×¼Ļ╣īņ¦Ć 27ņśłĻ░Ć ļ│┤Ļ│ĀļÉśņŚłņ£╝ļ®░[2] ņŻ╝ļĪ£ ņśüņĢäņŚÉņä£ ļłłĻ║╝ĒÆĆ ĒĢśļé┤ņĖĪņØś ņ£ĀļÅÖņä▒ ņóģĻ┤┤ļĪ£ ļéśĒāĆļé£ļŗż. ņóģņ¢æņØ┤ ņĢłņÖĆļź╝ ņ╣©ļ▓öĒĢśĻ▒░ļéś ņÖäņĀäĒ׳ ņĢłņÖĆ ļé┤ņŚÉ ņ£äņ╣śĒĢ£ ļ¬ćļ¬ć ņ”ØļĪĆļÅä ļ│┤Ļ│ĀļÉśņŚłĻ│Ā, ĒĢ£ ņśłņŚÉņä£ļŖö Ļ░üļ¦ē ĻĖ░ņ¦łņŚÉ ļ░£ņāØĒĢśņśĆļŗż[3]. ļ╣äĒŖ╣ņØ┤ņĀüņØĖ ņ×äņāüņ¢æņāüĻ│╝ ņśüņāüĻ▓Ćņé¼ Ļ▓░Ļ│╝ļź╝ ļ│┤ņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ ņłśņłĀ Ēøä ņĪ░ņ¦üļ│æļ”¼ĒĢÖņ£╝ļĪ£ ņ¦äļŗ©ĒĢ£ļŗż.
ĒĢ┤ņÖĖņŚÉņä£ļŖö ņÖĖņĢłĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ phakomatous choristomaņŚÉ ļīĆĒĢ┤ Romano et al [4], Harris et al [5]ņØ┤ ļ│┤Ļ│ĀĒĢ£ ņĀü ņ׳ņ£╝ļéś, ĻĄŁļé┤ņŚÉņä£ļŖö Shin et al [6]ņØ┤ ļ│┤Ļ│ĀĒĢ£ ļłłĻ║╝ĒÆĆņŚÉ ļ░£ņāØĒĢ£ ņ”ØļĪĆ ņØ┤ņÖĖņŚÉ ņÖĖņĢłĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ Ļ▓ĮņÜ░ņŚÉ ļīĆĒĢ┤ņä£ļŖö ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåņŚłļŗż. ņØ┤ņŚÉ ļ│Ė ņĀĆņ×ÉļōżņØĆ ĒĢśņé¼ĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ ņĢłņÖĆņØś phakomatous choristoma 1ņśłņŚÉ ļīĆĒĢśņŚ¼ ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
2Ļ░£ņøö ļé©ņĢäĻ░Ć ņČ£ņāØ ņŗ£ļČĆĒä░ ņ׳ņŚłļŹś ņÜ░ņĖĪ ņĢłņÖĆ ņóģĻ┤┤ļź╝ ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņśĆļŗż(Fig. 1A). ņŻ╝ļ│Ć ļČĆņóģņØ┤ļéś ļ░£ņĀü, ļłłļ¼╝ ĒØśļ”╝ņØĆ ņŚåņŚłĻ│Ā, ļŗżļźĖ ņĢłĻ│╝ņĀü ņØ┤ņāü ņåīĻ▓¼ņØĆ ņŚåņŚłļŗż. ņĢłņÖĆ ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņŚÉņä£ļŖö ņÜ░ņĖĪ ņĢłņÖĆ ĒĢśļé┤ņĖĪņŚÉ Ļ▓ĮļÅäņŚÉņä£ ņżæļō▒ļÅäļĪ£ ĻĘĀņØ╝ĒĢśĻ▓ī ņĪ░ņśüņ”ØĻ░ĢļÉśļŖö 1.0 ├Ś 0.8 ├Ś 0.7 cm Ēü¼ĻĖ░ņØś Ļ▓ĮĻ│äĻ░Ć ļ¬ģĒÖĢĒĢ£ ņóģņ¢æņØ┤ Ļ┤Ćņ░░ļÉśņŚłĻ│Ā, Ļ│©ļ»Ėļ×ĆņØ┤ļéś ņ╣©ļ▓ö ņåīĻ▓¼ņØĆ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż(Fig. 1B, C).
ņĀäņŗĀļ¦łņĘ©ĒĢśņŚÉ Ļ▓░ļ¦ēĻ▓Įņ£ĀņĀæĻĘ╝ņłĀņØä ĒåĄĒĢ┤ ņĢłņÖĆņĀłĻ░£ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, ņóģņ¢æņØ┤ ĒĢśņé¼ĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ ļ¬©ņŖĄņØä ĒÖĢņØĖĒĢśņśĆļŗż(Fig. 2A, B). ņĀłņĀ£ļÉ£ ņĪ░ņ¦üņØĆ 1.0 ├Ś 0.6 ├Ś 0.5 cm Ēü¼ĻĖ░ņśĆņ£╝ļ®░, ņśģņØĆ ņĢöņĀüņāēņ£╝ļĪ£ ļČĆļō£ļ¤ĮĻ▓ī ņ┤ēņ¦ĆļÉśņŚłļŗż(Fig. 2C). ņĪ░ņ¦üĻ▓Ćņé¼ Ļ▓░Ļ│╝ ņĮ£ļØ╝Ļ▓É ĻĖ░ņ¦ł ļé┤ņŚÉ ņāüĒö╝ņäĖĒżļĪ£ ĻĄ¼ņä▒ļÉ£ Ļ▒░ņ¦ōņāś ĻĄ¼ņĪ░(pseudglandular structure)Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłĻ│Ā, ļæÉĻ║╝ņÜ┤ ĻĖ░ņĀĆļ¦ēņØ┤ Ļ▒░ņ¦ōņāś ĻĄ¼ņĪ░ļź╝ ļæśļ¤¼ņŗĖĻ│Ā ņ׳ņŚłļŗż(Fig. 3A, B). ĻĖ░ņ¦ł ļé┤ņŚÉ ņØ╝ļČĆ ņé¼ņóģĒśĢ ņäØĒÜīĒÖö(psammomatous calcific foci)ņÖĆ Ļ┤Ćļé┤Ļ░ĢņØś ĒśĖņé░ņä▒ ļ¼╝ņ¦łļÅä Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 3B). ļ®┤ņŚŁņĪ░ņ¦üĒÖöĒĢÖ ņŚ╝ņāē Ļ▓░Ļ│╝ ņóģņ¢æņØś ņāüĒö╝ņäĖĒżļŖö S-100ņŚÉ Ļ░ĢĒĢ£ ļ®┤ņŚŁļ░śņØæņä▒, ņé¼ņØ┤ĒåĀņ╝ĆļØ╝Ēŗ┤ņŚÉ ĻĄŁņåīņĀüņØĖ ņ¢æņä▒ ņåīĻ▓¼ņØ┤ņŚłļŗż(Fig. 3C, D). ņØ┤ņŚÉ ĻĘ╝Ļ▒░ĒĢśņŚ¼ ĒĢśņé¼ĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ phkomatous choristomaļĪ£ ņ¦äļŗ©ĒĢśņśĆļŗż. ņłśņłĀ Ēøä 14Ļ░£ņøö ļÅÖņĢł Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņżæņØ┤ļ®░ ņ×¼ļ░£ ļśÉļŖö ļŗżļźĖ ņĢłĻ│╝ņĀü ņØ┤ņāü ņåīĻ▓¼ņØĆ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż.
Phakomatous choristomaņØś ĻĖ░ņøÉņØĆ ņØ┤ņåīņä▒ ņłśņĀĢņ▓┤ ņĪ░ņ¦üņ£╝ļĪ£[1,7], ļ│æņØĖņØĆ ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖņ£╝ļéś Zimmerman [1]ņØ┤ ņØ┤ņŚÉ ļīĆĒĢ£ Ļ░ĆņäżņØä ņĀ£ņŗ£ĒĢśņśĆļŗż. ņĢłĻĄ¼ ļ░£ņāØ ņŗ£ĻĖ░ņŚÉ ņłśņĀĢņ▓┤ļŖö Ēæ£ļ®┤ ņÖĖļ░░ņŚĮņØś ĒĢ©ņ×ģņŚÉ ņØśĒĢ┤ ĒśĢņä▒ļÉ£ ņłśņĀĢņ▓┤ņśżļ¬®(lens pit)ņØ┤ ņłśņĀĢņ▓┤ņåīĒż(lens vesicle)Ļ░Ć ļÉśņ¢┤ ĒśĢņä▒ļÉ£ļŗż. Zimmerman [1]ņØĆ ņØ╝ļČĆ ņłśņĀĢņ▓┤ ņĪ░ņ¦üņØ┤ ņłśņĀĢņ▓┤ņåīĒżļź╝ ĒśĢņä▒ĒĢśļŖö ļÅÖņĢł ļ╣äņĀĢņāüņĀüņ£╝ļĪ£ ĒīīņóģļÉśĻ│Ā, ņØ┤ļ¤¼ĒĢ£ ļ░░ņĢäņä▒ ņłśņĀĢņ▓┤ ņĪ░ņ¦üņØ┤ ņä▒ņןĒĢśņŚ¼ phakomatous choristoma ņóģņ¢æņØä ĒśĢņä▒ĒĢ£ļŗżĻ│Ā ņäżļ¬ģĒĢśņśĆļŗż. ļö░ļØ╝ņä£ ņóģņ¢æņØĆ ņłśņĀĢņ▓┤ņåīĒżņØś Ļ▓ĮļĪ£ļź╝ ļö░ļØ╝ ņ¢┤ļŖÉ Ļ││ņŚÉņä£ļéś ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż[1].
Zimmerman [1]ņØ┤ ņ▓śņØī phakomatous choristomaņŚÉ ļīĆĒĢ┤ ĻĖ░ņłĀĒĢ£ Ēøä Ēśäņ×¼Ļ╣īņ¦Ć 27ņ”ØļĪĆĻ░Ć ļ│┤Ļ│ĀļÉśņŚłļŗż[2]. ņØ┤ ņóģņ¢æņØĆ ņĀäĒśĢņĀüņ£╝ļĪ£ ņČ£ņāØ ņŗ£ ļ░£Ļ▓¼ļÉśļ®░ ņä£ņä£Ē׳ Ēü¼ĻĖ░Ļ░Ć ņ”ØĻ░ĆĒĢ£ļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ ļłłĻ║╝ĒÆĆņØś ĒĢśļé┤ņĖĪņŚÉ ļ░£ņāØĒĢśļŖöļŹ░, ņĢłņÖĆ ļé┤ļĪ£ ņ╣©ļ▓öĒĢśĻ▒░ļéś ņÖäņĀäĒ׳ ņĢłņÖĆ ļé┤ņŚÉņä£ ļ░£ņāØĒĢ£ ļ¬ćļ¬ć ņé¼ļĪĆļÅä ļ│┤Ļ│ĀļÉśņŚłļŗż. ņØ┤ņĀäņØś ļ¼ĖĒŚīņŚÉņä£ ņÖĖņĢłĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ Ļ▓ĮņÜ░ļŖö Romano et al [4], Harris et al [5], 2ņśłĻ░Ć ļ│┤Ļ│ĀļÉśņŚłņ£╝ļ®░, ĻĄŁļé┤ņŚÉņä£ļŖö ļ│Ė ņ”ØļĪĆĻ░Ć ņĢłņÖĆņŚÉ ļ░£ņāØĒĢ£ ņĄ£ņ┤ł ļ│┤Ļ│ĀņØ┤ļŗż.
ĒŖ╣ņ¦ĢņĀüņØĖ ņĪ░ņ¦üļ│æļ”¼ĒĢÖņĀü ņåīĻ▓¼ņØĆ ņĮ£ļØ╝Ļ▓É ĻĖ░ņ¦ł ļé┤ņØś Ļ▒░ņ¦ōņāś ĻĄ¼ņĪ░ļź╝ ļæśļ¤¼ņŗĖļŖö ļæÉĻ║╝ņÜ┤ ĻĖ░ņĀĆļ¦ē, ņĀĢņāü ļśÉļŖö ļ░▒ļé┤ņן ņłśņĀĢņ▓┤ņØś Ēö╝ņ¦łĻ│╝ ņ£Āņé¼ĒĢ£ ņāüĒö╝ņä¼(epithelial island) ņżæņĢÖņØś ĒśĖņé░ņä▒ļ¼╝ņ¦ł, ĒøäļéŁĒĢś ļ░▒ļé┤ņןņŚÉņä£ ļ│┤ņØ┤ļŖö ŌĆ£WedlŌĆØ ņäĖĒżņÖĆ ņ£Āņé¼ĒĢ£ Ēć┤Ē¢ēņä▒ ņāüĒö╝ņäĖĒżņØ┤ļŗż[1,8-10]. ņāüĒö╝ ņāēņåī Ļ│╝ļ”ĮĻ│╝ ņé¼ņóģĒśĢ ņäØĒÜīĒÖö ņåīĻ▓¼ļÅä ņØ┤ņĀä ļ¼ĖĒŚīņŚÉ ļ│┤Ļ│ĀļÉśņŚłļŗż[9,10]. ļ░▒ļé┤ņן ņłśņĀĢņ▓┤ņØś ļ╣äņĀĢņāüņĪ░ņ¦ü ņäØĒÜīĒÖöņØś ņĪ┤ņ×¼ļŖö Ļ│╝ļ”Į ņäØĒÜīņ¦ł ļ¼╝ņ¦łĻ│╝ ņäØĒÜī ņåīĻĄ¼(calcospherites) Ļ▓░ņĀĢņ▓┤ņØś ņØ┤ņ░©ņĀüņØĖ ņČĢņĀüņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢśļ®░, ņØ┤ņÖĆ ļÅÖņØ╝ĒĢ£ ĻĖ░ņĀäņØ┤ phakomatous choristomaņŚÉņä£ ļ╣äņĀĢņāüņĪ░ņ¦ü ņäØĒÜīĒÖöļź╝ ĒśĢņä▒ĒĢśļŖö ļŹ░ņŚÉ ĻĖ░ņŚ¼ĒĢ£ļŗż[6].
ņāüĒö╝ņä¼ņØĆ S-100Ļ│╝ ņØĖĻ░ä ņłśņĀĢņ▓┤ņØś ņŻ╝ņÜöĒĢ£ ļŗ©ļ░▒ņ¦łņØĖ ╬▒, ╬▓ Ļ▓░ņĀĢņŚÉ Ļ░ĢĒĢ£ ļ®┤ņŚŁļ░śņØæņä▒ņØä ļ│┤ņØ┤Ļ│Ā[7,10,11], ļ╣äļ®śĒŗ┤(ņØĖĻ░ä ņłśņĀĢņ▓┤ņāüĒö╝ņäĖĒżņŚÉ ĒŖ╣ņØ┤ņĀüņØĖ ņżæĻ░ä ņä¼ņ£Ā)ņŚÉ ņ¢æņä▒ ņåīĻ▓¼[7,10,12], ņé¼ņØ┤ĒåĀņ╝ĆļØ╝Ēŗ┤(ņØ╝ļ░śņĀüņ£╝ļĪ£ ļŗżļźĖ ņāüĒö╝ņäĖĒżņŚÉ ņĪ┤ņ×¼ĒĢśļŖö ņżæĻ░äņä¼ņ£Ā)ņŚÉ ņØīņä▒ ņåīĻ▓¼ņØä ļ│┤ņØĖļŗż[10]. ņØ┤ļ¤¼ĒĢ£ ņåīĻ▓¼ņØĆ phakomatous choristomaĻ░Ć ņłśņĀĢņ▓┤ ĻĖ░ņøÉņØ┤ļØ╝ļŖö Ļ▓āņØä ļÆĘļ░øņ╣©ĒĢ£ļŗż[7]. ņé¼ņØ┤ĒåĀņ╝ĆļØ╝Ēŗ┤ņØĆ ļ░£ņāØ ņ┤łĻĖ░ ļŗ©Ļ│ä ļÅÖņĢł ņłśņĀĢņ▓┤ņŚÉ ņĪ┤ņ×¼ĒĢśĻ│Ā ņØĖĻ░ä ļ░░ņĢä 8ņŻ╝ņ░© ņŗ£ĻĖ░ņŚÉ ņé¼ļØ╝ņ¦ĆļŖöļŹ░[11], phachomatous choristomaĻ░Ć S-100, ļ╣äļ®śĒŗ┤ņŚÉ ņ¢æņä▒, ņé¼ņØ┤ĒåĀņ╝ĆļØ╝Ēŗ┤ņŚÉ ņØīņä▒ ņåīĻ▓¼ņØä ļ│┤ņØ┤ļŖö Ļ▓āņØĆ ņłśņĀĢņ▓┤ ļČäĒÖöņÖĆ ņØ╝ņ╣śĒĢśĻ│Ā ņä▒ņłÖ ņłśņĀĢņ▓┤ņāüĒö╝ņäĖĒż ņåīĻ▓¼Ļ│╝ ļÅÖņØ╝ĒĢśļŗż[6,13]. ļ│Ė ņ”ØļĪĆņØś ĒÖśņĢäļŖö S-100ņŚÉ Ļ░ĢĒĢ£ ņ¢æņä▒, ņé¼ņØ┤ĒåĀņ╝ĆļØ╝Ēŗ┤ņŚÉ ĻĄŁņåīņĀüņØĖ ņ¢æņä▒ ņåīĻ▓¼ņØä ļ│┤ņśĆļŖöļŹ░, Blenc et al [14], Rosenbaum et al [7]ļÅä ņāüĒö╝ņäĖĒżĻ░Ć ņé¼ņØ┤ĒåĀņ╝ĆļØ╝Ēŗ┤ AE1/AE3ņŚÉ ĻĄŁņåīņĀüņØĖ ņäĖĒżņ¦ł ņŚ╝ņāēņØä ļ│┤ņØĖ Ļ▓ĮņÜ░ļź╝ ļ│┤Ļ│ĀĒĢśņśĆĻ│Ā ņØ┤Ļ▓āņØĆ phakomatous choristomaņØś ĻĖ░ņøÉņØ┤ Ēæ£ļ®┤ ņÖĖļ░░ņŚĮņØ┤ļØ╝ļŖö Ļ▓āņØä ļ░śņśüĒĢ£ļŗż[7].
Phakomatous choristomaļŖö ļ│┤ĒåĄ ļŗżļźĖ ņØ┤ņāüņØä ļÅÖļ░śĒĢśņ¦Ć ņĢŖņ£╝ļéś, ļłłļ¼╝Ļ┤Ć Ļ│äĒåĄņØś ĒÅÉņćäļéś[12] ņŗ£ņŗĀĻ▓ĮņØś ĒśĢņä▒ ņĀĆĒĢśļéś Ļ▓░ņåÉ ļō▒ņØś[15] ņäĀņ▓£ņä▒ ņĢłĻĄ¼ ņØ┤ņāüņØä ļÅÖļ░śĒĢśĻĖ░ļÅä ĒĢ£ļŗż. Ļ░Éļ│ä ņ¦łĒÖśņ£╝ļĪ£ ņ£ĀĒö╝ļéŁņóģ(dermoid cyst), ļłäļéŁļźś(dacryocele), ņśüņĢäĒśłĻ┤Ćņóģ(infantile hemangioma), ņĮ®ļŗżļלļü╝(chalazion), ļ”╝Ēöä ĻĖ░ĒśĢ(lymphatic malformation), ĒÜĪļ¼ĖĻĘ╝ņ£Īņóģ(rhabdomyosarcoma)ņØ┤ ņ׳ļŗż[4]. ņØ┤ ņżæņŚÉ ĒÜĪļ¼ĖĻĘ╝ņ£ĪņóģņØĆ ļ╣Āļź┤Ļ▓ī ņä▒ņןĒĢśļ®░ ņ╣©ņŖĄņä▒ņØ┤ Ļ░ĢĒĢ£ Ļ▓āņØ┤ ĒŖ╣ņ¦ĢņØ┤ļŗż. ļ»Ėņä▒ņłÖļÉ£ ņĢģņä▒ ņżæĻ░äņŚĮ ņäĖĒżļĪ£ ņØ┤ļŻ©ņ¢┤ņ¦Ćļ®░ Ļ│©Ļ▓®ĻĘ╝ņØś ļČäĒÖö ņĀĢļÅäņŚÉ ļö░ļØ╝ ņ¦äļŗ©ņØ┤ Ļ░ĆļŖźĒĢ£ļŹ░, ņĀäņé¼ņØĖņ×Éļŗ©ļ░▒(transcription factor protein)ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö myoD1Ļ│╝ myogeninņØä ĒÖĢņØĖĒĢśņŚ¼ ņ¦äļŗ©ĒĢĀ ņłś ņ׳ļŗż. myoD1Ļ│╝ myogeninņØĆ Ļ│©Ļ▓®ĻĘ╝ņØ┤ ļ░£ņāØĒĢĀ ļĢī ņĪ┤ņ×¼ĒĢśļ®░ ņŗĀĻ▓ĮņØ┤ ļČäĒżĒĢśĻ│Ā ĻĘ╝ņ£ĪņØ┤ ņä▒ņłÖĒĢĀ ļĢī ņé¼ļØ╝ņ¦ĆļŖö ņØĖņ×ÉņØ┤ļéś, ĒÜĪļ¼ĖĻĘ╝ņ£ĪņóģņŚÉņä£ļŖö ņØ┤ļ¤¼ĒĢ£ ņØĖņ×ÉļōżņØ┤ Ļ│©Ļ▓®ĻĘ╝ņŚÉ ļé©ņĢä ļ®┤ņŚŁņĪ░ņ¦üĒÖöĒĢÖņĀü Ļ▓Ćņé¼ņŚÉņä£ ĒÖĢņØĖņØ┤ Ļ░ĆļŖźĒĢśļŗż.
Phakomatous choristomaļŖö ļ¦żņÜ░ ļō£ļ¼╝Ļ│Ā ļ╣äĒŖ╣ņØ┤ņĀüņØĖ ņ×äņāüņ¢æņāüĻ│╝ ņśüņāüĻ▓Ćņé¼ Ļ▓░Ļ│╝ļź╝ ļ│┤ņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ ļ│┤ĒåĄ ņłśņłĀ ņĀäņŚÉ ņ¦äļŗ©ļÉśņ¦ĆļŖö ņĢŖņ£╝ļ®░, ņłśņłĀ Ēøä ņĪ░ņ¦üļ│æļ”¼ĒĢÖņĀü Ļ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ņĀĢĒÖĢĒĢśĻ▓ī ņ¦äļŗ©ĒĢĀ ņłś ņ׳ļŗż. ļ│Ė ņ”ØļĪĆņŚÉņä£ļÅä ņóģņ¢æņØś ņä▒ņן ņåŹļÅäĻ░Ć ļŖÉļ”¼Ļ│Ā ņ╣©ņŖĄņĀüņØĖ ņåīĻ▓¼ņØ┤ ņŚåņ¢┤ ņĢģņä▒ņóģņ¢æņØś Ļ░ĆļŖźņä▒ņØĆ ļé«ņĢśņ£╝ļéś ņłśņłĀ ņĀäņŚÉ ņĀĢĒÖĢĒ׳ ņ¦äļŗ©ĒĢĀ ņłśļŖö ņŚåņŚłļŗż. ņĀłņĀ£ ņāØĻ▓Ć Ēøä ņŗ£Ē¢ēĒĢ£ ļ®┤ņŚŁņĪ░ņ¦üĒÖöĒĢÖ ņŚ╝ņāēņŚÉņä£ ļŹ░ņŖżļ»╝(desmin), myoD1ņŚÉ ņØīņä▒ņØ┤ņ¢┤ņä£ ĒÜĪļ¼ĖĻĘ╝ņ£ĪņóģņØä ļ░░ņĀ£ĒĢśņśĆĻ│Ā, phakomatous choristomaņŚÉ ĒŖ╣ņØ┤ņĀüņØĖ ņåīĻ▓¼ņØä ļ│┤ņŚ¼ ņ¦äļŗ©ņØä ļé┤ļ”┤ ņłś ņ׳ņŚłļŗż. ņ╣śļŻīļŖö ņÖäņĀäĒĢ£ ņÖĖĻ│╝ņĀü ņĀłņĀ£ļź╝ ĒåĄĒĢ┤ ņä▒Ļ│ĄņĀüņ£╝ļĪ£ ņ╣śļŻī Ļ░ĆļŖźĒĢśļ®░[12], ļČłņÖäņĀäĒĢ£ ņÖĖĻ│╝ņĀü ņĀłņĀ£ļź╝ ņŗ£Ē¢ēĒĢ£ Ļ▓ĮņÜ░ņŚÉļÅä ņ×¼ļ░£ņØ┤ļéś ļŗżļźĖ ņĢłĻ│╝ņĀü ņØ┤ņāü ņåīĻ▓¼ņØ┤ ļé©ņØĆ Ļ▓ĮņÜ░ļŖö ļ│┤Ļ│ĀļÉśņ¦Ć ņĢŖņĢśļŗż[4]. ļ│Ė ņ”ØļĪĆņØś ĒÖśņĢäļÅä ņłśņłĀ Ēøä 14Ļ░£ņøö ļÅÖņĢł Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśņśĆņ£╝ļéś ņ×¼ļ░£ņØ┤ļéś ņé¼ņŗ£, ņĢłĻĄ¼ņÜ┤ļÅÖņØ┤ņāü ļō▒ ļŗżļźĖ ņĢłĻ│╝ņĀü ņØ┤ņāü ņåīĻ▓¼ņØĆ ņŚåņŚłļŗż.
ļ│Ė ņ”ØļĪĆļŖö ņĢłņÖĆņØś phakomatous choristomaĻ░Ć ĒĢśņé¼ĻĘ╝ņØä ņ╣©ļ▓öĒĢ£ ĻĄŁļé┤ ņĄ£ņ┤ł ļ│┤Ļ│ĀņØ┤ļŗż. ļ░£ņāØ ļ╣łļÅäĻ░Ć ļé«ņ¦Ćļ¦ī ņåīņĢäņØś ņĢłņÖĆ ĒĢśļé┤ņĖĪņŚÉ ļ░£ņāØĒĢ£ ņóģņ¢æ ņ¦äļŗ© ņŗ£ Ļ░Éļ│äņ¦äļŗ©ņ£╝ļĪ£ Ļ│ĀļĀżĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż.
Figure┬Ā1.
Preoperative clinical photograph and magnetic resonance images. (A) External photo of 2-month-old boy who had an inferomedial subcutaneous mass of the right orbit. (B, C) Contrast-enhanced magnetic resonance imaging of the orbit. A well-defined mass was located in the inferomedial portion of right orbit. There was mild to intermediate hyperintensity and homogeneous enhancement at T2 weighted image, without any bone destruction or invasion (B: coronal T2-weighted contrast-enhanced magnetic resonance imaging [MRI], C: axial T2-weighted contrast-enhanced MRI).

Figure┬Ā2.
Operative photograph. (A, B) Solid mass (white arrows) invaded the inferior oblique muscle (black arrows). (C) Gross image of excised mass. A dark red soft mass was observed.

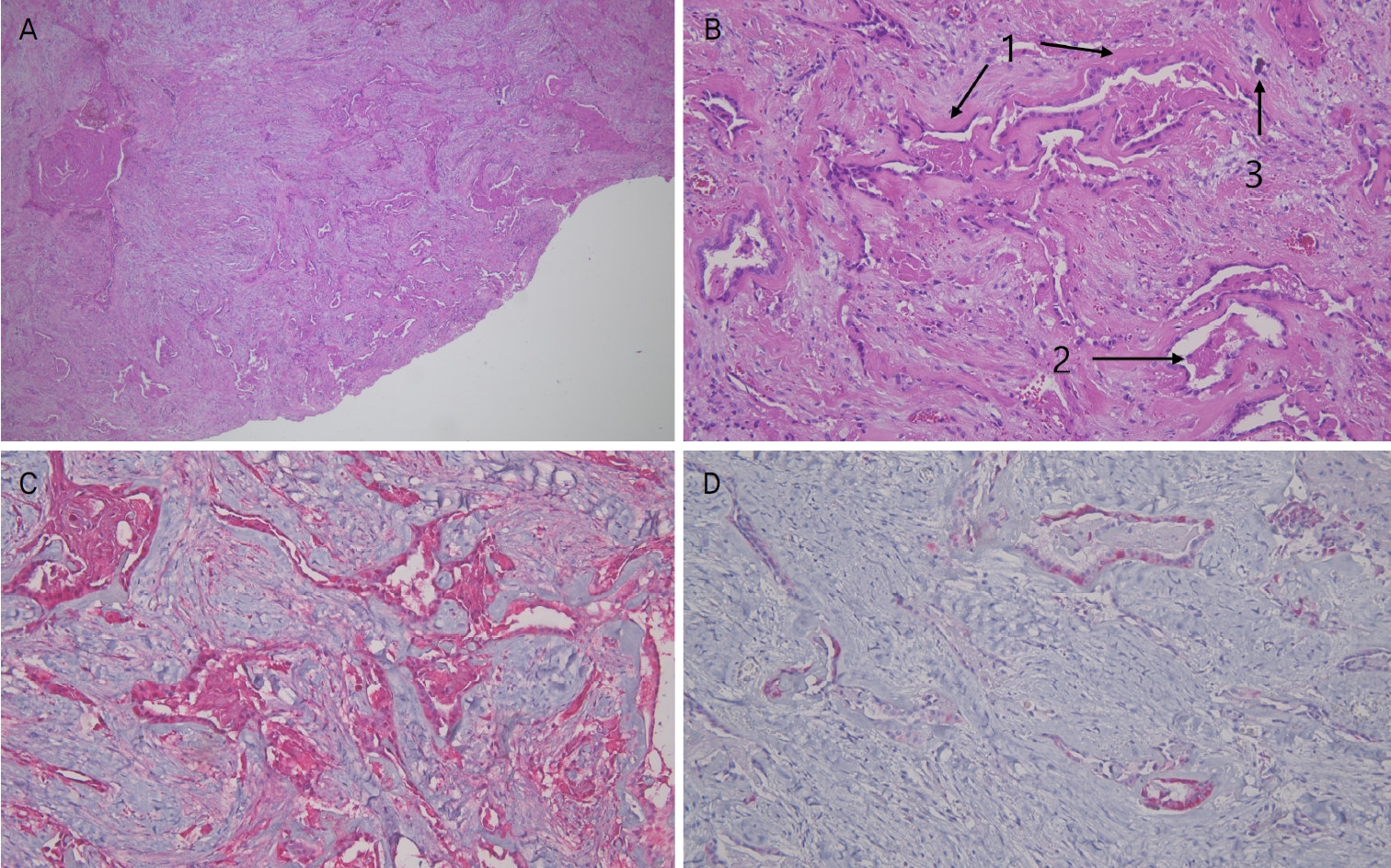
Figure┬Ā3.
Histopathological images. (A) Pseudoglandular structures embedded in collagenous stroma (hematoxylin-eosin stain [H&E], ├Ś40). (B) Thick basement membrane (1) surrounding pseudoglandular structures of epithelial islands. Eosionophilic material (2) inside the lumen. Psammomatous calcific foci (3) in the stroma (H&E stain, ├Ś200). (C) The epithelioid islands demonstrated strong immunoreactivity for S-100 protein (S-100, ├Ś200). (D) Focal immunoreactivity for cytokeratin (cytokeratin, ├Ś200).
REFERENCES
1) Zimmerman LE. Phakomatous choristoma of the eyelid. A tumor of lenticular anlage. Am J Ophthalmol 1971;71(1 Pt 2):169-77.
2) Rafizadeh SM, Ghadimi H, Nozarian Z. Phakomatous choristoma of the eyelid and orbit: a case report. Pediatr Dev Pathol 2020;23:296-300.


3) Adulkar N, Santhi R, Kim U. A unique case of intracorneal aberrant lenticular rest. J AAPOS 2013;17:326-7.


4) Romano RC, McDonough P, Salomao DR, Fritchie KJ. Phakomatous choristoma in a 10-week-old boy: a case report and review of the literature. Pediatr Dermatol 2015;32:405-9.


5) Harris BF, Harris JP, Ducey TJ, et al. Phakomatous choristoma of the orbit with involvement of the inferior oblique muscle. Ophthalmic Plast Reconstr Surg 2019;35:e10-9.


6) Shin HM, Song HG, Choi MY. Phakomatous choristoma of the eyelid. Korean J Ophthalmol 1999;13:133-7.


7) Rosenbaum PS, Kress Y, Slamovits TL, Font RL. Phakomatous choristoma of the eyelid. Immunohistochemical and electron microscopic observations. Ophthalmology 1992;99:1779-84.


8) McMahon RT, Font RL, McLean IW. Phakomatous choristoma of eyelid: electron microscopical confirmation of lenticular derivation. Arch Ophthalmol 1976;94:1778-81.


9) Tripathi RC, Tripathi BJ, Ringus J. Phakomatous choristoma of the lower eyelid with psammoma body formation: a light and electron microscopic study. Ophthalmology 1981;88:1198-206.


10) Ellis FJ, Eagle RC Jr, Shields JA, et al. Phakomatous choristoma (Zimmerman's tumor). Immunohistochemical confirmation of lens-specific proteins. Ophthalmology 1993;100:955-60.


11) Kasper M, Viebahn C. Cytokeratin expression and early lens development. Anat Embryol (Berl) 1992;186:285-90.


12) Verb SP, Roarty JD, Black EH, et al. Phakomatous choristoma: a rare orbital tumor presenting as an eyelid mass with obstruction of the nasolacrimal duct. J AAPOS 2009;13:85-7.


13) Michetti F, Rende M, Calogero G, et al. Immunochemical detection of S-100 protein in non-nervous structures of the rabbit eye. Brain Res 1985;332:358-60.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 1,842 View
- 44 Download
- Related articles
-
A Case of MALT Lymphoma with Left Inferior Rectus Muscle Invasion.2014 June;55(6)
The Effect of Modified Anterior Transposition of the Inferior Oblique Muscle.1997 March;38(3)
Ultrastructural Study on the Overacting Inferior Oblique Muscles.1993 April;34(4)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



