 |
 |
| J Korean Ophthalmol Soc > Volume 62(9); 2021 > Article |
|
국문초록
증례요약
54세 남자 환자가 1달 전에 우안 눈물흘림을 주소로 내원하였다. 양안 눈물길관류검사상 우안은 아래눈물점을 통해 관류하였을 때, 윗눈물점으로 역류가 관찰되었고 좌안은 정상 관류를 보였다. 안와 전산화단층촬영에서 우측 눈물주머니에 3.0 × 3.4 × 3.0 cm 크기의 경계가 불분명한 종괴가 발견되었고, 우측 눈물관, 비강 및 안와 하벽과 내벽을 침범한 것이 관찰되었다. 전신마취하에 우측 안와부 하측 절개를 통해 눈물주머니 부위의 종괴 생검을 시행하였고, 조직병리학적 검사에서 소세포신경내분비암종으로 진단되어 항암치료를 하였다.
ABSTRACT
Purpose
We report a case of primary small cell neuroendocrine carcinoma arising from the lacrimal sac.
Case summary
A 54-year-old man presented with epiphora that had been present for 1 month. He underwent lacrimal syringe analysis of the lower punctum in the right eye, which demonstrated fluid regurgitation from the upper punctum. Computed tomography revealed a 3.0 × 3.4 × 3.0 cm mass with an ill-defined margin in the right lacrimal sac, which demonstrated invasion of the lacrimal duct and bony destruction of the inferior and medial orbital walls. Incisional biopsy and histologic examination showed that the tumor was composed of small round tumor cells. On the basis of histopathological and immunohistochemical evaluations, a diagnosis of small cell neuroendocrine carcinoma was made. The patient received chemotherapy.
Conclusions
To the best of our knowledge, this is the first case of primary small cell neuroendocrine carcinoma arising from the lacrimal sac in Korea. Small cell neuroendocrine carcinoma in the lacrimal sac should be regarded as a differential diagnosis for patients with a nasolacrimal duct obstruction.
소세포신경내분비암종(small cell neuroendocrine carcinoma)은 신경내분비세포에서 기원하는 신경내분비종양의 아형으로 비교적 드문 종양이다[1,2]. 소세포신경내분비암종은 주로 50-70대 연령에서 호발하는 것으로 알려져 있다. 이 종양은 폐, 위장관, 난소, 방광 등 다양한 부위에서 발생한 것은 보고된 바 있으나, 눈물주머니에서 발생한 것은 매우 드물며 국내 발생은 첫 예이다[3,4]. 저자들은 눈물관막힘의 증상으로 내원한 환자에서 발견된 종괴의 조직검사 결과 눈물주머니에서 발생한 소세포신경내분비암종으로 진단된 1예를 경험하였기에 보고하는 바이다.
54세 남자가 1달 전부터 갑자기 시작된 우안 눈물 흘림을 주소로 내원하였다. 병력상 전신질환, 종양, 감염질환, 외상, 약물 복용력, 수술 및 안과 질환의 과거력은 없었다. 복시, 시력저하, 통증을 포함한 다른 동반 증상은 없었다. 초진 시 최대교정시력 우안 20/25, 좌안 25/25이었다. 이학적 검사에서 우측 안구 촉진 시 발적, 부종, 압통, 국소 열감, 안구돌출 등의 소견은 없었고, 안구운동검사에서 사시소견이나 안구운동제한은 없었다. 양안 눈물길관류검사상 우안은 아래눈물점을 통해 관류하였을 때 윗눈물점으로 역류가 관찰되었고 좌안은 정상 관류를 보였다. 코안을 내시경으로 관찰하였으나 특이 소견은 없었다.
임상적으로 코눈물관막힘(nasolacrimal duct obstruction)으로 생각되었으나, 비교적 젊은 나이와 1달 전에 발생한 갑작스러운 눈물흘림 이외의 특이 증상이 없어 추가적인 감별진단을 위해 안와 전산화단층촬영을 시행하였다. 안와전산화단층촬영 소견상 우측 하측부, 눈물주머니 및 눈물관에서 3.0 × 3.4 × 3.0 cm 크기의 경계가 불분명한 고음영의 종괴가 안와 하벽과 내벽을 침범한 것이 관찰되었다(Fig. 1). 전신마취하에 우측 안와부 하측 절개를 시행하여 눈물주머니 부위의 종괴 조직을 절개생검하였다. 광학현미경 소견상 종양세포의 핵은 둥글고 난원형이었고, 미세한 과립상의 염색질과 적은 양의 세포질을 나타내었다(Fig. 2A). 종양세포는 덩어리 혹은 기둥 모양으로 배열하고 있었다. 면역조직화학염색검사에서 종양세포는 시냅토파이신(synaptophysin), 크로모그라닌 A (chromogranin A)와 cytokeratin 20에 모두 음성이었고, cytokeratin (AE1/AE3)와 neuron specific enolase (NSE)에는 양성을 각각 나타내었다(Fig. 2B). 면역조직화학염색 결과 신경내분비표지자인 시냅토파이신과 크로모그라닌 A에 음성이었지만, 종양세포의 형태학적 특징과 cytokeratin (AE1/AE3)과 NSE에 양성인 점으로 소세포신경내분비암종으로 진단되었다.
암의 병기를 확인하기 위해 추가적으로 시행한 양전자방출전산화단층촬영장치(position emission tomography/computed tomography, PET/CT)검사에서 간의 구역(segment) 6에서 2 cm 크기의 대사 증가 소견을 확인하여, 눈물주머니에서 발생한 원발성 소세포신경내분비암종이 간으로 전이된 것이 관찰되었다(Fig. 3). 이후 추가적인 치료 및 평가를 위해 혈액종양내과로 전과하여 항암치료를 시행하였다. 3개월 후 시행한 안와 전산화단층촬영 소견상, 이전에 비하여 병변 크기의 차이는 없었다.
눈물주머니종양은 매우 드문 종양으로 국소적으로 침습을 하게 되면 예후가 좋지 않다[5]. 눈물주머니종양은 55%가 악성종양을 나타내며, 종양의 병기와 유형에 따라 다르지만, 평균 치사율은 38%로 보고되었다[5,6]. 임상적으로 눈물주머니종양은 복시, 눈꺼풀처짐, 안구운동제한, 안구통증, 안구돌출, 눈물관 폐쇄로 인한 눈물흘림, 눈물주머니 부위에서 만져지는 종괴 등의 증상이 관찰된다[7,8]. 만성눈물주머니염이나 안와조직염에서도 위와 같은 소견이 보일 수 있어 임상 소견만으로는 눈물주머니종양 구분이 쉽지 않다[9-11]. Ramberg et al [9]은 눈물기관계통(lacrimal drainage system)에서 종양 진단을 받은 539명의 환자 중 266명(49%)에서 증상이 있었고, 그 외에 특이 소견이 없는 환자 중 일부는 눈물주머니코안연결술(dacryocystorhinostomy) 중에 종양이 우연히 발견되었다고 보고하였다. 본 증례의 경우도 특이 과거력이 없는 50대 남성이 1달 전부터 갑작스러운 우안 눈물흘림을 나타내어 추가적인 감별을 위해 안와 전산화단층촬영검사를 시행하였다. 전산화단층촬영검사에서 눈물주머니 종괴가 발견되어 조직 절개생검을 하였고, 최종적으로 소세포신경내분비암종으로 진단되었다. 전산화단층촬영검사에서 종괴의 크기가 비교적 컸으나, 안와 내벽 및 하벽을 파괴하여 안와 자체에 미치는 종괴 효과가 상쇄되어 눈물흘림 외에 안구운동제한, 안구통증, 안구돌출 등의 소견이 저명하게 관찰되지 않았다. 따라서 일반적인 눈물흘림 양상을 보이지 않는 환자에게는 정확한 진단 및 치료를 위해 영상의학적 검사가 필요할 것이라 생각한다.
눈물주머니종양은 상피 종양과 비상피 종양으로 분류하며, 이 중 60-94%가 상피 종양이다[7]. Ramberg et al [9]은 상피종양에는 편평세포암종(squamous cell carcinoma) 55%, 이행세포암종(transitional cell carcinoma) 20%, 점액표피모양암종(mucoepidermoid carcinoma) 8%, 샘낭암종(adenoid cystic carcinoma) 6%, 소세포신경내분비암종 0.1%로 각각 보고하였다. 소세포신경내분비암종은 다양한 호르몬을 분비하는 내분비세포와 신경세포의 특징 모두 지닌 종양으로 조직학적으로 미분화 형태이고, 임상적으로 악성인 특징을 가지고 있다[3]. 소세포신경내분비암종은 폐, 소화기계, 비뇨기계, 두경부에서 발생할 수 있으며, 내분비 세포에서 기원한 종양으로 다양한 신경단백질을 분비한다[1]. 조직학적으로 종양세포는 둥글거나 타원형의 핵을 가지고, 핵소체는 보이지 않고 세포질의 양은 매우 적다. 신경단백질인 시냅토파이신, 크로모그라닌 A와 NSE을 분비하여 면역조직화학염색에서 양성을 보인다[12].
소세포신경내분비암종과 감별할 종양은 메르켈세포암종(Merkel cell carcinoma)과 전이성 소세포신경내분비암종이다[13]. 메르켈세포암종은 피부에 발생하는 일종의 소세포신경내분비암종으로 조직학적으로 본 증례와 유사하나 면역조작화학 염색에서 cytokeratin 20에 음성인 점이 본 증례와 맞지 않다. 전이성 소세포신경내분비암종은 PET검사에서 소세포신경내분비암종이 흔히 발생하는 폐에는 특이 병변이 관찰되지 않아서 전이성 종양을 배제할 수 있었다.
소세포신경내분비암종의 치료는 종양의 크기, 림프절 및 원격전이 유무의 병리학적 진단을 근거로 한다. 대체로 항암요법과 수술 또는 방사선치료를 병행하도록 권하고 있으나 아직까지 명확한 치료법이 정립되지 않았다[14]. 일반적으로는 폐외소세포암에서 항암치료가 효과적이며, 원발병소에 국한된 경우 수술적 치료 및 방사선치료, 항암요법을 병행하는 것이 효과적이라고 보고하였다[2]. Mittal et al [11]은 25세 여자가 안와에서의 소세포신경내분비암종으로 진단 받아 항암치료를 시행하였고, 추적 관찰에서 재발되어 18개월 뒤에 사망하였다고 보고하였다. 본 증례 환자의 경우 발견 당시 눈물주머니에서 발생한 소세포신경내분비암종 뿐 아니라 간으로 전이되어 항암요법으로 치료 중이나 아직 치료 효과가 명확하게 관찰되지는 않았다.
눈물주머니에서 발견된 소세포신경내분비암종은 매우 드물지만 예후가 매우 나쁘며 진행도 빠르다[5]. 진단 시 다른 기관으로 전이되었거나 빠르게 진행되어 타 장기로 전이될 수 있기 때문에 눈물주머니종양이 의심될 때 신속한 진단과 치료가 필요할 것으로 생각된다.
Figure 1.
Computed tomography (CT) findings of the orbit. (A) Coronal and (B) axial CT images show a 3.0 × 3.4 × 3.0 cm-sized mass (arrows) in the right lacrimal sac with the invasion of lacrimal duct and bony destruction of the inferior and inferomedial orbital wall.
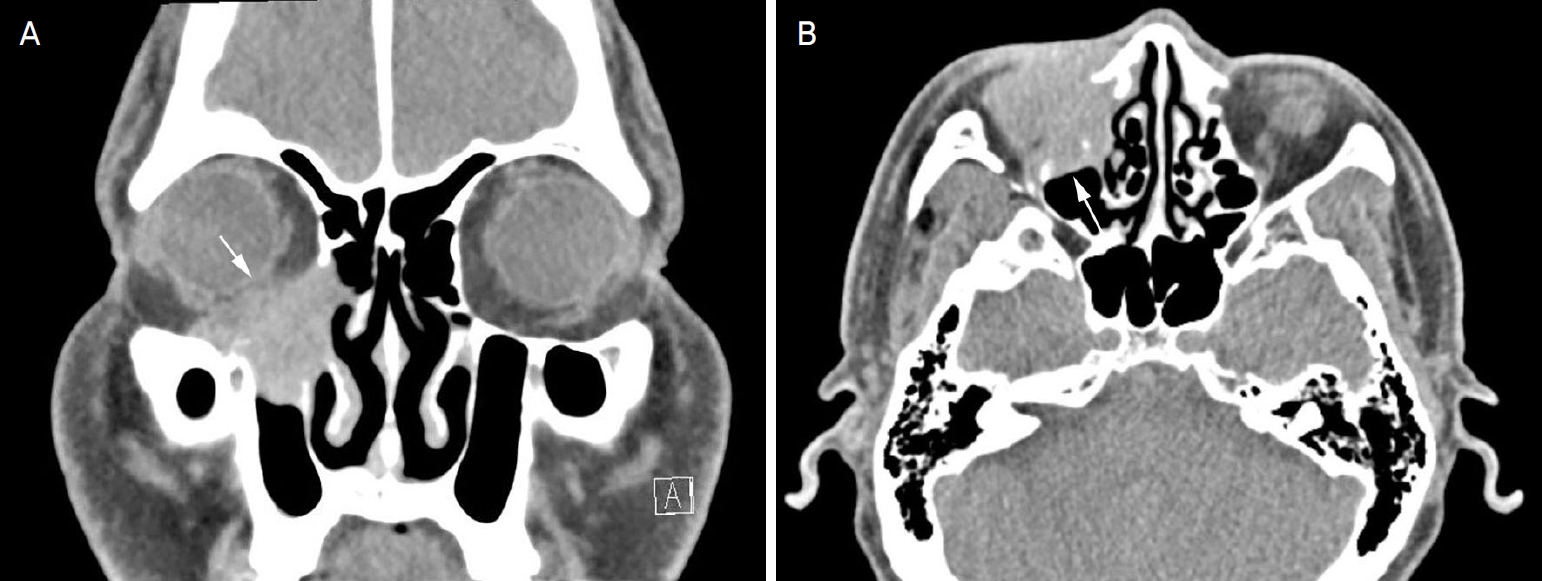
Figure 2.
Light microscopic findings. (A) The tumor is composed of small round cells with finely dispersed chromatin and scanty cytoplasm. The tumor cells are arranged in solid nests (hematoxylin-eosin stain, ×100). (B) The tumor cells show diffusely cytoplasmic positivity for neuron specific enolase (immunohistochemical stain, ×200).
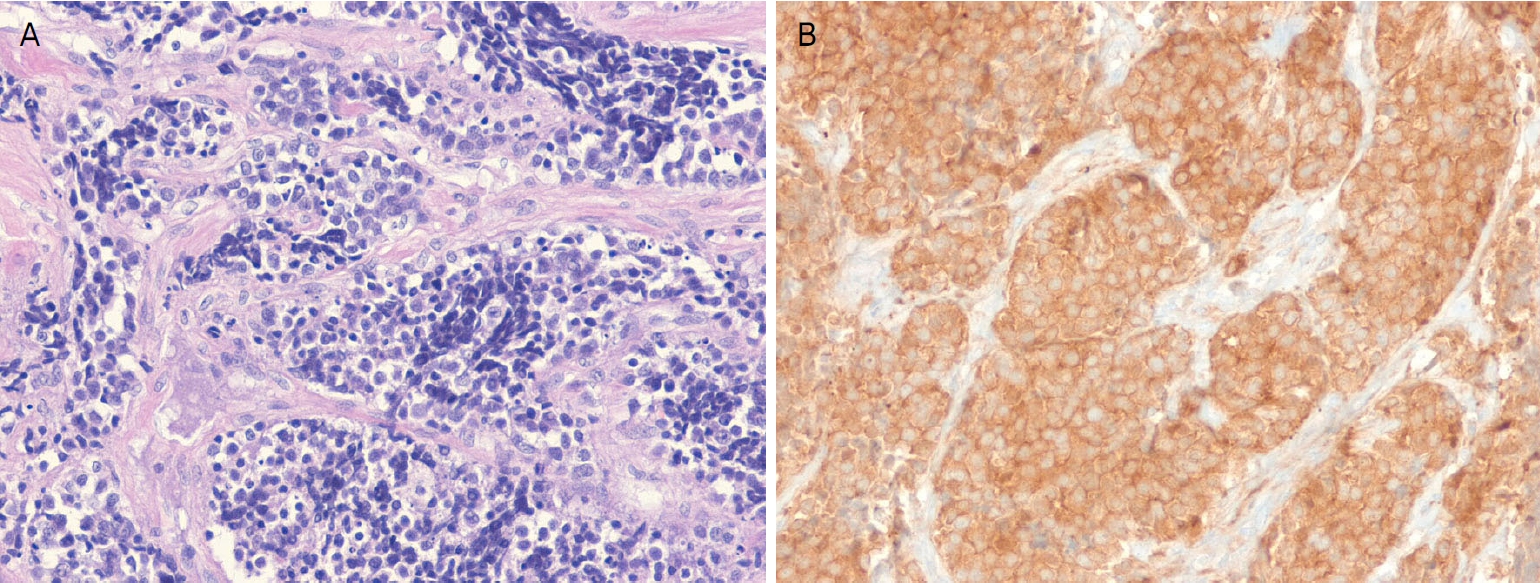
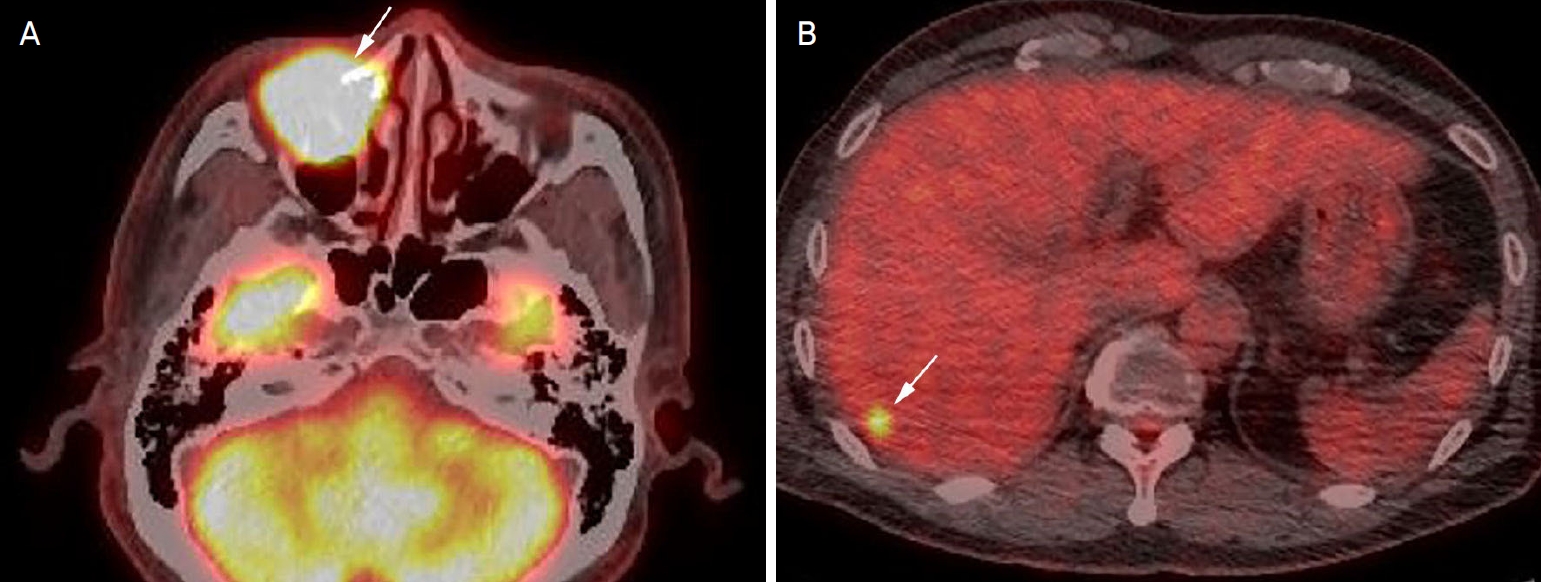
Figure 3.
Position emission tomography (fluorine-18-fluorodeoxyglucose positron emission tomography [18F-FDG PET])/computed tomography (CT) findings. (A) The abnormally increased radiotracer uptake lesion (arrow) is present in the right lacrimal sac area. (B) Intense FDG uptake lesion (arrow) is found in the liver, suggesting the metastasis of small cell neuroendocrine tumor.
REFERENCES
1) Wakaoka T, Mizuta K, Shibata H, et al. Eight cases of small cell neuroendocrine carcinoma of the head and neck. Nihon Jibiinkoka Gakkai Kaiho 2017;120:202-8.


2) Yalcin S. Introduction to neuroendocrine tumours. In: Yalcin S, Öberg K, ed. Neuroendocrine tumours. diagnosis and management, 1st ed. Berlin: Springer, 2015;chap. 1.
4) Lee SS, Lee JL, Ryu MH, et al. Extrapulmonary small cell carcinoma: single center experience with 61 patients. Acta Oncol 2007;46:846-51.


5) Goto T, Bandoh N, Nagato T, et al. Primary small cell carcinoma of lacrimal sac: case report and literature review. J Laryngol Otol 2010;124:1223-6.


6) Kim HJ, Langer PD. Lacrimal sac tumors: diagnosis and treatment. In: Servat JJ, Black EH, Nesi FA, Gladstone GJ, Calvano CJ, ed. Smith and Nesi’s ophthalmic plastic and reconstructive surgery. New York: Springer, 2012;chap. 40.
7) Montalban A, Liétin B, Louvrier C, et al. Malignant lacrimal sac tumors. Eur Ann Otorhinolaryngol Head Neck Dis 2010;127:165-72.


8) Krishna Y, Coupland SE. Lacrimal sac tumors--a review. Asia Pac J Ophthalmol (Phila) 2017;6:173-8.

9) Ramberg I, Toft PB, Heegaard S. Carcinomas of the lacrimal drainage system. Surv Ophthalmol 2020;65:691-707.


10) Wu W, Gan P, Xu Q, et al. Neuroendocrine carcinoma of the nasal cavity with epiphora as the first symptom: a case report. Medicine (Baltimore) 2020;99:e23502.



11) Mittal R, Kaza H, Agarwal S, et al. Small cell neuroendocrine carcinoma of the orbit presenting as an orbital abscess in a young female. Saudi J Ophthalmol 2019;33:308-11.


12) Scherübl H, Raue F, Frank-Raue K. Neuroendocrine tumors : classification, clinical presentation and imaging. Radiologe 2019;59:952-60.



13) Langfort R, Rudziński P, Burakowska B. Pulmonary neuroendocrine tumors. The spectrum of histologic subtypes and current concept on diagnosis and treatment. Pneumonol Alergol Pol 2010;78:33-46.





 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




