 |
 |
| J Korean Ophthalmol Soc > Volume 62(7); 2021 > Article |
|
국문초록
목적
섬유주세포에서 항혈관내피성장인자(anti-vascular endothelial growth factor, anti-VEGF)가 기질금속단백분해효소(matrix metalloproteinase, MMP)의 활성에 미치는 영향을 알아보고자 하였다.
대상과 방법
인체의 섬유주세포를 배양한 다음 0.25, 0.50 mg/mL anti-VEGF bevacizumab (BV)을 24시간 노출시킨 다음, carboxyfluorescein을 이용하여 섬유주단층세포층의 투과도를 측정하였고 trans-epithelial endothelial electrical resistance (TEER)를 측정하였다. Western blot으로 MMP-1/-2 단백의 활성을 측정하였으며 Griess assay를 이용하여 일산화질소(nitric oxide, NO)의 생성 정도를 측정하였다.
ABSTRACT
Purpose
To investigate the effects of anti-vascular endothelial growth factor (anti-VEGF) on the activity of matrix metalloproteinase (MMP) in human trabecular meshwork cells (HTMC).
Methods
Primary HTMC cultures were exposed to 0, 0.25, and 0.50 mg/mL anti-VEGF bevacizumab (BV) for 24 hours. The permeability through the trabecular meshwork cell monolayer was assessed using carboxyfluorescein and trans-epithelial endothelial electrical resistance (TEER). The levels of MMP-1/-2 were measured by Western blotting and the production of nitric oxide (NO) was assessed with the Griess assay.
Results
Bevacizumab at 0.50 mg/mL decreased the permeability of carboxyfluorescein significantly (p = 0.017) and did not affect TEER (p = 0.308). Administration of 0.50 mg/mL BV decreased MMP-1 and MMP-2 activities (p = 0.014, p = 0.016, respectively) and inhibited NO production significantly (p = 0.023).
혈관내피성장인자(vascular endothelial growth factor, VEGF)는 신생혈관생성의 중요한 매개체로서 주로 혈관내피세포에서 발현되는 특이 수용체에 결합하여 내피세포의 증식과 이동, 세포외기질의 분해와 같은 신생혈관생성작용을 나타낸다[1]. VEGF는 당뇨망막병증과 망막정맥폐쇄에 의한 신생혈관을 촉진하는 작용을 나타내는데, 임상적으로 신생혈관 억제 등을 목적으로 항혈관내피성장인자(anti-VEGF)로 만든 약제를 사용하고 있으나 부작용의 하나로 안압상승도 나타날 수 있다[2-4]. VEGF는 혈액뇌장벽의 투과도와 혈관내피세포의 투과도를 증가시키는 작용을 나타내며[5,6], 혈관내피세포와 평활근세포에서 VEGF의 작용기전으로 nitric oxide (NO)가 관여하는 것으로 알려져 있다[7,8]. 또한 안구 내에 조직과 망막혈관내피세포에서도 VEGF는 투과도를 증가시키며 이 과정에서도 NO가 관여한다고 알려져 있다[9,10].
섬유주는 방수유출로의 조절에 중요한 역할을 하는데, 섬유주를 통한 방수유출로의 저항이 증가되어 개방각녹내장을 유발하는 것으로 알려져 있다[11,12]. 섬유주를 통한 방수 유출에서 섬유주세포는 세포외기질의 대사를 조절하여 섬유주의 저항을 조절함으로써 안압을 유지하는 중요한 역할을 한다[13,14]. VEGF는 세포외기질을 분해하고 조절하는 역할을 하는 기질금속단백분해효소(matrix metalloproteinase, MMP)의 활성을 증가시키는데, 혈관내피세포에서 MMP-1과 MMP-2의 분비를 증가시키며 평활근세포에서도 MMP의 발현을 증가시킨다[15-17]. 섬유주세포는 혈관내피세포와 평활근세포의 성질을 나타내므로[18] anti-VEGF는 섬유주에서 MMP의 분비를 저하시켜 세포외기질의 축척을 유발하여 섬유주를 통한 방수유출을 저하시킬 가능성이 있을 것이나, 섬유주에서 anti-VEGF가 섬유주의 유출에 미치는 영향과 섬유주를 통한 방수유출을 촉진하는 작용을 나타내는 MMP에 대한 영향은 아직 자세히 밝혀지지 않았다. 이에 따라 본 연구에서는 배양한 사람의 섬유주세포를 이용하여 anti-VEGF가 섬유주의 투과도에 미치는 영향을 알아보고 세포외기질의 대사에 중요한 역할을 하는 MMP-1/-2의 분비에 미치는 영향을 알아보고자 하였다.
본 연구는 대구가톨릭대학병원 의학윤리심의위원회(Institutional Review Board, IRB)의 승인을 받았고(IRB 승인 번호: CR-19-059-L) 헬싱키선언을 따라 시행되었다. 기존의 안병력이 없는 안구이식에 동의한 50세 환자로부터 안구은행에서 얻은 사후 6시간 이내의 안구에서 전방각에서 섬유주를 벗겨내어 배양접시에 옮긴 후 항생제(antibiotic antimycotic solution containing penicillin, streptomycin and amphotericin B, Gibco, Invitrogen, Carlsbad, CA, USA)와 10% 우태아혈청(fetal bovine serum, FBS) (HyClone, Cytiva, Global Life Sciences Solutions USA LLC, Marlborough, MA, USA)이 포함된 Dulbecco’s modified Eagle’s medium (DMEM; Gibco, Invitrogen, Carlsbad, CA, USA) 배지를 사용하여 37°C, 5% CO2 배양기에서 초대배양하였다. 섬유주세포가 이식된 조직편 주위로 자라 나오는 양상과 형태학적으로 섬유주세포의 특징을 확인한 후 섬유주 조직의 이식편을 제거하고 배양을 계속하였으며 세포가 배양접시에 충만해지면 1:3의 비율로 트립신 처리하여 계대배양하였다. 배양된 세포를 섬유주세포 표지자(fibronectin, lamininm, vimentin)로 확인한 후 동결보존하였다. 실험을 위하여 동결보존한 세포를 해동한 후 배양한 다음 인체의 섬유주세포에 anti-VEGF 제제인 bevacizumab (BV; Avastin®, Genentech, South San Francisco, CA, USA)을 0.25, 0.50 mg/mL의 농도로 24시간 동안 노출시켰다. 이때 BV의 농도는 0.1% FBS가 포함된 DMEM 배지를 이용하여 희석하여 조절하였으며 대조군은 동량의 0.1% FBS가 함유된 DMEM을 사용하였다.
세포의 생존에 대한 효과는 3-[4, 5 -dimethylthiazol-2-yl]-2, 5-diphenyltetrazolium bromide (MTT; Sigma-Aldrich, MO, USA) assay를 이용하였으며 세포의 생존 정도는 실험군의 값을 약물처리를 하지 않은 대조군의 비로 나누어 백분율로 나타내었다.
Transwell (Pore size 0.3 ❍m, polycarbonate membrane, #3460, Corning Life Sciences, Tewksbury, MA, USA)의 내측 chamber에 세포가 단일 세포층으로 충만하게 자란 것을 확인한 후 BV에 24시간 노출시킨 후 투과도 검사를 시행하였다[19-21]. 내측 chamber에 자라고 있는 세포를 세척한 다음 50 mm carboxyfluorescein (Sigma, St. Louis, MO, USA)을 노출시키고 노출 2시간 후 외측 chamber로 투과된 carboxyfluorescein의 농도를 532 nm에서 분광형광계(Fluostar Optima, BMG Labtech, Ortenberg, Germany)로 측정하여 백분율로 나타내었다.
섬유주를 통한 투과도를 측정하기 위한 또 다른 방법으로 TEER assay를 시행하여 섬유주단층세포층의 저항도를 측정하였는데[22,23] TEER assay는 단층 세포층에서 전기적 저항이 증가할수록 투과도가 감소하는 원리를 이용한 방법이다. 섬유주세포를 내측 chamber에 충만하게 배양한 다음 BV에 24시간 노출시킨 후 TEER을 epithelial voltohmmeter (EVOM [2]; World Precision Instruments, Sarasota, FL, USA)를 이용하여 측정하였으며 그 결과를 net value (Ωcm2)로 기록하였다.
단백질 추출에는 RIPA buffer (Thermoscientific, Carlsbad, CA, USA)를 사용하였다. Cell lifter (Corning, Acton, MA, USA)로 세포를 모아 원심 분리하여 상층액을 모아 -80°C에 보관하였다. 단백질량은 BCA protein assay reagent kit (Thermoscientific, Carlsbad, CA, USA)를 사용하여 측정하였다. 정량한 샘플을 같은 양으로 NuPAGE 4-12% Bis-Tris gel (Invitrogen, Carlsbad, CA, USA)에 전기영동한 후 Xcell Surelock (Invitrogen, Carlsbad, CA, USA)을 이용하여 니트로셀룰로오스 막(Invitrogen, Carlsbad, CA, USA)에 1시간 동안 옮긴 다음 막 차단 용액(Invitrogen, Carlsbad, CA, USA)에서 1시간 동안 정치배양하였다. Goat anti-rabbit horseradish peroxidase-conjugated된 이차 항체(Santacruz Biotechnology Inc., Dallas, TX, USA)를 막 차단 용액에 1:3,000으로 희석하여 처리하고 상온에서 1시간 반응시켰다. 항체를 반응시킨 막을 SuperSignal West Pico Chemiluminescent Substrate (Thermoscientific, Carlsbad, CA, USA)를 이용하여 Gel Doc XR+ (Bio-rad, Hercules, CA, USA)로 단백의 발현양을 확인하였다. 이때 glyceraldehyde 3-phosphate dehydrogenase를 internal standard로 사용하였다.
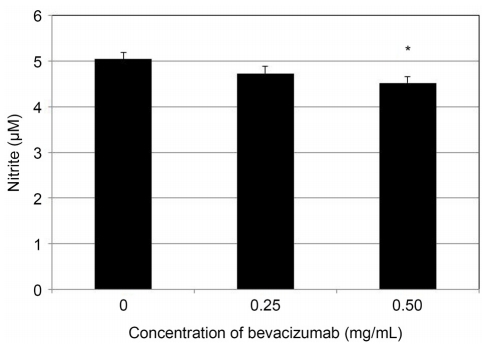
BV이 섬유주세포에서 내인성 일산화질소의 생성에 미치는 영향을 알아보기 위하여 Griess assay를[24] 시행하여 배지에서의 nitrite 생성량을 측정하였다. 약물처리한 세포 배지에 동량의 Griess 반응액(Sigma, St. Louis, MO, USA)을 섞은 후 96-well plate에 옮겨 NO 생성의 반응물인 아질산염(nitrite)의 양을 spectrophotometer로 540 nm에서 흡광도를 측정하여 정량하였다. 이때 표준치를 구하기 위해 sodium nitrite (Sigma, St. Louis, MO, USA)를 단계적으로 희석하여 사용하였다.
약제에 노출되지 않은 대조군에 비하여 0.25 mg/mL BV는 배지에서 nitrite의 생성에 유의한 영향을 미치지 않았으나(p=0.190), 0.50 mg/mL BV는 배지에서 nitrite의 생성량을 유의하게 증가시켰다(p=0.023) (Fig. 6).
Anti-VEGF는 재조합 단일클론 IgG 항체이며 안구 조직에 미치는 영향은 이미 잘 알려져 있다[17]. 임상적으로 사용되는 농도에서는 anti-VEGF는 독성을 유발하지 않는다는 보고도 있으나 고농도에 노출될 경우 섬유주세포에 대한 독성을 유발할 수 있다[25-28]. 그러나 본 실험에 사용된 저농도의 anti-VEGF는 기존 연구 결과와 마찬가지로 섬유주세포 생존에 유의한 영향을 미치지 않았다[25].
Anti-VEGF 제제의 부작용의 하나로 안압상승이 초래될 수 있는데[2-4], 안압상승의 기전은 아직 명확하게 밝혀지지 않았으나 그 기전의 하나로서 anti-VEGF는 NO의 생성을 억제하는 작용이 있으므로 섬유주에 노출될 경우 방수유출을 억제함으로써 안압상승을 유발하는 기전으로 작용할 가능성이 제시된 바 있다[27].
Anti-VEGF가 방수유출에 미치는 영향을 실험실 내 연구로 알아보기 위하여 시행한 anti-VEGF의 일종인 BV을 사용한 섬유주단층세포층의 투과도검사에서 0.50 mg/mL BV는 carboxyfluorescein의 투과도를 유의하게 감소시켰다. 따라서 anti-VEGF는 농도가 높을수록 섬유주세포의 투과도를 감소시킬 가능성이 있다.
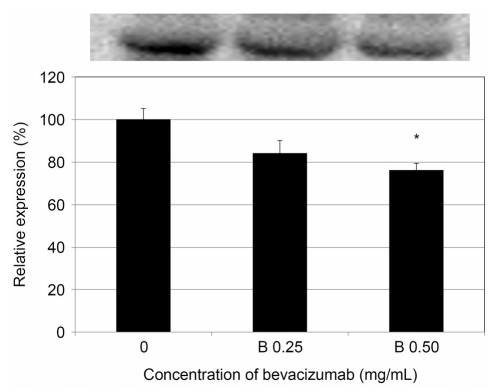
섬유주를 통한 방수유출의 저항을 조절하는 데에 있어서 MMP에 의한 세포외기질의 대사조절이 중요한 역할을 한다. 섬유주세포와 조직에서 다양한 종류의 MMP가 발현되는데 이들 MMP 중 MMP-1, 3, 9은 정상 상태에서는 발현이 미약하나 다양한 자극에 의해 발현이 증가되며, MMP-2는 비교적 많이 발현되는 것으로 알려져 있으므로[13,14] 본 연구에서는 MMP-1과 MMP-2의 발현을 조사하였다. VEGF는 혈관내피세포에서 MMP-1과 MMP-2의 분비를 증가시키며, 평활근세포에서도 MMP의 발현을 증가시키므로[15-17], anti-VEGF는 MMP의 활성을 감소시켜 세포외기질의 대사를 저해함으로써 섬유주의 저항을 증가시킬 가능성이 있으나, 인체의 섬유주세포에서 anti-VEGF가 섬유주세포의 MMP 활성에 미치는 영향은 아직 알려지지 않았다. 이에 따라 시행한 본 연구의 결과에서 BV는 MMP-1/-2의 활성을 각각 억제하였다. 따라서 anti-VEGF의 농도가 증가할수록 MMP 단백의 활성을 저하시켜 세포외기질의 축척을 유발하여 방수유출에 대한 섬유주의 저항을 증가시킬 수 있을 것이다[29,30].
VEGF가 투과도를 증가시키는 기전의 하나로 NO가 관여하는 것으로 알려져 있다[5-9,31]. NO는 섬유주를 이완시켜 방수유출을 증가시키는 작용을 나타내므로[32-34] anti-VEGF가 NO의 생성을 저하시킨다면 방수유출을 저하시킬 수 있을 것이다. MMP는 조직과 병적 상태에 따라 매우 다양한 작용을 나타내는데[35] NO와 MMP의 발현에 관한 상호작용에 대해서는 세포의 종류에 따라 다양한 결과가 보고되어 있으며 NO는 MMP-1의 발현을 촉진하기도 하고 MMP-2의 발현을 억제하기도 한다[36-38]. 이를 규명하기 위하여 BV을 이용하여 NO의 생성에 미치는 영향을 조사한 결과, 섬유주에서는 anti-VEGF가 NO의 생성을 억제하는 것으로 나타났으며[27] 이와 동반하여 MMP의 발현이 저하되었다. 이러한 결과로 보아 섬유주세포에서는 NO가 MMP의 발현을 저해할 가능성도 있을 것으로 생각된다. 본 연구에서는 MMP-1/-2의 발현에 미치는 영향을 조사하였는데 섬유주에서는 다양한 MMP와 그 저해제가 발현되므로[30,39] 여러 종류의 MMP에 미치는 영향과 NO와 MMP의 상호작용에 대해서는 향후 보다 자세한 연구를 요한다.
조직에서 용액의 투과경로는 세포경유경로와 세포주변 경로를 통해 투과되는데[40], 본 연구에서 BV는 세포주변경로를 통한 투과성을 나타내는 섬유주단층세포층의 carboxyfluorrescein 투과도를 감소시켰으나 섬유주단층세포층의 저항도에는 유의한 영향을 미치지 않았다. 그러나 섬유주에서는 세포주변경로를 통한 방수의 유출은 미미하며 주로 세포경유경로인 거대수포를 통해서 방수가 유출되므로[41-43] BV가 세포주변경로를 통한 유출을 시킨다는 본 연구의 실험실 내 결과는 실제 생체 내 섬유주 조직과의 조건은 다를 수 있다. 또한 두 경로는 서로 밀접하게 연관되어 조절될 뿐만 아니라[10,44] anti-VEGF가 세포경유경로를 통한 투과도를 증가시킨다는 보고도 있으므로[45], anti-VEGF가 세포경유경로에 미치는 영향을 완전히 배제할 수는 없을 것이며 이에 관해서는 향후 보다 자세한 연구를 요한다. 또한 본 실험에서는 임상적으로 사용 중인 BV를 희석하여 사용하였으므로 BV에 함유되어 있는 다양한 첨가물의 영향도 고려할 필요가 있을 것이다. 또한 anti-VEGF를 인체의 유리체내에 주사하는 경우 다양한 기전에 의해 안압이 상승할 수 있는 점도 고려해야 할 것이다[46]. 결론적으로 anti-VEGF는 섬유주세포의 투과도를 감소시켰으며, NO의 생성 저하와 함께 MMP의 분비를 감소시킴을 알 수 있었다.
Figure 1.
Effect of bevacizumab on the survival of cultured trabecular meshwork cells. Exposure to 0.25 mg/mL or 0.50 mg/mL bevacizumab did not affect cell survival significantly.
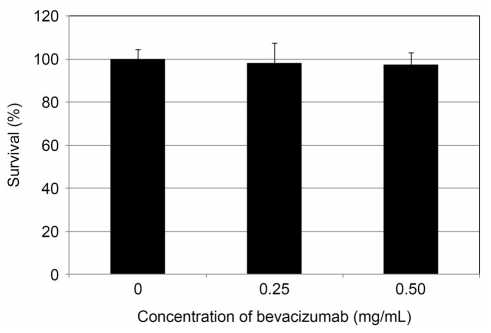
Figure 2.
Effect of bevacizumab on the permeability through trabecular monolayer. Exposure to 0.50 mg/mL bevacizumab decreased the permeability of carboxyfluorescein significantly compared to non-exposed control. Carboxyfluorescein intensity of outer chamber normalized to the mean value obtained using non-exposed control (permeability 100%). *p = 0.017.

Figure 3.
Effect of bevacizumab on the trans-endothelial electrical resistance (TEER) through trabecular monolayer. Exposure to 0.25 mg/mL or 0.50 mg/mL bevacizumab did not increase the TEER significantly compared to non-exposed control (p > 0.05).
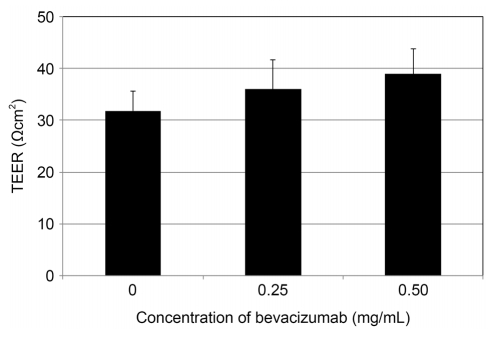
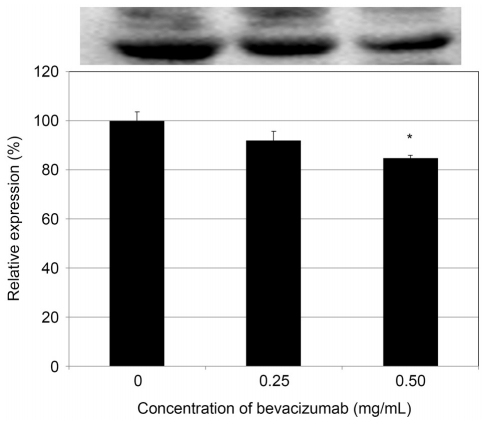
Figure 4.
Effect of bevacizumab on the activity of matrix metalloproteinase (MMP)-1 protein. Exposure to 0.50 mg/mL bevacizumab decreased MMP-1 activity significantly compared to non-exposed control. *p = 0.014.
REFERENCES
1) Ferrara N, Davis-Smyth T. The biology of vascular endothelial growth factor. Endocr Rev 1997;18:4-25.


2) Bakri SJ, McCannel CA, Edwards AO, Moshfeghi DM. Persisent ocular hypertension following intravitreal ranibizumab. Graefes Arch Clin Exp Ophthalmol 2008;246:955-8.


3) Kahook MY, Kimura AE, Wong LJ, et al. Sustained elevation in intraocular pressure associated with intravitreal bevacizumab injections. Ophthalmic Surg Lasers Imaging 2009;40:293-5.


4) Good TJ, Kimura AE, Mandava N, Kahook MY. Sustained elevation of intraocular pressure after intravitreal injections of anti- VEGF agents. Br J Ophthalmol 2011;95:1111-4.


5) Mayhan WG. VEGF increases permeability of the blood-brain barrier via a nitric oxide synthase/cGMP-dependent pathway. Am J Physiol 1999;276:C1148-53.


6) Breslin JW, Pappas PJ, Cerveira JJ, et al. VEGF increases endothelial permeability by separate signaling pathways involving ERK-1/2 and nitric oxide. Am J Physiol Heart Circ Physiol 2003;284:H92-100.


7) Bouloumié A, Schini-Kerth VB, Busse R. Vascular endothelial growth factor up-regulates nitric oxide synthase expression in endothelial cells. Cardiovasc Res 1999;41:773-80.


8) Dulak J, Józkowicz A, Dembinska-Kiec A, et al. Nitric oxide induces the synthesis of vascular endothelial growth factor by rat vascular smooth muscle cells. Arterioscler Thromb Vasc Biol 2000;20:659-66.


9) Tilton RG, Chang KC, LeJeune WS, et al. Role for nitric oxide in the hyperpermeability and hemodynamic changes induced by intravenous VEGF. Invest Ophthalmol Vis Sci 1999;40:689-96.

10) Lakshminarayanan S, Antonetti DA, Gardner TW, Tarbell JM. Effect of VEGF on retinal microvascular endothelial hydraulic conductivity: the role of NO. Invest Ophthalmol Vis Sci 2000;41:4256-61.

11) Alvarado J, Murphy C, Juster R. Trabecular meshwork cellularity in primary open-angle glaucoma and nonglaucomatous normals. Ophthalmology 1984;91:564-79.


12) Rohen JW, LÜtjen-Drecoll E, FlÜgel C, et al. Ultrastructure of the trabecular meshwork in untreated cases of primary open-angle glaucoma (POAG). Exp Eye Res 1993;56:683-92.

13) Keller KE, Aga M, Bradley JM, et al. Extracellular matrix turnover and outflow resistance. Exp Eye Res 2009;88:676-82.


14) Vranka JA, Kelley MJ, Acott TS, Keller KE. Extracellular matrix in the trabecular meshwork: intraocular pressure regulation and dysregulation in glaucoma. Exp Eye Res 2015;133:112-25.



15) Unemori EN, Ferrara N, Bauer EA, Amento EP. Vascular endothelial growth factor induces interstitial collagenase expression in human endothelial cells. J Cell Physiol 1992;153:557-62.


16) Lamoreaux WJ, Fitzgerald ME, Reiner A, et al. Vascular endothelial growth factor increases release of gelatinase A and decreases release of tissue inhibitor of metalloproteinases by microvascular endothelial cells in vitro. Microvasc Res 1998;55:29-42.


17) Wang H, Keiser JA. Vascular endothelial growth factor upregulates the expression of matrix metalloproteinases in vascular smooth muscle cells: role of flt-1. Circ Res 1998;83:832-40.

18) Stamer WD, Clark AF. The many faces of the trabecular meshwork cell. Exp Eye Res 2017;158:112-23.


19) Grimes PA, Stone RA, Laties AM, Li W. Carboxyfluorescein. A probe of the blood-ocular barriers with lower membrane permeability than fluorescein. Arch Ophthalmol 1982;100:635-9.


20) Araie M. Carboxyfluorescein. A dye for evaluating the corneal endothelial barrier function in vivo. Exp Eye Res 1986;42:141-50.


21) Lei Y, Stamer WD, Wu J, Sun X. Oxidative stress impact on barrier function of porcine angular aqueous plexus cell monolayers. Invest Ophthalmol Vis Sci 2013;54:4827-35.



22) Srinivasan B, Kolli AR, Esch MB, et al. TEER measurement techniques for in vitro barrier model systems. J Lab Autom 2015;20:107-26.



23) Wilhelm I, Fazakas C, Krizbai IA. In vitro models of the blood-brain barrier. Acta Neurobiol Exp (Wars) 2011;71:113-28.



24) Green LC, Wagner DA, Glogowski J, et al. Analysis of nitrate, nitrite, and [15N]nitrate in biological fluids. Anal Biochem 1982;126:131-8.


25) Kahook MY, Ammar DA. In vitro effects of antivascular endothelial growth factors on cultured human trabecular meshwork cells. J Glaucoma 2010;19:437-41.


26) Spitzer MS, Yoeruek E, Sierra A, et al. Comparative antiproliferative and cytotoxic profile of bevacizumab (Avastin), pegaptanib (Macugen) and ranibizumab (Lucentis) on different ocular cells. Graefes Arch Clin Exp Ophthalmol 2007;245:1837-42.


27) Kim SH, Kim JW. Effect of bevacizumab on survival and production of nitric oxide in trabecular meshwork cells. J Korean Ophthalmol Sci 2009;50:1404-8.

28) Kernt M, Welge-Lüssen U, Yu A, et al. Bevacizumab is not toxic to human anterior- and posterior-segment cultured cells. Ophthalmologe 2007;104:965-71.



29) Bradley JM, Vranka J, Colvis CM, et al. Effect of matrix metalloproteinases activity on outflow in perfused human organ culture. Invest Ophthalmol Vis Sci 1998;39:2649-58.

30) Pang IH, Hellberg PE, Fleenor DL, et al. Expression of matrix metalloproteinases and their inhibitors in human trabecular meshwork cells. Invest Ophthalmol Vis Sci 2003;44:3485-93.


31) Hood JD, Meininger CJ, Ziche M, Granger HJ. VEGF upregulates ecNOS message, protein, and NO production in human endothelial cells. Am J Physiol 1998;274:H1054-8.


32) Wiederholt M, Sturm A, Lepple-Wienhues A. Relaxation of trabecular meshwork and ciliary muscle by release of nitric oxide. Invest Ophthalmol Vis Sci 1994;35:2515-20.

33) Behar-Cohen FF, Goureau O, D’Hermies F, Courtois Y. Decreased intraocular pressure induced by nitric oxide donors is correlated to nitrite production in the rabbit eye. Invest Ophthalmol Vis Sci 1996;37:1711-5.

34) Nathanson JA, McKee M. Alterations of ocular nitric oxide synthase in human glaucoma. Invest Ophthalmol Vis Sci 1995;36:1774-84.

35) Löffek S, Schilling O, Franzke CW. Series "matrix metalloproteinases in lung health and disease": biological role of matrix metalloproteinases: a critical balance. Eur Respir J 2011;38:191-208.

36) Yoshida M, Sagawa N, Itoh H, et al. Nitric oxide increases matrix metalloproteinase-1 production in human uterine cervical fibroblast cells. Mol Hum Reprod 2001;7:979-85.


37) Chen HH, Wang DL. Nitric oxide inhibits matrix metalloproteinase-2 expression via the induction of activating transcription factor 3 in endothelial cells. Mol Pharmacol 2004;65:1130-40.


38) Gurjar MV, Sharma RV, Bhalla RC. eNOS gene transfer inhibits smooth muscle cell migration and MMP-2 and MMP-9 activity. Arterioscler Thromb Vasc Biol 1999;19:2871-7.


39) Alexander JP, Samples JR, Van Buskirk EM, Acott TS. Expression of matrix metalloproteinases and inhibitor by human trabecular meshwork. Invest Ophthalmol Vis Sci 1991;32:172-80.

40) Komarova Y, Malik AB. Regulation of endothelial permeability via paracellular and transcellular transport pathways. Annu Rev Physiol 2010;72:463-93.


42) Tripathi RC. Mechanism of the aqueous outflow across the trabecular wall of Schlemm's canal. Exp Eye Res 1971;11:116-21.


43) Tarkkanen A, Niemi M. Enzyme histochemistry of the angle of the anterior chamber of the human eye. Acta Ophthalmol (Copenh) 1967;45:93-9.


44) Salama NN, Eddington ND, Fasano A. Tight junction modulation and its relationship to drug delivery. Adv Drug Deliv Rev 2006;58:15-28.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 2,501 View
- 61 Download
- Related articles
-
Effect of Latanoprostene Bunod on the Permeability of Trabecular Meshwork Cells2024 February;65(2)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



