 |
 |
| J Korean Ophthalmol Soc > Volume 62(6); 2021 > Article |
|
ê”돞ìŽëĄ
ëȘ©ì
ê±°ì§ëčëë
čëŽì„ìì ìŽì ì ìíë ë°±ëŽì„ìì ìŽ ìŹì ìŁŒì ì ì ì ìíì 믞ìčë ìí„ì ììëłŽêł ì íìë€.
ëìêłŒ ë°©ëČ
ê±°ì§ëčëë
čëŽì„ìì ìŹì ìŁŒì ì ì ì ìí ë°ì ìì ìČŽì 51ìêłŒ ìžêł”ìì ìČŽì 40ìì ëí ìì ì±ì ì íí„ì ìŒëĄ ìĄ°ìŹíìë€. ìì ì±êł”ì ììíê°ë„ â„ 20%ìŽë©Žì ìì í ìì < 18 mmHgìž êČœì°ëĄ ì ìíìêł , ììíê°ì ìŹì© ììŽ ëŹì±í êČœì°ë„Œ ìì ì±êł”ìŽëŒ íìë€. Kaplan-Meier ììĄŽë¶ììŒëĄ ëì ì±êł”ë„ ì ëčê”íìë€. ìì ì€íšì ìí ììžì Cox ëčëĄìíëȘšíì ìŽì©íìŹ ë¶ìíìë€.
êČ°êłŒ
ì ìČŽ íê· êŽì°° êž°ê°ì 44.7 ± 28.0ê°ììŽìë€. ë§ì§ë§ êČœêłŒ êŽì°° ì ì”ìą
ììì ìì ìČŽììì 4.5 mmHg, ìžêł”ìì ìČŽììì 11.1 mmHg ê°ìíìë€(p=0.005). ìì ì±êł”ë„ ì ìì ìČŽìëłŽë€ ìžêł”ìì ìČŽììì ë ëììŒë(1ë
: 78.4 vs. 85.0%; 5ë
: 15.0 vs. 31.5%) í”êłì ì ìì±ì ììë€(p=0.068). ìŹì ìŁŒì ì ì ì€íšì ìí ììžì ìì í ìŽêž° ì ìì(hazard ratio=2.81, p=0.016)êłŒ ìì ì ìì ìČŽì ìíìë€(hazard ratio=1.97, p=0.040).
êČ°ëĄ
ê±°ì§ëčëë
čëŽì„ìì ìŹì ìŁŒì ì ì í ì„êž° ëì ì±êł”ë„ ì ìì ìČŽìêłŒ ìžêł”ìì ìČŽì ìŹìŽì ì ìí ì°šìŽë ìììŒë, ìì ìČŽì ìíë ìì ì€íšì ìí ììžìŽìë€. ë°ëŒì ëłž ì°ê”Źë ë°±ëŽì„ìŽ ëë°ë ê±°ì§ëčëë
čëŽì„ íììì ìŹì ìŁŒì ì ì ìŽ íìí êČœì° ë°±ëŽì„ìì ì 뚌ì ìííêł ìŹì ìŁŒì ì ì ì ëì€ì ìííë êČìŽ ë ëì ì íìŽ ë ì ììì 볎ìŹì€ë€.
ABSTRACT
Purpose
To determine whether previous cataract surgery affected the surgical prognosis of primary trabeculectomy with mitomycin- C (MMC) to treat exfoliative glaucoma (XFG).
Methods
This retrospective, consecutive study included 51 phakic eyes and 40 pseudophakic eyes of XFG patients that had previously undergone phacoemulsification via a temporal, clear corneal incision. All patients underwent primary trabeculectomy with MMC. Complete success was defined by an intraocular pressure (IOP) <18 mmHg and an IOP reduction â„ 20% without any glaucoma medication. The cumulative probabilities of success were compared using Kaplan-Meier survival analysis, and risk factors for surgical failure were analyzed using the Coxâs proportional hazards model.
Results
The mean follow-up period was 44.7 ± 28.0 months. The IOP had decreased by 4.5 mmHg in phakic eyes and 11.1 mmHg in pseudophakic eyes at the last visits after surgery (p = 0.005). The cumulative complete success rates were 78.4% at 1 year and 15.0% at 5 years for phakic eyes, and 85.0% and 31.5% for pseudophakic eyes. The complete success rates thus tended to be lower for phakic than pseudophakic eyes (p = 0.068). The risk factors associated with surgical failure were early postoperative hypotony (hazard ratio = 2.81, p = 0.016, complete success) and phakic status (hazard ratio = 1.97, p = 0.040, complete success).
Conclusions
The long-term outcomes of XFG patients whose pseudophakic eyes had undergone phacoemulsification prior to primary trabeculectomy with MMC were comparable to or better than those of patients with phakic eyes. Therefore, performing phacoemulsification first, followed by trabeculectomy, may be the better option if trabeculectomy is required by XFG patients with cataracts.
ê±°ì§ëčëìŠíê”°ì ëčì ìì íë „ëŻžìžììŹì ìŽìì ìí ìžíŹìž ëčëëŹŒì§ì ìčšì°©ìŽ ìì ìČŽ, íì±, ìŹì ìŁŒë„Œ íŹíší ì ìë¶ ìŹëŹ ë¶ììì êŽì°°ëë ì°ë č êŽë š ì§íìŽë€[1]. ê±°ì§ëčëìŠíê”°ì ìŹëŹ ìëŽ ìŽìì ëë°íëë°, íčí ë°±ëŽì„ì íì±ìŽë ê°ë°©ê° ëë íìê°ë
čëŽì„ì ìŽëí ìíìŽ ëë€êł ìë €ì ž ìë€[2].
ê±°ì§ëčëìŠíê”°ìì ë°ìí ë
čëŽì„(ê±°ì§ëčëë
čëŽì„)ì ìë°ê°ë°©ê°ë
čëŽì„ëłŽë€ ìììŽ ë ëêł , í룚 ëłëìŽ ìŹíë©°, ê°ìì€ëŹìŽ ììììčìŽ íí ìŒìŽëë€[3]. ëí, ìë°ê°ë°©ê°ë
čëŽì„ì ëčíŽ ë
čëŽì„ì± ìì êČœììì ì§íìŽ ëč ë„Žë©°[4], ììíê°ì ì ì ë°ìíë êž°ê°ìŽ ì§§êł êČ°ê” ìì ìĄ°ì ì ì€íšíë êČœì°ê° ë§ë€[5].
ê±°ì§ëčëë
čëŽì„ìì ìœëŹŒìčëŁë ë ìŽì ìčëŁëĄ ìì ìĄ°ì ì ì€íšíìì êČœì° ìŹì ìŁŒì ì ì ì ìíí ì ìë€[6]. ê°ë°©ê°ë
čëŽì„ íìë„Œ ëììŒëĄ ìŹì ìŁŒì ì ì ì ìíí ì°ê”Źìì, ìì ìČŽìëłŽë€ ìžêł”ìì ìČŽìì ìì ì€íšìšìŽ ëë€êł ìë €ì ž ìë€[7,8]. ëì ì€íšìšì ìŁŒì ììžì ììžĄ ê°êł”ë§ì ê° íì ìꞎ êČ°ë§íí°ì êŽë š ììŒë[9], ì”ê·Œìë íŹëȘ
ê°ë§ì ê°ëČìŒëĄ êČ°ë§ ì ê° ììŽ ìì ìČŽì íì ì ìííìŹ êČ°ë§ìŒìŠë°ìêłŒ êČ°ë§íí°ë„Œ ì”ìííìŹ ìì í ìŹêłŒíŹ ìì€ì ì€ìŽêł [10], 5-í룚ì€ëĄì°ëŒì€ìŽë ë§ìŽí ë§ìŽì C ê°ì íëìŹì ë„Œ ëłŽìĄ°ì ìŒëĄ ìŹì©íìŹ ìŹì ìŁŒì ì ì ì ì±êł”ë„ ì ëìŒ ì ìë€[11,12]. ë°ë©Žì, ìì ìČŽììì ì±êł”ì ìž ìŹì ìŁŒì ì ì ì ìíí íì ë°±ëŽì„ìŽ ìëĄ ë°ìíê±°ë êž°ìĄŽì ë°±ëŽì„ìŽ ì§ííìŹ ë°±ëŽì„ìì ìŽ íìí êČœì°ê° 8-47%ëĄ ìë €ì ž ììŒë©°[13-15], ìŹì ìŁŒì ì ì ì ë°ì ëì ë°±ëŽì„ìì ì ìíí êČœì° ìì ìĄ°ì ì ë¶ì ì ìž ìí„ì ëŒìčë€ë ëłŽêł ê° ìë€[16].
êł ë čìì ìŁŒëĄ ë°ìíë ê±°ì§ëčëë
čëŽì„ì íčì±ì ë°±ëŽì„ìŽ ëë°ëìŽ ìë êČœì°ê° ë§ìë° ê±°ì§ëčëë
čëŽì„ íììì ë°±ëŽì„ìì ììČŽê° ììíê° íšêłŒê° ìë€êł ìë €ì ž ìë€[17]. íì§ë§ ì ìê° ìĄ°ìŹí ë° ë°±ëŽì„ì ëë°í ê±°ì§ëčëë
čëŽì„ìì ì±êł”ì ìž ì„êž° ìì ìĄ°ì ì ìíŽ ìì ì ìčëŁê° íìí êČœì°, ìŽë€ ìì ì 뚌ì ìííë êČìŽ ìąì ì§ì ëí ì°ê”Źë íìŹêčì§ ììë€. ë°ëŒì ì ìë€ì ìŹì ìŁŒì ì ì ì ìí ë°ì ë€ìì ê±°ì§ëčëë
čëŽì„ íìë„Œ ëììŒëĄ ìŽì ì ìíë ë°±ëŽì„ìì ìŽ ìŹì ìŁŒì ì ì ì ìíì 믞ìčë ìí„êłŒ ìŹì ìŁŒì ì ì ì€íšì ìíìžìì ëíŽ ìĄ°ìŹíêł , ë°±ëŽì„ìŽ ëë°ë ê±°ì§ëčëë
čëŽì„ìì ë°±ëŽì„ìì êłŒ ë
čëŽì„ìì ì ìí ììì ëí ì íì ëìì ìŁŒêł ì íìë€.
2007ë
3ìë¶í° 2017ë
2ìêčì§ ìëšëíê”ëłì ìêłŒìì ê±°ì§ëčëë
čëŽì„ìŒëĄ ìŹì ìŁŒì ì ì ì ìí ë°êł 12ê°ì ìŽì ì¶ì êŽì°°ìŽ ê°ë„íìë 81ëȘ
91ìì ëììŒëĄ íìë€. ëłž ì°ê”Źë ëłžìì ììì°ê”ŹìŹìììí(Institutional Review Board, IRB)ì ìčìžì ë°ììŒë©°(ìčìž ëČíž: 2018-11-023) íŹì±í€ì ìžì ì€ìíìë€. ìŽì ì ë
čëŽì„ìì ì ìí ë°ìê±°ë ë°±ëŽì„ìì ì ëìì ìíí êČœì°ë ëììì ì ìžíìë€. ëì íìì ì°ë čêłŒ ì±ëł, ì ì ì§í ëë° ìŹë¶ë„Œ ìĄ°ìŹíììŒë©°, ì€ìŹê°ë§ëê»ì ìì¶ì„, ìì ì ììŒêČìŹ êČ°êłŒ, ìì ì ë°±ëŽì„ìì ì 돎, ìì ì í ìì ë° ììíê°ì ì ê°ì, ì”ëê”ì ìë „, ìì í í©ëłìŠ ë±ì ìëŹŽêž°ëĄì í”íìŹ íí„ì ìŒëĄ ìĄ°ìŹíìë€.
ê±°ì§ëčëìŠíê”°ì ì§ëšì ìžê·čë±í믞êČœêČìŹìì ëêł”ê°ì„ì늏ì ì íì ìž ëčëëŹŒì§ì ìčšì°©ì êŽì°°í ì ìê±°ë, ì°ë í ìì ìČŽì ëì íčì§ì ëčëëŹŒì§ì ìčšì°©ìŽ êŽì°°ëë êČœì°ëĄ íìë€. ê±°ì§ëčëë
čëŽì„ íììì ììíê°ì ì ìčëŁì ë°ììŽ ìë êČœì°ì ììíê°ì ì ìčëŁìë ë¶ê”Źíêł ìì êČœììì ì§íìŽ êŽì°°ëë êČœì°, í„í ìì êČœììì ì§íìŽ ììëë êČœì°ì ìì ì ìčëŁë„Œ ìííìë€. ëȘšë ìì ì í ëȘ
ì ì ì(S.C.C.)ì ìíŽ ê”Źíë§ì·š íì ìíëìë€. íìì êČ°ë§ ìíì ë°ëŒ ììŽìžĄìŽë ìëčìžĄì ì€ë¶êž°ì (limbus-based)ëĄ íìŹ í
ë
ŒëêłŒ ìêł”ë§ ìŹìŽë„Œ ì ê°íìŹ êČ°ë§ížì ë§ë€ìë€. êČ°ë§ížì ë§ë í ìœ 3.0 Ă 3.0 Ă 2.5 mm íŹêž°ì ìŹë€ëŠŹêŒŽ êł”ë§ížì êł”ë§ëê»ì 1/3-1/2 êčìŽëĄ ë§ë€ìë€. ì ìì íëšì ë°ëŒ 0.02% ëë 0.04% ëëì ë§ìŽí ë§ìŽì Cë„Œ ì ì ìì ì© ì€íì§ë„Œ êł”ë§íž ìë, ìêł”ë§êłŒ êČ°ë§í ìŹìŽì 2-4ë¶ê° ë
žì¶ìíš í ííìŒìĄìŒëĄ 충ë¶í ìžìČíìë€. ê°ë§ì€ë¶êČœêłë„Œ ë°ëŒì ìčŒëĄ ì ê°ë©Žì ë§ë ë€ì Kelly Descemet íìčë„Œ ìŹì©íìŹ ëŽìžĄ êł”ë§ ì ì ë„Œ ìíí í ìŁŒëłíì±ì ì ì ì ì€ìíìë€. 10-0 nylonì ìŽì©íìŹ êł”ë§íž ëȘšì늏ì ëšìëŽí©ì íìêł , íìì ë°ëŒ 9-0 nylonì ìŽì©íìŹ êł”ë§íž ëì¶ ì ëì ë°ëŒ ê°ëŽëŽí©ì ë¶ê°ì ìŒëĄ ìííìë€. êČ°ë§ížì 10-0 nylonì ìŽì©íìŹ í
ë
Œë ëŽí© í êČ°ë§ì ì°ì ëŽí©íìë€. ìì í ëȘšë íìë 0.5% levofloxacin, 1% prednisolone acetate ì ììĄ, 1% atropine ì ììĄì ìŹì©íììŒë©°, ììêČœêłŒì ë°ëŒ ê°ëíìë€. êČœêłŒ êŽì°° êž°ê° ëìì ë€ì ììììčìŽ ìê±°ë ìŹêłŒíŹíì±ìŽ ì ëì§ ììŒë©Ž ìíì ë°ëŒ ìì§ ìë°, ìë„Žêł€ë ìŽì ëŽí©ìŹì©íŽì ëë ê°ëŽëŽí©ìŹ ì ê±°ì ì ìííìë€.
ìì ì í ìë „ì êČœêłŒ êŽì°° ëì íìČìì 5 mì© ìë „íë„Œ ìŽì©íìŹ ì”ëê”ì ìë „ì ìžĄì íììŒë©°, ë¶ìì ìíŽ logarithm of the minimum angle of resolution (LogMAR) ìë „ìŒëĄ ëłííìë€. ììì êłšëë§ìíììêłëĄ ìžĄì íìêł , ìì ì ììì ìì ì ì”ìą
ìžë 방돞ìŒêłŒ ì
ì í ìì ì§ì ì ìžĄì í ììì íê· ìčëĄ íììŒë©° ìì í êČœêłŒ êŽì°° êž°ê° ëì ììì ìžĄì íìë€. ìŽìí ê°ë§ëê»ìžĄì êł(SP-3000; Tomey Co., Nagoya, Japan)ë„Œ ìŽì©íìŹ ì€ìŹê°ë§ëê»ë„Œ ìžĄì íìêł , ì ìŽì ìŽìí A-scan (UltraScan Imaging System, Alcon Laboratories Inc., Fort Worth, TX, USA)ì ìŹì©íìŹ ìì¶ì„ì ìžĄì íìë€. ìŹì ìŁŒì ì ì í êČœêłŒ êŽì°° ì€ ë°±ëŽì„ìŒëĄ ìží ì ìí ìë „ê°ìê° ìì ë ë°±ëŽì„ìì ì ìííììŒë©°, ëȘšë ë°±ëŽì„ìì ì ëìŒí ì ìì ìíŽ ìŽìžĄ íŹëȘ
ê°ë§ì ê°ë„Œ í”íŽ ìì ìČŽì íì ë° íë°©ìžêł”ìì ìČŽ ìœì
ì ëĄ ìíëìë€.
ìì ì±êł”ì ìì í ìì < 18 mmHgìŽë©° ììíê°ë„ â„ 20%ìž êČœì°ëĄ ì ìíìêł ììíê°ì ìŹì© ì 돎ì ë°ëŒ ìì ì±êł”êłŒ ë¶ë¶ ì±êł”ìŒëĄ ëëìë€. êČœêłŒ êŽì°° êž°ê° ì€ ì¶ê°ì ìž ë
čëŽì„ìì ì ìíë°ê±°ë ì”ëê”ì ìë „ìŽ êŽê° ëŹŽìž êČœì° ìì ì€íšëĄ ê°ìŁŒíìë€. ìì ì ë°±ëŽì„ìì ì ë°ì êž°ìë „ì ë°ëŒ ìì ìČŽìê”°(51ì)êłŒ ìžêł”ìì ìČŽìê”°(40ì)ìŒëĄ ëëìŽ ìê°êČœêłŒì ë°ë„ž ëì ì±êł”ë„ íê°ë„Œ ìíŽ Kaplan-Meier ììĄŽë¶ìì ìííììŒë©°, log rank testëĄ ë ê”°ì ìì ì±êł”ë„ ì ëčê”íìë€. ììžëŹ ìŹì ìŁŒì ì ì í ìíí ë°±ëŽì„ìì ì ìí„ì íê°íêž° ìíŽ ìì ìČŽìê”°ìì ìŹì ìŁŒì ì ì í êČœêłŒ êŽì°° ëì€ ë°±ëŽì„ìì ì ë°ìë ìì§ëš(29ì)êłŒ ë°ì§ ìì ìì§ëš(22ì)ìŒëĄ ìžë¶íìŹ ìì ì€íšì ìíìžìë„Œ ìŹìĄ°ìŹíìë€.
ìì ì€íšì ìí ììžì ìĄ°ìŹíêž° ìíŽ Cox ëčëĄìíëȘší(Cox proportional hazards model)ì ìŹì©íìë€. ëìŽ, ëčëš ë° êł íì ëë° ìŹë¶, ë°±ëŽì„ìì êž°ìë „, ìì ì ìì, ììíê°ì ê°ì, ìì í ìŽêž° ì ìì, ì ë°©ì¶í ì 돎, ìì ì ë°© ì 돎ì 9ê°ì§ ëłìë„Œ ê°ìì ìíìžìëĄ ê°ìŁŒíìë€. ìì í í©ëłìŠ ìĄ°ìŹìì ìì ì ë°©ì ê°ë§ëŽíŒê° ìŁŒëłë¶ íì±ì ì ìŽí ì ë ìŽììŒëĄ ì ë°©ìŽ ììì§ êČœì° ëë ì ë°© ìŹíì±ì ìíí êČœì°ëĄ, ì ë°©ì¶íì ì ë°©ì íìĄì ìž”ìŽ ì§ êČœì°ëĄ, ìì í ìŽêž° ì ììì ìì í 1ê°ì ëŽì 3ëČ ìŽìì ì°ìë ìì ìžĄì ìì 5 mmHg ìŽíëĄ ìžĄì ë êČœì°ëĄ ì ìíìë€. ìëŁì í”êłìČ늏ë SPSS í”êłíëĄê·žëš version 20.0 (PASW statistics 20.0 for windows, IBM Corp., Armonk, NY, USA)ì ìŽì©íìŹ chi-square testì independent t-testëĄ ë¶ìíìêł , í”êłíì ì ìì±ì pê°ìŽ 0.05 ìŽíìž êČìŒëĄ íì íìë€.
ê±°ì§ëčëë
čëŽì„ìŒëĄ ì§ëšë°êł ìŹì ìŁŒì ì ì ì ìíí 91ì ì€ ë°±ëŽì„ìì êž°ìë „ìŽ ìë ìì ìČŽìê”°ì 51ì(56.0%)ìŽììŒë©°, ìžêł”ìì ìČŽìê”°ì 40ì(44.0%)ìŽìë€. ìžêł”ìì ìČŽìê”° ëȘšë ìŽìžĄíŹëȘ
ê°ë§ì ê°ë„Œ í”í ìì ìČŽì íì ë° íë°©ìžêł”ìì ìČŽ ìœì
ì ì ìíë°ìë€. ìžêł”ìì ìČŽìê”°ìì ìŹì ìŁŒì ì ì ì êłŒê±° ë°±ëŽì„ìì í íê· 107.5 ± 70.1ê°ì(ëČì: 6-261ê°ì) íì ìíëìë€.
ìì ìČŽìê”°ì íê· ì°ë čì 64.3 ± 8.4ìžìêł ëšìê° 39ì(76.5%), ìŹìê° 12ì(23.5%)ìŽìë€. ìžêł”ìì ìČŽìê”°ì íê· ì°ë čì 71.6 ± 6.7ìžìêł , ëšìê° 32ì(80.0%), ìŹìê° 8ì(20.0%)ìŽìë€. íê· ì°ë čì ìžêł”ìì ìČŽìê”°ìì í”êłì ìŒëĄ ì ìíêČ ë§ììŒë ì±ëłì ë ê”° ê°ì í”êłì ìŒëĄ ì ìí ì°šìŽë„Œ 볎ìŽì§ ììë€(Table 1, p<0.001, p=0.687). ëë°ë ì ì ì§í ì€ ëčëšë ìì ìČŽìê”°ìì 5ì(9.8%), ìžêł”ìì ìČŽìê”°ìì 7ì(17.5%)ìŒëĄ ë ê”° ê° í”êłì ìŒëĄ ì ìí ì°šìŽë ììêł , êł íìì ê° ê”°ìì 15ì(29.4%)êłŒ 22ì(55.0%)ìŒëĄ ìžêł”ìì ìČŽìê”°ìì ë ë§ìë€(Table 1, p=0.281, p=0.014).
ìì ì ìíí ììŒêČìŹì mean deviationêłŒ pattern standard deviationì ìì ìČŽìê”°ìì ê°ê° -24.1 ± 8.2 dB, 7.0 ± 3.4 dBìŽìêł , ìžêł”ìì ìČŽìê”°ììë -21.9 ± 10.2 dB, 6.0 ± 3.4 dBëĄ ë ê”° ê°ì í”êłì ìŒëĄ ì ìí ì°šìŽë ììë€(Table 1, p=0.280, p=0.179). ìì ì ì”ëê”ì ìë „(LogMAR)ì ìì ìČŽìê”°ìì 0.533 ± 0.633, ìžêł”ìì ìČŽìê”°ìì 0.529 ± 0.630ìŒëĄ ë ê”° ê°ì ì ìí ì°šìŽë ìììŒë©°, ì€ìŹê°ë§ëê» ë° ìì¶ì„ë ë ê”° ê°ì ì ìí ì°šìŽë ììë€(Table 1, p=0.975, p=0.793, p=0.841). ìì ì íê· ììì ìì ìČŽìê”°ìì 22.8 ± 7.5 mmHg, ìžêł”ìì ìČŽìê”°ìì 25.3 ± 7.1 mmHgëĄ ìžêł”ìì ìČŽìê”°ìì ë ëìì§ë§ í”êłì ìŒëĄ ì ìí ì°šìŽë ìììŒë©°, ìì ì ìŹì©í íê· ììíê°ì ê°ìë ë ê”° ê°ì ì ìí ì°šìŽë ììë€(Table 1, p=0.121, p=0.714).
ìì í íê· êČœêłŒ êŽì°° êž°ê°ì 44.7 ± 28.0ê°ììŽìë€. ìì ìČŽìê”°ì íê· êČœêłŒ êŽì°° êž°ê°ì 50.1 ± 31.7ê°ììŽììŒë©°, ìžêł”ìì ìČŽìê”°ì íê· êČœêłŒ êŽì°° êž°ê°ì 37.9 ± 21.0ê°ìëĄ ìì ìČŽìê”°ì íê· êČœêłŒ êŽì°° êž°ê°ìŽ ë êžžìë€(Table 2, p=0.030). ìì ìČŽìê”°ììë 29ì(56.9%)ìŽ ë°±ëŽì„ìŒëĄ ìžíŽ ì ìí ìë „ì íë„Œ 볎ììŒë©°, êČœêłŒ êŽì°° êž°ê° ëì ë°±ëŽì„ìì ì ìííìë€. ìŹì ìŁŒì ì ì í ë°±ëŽì„ìì ìíêčì§ íê· 22.2 ± 21.7ê°ì(ëČì: 6-48ê°ì)ìŽ ê±žë žë€. ìŹì ìŁŒì ì ì í ë§ì§ë§ 방돞ì ìžĄì í ììì ìì ìČŽìê”°ìì 18.4 ± 8.9 mmHgìŽììŒë©°, ìžêł”ìì ìČŽìê”°ìì 14.1 ± 8.4 mmHgëĄ ìì ìČŽìê”°ìì ë ëììŒë©°(Table 2, p=0.024), ììíê° ì ë ëí ìžêł”ìì ìČŽìê”°ìì ë ë§ìŽ ê°ìíìë€(4.5 vs. 11.1 mmHg, p=0.005). ìŹì©í íê· ììíê°ì ê°ìë 1.9 ± 1.7ê°, 1.1 ± 1.6ê°ëĄ ìì ìČŽìê”°ìì ë ë§ìë€(Table 2, p=0.018).
ìì í ììíê° ì ëì ë°ëŒ Kaplan-Meier ììĄŽë¶ìì ìŽì©íŽ ëì ì±êł”ë„ ì ëčê” ë¶ìíìì ë ìì ì±êł”ë„ ì ìì ìČŽìê”°ìì 1ë
짞 78.4%, 5ë
짞 15.0%ìêł , ìžêł”ìì ìČŽìê”°ìì ê°ê° 85.0%, 31.5%ìë€. ìì ì±êł”ë„ ì ìì ìČŽìê”°ìì ëźì êČœí„ì 볎ìì§ë§ ë ê”° ê°ì í”êłì ìŒëĄ ì ìí ì°šìŽë ììë€(Fig. 1, p=0.068). ë¶ë¶ ì±êł”ë„ ì ìì ìČŽìê”°ìì 1ë
짞 96.1%, 5ë
짞 58.3%ìêł , ìžêł”ìì ìČŽìê”°ìì ê°ê° 100.0%, 63.8%ììŒë©°, ë ê”° ê°ì ì ìí ì°šìŽë ììë€(Fig. 2, p=0.553). ìì ìČŽìê”°ìì ìŹì ìŁŒì ì ì ìí í ë°±ëŽì„ìì ì ìíí ìì ì ì€ë ì ëšíìì ë 5ë
ëì ì±êł”ë„ ì ìì ì±êł”ë„ 32.9%, ë¶ë¶ ì±êł”ë„ 70.2%ëĄ ëììĄìŒë, ìžêł”ìì ìČŽìê”°êłŒ ëčê”íì ë í”êłì ìŒëĄ ì ìí ì°šìŽë 볎ìŽì§ ììë€(p=0.576, p=0.863, log-rank test).
Cox ëčëĄìííê·ëȘšíìì ìì í ìŽêž° ì ìì(HR=2.81, p=0.016, ìì ì±êł”)êłŒ ìì ìČŽì ìí(HR=1.97, p=0.040, ìì ì±êł”)ê° ìì ì€íšì ìí ìžìëĄ ëíëŹë€. ìì ìČŽìê”°ì ìŹì ìŁŒì ì ì í ë°±ëŽì„ìì ì ìíí ìì§ëš(29ì)êłŒ ìííì§ ìì ìì§ëš(22ì)ìŒëĄ ìžë¶íìŹ Cox ëčëĄìííê·ëȘšíì ìííìì ë, ë°±ëŽì„ìì ìì§ëšììë ìŽêž° ì ììêłŒ ìì ìČŽì ìíê° ìŹì í ì ìí ìíìžìëĄì ë ëë ·í ì ìì±ì 볎ììŒë, ë°±ëŽì„ìì ì ë°ì§ ìì ìì§ëšììë ì ìíì§ ììë€(Table 3). ë¶ë¶ ì±êł”ì êž°ì€ìŒëĄ íìì ëë ì ìí ìí„ì 믞ìčë ìí ìžìë ììë€(Table 4).
ìì í í©ëłìŠì ìì ìČŽìê”°ìì ìì í ìì ì ë°©ìŽ 8ì(15.7%)ìŒëĄ ê°ì„ ë§ìêł , ìžêł”ìì ìČŽìê”°ììë 맄ëœë§ë°ëŠŹê° 7ì(17.5%)ìŒëĄ ê°ì„ ë§ìë€. ìì í ìŽêž° ì ììì ìì ìČŽìê”°ìì 4ì(7.8%), ìžêł”ìì ìČŽìê”°ìì 6ì(15.0%)ìŒëĄ ë ê”° ê°ì í”êłì ìŒëĄ ì ìí ì°šìŽë„Œ 볎ìŽì§ ììë€(p=0.325). ìŽìžì ë€ë„ž í©ëłìŠììë ë ê”° ê°ì ì ìí ë°ì ëčëì ì°šìŽë„Œ 볎ìŽì§ ììë€(Table 5).
ê±°ì§ëčëìŠíê”°ì ìŽì°šê°ë°©ê°ë
čëŽì„ì ê°ì„ íí ììžìŽë©°, ì°ë č êŽë š ì§íìŒëĄ ë°±ëŽì„ìŽ íí ëë°ëë€[2]. ëłž ì°ê”Źë ê±°ì§ëčëë
čëŽì„ìì ìŽì ë°±ëŽì„ìì í ìžêł”ìì ìČŽì ìíê° ìŹì ìŁŒì ì ì ì ìíì 믞ìčë ìí„ì ìĄ°ìŹíêž° ìíŽ ê±°ì§ëčëë
čëŽì„ íìì ìŹì ìŁŒì ì ì ìí êČ°êłŒë„Œ ìì ìČŽìêłŒ ìžêł”ìì ìČŽììŒëĄ ëëìŽ ëčê” ë¶ìíìë€. ìŽëČ ì°ê”Źë„Œ í”íŽ ìì ìČŽìêłŒ ìŽêž° ì ìììŽ ìì ì€íšì ìíìžììì íìžíììŒë©° ìíìžìëĄì ìì ìČŽìì ì ìì±ì êČœêłŒ êŽì°° ëì€ ë°±ëŽì„ìì ì ë°ì íììì ë ëë ·íìë€. ìŹì ìŁŒì ì ì í 5ë
ì ëì ìì ì±êł”ë„ ì ìì ìČŽì(15.0%)ëłŽë€ ìžêł”ìì ìČŽì(31.5%)ìì ë ëì êČœí„ì 볎ìêł ìì ìČŽììì ë°±ëŽì„ìì ìí ìì ì ì€ë ì ëšíìì ëë ë ê”°ì ëì ì±êł”ë„ (32.9% vs. 31.5%)ìŽ ëčì·íìë€.
ë°±ëŽì„ìŽ ëë°ë ë
čëŽì„ìììë ì±êł”ì ìž ìŹì ìŁŒì ì ì ìí íìë ì¶ê°ì ìž ë°±ëŽì„ìì ìŽ íìíë©° ì¶í ìííë ë°±ëŽì„ìì í ìììĄ°ì ì ì€íšíë êČœì°ê° íí ë°ìíë€. ë
čëŽì„ìì ìí í ìììŽ ì±êł”ì ìŒëĄ ì ì§ëë íìë„Œ ëììŒëĄ í ì í„ì ì°ê”Ź[16]ìì íŹëȘ
ê°ë§ì ê°ë„Œ í”í ìì ìČŽì íì ì ìííìì ë ì ë°ì íìê° ìì í 1ë
짞 2 mmHg ìŽìì ììììčì 볎ìêł ìŹêłŒíŹì íí ëí ëëč ìĄë€êł ë°ííìë€. ìë°ê°ë°©ê°ë
čëŽì„ íìë§ì ëììŒëĄ í íí„ì ì°ê”Ź[18] ëí ìì ìČŽì íì ì ìí í ìê°ì ë°ëŒ ìŹêłŒíŹì íŹêž°ê° ì€ìŽë€êł ìŹì ìŁŒì ì ì ë§ ìíí êČœì°ëłŽë€ ì„êž° ì±êł”ë„ ìŽ ëšìŽì§ë€êł ëłŽêł íìë€. ìŽë ëŻ ìŹì ìŁŒì ì ì í ë°±ëŽì„ìì ìŽ êž°ìĄŽì ìŹêłŒíŹ êž°ë„ì ëšìŽëšëŠŹêł ììì ììčìíšë€êł ìë €ì ž ìëë°, ìŽë ìì í ìŽêž° ë°©ì ìì±ì ê°ì, ìì í ì ë°©ìì€ëĄ ìží ì ì°©ìŒëĄ ë°©ìì ì¶ëĄ íì, ìì ìČŽìì ëì€ë ëšë°±ì§ìŽë ìŒìŠ ë¶ì°ëŹŒ, ìŽì ë°ë„ž ìŹêłŒíŹì ìŹì íì ìì¶ ë±ìŽ ê·ž ììžìŒëĄ ì ìëêł ìë€[19-21].
ëłž ì°ê”Źì ëŹëŠŹ ìë°ê°ë°©ê°ë
čëŽì„ìì ìíë ìŹì ìŁŒì ì ì ì ìíë ìžêł”ìì ìČŽììì ìì ìČŽìëłŽë€ ë¶ì ì ìŽëŒë ì°ê”Źê° ëë¶ë¶ìŽë€. ìë°ê°ë°©ê°ë
čëŽì„ íìë„Œ ëììŒëĄ í íí„ì ì°ê”Ź[10]ë ììžĄêČ°ë§ì ê°ë„Œ í”íŽ ìì ìČŽì íì ì ìííë ìžêł”ìì ìČŽììŽ ìŹì ìŁŒì ì ì ì ì€íš ìí ììžìŽëŒêł ëłŽêł íìë€. ë€ ìŽì ì í„ì ì°ê”Ź[22]ìì ê°ë°©ê°ë
čëŽì„ì ìíë ìŹì ìŁŒì ì ì ì ëì ì±êł”ë„ ì ê°êł”ë§ì ê°ëĄ ìì ìČŽì íì ì ìíë°ì ìžêł”ìì ìČŽìê”°ìŽ ìì ìČŽìê”°ëłŽë€ ë ëźìë€êł ëłŽêł íìë€. ë ì°ê”Źì êł”í”ì ì ë°±ëŽì„ìì ìì ìíí êČ°ë§ì ê°ê° ìŹì ìŁŒì ì ì ì ë¶ì ì ìí„ì 믞ìčë€ë êČìŽë€. êČ°ë§ìêČ í ìžíŹíì ìĄ°ìŹë„Œ ì€ìí ì°ê”Ź[23]ìì ìŽì ì êČ°ë§ì ìčšëČí ìëŽ ìì ìŽ êČ°ë§ì ìŹì ììžíŹì ìŒìŠìžíŹë„Œ ìŠê°ìí€êł ìŹì ìŁŒì ì ì ì ì€íšìšì ëìžë€ë ëłŽêł ê° ìŽë„Œ ë·ë°ìčšíë€êł ìê°íë€. ë°ë©Žì ë€ë„ž ì°ê”Ź[24]ìì íŹëȘ
ê°ë§ì ê°ë„Œ í”íŽ ìì ìČŽì íì ì ìíë°ì íìë€ì ìŹì ìŁŒì ì ì ì ì„êž° ìì ì±ì ì ìì ìČŽìêłŒ ëčì·í êČ°êłŒë„Œ ëłŽìŹ ì”ê·Œ 볎ížì ìŒëĄ ìí ì€ìž ìì ìČŽì íì ì í„í ìŹì ìŁŒì ì ì ì ì±ì ì 믞ìčë ìí„ìŽ ì íì ìŒ êČìŒëĄ 볎ìžë€. ê±°ì§ëčëë
čëŽì„ íìë„Œ ëììŒëĄ í ëłž ì°ê”Źë ìŽì ì íŹëȘ
ê°ë§ì ê°ë„Œ í”íŽ ìì ìČŽì íì ì ìíë°ì ìžêł”ìì ìČŽìì ëí ìŹì ìŁŒì ì ì ì ì„êž° ëì ì±êł”ë„ ìŽ ìì ìČŽìì ëì ì±êł”ë„ ëłŽë€ ëìì§ ììì 볎ìŹìŁŒìë€.
ìŽ êČ°êłŒë ë°±ëŽì„ìŽ ëë°ë ê±°ì§ëčëë
čëŽì„ì ìì ì ìčëŁì ììë„Œ êČ°ì íšì ììŽì ì ì”í ì ëłŽê° ë ì ìë€êł ìê°íë€. ìŠ, ê±°ì§ëčëë
čëŽì„ìì íŹëȘ
ê°ë§ì ê°ë„Œ í”í ë°±ëŽì„ìì ìŽ í„í ìŹì ìŁŒì ì ì ì ì±ì ì 믞ìčë ëì ìí„ì ë°°ì í ì ìì êČìŒëĄ 볎ìžë€. ëí, ê±°ì§ëčëë
čëŽì„ìì ë°±ëŽì„ìì ì 뚌ì ì ííë êČìŽ íìì ìë „ê°ì êłŒ ììíê°ì êžì ì ìž ìí„ì ì€ë€ë ëłŽêł ê° ìë€. ê±°ì§ëčëë
čëŽì„ìì ë°±ëŽì„ìì ììČŽì ììíê° íšêłŒê° ìë°ê°ë°©ë
čëŽì„ëłŽë€ ë íŹêž° ë돞ì ë°±ëŽì„ìŽ ëë°ë ê±°ì§ëčëë
čëŽì„ìììë ì°ì ì ìŒëĄ ë°±ëŽì„ìì ìŽ ì íë ì ìë ê·Œê±°ê° ë ì ìë€[25]. ê±°ì§ëčëë
čëŽì„ íììêČ ë°±ëŽì„ìì ì ìííë©Ž ì ë°©ê°ìŽ ëìŽì§êł íì±ìì ìČŽë§ì°°ìŽ ê°ìíë©°, ìì ì€ ì ëì ì ë„Œ í”íŽ ëčëëŹŒì§ì ë¶ë¶ì ìŒëĄ ì ê±°í ì ììŒë©°, ìŹì ìŁŒì ì¶ì ë ììë„Œ íĄì
íšìŒëĄìš ìŹì ìŁŒì ë°©ìì ì¶ë„ ì ìŠê°ììŒ ììíê° íšêłŒë„Œ ì»ì ì ìë€[17]. ê±°ì§ëčëìŠíê”° íìë„Œ ëììŒëĄ í ìì ìČŽì íì ì ììíê° íšêłŒì ëí ì í„ì ì°ê”Źìì 2ë
í ììíê° ì ëë ëìĄ°ê”°ëłŽë€ ê±°ì§ëčëìŠíê”°ìì ë ì»žêł , ê±°ì§ëčëìŠíê”°êłŒ ë
čëŽì„ ëłí©ê”°ìì ììíê°ìŽ ë íì°íë€êł ëłŽêł ë í íì ì°ê”Źììë ê±°ì§ëčëìŠíê”°ììì ë°±ëŽì„ìì ì ëë ·í ììíê° íšêłŒê° íìžë ë° ìë€[25-27].
ëłž ì°ê”Źìì ìŹì ìŁŒì ì ì ì ë ë€ë„ž ì€íš ìíìžìë ìì í ìŽêž° ì ìììŽìë€. ìŒë°ì ìŒëĄ ìŽêž° ì ììì êł”ë§ì ê°ì ë°©ì íëŠì ì€ìŽêł ìŒìŠë§€ê°ëŹŒì ë°©ì¶íë©° íìĄë°©ìì„ëČœì ìììíšë€. êČ°êłŒì ìŒëĄ, ì§ìì ìž êČ°ë§ ìŒìŠì ìŽëíìŹ ìŹêłŒíŹì íí°ë„Œ ìŠê°ìíšë€êł ìë €ì ž ìë€[28]. ìŽëŹí ìŹêłŒíŹì íí°ë ì„êž°ì ìŒëĄ ìŹêłŒíŹ êž°ë„ì ì íìíŹ ì ìë€[19]. ë°ëŒì ê±°ì§ëčëë
čëŽì„ìì ìŹì ìŁŒì ì ì í ìŽêž° ì ìììŽ ìêž°ì§ ìëëĄ ìŁŒìíìŹìŒ íë€.
ëłž ì°ê”Źë íí„ì ì°ê”ŹëĄ íêłì ì ê°ì§ì§ë§ ì°ìì ì°ê”ŹëĄ ì í íží„ì ì”ìííìë€. ëí íê· ì°ë čì ìžêł”ìì ìČŽìê”°ìŽ ìì ìČŽìê”°ëłŽë€ ë ë§ìëë°, êł ë čìì ìŹì ìŁŒì ì ì íì ìŹì ììžíŹì ìŒìŠìžíŹì íì±íê° ì ìŽ ë ëì ìì êČ°êłŒë„Œ ê°ì žìì ì ìë€[29]. íì§ë§ ë ê”° ê°ì ëìŽ ì°šìŽë 7.3ìžëĄ ìëì ìŒëĄ ëìŽ ì°šê° ë§ì§ ìììŒë©°, Cox ëčëĄìíëȘšíìì ëìŽë ìì ì€íš ìíìžìê° ìëìë€. ìŽìžì ìŹì ìŁŒì ì ì í ìŹêłŒíŹì ííë„Œ ëčê”íì§ ëȘ»íë€ë ì íì ìŽ ìë€.
êČ°ëĄ ì ìŒëĄ ìŽì ì ìì ìČŽì íì ì ìíí ê±°ì§ëčëë
čëŽì„ìì ìŹì ìŁŒì ì ì í ì„êž° ëì ì±êł”ë„ ì ì”ìí ìì ìČŽìëłŽë€ ëźì§ ìììŒë©°, ê±°ì§ëčëë
čëŽì„ìì ìì ìČŽì ìíë ì„êž°ì ìŒëĄ ìŹì ìŁŒì ì ì ì ìí ììžìŒëĄ ìì©íìë€. ë°ëŒì ëłž ì°ê”Źì êČ°êłŒë ë°±ëŽì„ìŽ ëë°ë ê±°ì§ëčëë
čëŽì„ìì ìŹì ìŁŒì ì ì ìŽ íìí êČœì° íŹëȘ
ê°ë§ì ê°ë„Œ í”íŽ ë°±ëŽì„ìì ì 뚌ì ìííêł ìŹì ìŁŒì ì ì ì ëì€ì ìííë êČìŽ ë ëì ì íìŽ ë ì ììì ììŹíë©°, ì¶í ì„êž° ìíì ëí ì í„ì ëčê” ì°ê”Źê° íìíë€êł ìê°íë€.
Figure 1.
Results of Kaplan-Meier survival analysis with complete success (postoperative intraocular pressure [IOP] < 18 mmHg and IOP reduction â„ 20% without medication). Cumulative probability of success was tended to be lower for phakic eyes (solid line) than for pseudophakic eyes (broken line) (p = 0.068, Mantel-Cox log-rank test).

Figure 2.
Results of Kaplan-Meier survival analysis with qualified success (postoperative intraocular pressure [IOP] < 18 mmHg and IOP reduction â„ 20% with or without medication). Cumulative probability of success was not significantly different between phakic eyes (solid line) and pseudophakic eyes (broken line) (p = 0.553, Mantel-Cox log-rank test).
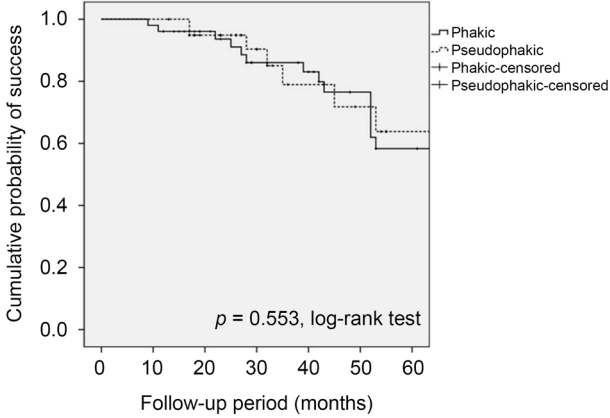
Table 1.
Baseline characteristics of the phakic and pseudophakic eye groups
| Characteristic | Phakic eyes (n = 51) | Pseudophakic eyes (n = 40) | p-value |
|---|---|---|---|
| Age (years) | 64.3 ± 8.4 | 71.6 ± 6.7 | <0.001* |
| Sex (M/F) | 39/12 | 32/8 | 0.687â |
| Laterality (OD/OS) | 24/27 | 23/17 | 0.323â |
| DM (+/-) | 5/46 | 7/33 | 0.281â |
| HTN (+/-) | 15/36 | 22/18 | 0.014â |
| CCT (Όm) | 533.6 ± 41.6 | 535.8 ± 39.2 | 0.793* |
| Visual field global indices | |||
| âMD (dB) | -24.1 ± 8.2 | -21.9 ± 10.2 | 0.280* |
| âPSD (dB) | 7.0 ± 3.4 | 6.0 ± 3.4 | 0.179* |
| Preoperative IOP (mmHg) | 22.8 ± 7.5 | 25.3 ± 7.1 | 0.121* |
| Preoperative medication (n) | 3.9 ± 0.6 | 3.9 ± 0.6 | 0.714* |
| Preoperative BCVA (LogMAR) | 0.533 ± 0.633 | 0.529 ± 0.630 | 0.975* |
| Axial length (mm) | 23.7 ± 1.1 | 23.7 ± 0.9 | 0.841* |
Values are presented as mean ± standard deviation unless otherwise indicated.
M/F = male/female; OD = oculus dexter; OS = oculus sinister; DM = diabetes mellitus; HTN = hypertension; CCT = central corneal thickness; MD = mean deviation; PSD = pattern standard deviation; IOP = intraocular pressure; BCVA = best corrected visual acuity; LogMAR = logarithm of the minimum angle of resolution.
Table 2.
Preoperative and postoperative IOP and numbers of glaucoma medications
| Characteristic | Phakic eyes (n = 51) | Pseudophakic eyes (n = 40) | p-value* |
|---|---|---|---|
| Preoperative IOP (mmHg) | 22.8 ± 7.5 | 25.3 ± 7.1 | 0.121 |
| Preoperative medication (n) | 3.9 ± 0.6 | 3.9 ± 0.6 | 0.714 |
| Postoperative follow-up period (months) | 50.1 ± 31.7 | 37.9 ± 21.0 | 0.030 |
| Postoperative IOP (mmHg) | 18.4 ± 8.9 | 14.1 ± 8.4 | 0.024 |
| Postoperative medication (n) | 1.9 ± 1.7 | 1.1 ± 1.6 | 0.018 |
Table 3.
Results of Cox proportional hazards regression analysis of complete success
| Parameter |
Total (n = 91) |
Pseudophkic and phakic eyes who underwent subsequent cataract surgery (n = 69) |
Pseudophkic and phakic eyes without subsequent cataract surgery (n = 62) |
|||
|---|---|---|---|---|---|---|
| Hazard ratio (95% CI) | p-value* | Hazard ratio (95% CI) | p-value* | Hazard ratio (95% CI) | p-value* | |
| Age (< 60 years) | 0.854 (0.417-1.750) | 0.667 | 0.538 (0.169-1.714) | 0.294 | 0.757 (0.257-2.227) | 0.613 |
| Diabetes | 0.684 (0.262-1.785) | 0.438 | 1.020 (0.336-3.093) | 0.973 | 0.462 (0.121-1.755) | 0.257 |
| Hypertension | 1.716 (0.910-3.236) | 0.095 | 1.397 (0.670-2.912) | 0.373 | 1.625 (0.661-3.995) | 0.290 |
| Phakic status | 1.973 (1.032-3.771) | 0.040 | 2.144 (1.055-4.357) | 0.035 | 2.114 (0.800-5.590) | 0.131 |
| Preoperative IOP â„ 25 mmHg | 1.155 (0.629-2.121) | 0.641 | 1.442 (0.686-3.033) | 0.335 | 0.685 (0.315-1.491) | 0.341 |
| Preoperative medication > 3 | 0.886 (0.430-1.826) | 0.743 | 0.917 (0.345-2.438) | 0.862 | 0.597 (0.241-1.478) | 0.265 |
| Early postoperative hypotony | 2.805 (1.211-6.499) | 0.016 | 3.923 (1.506-10.217) | 0.005 | 2.672 (0.927-7.704) | 0.069 |
| Hyphema | 1.454 (0.548-3.857) | 0.452 | 1.397 (0.462-4.227) | 0.554 | 0.925 (0.112-7.627) | 0.942 |
| Shallow anterior chamber | 1.464 (0.636-3.371) | 0.370 | 0.963 (0.358-2.592) | 0.940 | 1.948 (0.528-7.180) | 0.317 |
Table 4.
Results of Cox proportional hazards regression analysis of qualified success
| Parameter |
Total (n = 91) |
Pseudophkic and phakic eyes who underwent subsequent cataract surgery (n = 69) |
Pseudophkic and phakic eyes without subsequent cataract surgery (n = 62) |
|||
|---|---|---|---|---|---|---|
| Hazard ratio (95% CI) | p-value* | Hazard ratio (95% CI) | p-value* | Hazard ratio (95% CI) | p-value* | |
| Age (< 60 years) | 1.719 (0.680-4.346) | 0.252 | 2.042 (0.496-8.404) | 0.323 | 0.781 (0.127-4.801) | 0.790 |
| Diabetes | 0.364 (0.073-1.812) | 0.217 | 1.030 (0.121-8.799) | 0.978 | 0.181 (0.012-2.801) | 0.221 |
| Hypertension | 1.583 (0.669-3.746) | 0.296 | 1.016 (0.332-3.112) | 0.978 | 1.512 (0.324-7.062) | 0.599 |
| Phakic status | 1.180 (0.406-3.434) | 0.761 | 1.449 (0.436-4.823) | 0.545 | 1.675 (0.269-10.409) | 0.580 |
| Preoperative IOP â„ 25 mmHg | 0.443 (0.179-1.096) | 0.078 | 0.340 (0.097-1.195) | 0.093 | 0.588 (0.171-2.018) | 0.399 |
| Preoperative medication > 3 | 1.256 (0.442-3.563) | 0.669 | 0.586 (0.136-2.516) | 0.472 | 1.147 (0.278-4.738) | 0.849 |
| Early postoperative hypotony | 1.910 (0.530-6.882) | 0.323 | 2.342 (0.550-9.965) | 0.250 | 1.946 (0.377-10.058) | 0.427 |
| Hyphema | 2.368 (0.672-8.342) | 0.180 | 1.746 (0.390-7.817) | 0.466 | 3.986 (0.317-50.083) | 0.284 |
| Shallow anterior chamber | 0.593 (0.164-2.145) | 0.426 | 0.340 (0.040-2.886) | 0.323 | 1.120 (0.144-8.713) | 0.914 |
Table 5.
Postoperative complications
| Parameter | Phakic (n = 51) | Pseudophakic (n = 40) | p-value |
|---|---|---|---|
| Early postoperative wound leak | 5 (9.8) | 5 (12.5) | 0.683* |
| Early postoperative hypotony | 4 (7.8) | 6 (15.0) | 0.325â |
| Hyphema | 7 (13.7) | 1 (2.5) | 0.074â |
| Shallow anterior chamber | 8 (15.7) | 2 (5.0) | 0.176â |
| Serous choroidal detachment | 4 (7.8) | 7 (17.5) | 0.203â |
| Corneal decompensation | 3 (5.9) | 1 (2.5) | 0.628â |
| Endophthalmitis | 0 | 0 | N/A |
REFERENCES
1) Ritch R, Schlötzer-Schrehardt U. Exfoliation (pseudoexfoliation) syndrome: toward a new understanding. Proceedings of the first international think tank. Acta Ophthalmol Scand 2001;79:213-7.


2) Ritch R. Exfoliation syndrome-the most common identifiable cause of open-angle glaucoma. J Glaucoma 1994;3:176-7.


3) Olivius E, Thorburn W. Prognosis of glaucoma simplex and glaucoma capsulare. A comparative study. Acta Ophthalmol (Copenh) 1978;56:921-34.

4) Heijl A, Bengtsson B, Hyman L, et al. Natural history of open-angle glaucoma. Ophthalmology 2009;116:2271-6.


5) Futa R, Shimizu T, Furuyoshi N, et al. Clinical features of capsular glaucoma in comparison with primary open-angle glaucoma in Japan. Acta Ophthalmol (Copenh) 1992;70:214-9.


6) Konstas AG, Jay JL, Marshall GE, Lee WR. Prevalence, diagnostic features, and response to trabeculectomy in exfoliation glaucoma. Ophthalmology 1993;100:619-27.


7) Shingleton BJ, Alfano C, O'Donoghue MW, Rivera J. Efficacy of glaucoma filtration surgery in pseudophakic patients with or without conjunctival scarring. J Cataract Refract Surg 2004;30:2504-9.


8) Fontana H, Nouri-Mahdavi K, Caprioli J. Trabeculectomy with mitomycin C in pseudophakic patients with open-angle glaucoma: outcomes and risk factors for failure. Am J Ophthalmol 2006;141:652-9.


9) Broadway DC, Chang LP. Trabeculectomy, risk factors for failure and the preoperative state of the conjunctiva. J Glaucoma 2001;10:237-49.


10) Takihara Y, Inatani M, Seto T, et al. Trabeculectomy with mitomycin for open-angle glaucoma in phakic vs pseudophakic eyes after phacoemulsification. Arch Ophthalmol 2011;129:152-7.


11) Prata JĂșnior JA, Minckler DS, Baerveldt G, et al. Trabeculectomy in pseudophakic patients: postoperative 5-fluorouracil versus intraoperative mitomycin C antiproliferative therapy. Ophthalmic Surg 1995;26:73-7.

12) Scott IU, Greenfield DS, Schiffman J, et al. Outcomes of primary trabeculectomy with the use of adjunctive mitomycin. Arch Ophthalmol 1998;116:286-91.


13) Clarke MP, Vernon SA, Sheldrick JH. The development of cataract following trabeculectomy. Eye (Lond) 1990;4(Pt 4):577-83.


15) Daugeliene L, Yamamoto T, Kitazawa Y. Cataract development after trabeculectomy with mitomycin C: a 1-year study. Jpn J Ophthalmol 2000;44:52-7.


16) Klink J, Schmitz B, Lieb WE, et al. Filtering bleb function after clear cornea phacoemulsification: a prospective study. Br J Ophthalmol 2005;89:597-601.



17) Damji KF, Konstas AG, Liebmann JM, et al. Intraocular pressure following phacoemulsification in patients with and without exfoliation syndrome: a 2 year prospective study. Br J Ophthalmol 2006;90:1014-8.



18) SaĆaga-Pylak M, Kowal M, Zarnowski T. Deterioration of filtering bleb morphology and function after phacoemulsification. BMC Ophthalmol 2013;13:17.



19) Maumenee AE. External filtering operations for glaucoma: the mechanism of function and failure. Trans Am Ophthalmol Soc 1960;58:319-28.


20) Addicks EM, Quigley HA, Green WR, Robin AL. Histologic characteristics of filtering blebs in glaucomatous eyes. Arch Ophthalmol 1983;101:795-8.


21) Yamagami S, Araie M, Mori M, Mishima K. Posterior chamber intraocular lens implantation in filtered or nonfiltered glaucoma eyes. Jpn J Ophthalmol 1994;38:71-9.

22) Takihara Y, Inatani M, Ogata-Iwao M, et al. Trabeculectomy for open-angle glaucoma in phakic eyes vs in pseudophakic eyes after phacoemulsification: a prospective clinical cohort study. JAMA Ophthalmol 2014;132:69-76.


23) Broadway DC, Grierson I, Hitchings RA. Local effects of previous conjunctival incisional surgery and the subsequent outcome of filtration surgery. Am J Ophthalmol 1998;125:805-18.


24) Supawavej C, Nouri-Mahdavi K, Law SK, Caprioli J. Comparison of results of initial trabeculectomy with mitomycin C after prior clear-corneal phacoemulsification to outcomes in phakic eyes. J Glaucoma 2013;22:52-9.


25) Shingleton BJ, Heltzer J, O'Donoghue MW. Outcomes of phacoemulsification in patients with and without pseudoexfoliation syndrome. J Cataract Refract Surg 2003;29:1080-6.


26) Merkur A, Damji KF, Mintsioulis G, Hodge WG. Intraocular pressure decrease after phacoemulsification in patients with pseudoexfoliation syndrome. J Cataract Refract Surg 2001;27:528-32.


27) Chen PP, Lin SC, Junk AK, et al. The effect of phacoemulsification on intraocular pressure in glaucoma patients: a report by the American Academy of Ophthalmology. Ophthalmology 2015;122:1294-307.






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




