 |
 |
| J Korean Ophthalmol Soc > Volume 62(5); 2021 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ(Descemet membrane endothelial keratoplasty) ņŗ£Ē¢ē Ēøä ņØ┤ņŗØĒÄĖ ņŗżĒī©Ļ░Ć ļ░£ņāØĒĢ£ ĒÖśņ×ÉņŚÉĻ▓ī ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņ×¼ņŗ£ļÅäĒĢśņŚ¼ ņä▒Ļ│ĄĒĢ£ Ļ▓ĮĒŚśņØä ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņ”ØļĪĆņÜöņĢĮ
47ņäĖ ņŚ¼ņ×É ĒÖśņ×ÉņŚÉĻ▓ī ņóīņĢł Ēæ╣ņŖż Ļ░üļ¦ēļé┤Ēö╝ņØ┤ņāüņ”Ø(FuchsŌĆÖ endothelial dystrophy) ņ¦äļŗ©ņ£╝ļĪ£ ļ│ĖņøÉņŚÉņä£ ņóīņĢł ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”ØņØĆ ņŚåņŚłņ£╝ļéś ņłśņłĀ 6ņŻ╝ Ēøä Ļ░üļ¦ēļČĆņóģ ļ░Å ņłśĒżĻ░Ć ļ░£ņāØĒĢśņŚ¼ Ļ░łņłśļĪØ ņĢģĒÖöļÉśņŚłņ£╝ļ®░, ņŗ£ļĀź ļśÉĒĢ£ Ļ░ÉĒć┤ļÉśņ¢┤ ņłśņłĀ 7Ļ░£ņøö Ēøä ņØ┤ņŗØĒÄĖ ņŗżĒī© ņ¦äļŗ©ĒĢśņŚÉ ņóīņĢł ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ļŗżņŗ£ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņ×¼ņłśņłĀ Ēøä 8Ļ░£ņøöņ¦Ė ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ Ļ░üļ¦ēņØĆ Ēł¼ļ¬ģĒĢśļ®░ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź 0.6 ļé┤ņÖĖļĪ£ ņ£Āņ¦ĆļÉśĻ│Ā ņ׳ļŗż.
Ļ▓░ļĪĀ
ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ ņŗ£Ē¢ē Ēøä ņØ┤ņŗØĒÄĖ ņŗżĒī©Ļ░Ć ļ░£ņāØĒĢ£ ĒÖśņ×ÉņŚÉņä£ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņ×¼ņŗ£Ē¢ēĒĢśņśĆļŖöļŹ░, ņłśņłĀ ņżæ ĻĖ░ņĪ┤ņØś ļŹ░ņŖżļ®öļ¦ēņØĆ ņ¢┤ļĀĄņ¦Ć ņĢŖĻ▓ī ņś©ņĀäĒ׳ ņĀ£Ļ▒░ĒĢĀ ņłś ņ׳ņŚłņ£╝ļ®░ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ ņä▒Ļ│ĄņĀüņØĖ Ļ▓░Ļ│╝ļź╝ ņ¢╗ņØä ņłś ņ׳ņŚłļŗż.
ABSTRACT
Purpose
To report a case of secondary Descemet membrane endothelial keratoplasty (DMEK) for graft failure after primary DMEK.
Case summary
A 47-year-old female underwent primary DMEK in her left eye with a diagnosis of FuchsŌĆÖ endothelial dystrophy. At 6 weeks later, corneal stromal edema with epithelial and subepithelial bullae was first observed. From that point on, the condition of the cornea and the visual acuity continued to degrade. After 7 months, a second DMEK procedure (i.e., a repeat DMEK) for graft failure was performed successfully without any complications. Since the second procedure, the cornea has been clear, and the best-corrected visual acuity has remained at 0.6 for 8 months.
ļé┤Ēö╝ņäĖĒżņØś ņØ┤ņāüņØ┤ ņøÉņØĖņØ┤ ļÉśļŖö Ļ░üļ¦ēņ¦łĒÖśņØĆ Ļ░üļ¦ēņØ┤ņŗØņłĀņØś ĒØöĒĢ£ ņĀüņØæņ”Øņ£╝ļĪ£, Ļ│╝Ļ▒░ņŚÉļŖö ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀ(Penetrating keratoplasty)ņØä ņŻ╝ļĪ£ ņŗ£Ē¢ēĒĢśņśĆņ¦Ćļ¦ī, ĒĢ£ĒÄĖņ£╝ļĪ£ ļé┤Ēö╝ņäĖĒżņĖĄņØä ņäĀĒāØņĀüņ£╝ļĪ£ ņØ┤ņŗØĒĢśļĀżļŖö ļČĆļČäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀ(Lamella keratoplasty)ņØś ņŗ£ļÅäĻ░Ć ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņ׳ņŚłļŗż. ņØ┤ņŚÉ ļö░ļØ╝ Ļ░üļ¦ēļé┤Ēö╝ņÖĆ ļŹ░ņŖżļ®öļ¦ēļ¦īņØä ņäĀĒāØņĀüņ£╝ļĪ£ ņØ┤ņŗØĒĢśļŖö ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ(Descemet membrane endothelial keratoplasty, DMEK)ņØ┤ Melles et al [1]ņŚÉ ņØśĒĢśņŚ¼ ņåīĻ░£ļÉśĻĖ░ņŚÉ ņØ┤ļź┤ļŖöļŹ░, Ēæ╣ņŖż Ļ░üļ¦ēļé┤Ēö╝ņØ┤ņāüņ”Ø(FuchsŌĆÖ endothelial dystrophy) 200ļĪĆņŚÉ ņŗ£Ē¢ēĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ 80%ņØś ĒÖśņ×ÉĻ░Ć 0.8 ņØ┤ņāüņØś ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØä ļ│┤ņØ┤ļŖö ļō▒[2] ņĪ░ĻĖ░ņŚÉ ļŹö ļéśņØĆ ņŗ£ļĀźĒÜīļ│ĄņØä ņ¢╗ņØä ņłś ņ׳ļŖö Ļ░Ćņן ņØ┤ņāüņĀüņØĖ ļé┤Ēö╝ņäĖĒżņØ┤ņŗØņłĀņ×äņØ┤ ņ×ģņ”ØļÉśĻ│Ā ņ׳ļŗż. ĒĢśņ¦Ćļ¦ī ņĄ£ĻĘ╝ ļōżņ¢┤ ĻĘĖ ņŗ£Ē¢ē ĒܤņłśĻ░Ć ņ”ØĻ░ĆĒĢ©ņŚÉ ļö░ļØ╝ ņØ┤ņŗØ ņŗżĒī© ņé¼ļĪĆ ļśÉĒĢ£ ļ¦ÄņĢäņ¦ĆĻ│Ā ņ׳ļŖöļŹ░, ņØ┤ļĪ£ ņØĖĒĢśņŚ¼ 2ņ░© Ļ░üļ¦ēņØ┤ņŗØņØä ņŗ£ļÅäĒĢĀ ņŗ£ ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀ, ļŹ░ņŖżļ®öļ¦ēļ░Ģļ”¼ņ×ÉļÅÖļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ(Descemet Stripping automated endothelial Keratoplasty, DSaEK) Ēś╣ņØĆ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ ņ×¼ņŗ£ļÅä ļō▒ņØä Ļ│äĒÜŹĒĢĀ ņłś ņ׳ļŗż. ņĀĆņ×ÉļōżņØĆ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢ£ Ēøä ņØ┤ņŗØĒÄĖ ņŗżĒī©Ļ░Ć ļ░£ņāØĒĢ£ Ļ▓ĮņÜ░ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņä▒Ļ│ĄņĀüņ£╝ļĪ£ ņ×¼ņŗ£Ē¢ēĒĢ£ ņ”ØļĪĆļź╝ ņāüņäĖĒĢ£ ņäżļ¬ģĻ│╝ ĒĢ©Ļ╗ś ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
47ņäĖ ņŚ¼ņ×É ĒÖśņ×ÉĻ░Ć ņ¢æņĢł Ēæ╣ņŖż Ļ░üļ¦ēļé┤Ēö╝ņØ┤ņāüņ”Ø ņ¦äļŗ©ņ£╝ļĪ£ ĒāĆļ│æņøÉņŚÉņä£ 2009ļģäņŚÉ ņ▓½ ņÜ░ņĢł ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀ, 2013ļģäņŚÉ ļæÉ ļ▓łņ¦Ė ņÜ░ņĢł ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ē ļ░øņĢśĻ│Ā, 2018ļģä ņĀĆņ×É ņżæ ĒĢ£ ļ¬ģ(H.H.S)ņŚÉĻ▓ī ņäĖ ļ▓łņ¦Ė ņÜ░ņĢł ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēļ░øņĢśļŗż. ĻĘĖ Ēøä ņóīņĢł ļśÉĒĢ£ ņŗ£ļĀźņØ┤ ņ¦ĆņåŹņĀüņ£╝ļĪ£ Ļ░ÉĒć┤ĒĢśņŚ¼ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ ņÜ░ņĢł 0.125, ņóīņĢł 0.02ņśĆņ£╝ļ®░, Ļ│©ļō£ļ¦īņĢĢĒÅēņĢłņĢĢĻ│äļĪ£ ņĖĪņĀĢĒĢ£ ņĢłņĢĢņØĆ ņÜ░ņĢł 13 mmHg, ņóīņĢł 33 mmHgņśĆļŗż. ņäĖĻĘ╣ļō▒Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņŚÉņä£ ņÜ░ņĢł Ļ░üļ¦ē ņØ┤ņŗØĒÄĖņØĆ ņל ņ£Āņ¦ĆļÉśĻ│Ā ņ׳ņŚłņ£╝ļéś, ņóīņĢłņØĆ ņłśĒżļź╝ ļÅÖļ░śĒĢ£ ļ»Ėļ¦īņä▒ņØś Ļ░üļ¦ēļČĆņóģĻ│╝ Ēś╝Ēāü, ļŹ░ņŖżļ®öļ¦ēņŻ╝ļ”ä, Ļ░üļ¦ēļé┤Ēö╝ņĖĄņØś ĻĄ¼ĒāĆĒāĆĻ░Ć Ļ┤Ćņ░░ļÉśņŚłĻ│Ā, ļ░śļ®┤ ļ░▒ļé┤ņןņØĆ Ļ▒░ņØś ņ¦äĒ¢ēļÉśņ¦Ć ņĢŖņØĆ ņāüĒā£ņśĆļŗż. Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņŚÉņä£ ņóīņĢłņØĆ Ļ░üļ¦ēļČĆņóģĻ│╝ Ēś╝Ēāüņ£╝ļĪ£ ņĀĢĒÖĢĒĢ£ Ļ▓Ćņé¼Ļ░Ć ļČłĻ░ĆĒĢśņśĆļŗż. ņĀäņĢłļČĆļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗śļŖö ņÜ░ņĢł ņĢĮ 560 ╬╝m, ņóīņĢł ņĢĮ 710 ╬╝mņśĆļŗż. ņØ┤ņŚÉ ņóīņĢł Ēæ╣ņŖż Ļ░üļ¦ēļé┤Ēö╝ņØ┤ņāüņ”ØņŚÉ ļö░ļźĖ Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļČĆņĀä ņ¦äļŗ©ņ£╝ļĪ£ 2019ļģä 5ņøö 13ņØ╝ ņóīņĢł ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņĀĆņ×É ņżæ ĒĢ£ ļ¬ģ(H.H.S)ņŚÉĻ▓ī ņŗ£Ē¢ē ļ░øņĢśļŗż. ņłśņłĀ ņĀä ļĀłņØ┤ņĀĆĒÖŹņ▒äņĀłĻ░£ņłĀņØĆ ļö░ļĪ£ ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņĢśļŗż. ļŹ░ņŖżļ®öļ¦ēņØ┤ ļ░Ģļ”¼ ņ▓śļ”¼ļÉ£ ņāüĒā£ņØś Ļ░üļ¦ēņØä ņłśņ×ģĒĢśņŚ¼ ņłśņłĀņØä ņ¦äĒ¢ēĒĢśņśĆļŖöļŹ░, ņłĀņ×ÉĻ░Ć Ļ░üļ¦ēņØä ĒÄĆņ╣śĒĢśĻ│Ā ļŹ░ņŖżļ®öļ¦ē ļ░Å ļé┤Ēö╝ņäĖĒżņĖĄļ¦īņØä ļ▓ŚĻ▓©ļé┤ļŖö Ļ│╝ņĀĢņŚÉņä£ ļé┤Ēö╝ņäĖĒżņŚÉ ņåÉņāüņØ┤ ļ░£ņāØĒĢśņśĆļŗż. Ļ░üļ¦ē ņØ┤ņĖĪņŚÉ ņŻ╝ļÉ£ ņĀłĻ░£ņ░ĮņØä ļ¦īļōżņ¢┤ ņØ┤ņŗØĒÄĖņØä ņéĮņ×ģĒĢśĻ│Ā, ņłśņŚ¼ ņĢłĻĄ¼ ļé┤ņŚÉņä£ ņØ┤ņŗØĒÄĖņØä ĒÄĖ ļŗżņØī Ļ│ĄĻĖ░ļź╝ ņĀäļ░®ņŚÉ ņŻ╝ņ×ģĒĢśņŚ¼, ņłśņŚ¼ Ļ░üļ¦ēĒøäļČĆņŚÉ ļČĆņ░®ņŗ£ĒéżļŖö ļō▒ņØś ņłśņłĀ Ļ│╝ņĀĢņØĆ ļ¼┤ļ”¼ ņŚåņØ┤ ņ¦äĒ¢ēļÉśņŚłļŗż.
ņłĀ Ēøä 1Ļ░£ņøöņ¦Ė ņóīņĢł ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ 0.5Ļ╣īņ¦Ć ņĖĪņĀĢļÉśņŚłĻ│Ā, ņĀäņĢłļČĆļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗śļŖö ņĢĮ 500 ╬╝m ņĀĢļÅäņśĆņ£╝ļ®░, ņØ┤ņŗØĒÄĖļ░Ģļ”¼ ļō▒ ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ĻĘĖļ¤¼ļéś Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļ░ĆļÅäļŖö ņĖĪņĀĢļÉśņ¦Ć ņĢŖņĢśļŗż. ņłśņłĀ Ēøä 6ņŻ╝ņ¦Ė ņóīņĢł Ļ░üļ¦ē ņØ┤ņĖĪņŚÉņä£ ļČĆņóģ ļ░Å ņāüĒö╝ņĖĄ ņłśĒżĻ░Ć Ļ┤Ćņ░░ļÉśĻĖ░ ņŗ£ņ×æĒĢśņśĆļŗż. Ļ│Āņןņä▒ ņŗØņŚ╝ņłś ņĢłņĢĮ(Muro 128┬«; Sodium chloride 5%, Bausch & Lomb, Rochester, NY, USA)ņØä ĒĢśļŻ© 2-4ĒÜī ņĀÉņĢłĒĢśļÅäļĪØ ņ▓śļ░®ĒĢśņśĆņØīņŚÉļÅä Ļ░łņłśļĪØ ņóīņĢł Ļ░üļ¦ēļČĆņóģņØ┤ ņĢģĒÖöļÉśņŚłļŗż(Fig. 1A). ņłśņłĀ Ēøä 7Ļ░£ņøöņ¦Ė ņāüĒö╝ņĖĄņØś ņłśĒż ļ░Å Ļ░üļ¦ēļČĆņóģņØĆ ņĀä ņśüņŚŁņ£╝ļĪ£ ĒÖĢļīĆļÉśņ¢┤ ņĀäņĢłļČĆļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗śļŖö ņĢĮ 680 ╬╝m ņĀĢļÅäņśĆņ£╝ļ®░(Fig. 1B), ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź ļśÉĒĢ£ 0.06ņ£╝ļĪ£ Ļ░ÉņåīĒĢśņŚ¼, ņóīņĢł Ļ░üļ¦ēļé┤Ēö╝ ņØ┤ņŗØ ņŗżĒī©ļĪ£ ĒīÉļŗ©ĒĢśņŚ¼ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØ ņ×¼ņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż.
ņ×¼ņłśņłĀņØĆ ļīĆņ▓┤ļĪ£ ņ▓½ ņłśņłĀĻ│╝ ļÅÖņØ╝ĒĢ£ Ļ│╝ņĀĢņ£╝ļĪ£ ņĀäņŗĀļ¦łņĘ©ĒĢśņŚÉ ņ¦äĒ¢ēļÉśņŚłļŗż. ņÜ░ņäĀ ņłśņłĀ ņŗ£ņĢ╝ ĒÖĢļ│┤ļź╝ ņ£äĒĢśņŚ¼ Ļ░üļ¦ēņāüĒö╝ļź╝ ļ▓ŚĻ▓© ļé┤ņŚłļŗż(Fig. 2A). ĻĘĖ Ēøä Ļ░üļ¦ē ņØ┤ņĖĪņŚÉ ļŗżņŗ£ ņŻ╝ ņĀłĻ░£ņ░ĮņØä ļ¦īļōżņŚłĻ│Ā, ņĀäļ░®ņ▓£ņ×ÉļŖö Ļ░üļ¦ē ņŻ╝ļ│ĆļČĆ 2ņŗ£, 4ņŗ£ ļ░Å 10ņŗ£ ļ░®Ē¢źņŚÉ ĒĢ┤ļæÉņŚłļŗż(Fig. 2B). ņ▓½ ļ▓łņ¦Ė ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņŚÉņä£ļŖö ļŹ░ņŖżļ®öļ¦ē ņĀ£Ļ▒░ ņŗ£ņŚÉ ņĀäļ░®ņØä Ļ│ĄĻĖ░ļĪ£ ņ▒äņÜ┤ ņāüĒā£ņŚÉņä£ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļéś, ņĀłĻ░£ņ░Įņ£╝ļĪ£ Ļ│ĄĻĖ░Ļ░Ć Ļ│äņåŹ ļ╣ĀņĀĖ ņłśņłĀņŚÉ ņ¢┤ļĀżņøĆņØ┤ ņ׳ņŚłļŗż. ņ×¼ņłśņłĀņŚÉņä£ļŖö ņĀÉĒāäļ¼╝ņ¦ł(Hyal2000┬«; LG Life Sciences, Seoul, Korea)ņØä ņĀäļ░®ņŚÉ ņ▒äņÜ┤ Ēøä Reverse Sinskey hookņØä ņØ┤ņÜ®ĒĢśņŚ¼ ĻĖ░ņĪ┤ ļŹ░ņŖżļ®öļ¦ē ņØ┤ņŗØĒÄĖņØä ļ░Ģļ”¼ĒĢśņśĆļŗż(Fig. 2C). ļśÉĒĢ£ ņ▓½ ļ▓łņ¦Ė ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņŚÉņä£ļŖö ļ▓ŚĻ▓©ļé╝ ļŹ░ņŖżļ®öļ¦ēņØä ļ»Ėļ”¼ ĒØĀņ¦æņØä ļé┤ļŖö scoring Ēøä ļŹ░ņŖżļ®öļ¦ēņØä ļ▓ŚĻ▓©ļāłņ£╝ļéś, ļæÉ ļ▓łņ¦Ė ņłśņłĀņŚÉņä£ļŖö scoringņØ┤ ĒĢäņÜö ņŚåņŚłļŗż. ļŹ░ņŖżļ®öļ¦ēņØä ļ▓ŚĻĖĖ ļĢī ņŗ¼ĒĢ£ ņ£Āņ░®ņØĆ ļ░£Ļ▓¼ļÉśņ¦Ć ņĢŖņĢśļŗż. ņĄ£ņóģņĀüņ£╝ļĪ£ ņłśņĀĢņ▓┤ļéŁņøÉĒśĢņĀłĻ░£ņÜ® ĒżņģēņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļŹ░ņŖżļ®öļ¦ē ņØ┤ņŗØĒÄĖņØä ņĀ£Ļ▒░ĒĢśņśĆļŗż(Fig. 2D). ņĀ£Ļ▒░ĒĢ£ ļŹ░ņŖżļ®öļ¦ē ņØ┤ņŗØĒÄĖņØĆ ņłśņłĀņŗż Ēśäļ»ĖĻ▓ĮņØä ĒåĄĒĢśņŚ¼ ņś©ņĀäĒĢ£ ņĀ£Ļ▒░Ļ░Ć ņØ┤ļżäņ¦ä Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż(Fig. 2E). ĻĘĖ Ēøä ņĀäļ░® ļé┤ ļé©ņĢäņ׳ļŖö ņĀÉĒāäļ¼╝ņ¦ł ļō▒ņØĆ Irrigation & Aspirationņ£╝ļĪ£ņŹ© ņĀ£Ļ▒░ĒĢśņśĆļŗż. Ļ│ĄņŚ¼ Ļ░üļ¦ēņØĆ ļé┤Ļ│╝ņĀü, ņĢłĻ│╝ņĀü ļ│æļĀźņØ┤ ņŚåļŖö 52ņäĖ ņŚ¼ņä▒ ļćīņé¼ņ×ÉņØś ĻĄŁļé┤ ĻĖ░ņ”Ø Ļ░üļ¦ēņ£╝ļĪ£, Ļ░üļ¦ēļé┤Ēö╝ņäĖĒż ņłśļŖö 2,604/mm2ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż. ļ│Ė ņłśņłĀ 6ņØ╝ ņĀäņŚÉ ņĀüņČ£ļÉśņŚłĻ│Ā, 5ņØ╝ ņĀä ņĀĆņ×É ņżæ ĒĢ£ ļ¬ģ(H.H.S)ņŚÉ ņØśĒĢśņŚ¼ ļŗżļźĖ ĒÖśņ×ÉņØś ņŗ¼ļČĆĒæ£ņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀņŚÉ ņé¼ņÜ®ļÉśĻ│Ā ļé©ņØĆ ļŹ░ņŖżļ®öļ¦ē ļ░Å ļé┤Ēö╝ņäĖĒżņĖĄņØä Ļ░üļ¦ēļ│┤ņĪ┤ņĢĪ(Optisol┬«; Chiron Ophthalmics, Irvine, CA, USA)ņŚÉ ļ│┤ņĪ┤ĒĢ£ ņāüĒā£ņśĆļŗż. ņØ┤ņŗØĒÄĖņØś Ēü¼ĻĖ░ļŖö ņ▓½ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ ļĢīņÖĆ Ļ░ÖņØĆ Ēü¼ĻĖ░ņØĖ 7.5 mmļĪ£ Ļ▓░ņĀĢĒĢśņśĆļŗż. ņØ┤ņŗØĒÄĖņØĆ ņłśņłĀņŗżņŚÉņä£ ĒŖĖļ”ĮĒīÉ ļĖöļŻ© ņÜ®ņĢĪ(Vision Blue┬«, 0.06% Trypan blue; D.O.R.C., Zuiland, Netherlands)ņ£╝ļĪ£ 2ļČäĻ░ä ņŚ╝ ņāē Ēøä ĒÅēĒśĢņŚ╝ņĢĪ(Balanced Salt Solution [BSS] Plus┬«; Alcon Laboratories Inc., Fort Worth, TX, USA)ņ£╝ļĪ£ ņŚ╝ņāēņĢĮņØä ņäĖņ▓Ö, ĻĘĖ Ēøä ĒŖĖļ”ĮĒīÉ ļĖöļŻ© ņÜ®ņĢĪņ£╝ļĪ£ 2ļČäĻ░ä ļŗżņŗ£ ņŚ╝ņāēĒĢśņśĆļŗż. ĻĘĖ Ēøä ņĀĆņ×ÉļōżņØ┤ Ļ░£ļ░£ĒĢ£ ņØ┤ņżæ ņ║Éļē╝ļØ╝ ņłśĻĖ░(double cannula maneuver)ļź╝ ĒåĄĒĢśņŚ¼ ņØ┤ņŗØĒÄĖņØä ņØ┤ņżæ ļĪż(Double roll)ĻĄ¼ņĪ░Ļ░Ć ļÉśĻ▓ī ĒĢ£ Ēøä(Fig. 2F), ļ│ĆĒśĢļÉ£ ņĪ┤ņŖż ĒŖ£ļĖī(Modified Jones tube)ņŚÉ ļŹ░ņŖżļ®öļ¦ēņØś ļ░®Ē¢źņØä ĒÖĢņØĖĒĢśļ®░ ļ╣©ņĢäļōżņśĆļŗż(Fig. 2G). ĒÅēĒśĢ ņŚ╝ņĢĪņØä ņĀäļ░®ņŚÉ ņ▒äņøī ņĀüļŗ╣ĒĢ£ ņĀäļ░®Ļ╣ŖņØ┤ļź╝ ņ£Āņ¦ĆĒĢśļÅäļĪØ ĒĢśņśĆĻ│Ā, ņØ┤ņŗØĒÄĖņØ┤ ļÆżņ¦æĒ׳ņ¦Ć ņĢŖļÅäļĪØ ļ░®Ē¢źņŚÉ ņ£ĀņØśĒĢśļ®░ ļ│ĆĒśĢļÉ£ ņĪ┤ņŖż ĒŖ£ļĖīļź╝ ņŻ╝ņĀłĻ░£ņ░ĮņŚÉ ņéĮņ×ģ, ņĀłĒÄĖņØä ņĀäļ░®ņŚÉ ņŻ╝ņ×ģĒĢśņśĆļŗż(Fig. 2H). ĻĘĖ Ēøä 10-0 Nylonņ£╝ļĪ£ ņŻ╝ņĀłĻ░£ņ░ĮņØä ļ┤ēĒĢ®ĒĢśņśĆĻ│Ā, ņØ┤ņŗØĒÄĖņØś ļé┤Ēö╝ņäĖĒżĻ░Ć ņĢäļלļĪ£ Ē¢źĒĢśļÅäļĪØ ņś¼ļ░öļź┤Ļ▓ī ņéĮņ×ģļÉ£ Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż. ĻĘĖ Ēøä Dirisamer ņłĀĻĖ░[3]ļĪ£ Ļ░üļ¦ē ņÖĖļČĆ Ēæ£ļ®┤ņØä ĒåĄĒĢśņŚ¼ ĒĢ£ ņ║Éļē╝ļØ╝ļĪ£ļŖö ņØ┤ņŗØĒÄĖ ĒĢ£ņ¬Į ļüØņØä ļłīļ¤¼ Ļ│ĀņĀĢĒĢśĻ│Ā, ļæÉ ļ▓łņ¦Ė ņ║Éļē╝ļØ╝ļĪ£ļŖö ļŗżļźĖ ĒĢ£ņ¬ĮņØś ļĪżņØä ļ░Ćņ¢┤ ĒÄ╝ņ│żļŗż(Fig. 2I). ņØ┤ņŗØĒÄĖņØ┤ļŗż ĒÄ┤ņ¦ä ļŗżņØī 4ņŗ£ ļ░®Ē¢źņØś Ļ░üļ¦ē ņ▓£ņ×É ļČĆņ£äļĪ£ ņ║Éļē╝ļØ╝ļź╝ ņéĮņ×ģ, ņØ┤ņŗØĒÄĖ ņĢäļלņŚÉ ņ£äņ╣śĒĢśļÅäļĪØ ĒĢ£ Ēøä ņĀäļ░®ņŚÉ Ļ│ĄĻĖ░ļź╝ Ļ░ĆļōØ ņŻ╝ņ×ģĒĢśņśĆļŗż(Fig. 2J). ņłśņłĀņŗżņŚÉņä£ ĒÖśņ×ÉļŖö 60ļČäĻ░ä ņĢÖņÖĆņ£äļź╝ ņ£Āņ¦ĆĒĢśņŚ¼ ņĀłĒÄĖņØ┤ ņłśņŚ¼Ļ░üļ¦ēĻ░äņ¦ł ĒøäļČĆņŚÉ ņĄ£ļīĆĒĢ£ ļČĆņ░®ļÉśļÅäļĪØ ĒĢśņśĆļŗż. ņĄ£ņóģņĀüņ£╝ļĪ£ ļÅÖĻ│Ą ņ░©ļŗ©ņØä ļ░®ņ¦ĆĒĢśĻ│Āņ×É ņĀäļ░®ņØś Ļ│ĄĻĖ░ļź╝ ņĀäļ░® ņĀäņ▓┤ ņÜ®ņĀüņØś ņĢĮ 40% ņĀĢļÅäļ¦ī ļé©ĻĖ░Ļ│Ā ņłśņłĀņØä ņóģļŻīĒĢśņśĆļŗż.
ņłśņłĀ Ēøä ņČ®ļČäĒ׳ ņĀłĒÄĖņØ┤ ņ£Āņ░®ļÉĀ ļĢīĻ╣īņ¦Ć ĒÖśņ×ÉļŖö ņ×ģņøÉĒĢśņŚ¼ 1-2ņØ╝Ļ░ä Ļ░ĆļŖźĒĢ£ ĒĢ£ ņĢÖņÖĆņ£ä ņāüĒā£ļź╝ ņ£Āņ¦ĆĒĢśņśĆņ£╝ļ®░, Ļ░ÉņŚ╝ ņśłļ░®ņØä ņ£äĒĢśņŚ¼ ļ╣äĻ░Ćļ¬®ņŖż ņĀÉņĢłņĢĪ(Vigamox┬«, Moxifloxacin 0.5%; Alcon, Fort Worth, TX, USA)ņØä ĒĢśļŻ© 4ĒÜī, ņØ┤ņŗØĒÄĖ Ļ▒░ļČĆ ļ░śņØæ ļ░®ņ¦Ćļź╝ ņ£äĒĢśņŚ¼ ļĪ£Ēģīļ¦źņŖż ņĀÉņĢłņĢĪ(Lotemax┬«, Loteprednol etabonate 0.5%; Bausch & Lomb, Rochester, NY, USA)ņØä ĒĢśļŻ© 4ĒÜī ņĀÉņĢłĒĢśļÅäļĪØ ĒĢśņśĆļŗż. ņ×ģņøÉ ĻĖ░Ļ░ä ņżæ ņØ┤ņŗØĒÄĖļ░Ģļ”¼ ņåīĻ▓¼ņØĆ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢä, ņĀäļ░® ļé┤ Ļ│ĄĻĖ░ņŻ╝ņ×ģņłĀņØ┤ ņČöĻ░ĆļĪ£ ĒĢäņÜöĒĢśņ¦ĆļŖö ņĢŖņĢśļŗż.
ņłśņłĀ 6ņŻ╝ Ēøä ņŗ£Ē¢ēĒĢ£ ņóīņĢł Ļ▓Įļ®┤Ēśäļ»ĖĻ▓ĮĻ▓Ćņé¼ņŚÉņä£ ļŗżļ®┤ņä▒ 40%, ļŗżĒśĢņä▒ 48%, Ļ░üļ¦ēļé┤Ēö╝ņäĖĒżļ░ĆļÅä 667 cells/mm2ļĪ£ ņĖĪņĀĢļÉśņŚłĻ│Ā, ņĀäņĢłļČĆļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ ņżæņŗ¼Ļ░üļ¦ēļæÉĻ╗śļŖö ņĢĮ 430 ╬╝m ņĀĢļÅäļĪ£ ļČĆņóģ ņŚåņØ┤ ņ£Āņ¦ĆļÉśĻ│Ā ņ׳ņŚłļŗż(Fig. 3A). ņłśņłĀ Ēøä 3Ļ░£ņøö ņóīņĢł ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØĆ 0.6, ņĢłņĢĢņØĆ 18 mmHgļĪ£ ņĖĪņĀĢļÉśņŚłņ£╝ļ®░, ņłśņłĀ ņĀä Ļ┤Ćņ░░ļÉśņŚłļŹś Ļ░üļ¦ēļČĆņóģ ļ░Å ņāüĒö╝ņĖĄ ņłśĒż ļČĆņ£äļŖö ĒśĖņĀäļÉśņŚłļŗż(Fig. 3B). ņłśņłĀ Ēøä 8Ļ░£ņøöņ¦Ė, ņŚ¼ņĀäĒ׳ ņØ┤ņŗØĒÄĖļ░Ģļ”¼ ļō▒ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀź 0.6 ļé┤ņÖĖļź╝ ņ£Āņ¦ĆĒĢśļ®┤ņä£ ņÖĖļל ĒåĄĒĢśņŚ¼ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ņżæņØ┤ļŗż.
Han et al [4]ņØĆ 9ļ¬ģ 10ņĢłņŚÉņä£ņØś ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ 1ļģä ņ×äņāüĻ▓ĮĻ│╝ļź╝ ļ│┤Ļ│ĀĒĢśļ®┤ņä£ ņØ╝ņ░© Ļ░üļ¦ēņĀłĒÄĖ ņāØņ░®ņŗżĒī©Ļ░Ć ņ׳ņŚłļŹś 1ņĢłņŚÉņä£ 2Ļ░£ņøö ļÆż ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņ×¼ņŗ£Ē¢ēĒĢśņśĆļŗżĻ│Ā ĒĢśņśĆļŗż. ĻĘĖļ¤¼ļéś ļ│Ė ņ”ØļĪĆļ│┤Ļ│ĀņŚÉņä£ļŖö ņ×¼ņŗ£Ē¢ēļÉ£ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņŚÉ ļīĆĒĢśņŚ¼ ĻĖ░ņĪ┤ ļŹ░ņŖżļ®öļ¦ē ņØ┤ņŗØĒÄĖņØś ņĀ£Ļ▒░ļź╝ ĒżĒĢ©ĒĢśņŚ¼ ņłĀĻĖ░ņŚÉ ņżæņĀÉņØä ļæÉĻ│Ā ņ×ÉņäĖĒ׳ ļ¼śņé¼ĒĢśņśĆļŗżļŖö ņĀÉņŚÉņä£ ņ░©ņØ┤Ļ░Ć ņ׳ļŗż.
ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØĆ ņłśņŚ¼ Ļ░üļ¦ēņŚÉņä£ ļŹ░ņŖżļ®öļ¦ē ļ░Å ļé┤Ēö╝ņäĖĒżņĖĄņØä ņĀ£Ļ▒░ĒĢśĻ│Ā, Ļ│ĄņŚ¼ Ļ░üļ¦ēņŚÉņä£ļÅä ļŹ░ņŖżļ®öļ¦ēĻ│╝ ļé┤Ēö╝ņäĖĒżņĖĄļ¦īņØä ĒżĒĢ©ĒĢ£ ņĀłĒÄĖņØä ņĀ£ņ×æ, ņØ┤ļź╝ ņłśņŚ¼ ņĢłĻĄ¼ ņĀäļ░®ņŚÉ ņéĮņ×ģĒĢśņŚ¼ Ļ│ĄĻĖ░ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņłśņŚ¼Ļ░üļ¦ēĻ░äņ¦ł ĒøäļČĆņŚÉ ļČĆņ░®ĒĢśļŖö ļČĆļČäņĖĄ Ļ░üļ¦ēņØ┤ņŗØņłĀņØ┤ļŗż. ņØ┤ļ¤░ ĒŖ╣ņä▒ņØĆ ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀņØś ļŗ©ņĀÉņ£╝ļĪ£ ņ¦ĆņĀüļÉśļŖö ņśżļ×£ ņ░Įņāü ĒÜīļ│Ą ĻĖ░Ļ░ä, ļ┤ēĒĢ®ņé¼ļĪ£ ņØĖĒĢ£ Ļ░ÉņŚ╝, Ļ░üļ¦ēļ»Ėļ×Ć ļ░Å ĻČżņ¢æ, ņØ┤ņ░©ļģ╣ļé┤ņן ļ░Å ļ░▒ļé┤ņן ļ░£ņāØ ļō▒ņØś ĒĢ®ļ│æņ”Ø[5]ņØä ĒśäņĀĆĒ׳ ņżäņØ╝ ņłś ņ׳ļŗż. ļśÉĒĢ£ ņłśņłĀņŚÉ ņØśĒĢśņŚ¼ ņ£Āļ░£ļÉśļŖö ļé£ņŗ£Ļ░Ć ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņŚÉ ļ╣äĒĢśņŚ¼ Ļ▒░ņØś ņŚåņ£╝ļ®░, ĒŖ╣Ē׳ Ļ│ĄņŚ¼Ļ░üļ¦ēņŚÉņä£ ņŗżņ¦ł ņĪ░ņ¦üņØä ņĀ£Ļ▒░ĒĢśņŚ¼ Ļ│ĄņŚ¼-ņłśņŚ¼ Ļ░üļ¦ē Ļ▓ĮĻ│äļ®┤ņØś ļČłĻĘĀņØ╝ĒĢ©Ļ│╝ ņŗżņ¦ł ļæÉĻ╗śņØś ļČłĻĘ£ņ╣ÖĒĢ©ņØä ņŚåņĢĀ Ļ░üļ¦ē Ēøäļ®┤ņØś ĻĘĀņØ╝ĒĢ©ņØä ņ”ØļīĆņŗ£Ēé┤ņ£╝ļĪ£ņŹ©[6] ļŹ░ņŖżļ®öļ¦ēļ░Ģļ”¼ļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņŚÉ ļ╣äĒĢ┤ņä£ļÅä ļŹö ļ╣Āļź┤Ļ│Ā ļéśņØĆ ņŗ£ļĀźĒśĖņĀäņØä Ļ░ĆņĀĖļŗżņżĆļŗż[7]. ļ®┤ņŚŁ Ļ▒░ļČĆ ļ░śņØæ ļśÉĒĢ£ ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņŚÉ ļ╣äĒĢśņŚ¼ Ēø©ņö¼ ņĀüĻ▓ī ļéśĒāĆļé┤ļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż[8]. ņØ┤ļ¤░ ņןņĀÉņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØĆ ņłĀĻĖ░ņØś ļé£ņØ┤ļÅäĻ░Ć ļåÆņĢä ņŗżĒī© Ļ░ĆļŖźņä▒ņØ┤ ņāüļīĆņĀüņ£╝ļĪ£ ļåÆļŗż. ņØ┤ņŗØĒÄĖņØä ļ¦īļō£ļŖö Ļ│╝ņĀĢņŚÉņä£ Ļ░üļ¦ēļé┤Ēö╝ņĖĄņŚÉ ļ¼╝ļ”¼ņĀü ņåÉņāüņØ┤ ļ░£ņāØĒĢśņŚ¼ ņś©ņĀäĒĢ£ ņĀłĒÄĖņØä ņ¢╗ņ¦Ć ļ¬╗ĒĢśļŖö Ļ▓ĮņÜ░ļÅä ņ׳ņ£╝ļ®░, ņØ┤ņŗØĒÄĖņØś ļæÉĻ╗śĻ░Ć ņ¢ćņĢä ņØ┤ņŗØĒĢśļŖö ļÅäņżæ ļé┤Ēö╝ņäĖĒżņŚÉ ņåÉņāüņØ┤ ļ░£ņāØĒĢĀ Ļ░ĆļŖźņä▒ļÅä Ēü¼ļŗż. ĒŖ╣Ē׳ ņ┤łņŗ¼ņ×ÉņŚÉ ņØśĒĢśņŚ¼ ņŗ£Ē¢ēļÉ£ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ 25ļĪĆņŚÉņä£ ņłĀ Ēøä 6Ļ░£ņøöņŚÉ Ļ░üļ¦ēļé┤Ēö╝ņäĖĒż ņłśĻ░Ć 45.5% Ļ░ÉņåīĒĢ£ ļ│┤Ļ│Ā[9]ļŖö ņØ┤ļź╝ ļÆĘļ░øņ╣©ĒĢ£ļŗż. Ļ▓īļŗżĻ░Ć ņĀłĒÄĖņØś ņ£äņĢäļלĻ░Ć ļÆżņ¦æĒśĆņä£ Ļ░üļ¦ēļé┤Ēö╝Ļ░Ć ĻĖ░ļŖźņØä ļ¬╗ĒĢśļŖö Ļ▓ĮņÜ░ļÅä ņ׳ļŗż. ĻĘĖļ¤¼ļéś Ļ░Ćņן ĒØöĒĢ£ ņŗżĒī© ņØ┤ņ£ĀļŖö ņØ┤ņŗØĒÄĖņØ┤ ņłśņŚ¼ Ļ░üļ¦ēĻ░äņ¦ł ĒøäļČĆņŚÉ ņÖäļ▓ĮĒĢśĻ▓ī ņ£Āņ░®ļÉśņ¦Ć ņĢŖĻ│Ā ļČäļ”¼ļÉśļŖö Ļ▓ĮņÜ░ņØ┤ļŗż. ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØĆ ļŗżļźĖ Ļ░üļ¦ēņØ┤ņŗØņłĀņŚÉ ļ╣äĒĢśņŚ¼ ņØ┤ņŗØĒÄĖ ņ×¼ļČĆņ░®ņØä ņ£äĒĢ┤ ņĀäļ░® ļé┤ Ļ│ĄĻĖ░ ņŻ╝ņ×ģņØä ĒĢ┤ņĢ╝ ĒĢśļŖö ļ╣łļÅäĻ░Ć ņ×”ņØĆļŹ░, Dirisamer et al [2]ņŚÉ ļö░ļź┤ļ®┤ 200ņĢłņØś ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ Ēøä 9%ņŚÉņä£ Ļ░üļ¦ēņĀłĒÄĖļČäļ”¼ļź╝ ļ│┤ņśĆĻ│Ā, ņØ┤ ņżæ 4%ņŚÉņä£ļŖö ņÖäņĀä ļČäļ”¼, 5%ņŚÉņä£ļŖö ļČĆļČä ļČäļ”¼ļź╝ ļ│┤ņśĆļŗż. ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ Ēøä ņĀäļ░® ļé┤ Ļ│ĄĻĖ░ņŻ╝ņ×ģņłĀņØä ļŗżņŗ£ ņŗ£Ē¢ēĒĢ£ Ļ▓ĮņÜ░ļŖö 11-82%ļĪ£[7,10,11] ļŗżņ¢æĒĢśĻ▓ī ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ņ£╝ļ®░, Ļ░üļ¦ēļČĆņóģņØ┤ ņóĆņ▓┤ ĒśĖņĀäļÉśņ¦Ć ņĢŖņĢä ņ×¼ņØ┤ņŗØņØä ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢśļŖö Ļ▓ĮņÜ░ļÅä 4-22% [10,11]ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż. ņØ┤ļ¤¼ĒĢ£ ņĀłĒÄĖ ņ£Āņ░®ņØś ņ¢┤ļĀżņøĆĻ│╝ Ļ│ĄĻĖ░ņŻ╝ņ×ģņłĀņØś ĒĢäņÜö, Ļ░üļ¦ēļČĆņóģņØś ņ¦ĆņåŹ ļō▒ņØĆ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØś ĒĢ£Ļ│äņĀÉņ£╝ļĪ£ ļé©ņĢä ņ׳ļŗż.
ļ│Ė ņ”ØļĪĆņŚÉņä£ ņ▓½ ļ▓łņ¦ĖļĪ£ ņŗ£Ē¢ēĒĢ£ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņŚÉņä£ļŖö ļŹ░ņŖżļ®öļ¦ēņØ┤ ļ░Ģļ”¼ ņ▓śļ”¼ļÉ£ ņāüĒā£ņØś ņłśņ×ģ Ļ░üļ¦ēņØä ņé¼ņÜ®ĒĢśņśĆļŖöļŹ░, ņłĀņ×ÉĻ░Ć Ļ░üļ¦ēņØä ĒÄĆņ╣śĒĢśĻ│Ā ļŹ░ņŖżļ®öļ¦ē ļ░Å ļé┤Ēö╝ņäĖĒżņĖĄļ¦īņØä ļ▓ŚĻ▓©ļé┤ļŖö Ļ│╝ņĀĢņŚÉņä£ ļé┤Ēö╝ņäĖĒżņŚÉ ņåÉņāüņØ┤ ļ░£ņāØĒĢśņśĆļŗż. ļ░öļĪĀ ĻĖ░ņ”ØĻ░üļ¦ē ĒÄĆņ╣ś(Barron Corneal Punch)ļĪ£ ĻĖ░ņ”ØĻ░üļ¦ēņØś ļé┤Ēö╝ņ¬ĮņŚÉ ņé┤ņ¦Ø ĒÄĆņ╣śļź╝ ĒĢ£ ļŗżņØī Ēżņģēņ£╝ļĪ£ Ļ░Ćņןņ×Éļ”¼ ļŹ░ņŖżļ®öļ¦ēņØä ļ▓ŚĻ▓©ļé┤ļŖö Ļ│╝ņĀĢņŚÉņä£ ĒÄĆņ╣śĻ░Ć ņÖäļ▓ĮĒĢśņ¦Ć ņĢŖņĢä ņżæņŗ¼ļČĆ ļŹ░ņŖżļ®öļ¦ēĻ╣īņ¦Ć ĒĢ©Ļ╗ś ļüīļĀżļéśņÖöļŗż. ļŗ╣ņŗ£ ņłĀņ×ÉļŖö ņØ┤ļź╝ ņØĖņ¦ĆĒĢśņ¦Ć ļ¬╗ĒĢśņśĆĻ│Ā ņżæņŗ¼ļČĆ ļŹ░ņŖżļ®öļ¦ēņØä ņ░ŠļŖö ļÅÖņĢł ņżæņŗ¼ļČĆ ļŹ░ņŖżļ®öļ¦ēņØĆ ņŻ╝ļ│ĆļČĆ ļŹ░ņŖżļ®öļ¦ēĻ│╝ ĒĢ©Ļ╗ś ļŁēņ│Éņ¦ä ņ▒ä ļ░®ņ╣śļÉśņŚłļŗż. ņØ┤ļź╝ ņØĖņ¦ĆĒĢśĻ│Ā ļŹ░ņŖżļ®öļ¦ēņØä ļŗżņŗ£ ĒÅēĒśĢņŚ╝ņĢĪņŚÉ ļŗ┤ĻĘ╝ Ēøä ļ»ĖņäĖĻ░Ćņ£äļĪ£ ņŻ╝ļ│ĆļČĆņÖĆ ņżæņŗ¼ļČĆņØś ļŹ░ņŖżļ®öļ¦ēņØä ļČäļ”¼ĒĢśņśĆļŗż. ņØ┤ļ¤¼ĒĢ£ Ļ│╝ņĀĢņŚÉņä£ ļé┤Ēö╝ņäĖĒżņØś ļ¼╝ļ”¼ņĀü ņåÉņāüņØ┤ ļ░£ņāØĒĢśņśĆņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. ļśÉĒĢ£ ņ▓½ ņłśņłĀ Ēøä Ļ░üļ¦ēļČĆņóģņØ┤ ņ▓śņØī Ļ┤Ćņ░░ļÉ£ ņŗ£ĻĖ░Ļ░Ć ņłśņłĀ Ēøä 6ņŻ╝ņ¦ĖļĪ£ ļ╣äĻĄÉņĀü ņØ╝ļĀĆļŗżļŖö ņĀÉņŚÉņä£ ņ▓½ ļ▓łņ¦Ė ņłśņłĀņØś ņŗżĒī© ņøÉņØĖņØ┤ ļ®┤ņŚŁĒĢÖņĀü Ļ▒░ļČĆ ļ░śņØæļ│┤ļŗżļŖö ņØ┤ņŗØĒÄĖņØś ĻĖ░Ļ│äņĀü ņåÉņāü ļĢīļ¼Ėņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
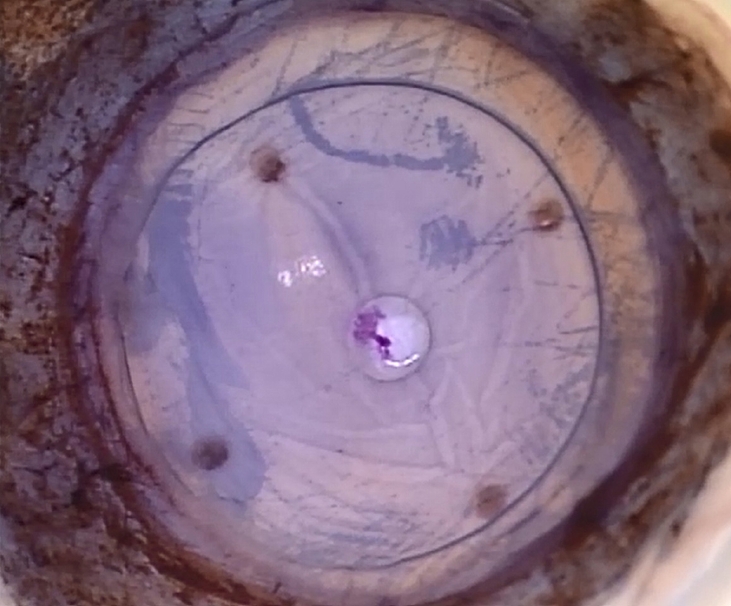
ļ│Ė ņ”ØļĪĆņŚÉņä£ ļæÉ ļ▓łņ¦ĖļĪ£ ņŗ£Ē¢ēĒĢ£ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØś Ļ▓ĮņÜ░ ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”ØņØĆ ņĢäņ¦ü ļ░£ņāØĒĢśņ¦Ć ņĢŖņĢśņ£╝ļéś ņłĀ Ēøä Ļ░üļ¦ēļé┤Ēö╝ņäĖĒż ņłśĻ░Ć 667 cells/mm2ļĪ£ ļé«Ļ▓ī ņĖĪņĀĢļÉśņŚłļŗż. ĻĘĖ ņøÉņØĖņ£╝ļĪ£ ņ▓½ ļ▓łņ¦Ė ĻĖ░ņ”Ø Ļ░üļ¦ēņØś ļ▓äĒŖĖļŗØ(Corneal buttoning) Ļ│╝ņĀĢņŚÉņä£ ļ░£ņāØĒĢ£ ļ¼╝ļ”¼ņĀüņØĖ ņåÉņāü Ļ░ĆļŖźņä▒ņØ┤ ņ׳ļŗż. ņłśņłĀ ņśüņāüņØä ņČöĒøä ļČäņäØĒĢ£ Ļ▓░Ļ│╝, Ļ░üļ¦ēļé┤Ēö╝Ļ░Ć ĒŖĖļ”ĮĒīÉ ļĖöļŻ© ņÜ®ņĢĪņŚÉ ņŚ╝ņāēļÉ£ ļ®┤ņĀüņØä ņĖĪņĀĢĒĢ┤ļ│┤ļŗł ĒŖĖļ”ĮĒīÉ ļĖöļŻ© ņÜ®ņĢĪņŚÉ ņŚ╝ņāēļÉ£ ņåÉņāü ļ®┤ņĀü ļ╣äņ£©ņØĆ ņ¦üĻ▓Į 8.0 mmņØś ņøÉ ņśüņŚŁņŚÉņä£ 18.4%ļĪ£ ņĖĪņĀĢļÉśņŚłļŗż(Fig. 4). ļæÉ ļ▓łņ¦Ė ņøÉņØĖņ£╝ļĪ£ļŖö ņØ┤ņŗØĒÄĖņØä ņłśņŚ¼Ļ░üļ¦ēĻĖ░ņ¦ł ĒøäļČĆņŚÉ ļČĆņ░®ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ņłśņłĀ ņżæ 60ļČäĻ░ä ņĀäļ░®ņØä Ļ│ĄĻĖ░ļĪ£ Ļ░ĆļōØ ņ▒äņÜ┤ ņ▒ä ņ£Āņ¦ĆĒĢśļŖö Ļ│╝ņĀĢņŚÉņä£ ņĢłņĢĢņØä ņĖĪņĀĢĒĢśņ¦Ć ņĢŖņĢśļŖöļŹ░, ļŗ╣ņŗ£ ņĢłņĢĢņØ┤ ļåÆĻ▓ī ņ£Āņ¦ĆļÉśņ¢┤ Ļ░üļ¦ēļé┤Ēö╝Ļ░Ć ņåÉņāü ļ░øņĢśņØä Ļ░ĆļŖźņä▒ļÅä ņ׳ļŗż. Dapena [12]ļŖö ņØ┤ļĢī ņĀäļ░®ņØś ņĢĢļĀźņØä ņĢĮ 20 mmHgļĪ£ ņ£Āņ¦ĆĒĢśļÅäļĪØ ĻČīņןĒĢśĻ│Ā ņ׳ņ£╝ļéś, ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ņłśņłĀ ņżæ ņĢłņĢĢņØä ņĖĪņĀĢĒĢśņ¦Ć ņĢŖņĢä ņĢī ņłś ņŚåņŚłļŗż. ņäĖ ļ▓łņ¦Ė, ĒŖĖļ”ĮĒīÉ ļĖöļŻ© ņÜ®ņĢĪņ£╝ļĪ£ 4ļČä ņØ┤ĒĢśņØś ņŗ£Ļ░ä ļÅÖņĢł ņØ┤ņŗØĒÄĖņØä ņŚ╝ņāēĒĢśļŖö Ļ▓ĮņÜ░ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ Ļ░üļ¦ēļé┤Ēö╝ ņåÉņāüņØ┤ ļ░£ņāØĒĢśņ¦Ć ņĢŖļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļéś[13], ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ņĀĢĒÖĢĒ׳ 4ļČäĻ░ä ņŚ╝ņāēņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ»ĆļĪ£ ĒŖĖļ”ĮĒīÉ ļĖöļŻ©ņŚÉ ņØśĒĢ£ Ļ░üļ¦ēļé┤Ēö╝ņŚÉ ņåÉņāüņØś Ļ░ĆļŖźņä▒ņØä ņÖäņĀäĒ׳ ļ░░ņĀ£ĒĢĀ ņłśļŖö ņŚåļŗż.
Ļ░üļ¦ēļČĆņóģņØ┤ ļÅÖļ░śļÉ£ ņØ┤ņŗØĒÄĖ ņŗżĒī©Ļ░Ć ļ░£ņāØļÉĀ ņŗ£ ņÜ░ņäĀ ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀņØä Ļ│ĀļĀżĒĢĀ ņłś ņ׳ņ¦Ćļ¦ī, ņĄ£ĻĘ╝ ļōżņ¢┤ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØś ļ│┤ĻĖēņØ┤ ĒÖĢļīĆļÉ©ņŚÉ ļö░ļØ╝ ĻĘĖ ĻĖ░ļ▓ĢĻ│╝ ņśłĒøä ļśÉĒĢ£ ļ░£ņĀäĒĢśņŚ¼ ņØ┤ņ░© ļČĆļČäņĖĄĻ░üļ¦ēņØ┤ņŗØņłĀļĪ£ņä£ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØ┤ ņĀÉņ░© ņŗ£ļÅäļÉśĻ│Ā ņ׳ļŗż. Baydoun et al [14]ņØĆ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ Ēøä ņ×¼ņ░© ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢ£ 17ļĪĆļź╝ 1ļģäĻ░ä Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢ£ ļ░öļź╝ ļ│┤Ļ│ĀĒĢśņśĆļŖöļŹ░, ņØ┤ ņżæ 3ļĪĆņØś ņŗżĒī©Ļ░Ć ņĄ£ņóģņĀüņ£╝ļĪ£ ļ░£ņāØĒĢśņśĆņØīņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. 1ļĪĆņŚÉņä£ļŖö ņØ┤ņŗØĒÄĖļ░Ģļ”¼Ļ░Ć Ēü¼Ļ▓ī ļ░£ņāØĒĢśņśĆņ£╝ļéś ņĀäļ░® ļé┤ Ļ│ĄĻĖ░ņŻ╝ņ×ģņłĀļĪ£ņŹ© ņ×¼ļČĆņ░®ņŚÉ ņä▒Ļ│ĄĒĢśņŚ¼ ņ┤Ø 14Ļ▒┤ņØ┤ ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ ņ£Āņ¦ĆļÉśņŚłļŗż. ĒŖ╣Ē׳ ņĄ£ļīĆĻĄÉņĀĢņŗ£ļĀźņØś Ļ▓ĮņÜ░ 1.2 ņØ┤ņāüņØ┤ 1ļĪĆ, 1.0 ņØ┤ņāüņØ┤ 3ļĪĆ, 0.8 ņØ┤ņāüņØ┤ 8ļĪĆņśĆņ£╝ļ®░, Ļ░üļ¦ēļé┤Ēö╝ņäĖĒż ņłśļŖö ņłśņłĀ ņĀä 2,580 ┬▒ 173 cells/mm2ņŚÉņä£ ņØ┤ņŗØ 1ļģä Ēøä 1,294 ┬▒ 459 cells/mm2ļĪ£ ņ¢æĒśĖĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż. ņØ┤ņŗØĒÄĖ ņŗżĒī©Ļ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ļŖö Ļ░üļ¦ēļČĆņóģņØ┤ ņŗ¼ĒĢ£ Ļ▓ĮņÜ░Ļ░Ć ļ¦ÄņĢä, ņ×¼ņłśņłĀļĪ£ņä£ ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ēĒĢśĻ▓ī ļÉ£ļŗżļ®┤ ņĀäļ░®ņŚÉ ņŻ╝ņ×ģļÉ£ ņ¢ćņØĆ ļŹ░ņŖżļ®öļ¦ē ņĀłĒÄĖņØä ļŗżļŻ©ĻĖ░ Ēלļōż Ļ▓āņØ┤ļØ╝ļŖö ņÜ░ļĀżĻ░Ć ļ¦ÄņØĆļŹ░, ņØ┤ļź╝ ĻĘ╣ļ│ĄĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ņłśņłĀ ņżæ ņĀäļ░®ņØä Ļ│ĄĻĖ░ļĪ£ Ļ░ĆļōØ ņ▒äņÜ░Ļ│Ā ĒŖĖļ”ĮĒīÉ ļĖöļŻ© ņŚ╝ņāēņĢĮņØä ņé¼ņÜ®ĒĢśņŚ¼ ņØ┤ņŗØĒÄĖņØś Ļ░Ćņŗ£ļÅäļź╝ ļåÆņØ┤ļŖö ĻĖ░ļ▓Ģ[14] ļśÉĒĢ£ ĒĢ┤ļŗ╣ ņŚ░ĻĄ¼ņŚÉņä£ ņĀ£ņĢłĒĢśĻ│Ā ņ׳ļŗż.
ļ│Ė ņ”ØļĪĆņØś Ļ▓ĮņÜ░ ļŹ░ņŖżļ®öļ¦ē ņĀ£Ļ▒░ņŗ£ ņĀäļ░®ņØä ņĀÉĒāäļ¼╝ņ¦ł(Hyal2000┬«, LG Life Sciences)ļĪ£ ņ▒äņÜ░Ļ│Ā ņŗ£Ē¢ēĒĢśņśĆļŗż. ņĀäļ░®ņØä ņĀÉĒāäļ¼╝ņ¦ł(Hyal2000┬«, LG Life Sciences)ļĪ£ ņ▒äņÜ░ļŖö ļ░®ļ▓ĢņØś ņןņĀÉņØĆ ņĀäļ░®ņØ┤ ņĢłņĀĢņĀüņ£╝ļĪ£ ņ£Āņ¦ĆļÉ£ļŗżļŖö ņĀÉņØ┤ļŗż. ņĀäļ░®ņØä Ļ│ĄĻĖ░ļĪ£ ņ▒äņÜ░ļ®┤ Ļ│ĄĻĖ░Ļ░Ć ņĀłĻ░£ņ░Įņ£╝ļĪ£ Ļ│äņåŹ ļ╣ĀņĀĖļéśĻ░Ć Ļ│ĄĻĖ░ļź╝ ļ░śļ│ĄņĀüņ£╝ļĪ£ ņŻ╝ņ×ģĒĢśļ®┤ņä£ ļŹ░ņŖżļ®öļ¦ēņØä ņĀ£Ļ▒░ĒĢ┤ņĢ╝ ĒĢ£ļŗż. ņĀäļ░®ņØä ņĀÉĒāäļ¼╝ņ¦łļĪ£ ņ▒äņÜ░ļŖö ļ░®ļ▓ĢņØś ļŗ©ņĀÉņØĆ Ļ│ĄĻĖ░ļź╝ ļäŻņŚłņØä ļĢīņŚÉ ļ╣äĒĢśņŚ¼ ļ░Ģļ”¼ ņżæņØĖ ļŹ░ņŖżļ®öļ¦ēņØ┤ ņל ļ│┤ņØ┤ņ¦Ć ņĢŖļŖöļŗżļŖö ņĀÉņØ┤ļŗż. ļśÉĒĢ£ ļŹ░ņŖżļ®öļ¦ē ņĀ£Ļ▒░ ĒøäņŚÉļŖö ņĀäļ░®ņØś ņĀÉĒāäļ¼╝ņ¦łņØĆ ļ¬©ļæÉ ņĀ£Ļ▒░ĒĢśņŚ¼ ņČöĒøä ņØ┤ņŗØĒÄĖņØś ņ£Āņ░® Ļ│╝ņĀĢņØä ļ░®ĒĢ┤ĒĢśņ¦Ć ņĢŖļÅäļĪØ ņŻ╝ņØśĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż. ĒŖ╣Ē׳ ļČäņé░ņä▒ ņĀÉĒāäļ¼╝ņ¦ł(Dispersive OVD, Viscoat┬«; Alcon Laboratories, Inc. Fort Worth, TX, USA)ņØś Ļ▓ĮņÜ░ļŖö Ļ░üļ¦ēĻĖ░ņ¦łĒøäļČĆņŚÉ ņ£Āņ░®ļÉśļ»ĆļĪ£ ņé¼ņÜ®ĒĢśņŚ¼ņä£ļŖö ņĢł ļÉ£ļŗż.
ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņŗ£Ē¢ē ļ░øņØĆ Ļ░üļ¦ēņØś Ļ▓ĮņÜ░ ļŹ░ņŖżļ®öļ¦ēņØ┤ Ļ░üļ¦ēĻĖ░ņ¦ł ĒøäļČĆņŚÉ ļŹö Ļ░ĢĒĢśĻ▓ī ņ£Āņ░®ļÉśļŖö Ļ▓ĮņÜ░Ļ░Ć ļ¦ÄļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ņ¢┤[14], ĻĖ░ņĪ┤ ņØ┤ņŗØĒÄĖņØä ņś©ņĀäĒ׳ ņĀ£Ļ▒░ĒĢśļŖö Ļ▓āņØ┤ Ļ╣īļŗżļĪ£ņÜĖ ņłś ņ׳ļŗż. ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ĻĖ░ņĪ┤ ņØ┤ņŗØĒÄĖņØś ņ£Āņ░®ņØ┤ ņŗ¼ĒĢśņ¦Ć ņĢŖņĢśĻ│Ā Reverse sinskey hookĻ│╝ ņłśņĀĢņ▓┤ļéŁņøÉĒśĢņĀłĻ░£ņÜ® ĒżņģēņØä ņé¼ņÜ®ĒĢ©ņ£╝ļĪ£ņŹ© ļ╣äĻĄÉņĀü ņēĮĻ▓ī ĻĖ░ņĪ┤ ņØ┤ņŗØĒÄĖņØä ņĀ£Ļ▒░ĒĢĀ ņłś ņ׳ņŚłļŗż.
ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ņØ┤ņ░© ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØś ņØ┤ņŗØĒÄĖņØä ņØ╝ņ░©ņÖĆ ļÅÖņØ╝ĒĢ£ Ēü¼ĻĖ░ļĪ£ ņĀ£ņ×æĒĢśņŚ¼ ņØ┤ņŗØĒĢśņśĆĻ│Ā, ņČöĻ░ĆņĀüņØĖ Ļ│ĄĻĖ░ ņŻ╝ņ×ģ ņŚåņØ┤ ĒĢ£ ļ▓łņŚÉ ņāØņ░®ņØ┤ ņל ņØ┤ļŻ©ņ¢┤ņĪīļŗż. ņØ┤ņĀä ņØ┤ņŗØ ņ£äņ╣śņŚÉ ņĀĢĒÖĢĒ׳ ņāłļĪ£ņÜ┤ ņØ┤ņŗØĒÄĖņØ┤ ļČĆņ░®ļÉśļŖö Ļ▓āņØĆ ņ¢┤ļĀĄĻ▓Āņ¦Ćļ¦ī, ņØ┤ņ░© ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ ņŗ£Ē¢ē ņŗ£ ņØ┤ņŗØĒÄĖ Ēü¼ĻĖ░ļź╝ ņØ╝ņ░© ņłśņłĀ ļĢīņÖĆ Ļ░ÖņØĆ Ēü¼ĻĖ░ļĪ£ ņżĆļ╣äĒĢśņŚ¼ļÅä ļ¼┤ļ”¼Ļ░Ć ņŚåļŖö Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ļ│Ė ļģ╝ļ¼ĖņŚÉņä£ļŖö ņØ╝ņ░© ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ ņØ┤Ēøä ņØ┤ņ░© ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņä▒Ļ│ĄņĀüņ£╝ļĪ£ ņŗ£Ē¢ēĒĢ£ ņ”ØļĪĆļź╝ ņāüņäĖĒĢ£ ņłśņłĀ Ļ│╝ņĀĢĻ│╝ ĒĢ©Ļ╗ś ļ│┤Ļ│ĀĒĢ£ļŗż. ĻĖ░ņĪ┤ ņØ┤ņŗØĒÄĖņØĆ ņśłņāüĻ│╝ ļŗ¼ļ”¼ ņ£Āņ░®ņØ┤ ņŗ¼ĒĢśņ¦Ć ņĢŖņĢśĻ│Ā, Reverse sinskey hookĻ│╝ ņłśņĀĢņ▓┤ļéŁņøÉĒśĢņĀłĻ░£ņÜ® ĒżņģēņØä ņé¼ņÜ®ĒĢ©ņ£╝ļĪ£ņŹ© ļ╣äĻĄÉņĀü ņēĮĻ▓ī ņÖäņĀäĒ׳ ņĀ£Ļ▒░ĒĢĀ ņłś ņ׳ņŚłļŗż. ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀ Ēøä ņŗżĒī©Ļ░Ć ļ░£ņāØĒĢĀ ņŗ£ ņĀäņĖĄĻ░üļ¦ēņØ┤ņŗØņØ┤ļéś ļŹ░ņŖżļ®öļ¦ēļ░Ģļ”¼ņ×ÉļÅÖļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä Ļ│ĀļĀżĒĢśĻĖ░ ņē¼ņÜ░ļéś, ļŹ░ņŖżļ®öļ¦ēļé┤Ēö╝Ļ░üļ¦ēņØ┤ņŗØņłĀņØä ņ×¼ņŗ£ļÅäĒĢśļŖö Ļ▓āļÅä ņóŗņØĆ ļ░®ļ▓Ģ ņżæ ĒĢśļéśņØ╝ Ļ▓āņØ┤ļŗż.
Figure┬Ā1.
Preoperative images, before repeat Descemet membrane endothelial keratoplasty (DMEK). (A) Preoperative cornea at slit lamp examination. Moderate edematous cornea with DescemetŌĆÖs membrane foldings and microbullae were observed. (B) Preoperative anterior segment optical coherence tomography (DRI OCT Triton┬«; Topcon, Tokyo, Japan).
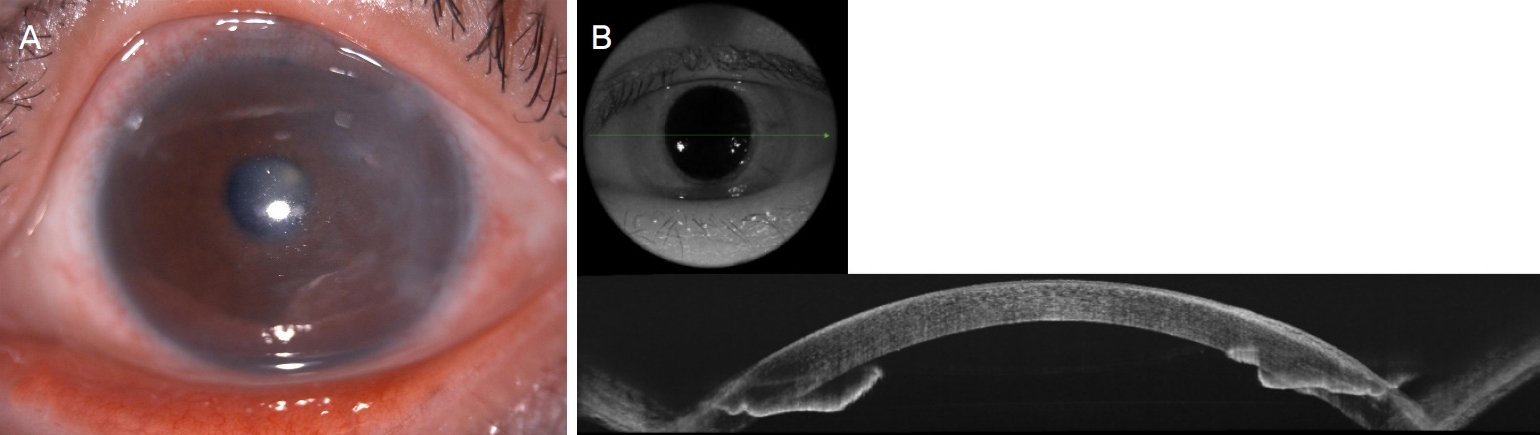
Figure┬Ā2.
Intraoperative images of repeat Descemet membrane endothelial keratoplasty (DMEK). (A) The corneal epithelium was peeled off for better surgical field of view. (B) Three small incisions (blue arrows) and main incision at the temporal side were made. (C) Former DMEK graft was dissected by the reversed Sinskey hook. (D) The graft was totally removed by the continuous curvilinear capsulorhexis forceps. (E) Removed graft was observed. (F) Prestripped new DMEK graft was being prepared by "double-cannula" method. (G) The graft was being loaded into the modified Jones tube. (H) The graft was inserted into the anterior chamber through modified Jones tube. (I) The DMEK graft was centered by Dirisamer technique. (J) The anterior chamber was fully filled with air for 60 minutes.

Figure┬Ā3.
Postoperative images after repeat Descemet membrane endothelial keratoplasty (DMEK). (A) Anterior segment optical coherence tomography (OCT) (DRI OCT Triton®; Topcon, Tokyo, Japan) 6 weeks after repeat DMEK. No detachment of the graft was observed. (B) Three months after repeat DMEK, the cornea at slit lamp examination.

REFERENCES
1) Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea 2006;25:987-90.

2) Dirisamer M, Ham L, Dapena I, et al. Efficacy of Descemet membrane endothelial keratoplasty: clinical outcome of 200 consecutive cases after a learning curve of 25 cases. Arch Ophthalmol 2011;129:1435-43.


3) Dirisamer M, van Dijk K, Dapena I, et al. Prevention and management of graft detachment in Descemet membrane endothelial keratoplasty. Arch Ophthalmol 2012;130:280-91.


4) Han GL, Hyun J, Lim DH, et al. Clinical outcomes of DescemetŌĆÖs membrane endothelial keratoplasty: a 1-year retrospective study. J Korean Ophthalmol Soc 2015;56:1489-96.

5) Ing JJ, Ing HH, Nelson LR, et al. Ten-year postoperative results of penetrating keratoplasty. Ophthalmology 1998;105:1855-65.


6) Rudolph M, Laaser K, Bachmann BO, et al. Corneal higher-order aberrations after DescemetŌĆÖs membrane endothelial keratoplasty. Ophthalmology 2012;119:528-35.


7) Tourtas T, Laaser K, Bachmann BO, et al. Descemet membrane endothelial keratoplasty versus descemet stripping automated endothelial keratoplasty. Am J Ophthalmol 2012 153:1082-90. e2.


8) Boisjoly HM, Tourigny R, Bazin R, et al. Risk factors of corneal graft failure. Ophthalmology 1993;100:1728-35.


9) Hlinomazov├Ī Z, Hor├Īckov├Ī M, Pirnerov├Ī L. DMEK (Descemet membrane endothelial keratoplasty)-early and late postoperative complications. Cesk Slov Oftalmol 2011;67:75-9.

10) Price MO, Giebel AW, Fairchild KM, et al. DescemetŌĆÖs membrane endothelial keratoplasty: prospective multicenter study of visual and refractive outcomes and endothelial survival. Ophthalmology 2009;116:2361-8.


11) Dapena I, Ham L, Droutsas K, et al. Learning curve in DescemetŌĆÖs membrane endothelial keratoplasty: first series of 135 consecutive cases. Ophthalmology 2011;118:2147-54.


12) Dapena I. How to get started with standardized ŌĆśno-touchŌĆÖ Descemet membrane endothelial keratoplasty (DMEK). Rotterdam: NIIOS, 2014;69.




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




