피브린 접착제를 이용한 공막 내 인공수정체고정술의 안축장 및 전방깊이에 따른 효과 분석
Effects of Axial Length and Anterior Chamber Depth on Intrascleral Fixation Using a Fibrin Adhesive
Article information
Abstract
목적
유리체절제술과 피브린 접착제를 이용한 공막 내 인공수정체고정술을 실시한 환자에서 안축장 길이와 전방깊이에 따른 효과 차이를 알아보고자 한다.
대상과 방법
인공수정체 이탈 환자에 대한 치료로 유리체절제술과 피브린 접착제를 이용한 공막 내 인공수정체고정술 후 6개월 이상 경과 관찰이 가능한 61명, 61안에 관하여 후향적으로 분석하였다. 안축장의 길이에 따라 22 mm 미만을 1군, 22 mm 이상, 25 mm 미만을 2군, 25 mm 이상을 3군, 전방깊이가 3.0 mm 미만을 A군, 3.0 mm 이상, 3.6 mm 미만을 B군, 3.6 mm 이상을 C군으로 나누어 각 군의 술 전후 교정 시력, 구면값, 원주값, 구면렌즈대응치를 측정 비교 분석하였다.
결과
술 전후 최대교정시력의 유의미한 향상을 확인할 수 있었으며, 술 전후 구면값, 구면렌즈대응치는 모든 군에서 유의미한 차이를 관찰할 수 있었다(p<0.05). 다만 안축장의 길이와 전방깊이가 길어질수록 Haptic slippage, IOL dislocation 등의 합병증 발생률이 증가함을 확인할 수 있었다.
결론
안축장의 길이와 전방깊이는 굴절이상에 영향을 줄 수 있어 수술 방법을 선택할 때 고려 요인 중 하나이다. 피브린 접착제를 이용한 공막 내 인공수정체고정술 후 최대교정시력, 구면값, 구면렌즈대응치의 유의한 향상으로 시력호전을 확인할 수 있고 술 후 원주값의 유의한 변화가 없어 인공수정체의 뒤틀림과 난시의 유발이 낮음을 알 수 있다.
Trans Abstract
Purpose
The purpose of this study was to evaluate the effect of axial length and anterior chamber depth in vitrectomy and intraocular lens intrascleral fixation with a fibrin adhesive.
Methods
The study retrospectively reviewed 61 eyes of 61 patients, who were followed up for over 6 months after surgery. The patients were divided into three groups according to their axial length: group 1, < 22 mm; group 2, 22 to < 25 mm; and group 3, > 25 mm. The patients were further divided into three sub-groups according to their anterior chamber depth: group A, < 3.0 mm; group B, 3.0 mm to < 3.6 mm; and group C, > 3.6 mm. We measured and analyzed the best-corrected visual acuity, spherical value, cylindrical value, and spherical equivalent of each group before surgery and at 6 months postoperatively.
Results
When comparing the groups preoperatively and postoperatively, the best-corrected visual acuity, spherical value, and spherical equivalent showed significant improvement in all groups (p < 0.05). The incidence of complications, such as haptic slippage and intraocular lens dislocation, increased with the axial length and anterior chamber depth.
Conclusions
The use of fibrin adhesive for intraocular lens intrascleral fixation improves visual acuity and reduces refractive error. Postoperatively, there was no significant change in cylindrical value. Because axial length and anterior chamber depth affect refractive error, both should be considered in correlation with the surgical method.
인공수정체공막고정술은 인공수정체삽입술을 시행할 수 없는 환자에서 선택할 수 있는 수술 방법으로 인공수정체의 지지 역할을 할 수 있는 구조물의 손상이 있는 경우나 인공수정체의 위치이동이 발생한 환자에서 재고정이 필요할 때 시행한다. 구조물의 손상을 유발할 수 있는 예로는 외상으로 인한 섬모체소대가 약해졌거나 백내장수술 중 후낭파열, 낭내적출술로 인한 후낭이 제거된 상태 등이 있다[1-4].
인공수정체공막고정술은 크게 외부(ab externo) 공막고정술과 내부(ab interno) 공막고정술로 나눌 수 있으며, 인공수정체의 지지부를 공막 내에 직접 삽입하여 고정하거나 공막절편을 만든 후 그 아래에 봉합사를 이용해 매듭 고정하는 방법, 조직적찹제를 사용하여 고정하는 방법 등이 있다. 최근에는 공막편이나 공막내 매듭 묻기, 공막고랑 등을 이용해 매듭의 노출을 줄여 합병증 발생을 줄이고, 수술 시간을 단축하고 최종적으로 환자의 불편감을 줄일 수 있는 수정된 수술 술기들이 소개되고 있다[5-10].
수술 방법 중 봉합사를 이용하여 매듭을 만든 인공수정체공막고정술에서는 봉합사 자체가 술 후 염증, 이물감, 육아종, 혈종형성 등의 합병증을 유발할 수 있지만 인공수정체의 중심이탈이나 기울어짐 등의 위치 변화가 발생할 가능성이 큰 단점이 있다[11,12]. 이를 해결하기 위해 조직 부착시 봉합사 대신 조직 접착제를 사용하는 수술 술기가 소개되고 있으며, 사용되는 조직접착제는 피브리노겐-트롬빈으로 이루어진 생체 조직적찹제로서 지금까지 안과 영역에서 결막 및 양막부착이나 안성형, 안와수술, 각막이식 등에 다양하게 이용되어 왔다[13-17].
술 전 안축장, 전방깊이, 각막굴절력 등 생체계측의 오차가 적어야 인공수정체 도수계산의 오류가 줄어들며, 원하는 굴절력을 얻을 수 있어 환자의 만족도를 높일 수 있다. 일반적으로 안축장이 짧은 환자에서 수술 시 평균 안축장의 환자보다 전방깊이와 각막굴절력에 따른 술 후 굴절이상이 커질 수 있다. 술 후 굴절력을 정확히 예측하기 위해서는 생체계측자료 및 인공수정체 도수계산 공식의 정확성, 인공수정체 질적 정확성, 술자의 특성을 고려한 임상적인 변수 등 여러 가지 요소를 고려하여 선택하게 되며 이런 요소들은 인공수정체공막고정술에도 동등하게 고려된다[18-21]. 본 연구에서는 봉합사를 이용하지 않고 조직접착제를 사용해 인공수정체공막내고정술을 유리체전절제술과 동시 시행한 환자들의 술 후 교정시력, 구면값, 원주값, 구면렌즈 대응치 변화 등을 안축장 길이 및 전방깊이에 따라 비교 분석해보았다.
대상과 방법
본 연구는 메리놀병원 임상시험심사위원회의 심의 및 승인을 받았다(승인 번호: MMC/2019-291). 2014년 1월 1일부터 2019년 12월 31일까지 본원에서 1명의 동일 술자(J.M.P)에게 인공수정체공막내고정술을 시행 받고 6개월 이상 추적 관찰이 가능하였던 총 61명 61안을 대상으로 하여 의무 기록을 후향적으로 분석하여 시행하였다. 당뇨나 기타 망막병변으로 인하여 안축장 및 전방깊이의 측정에 오류가 있는 환자나 수술 후 합병증으로 시력측정, 자동굴절검사에 영향을 줄 수 있는 경우는 제외하였으며, 시력 측정 및 검사 협조가 되지 않는 환자의 경우도 제외하였다.
모든 환자의 수술 전 검사로는 시력 및 안압검사, 자동굴절검사기(KR-8800; Topcon, Tokyo, Japan)를 사용하여 굴절력, 구면값, 원주값, 구면렌즈대응치를 확인하고 이를 바탕으로 최대교정시력을 측정하였다. 안축장과 전방깊이의 측정은 IOL Master® (Carl Zeiss, Jena, Germany)를 이용하였으며, 세극등현미경검사 및 산동 후 검사를 통하여 술 후 합병증을 확인하였다[22,23].
수술 방법(Fig. 1)은 2시와 8시 방향의 결막을 절개하여 공막을 노출시키고 각막윤부로부터 2 mm 떨어진 부분을 밀림자를 이용해 표시한 다음, 각막윤부와 평행하게 공막에 Stab knife를 이용해 약 2 mm 길이로 절개하여 인공수정체의 지지부를 고정할 고랑을 만들었다. 고정술 시행 전에 유리체절제술을 시행하지 않았던 환자들은 모두 유리체절제술을 시행하였다. 그 후 2시, 8시 공막부에 수직으로 25게이지 바늘을 이용해 구멍을 낸 다음, 눈속 집게를 통과시켜 인공수정체의 지지부를 잡아 안구 밖으로 빼내고, 26게이지 바늘을 이용해 각막윤부와 평행한 공막터널을 만들어 지지부를 삽입하여 고정하였다. 수술에 사용한 인공수정체는 MN60AC AcrySof® (Alcon Inc., Fort Worth, TX, USA)를 사용하였다.

Technique for the intrascleral fixation of intraocular lens. (A) The conjunctival flap is made by tenotomy scissors and the sclera is exposed. (B) Electrocautery was performed on the exposed sclera. (C) Two scleral grooves are made using a stab knife on the sclera parallel to the limbus. (D) The leading haptic of intraocular lens is grasped with 25-gauge intraocular forceps and the leading haptic is pulled through the transscleral incision. (E) Two scleral tunnels are made using a 26-gauge needle on the sclera parallel to the limbus. (F) The McPherson forceps grasps the externalized haptic, then inserts into the scleral tunnel. (G, H) Fibrin glue is used to fix the sclera and conjunctiva.
공막에 지지부를 고정하는 공간과 결막편을 만들 때 출혈 및 혈관은 전기소작술로 지혈하였으며, 노출된 공막 부위를 면봉을 이용하여 건조시킨 다음 집게로 절개된 결막편을 젖힌 후, 피브리노겐-트롬빈(Green Plast Kit®; Green Cross, Seongnam, Korea) 조직접착제가 담긴 주사기 용액을 차례로 떨어뜨렸다. 그 후 즉시 결막편을 접촉시키고 집게와 면봉을 이용하여 압박하여 유착을 유도했으며 절개된 결막의 가장자리를 집게로 잡아 경계 부위에 최대한 맞추면서 유착을 유도하였다.
통계적 검정은 SPSS 21 (IBM Corp., Armonk, NY, USA) 프로그램을 이용하였으며, Wilcoxon’s signed-ranks test를 이용하여 술 전후 측정값을 분석하였다. 각 군과의 비교는 Kruskall Wallis test를 통하여 분석하였다. 모든 분석에서 p값이 0.05 미만인 경우를 통계학적으로 유의한 것으로 간주하였다.
결 과
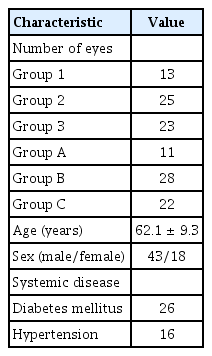
연구 대상 환자들은 평균 연령 62.1 ± 9.3세였으며, 남성 43명 43안, 여성 18명 18안이었으며(Table 1), 안축장의 길이와 전방깊이의 관계는 양의 상관관계를 보였다(Fig. 2). 피브린 접착제를 이용한 공막 내 인공수정체고정술의 효과에 대해 알아보기 위해 측정된 전체 대상 환자들의 평균을 기준으로 하여 구분하였다. 안축장의 길이에 따라 1군(< 23 mm), 2군(23-25 mm), 3군(> 25 mm)으로 나누었다. 또 전방깊이에 따라 A군(< 3.0 mm), B군(3.0-3.6 mm), C군(> 3.6 mm)으로 나누었다. 각 군의 술 전과 술 후의 최대교정시력은 Snellen 시력을 logarithm of the minimal angle resolution (logMAR)로 변환하여 비교 분석하였고, 구면값, 원주값, 구면렌즈대응치를 측정하여 비교 분석하였다. 모든 측정값은 술 전과 술 후 1, 6개월을 기준으로 하여 측정하여 비교분석하였다.

Scatterplot of the correlation between the axial length and the anterior chamber (A/C) depth. There is a positive correlation between the axial length and the anterior chamber depth.
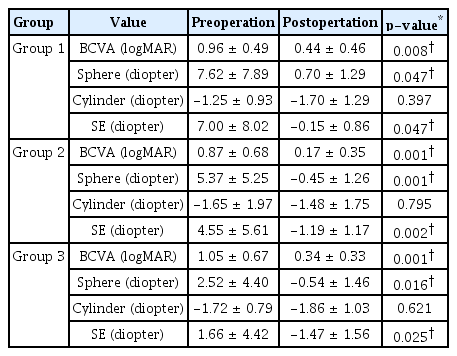
안축장 길이를 기준으로 나눈 군을 분석했을 때 술 전 최대교정시력(logMAR)은 1군에서 0.96 ± 0.49, 2군에서 0.87 ± 0.68, 3군에서 1.05 ± 0.67이었고, 술 후 최대교정시력(logMAR)은 1군에서 0.44 ± 0.46, 2군에서 0.17 ± 0.35, 3군에서 0.34 ± 0.33으로 모든 군에서 유의한 향상을 관찰할 수 있었다(p<0.05) (Table 2). 술 전 구면값(diopter, D)은 1군에서 7.62 ± 7.89 D, 2군에서 5.37 ± 5.25 D, 3군에서 2.52 ± 4.40 D였으며 술 후 구면값(D)은 1군에서 0.70 ± 1.29 D, 2군에서 -0.45 ± 1.26 D, 3군에서 -0.54 ± 1.46 D로 관찰되었으며 모든 군에서 유의한 차이를 관찰할 수 있었다(p<0.05) (Table 2). 술 전 구면렌즈대응치(spherical equivalent, D)는 1군에서 7.00 ± 8.02 D, 2군에서 4.55 ± 5.61 D, 3군에서 1.66 ± 4.42 D였으며, 술 후 구면렌즈대응치(spherical equivalent, D)는 1군에서 -0.15 ± 0.86 D, 2군에서 -1.19 ± 1.17 D, 3군에서 -1.47 ± 1.56 D로 확인되었으며 모든 군에서 유의한 차이를 관찰할 수 있었다(p<0.05) (Table 2).
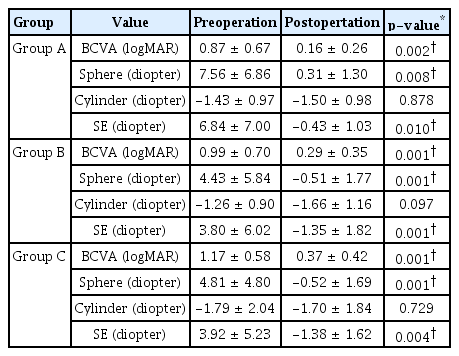
전방깊이를 기준으로 나눈 군을 분석했을 때 술 전 최대교정시력(logMAR)은 A군에서 0.87 ± 0.67, B군에서 0.99 ± 0.70, C군에서 1.17 ± 0.58이었고 술 후 최대교정시력(logMAR)은 A군에서 0.16 ± 0.26, B군에서 0.29 ± 0.35, C군에서 0.37 ± 0.42로 모든 군에서 유의한 향상을 관찰할 수 있었다(p<0.05) (Table 3). 술 전 구면값은 A군에서 7.56 ± 6.86 D, B군에서 4.43 ± 5.84 D, C군에서 4.81 ± 4.80 D였으며, 술 후 구면값은 A군에서 0.31 ± 1.30 D, B군에서 -0.51 ± 1.77 D, C군에서 -0.52 ± 1.69 D로 관찰되었으며 모든 군에서 유의한 차이를 관찰할 수 있었다(p<0.05) (Table 3). 술 전 구면렌즈대응치(spherical equivalent, D)는 A군에서 6.84 ± 7.00 D, B군에서 3.80 ± 6.02 D, C군에서 3.92 ± 5.23 D였으며, 술 후 구면렌즈대응치(spherical equivalent, D)는 A군에서 -0.43 ± 1.03 D, B군에서 -1.35 ± 1.82 D, C군에서 -1.38 ± 1.62 D로 확인되었으며 모든 군에서 유의한 차이를 관찰할 수 있었다(p<0.05) (Table 3).
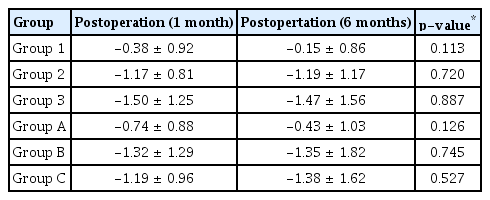
술 후 1개월과 술 후 6개월의 구면렌즈대응치를 비교 분석하였을 때 1군에선 -0.38 ± 0.92 D에서 -0.15 ± 0.86 D, 2군에선 -1.17 ± 0.81 D에서 -1.19 ± 1.17 D, 3군에선 -1.50 ± 1.25 D에서 -1.47 ± 1.56 D로 확인되었으며, 술 후 1개월과 술 후 6개월의 변화에서 모든 군에 유의한 차이가 없었다(p<0.05) (Table 4). 또한 A군에선 -0.74 ± 0.88 D에서 -0.43 ± 1.03 D, B군에선 -1.32 ± 1.29 D에서 -1.35 ± 1.82 D, C군에선 -1.19 ± 0.96 D에서 -1.38 ± 1.62 D로 확인되었으며 술 후 1개월과 술 후 6개월의 변화에서 모든 군에 유의한 차이가 없었다(p<0.05) (Table 4). 또한 술 후 6개월의 구면렌즈대응치를 비교 분석했을 때 1-3군의 각 군과의 비교 결과(p=0.321) 및 A-C군의 각 군과의 비교 결과(p=0.121)에서도 유의한 차이를 확인할 수 없었다.
모든 군에서 최대교정시력, 구면값, 구면렌즈대응치의 술 전후 유의미한 차이를 확인할 수 있었던 반면에 여섯 군 모두에서 술 전후 원주값은 유의한 차이가 없었다. 술 후 합병증으로는 Haptic slippage (7안), IOL dislocation (4안), Optic capture (1안)의 합병증이 발생함을 알 수 있었으며 안축장 및 전방깊이의 길이가 길어질수록 합병증 유발률이 높게 나타났다(Table 5).
고 찰
고령 인구의 증가로 백내장수술의 빈도가 증가하고, 술 후 합병증 중의 하나인 인공수정체 이탈의 발생 빈도가 증가하고 있다. 이에 따라 이탈된 인공수정체를 고정하는 수술 방법의 수요 또한 증가하게 되었으며, 현재까지 인공수정체의 종류와 다양한 수술 방법 등에 대한 연구, 수술 후 좋은 시력결과 및 예후와 수술 시간 단축으로 인한 합병증 방지 및 인공수정체 이탈 재발 방지 등에 대한 여러 연구들이 진행되어 왔다.
최근 인공수정체 공막봉합고정술은 모양체소대가 약한 환자, 이전의 수정체낭내적출술 또는 외상에 의해 수정체가 없는 무수정체안 환자, 이전에 삽입한 인공수정체가 탈구된 환자 그리고 백내장수술 중 후낭이나 섬모체소대가 심하게 손상된 환자 등 섬모체소대와 수정체낭의 지지가 충분하지 않은 환자에서 시행되고 있다. 인공수정체 공막봉합고정술은 초기에는 기술적으로 어렵고, 수술 시간도 오래 걸리며, 수술 중 모양체 통과에 따른 출혈의 위험이 많고, 각막부전, 지속적 안압상승, 황반부종, 유리체출혈, 망막박리, 맥락막상강출혈, 공막 봉합 고정에 의한 안내염, 봉합미란 등의 위험이 많은 것으로 보고되어 왔다. 하지만 이후 여러 가지 변형된 수술 방법들이 많이 제시되며 수술 기법이 발전함에 따라 현재는 수술의 안전성도 인정되고, 시력회복에 유용한 수술로 받아들여지고 있다[5-10].
일반적으로 인공수정체 공막봉합고정술은 인공수정체가 안구 내에서 중심에 정확하게 위치하기 위해서는 인공수정체의 지지부가 안정적이고 대칭적으로 고정되어야 하지만, 공막봉합고정술 시 인공수정체는 온전한 수정체낭의 충분한 지지를 받지 못하고, 몇 개의 매듭으로만 고정이 되는 단점이 있다[24,25]. 또한 인공수정체공막고정술에서 유리체절제술이 동시에 시행되면 공막 고정 시 정확한 위치에 안정적으로 인공수정체를 위치시키는 데 장애가 될 수 있는 유리체, 수정체 잔유물 및 증식성 막이 완전히 제거되기 때문에 난시 변화를 피할 수 있다고 기존 연구에서 설명하고 있다[26,27].
이처럼 인공수정체 위치의 불안정성 외에 유리체절제술의 시행 여부, 봉합사의 공막 관통 부위의 불일치, 지지부 봉합사의 뒤틀림, 봉합사 장력의 비대칭 등 수술 후 인공수정체의 편위에 영향을 미치므로 이와 같은 요소들이 공막봉합고정술 후 인공수정체의 기울어짐이나 중심이탈의 원인이 될 것이라 예측할 수 있다. 인공수정체의 기울어짐이나 중심이탈은 수술 후 굴절이상을 크게 하고, 시력에도 영향을 미칠 수 있으므로, 수술 시 봉합사의 위치 선정에 주의해야 하고, 동일한 장력으로 봉합사를 당겨야 하며, 봉합사의 공막 고정에까지 세심한 주의를 기울여야 한다. 굴절력 변화는 공막고정 봉합의 위치와 환자의 모양체 고랑의 위치, 인공수정체 도수를 구하는 기술의 차이, 수술 술기에 따른 개인차가 있을 수 있다.
공막절편을 만들어 인공수정체의 지지부를 절편 아래에 조직접착제를 이용하여 접착시켜 고정하는 방법이나 공막봉합사를 공막층 내로 지그재그 형태로 통과시켜 매듭 없이 고정하는 방법과 같은 무봉합 인공수정체공막고정술은 봉합 인공수정체공막고정술에 비해 공막고정사 이완으로 인한 인공수정체 기울어짐, 중심이탈과 같은 합병증이 발생할 가능성이 상대적으로 크고, 공막고정사 이완으로 인하여 난시, 고위 구면수차가 발생해 시기능 및 품질 저하가 발생할 수 있다고 보고되고 있다[28,29]. 본 연구에서는 앞서 서술한 방법에서 생길 수 있는 단점인 공막절편을 만드는 과정이나 공막에 봉합을 하는 과정에서 소모되는 시간적 효율성의 저하를 극복하기 위해 공막고랑에 인공수정체의 지지부를 삽입한 후 조직접착제를 이용하여 인공수정체의 안정적인 고정을 유도하는 방법을 시도하였다(Fig. 1). 또한 술 후 1개월, 술 후 6개월까지 시간 변화를 추적 관찰하여 술 후 인공수정체의 상태 및 환자의 시기능의 변화를 분석했다.
수술에 사용한 조직 접착제는 조직 부착 시 봉합사를 대신할 수 있는 방법으로, 부착과 관련된 수술 시간의 감소, 봉합에 의한 여러 가지 합병증 등을 줄일 수 있는 것으로 알려져 있어 안과 영역에서는 안성형수술에서 연부조직의 부착, 사시수술에서 결막부착, 녹내장여과수술 후 누출의 폐쇄, 양막이식술, 결막이완증, 익상편수술 등에서 다양하게 이용되었다. 조직접착제는 시아노아크릴과 같은 합성조 직접착제와 피브린과 같은 생체조직접착제로 구분될 수 있다. 합성조직접착제는 강한 부착력을 가지지만 독성, 이물반응이 심해 사용이 제한적인 것에 반하여 본 연구에 사용한 피브린과 같은 생체조직접착제는 염증 반응 및 독성이 적고 불규칙한 표면에서도 사용이 가능한 장점이 있어 널리 이용되고 있다. 피브린 접착제는 피브리노겐, 트롬빈 두 가지 주사액으로 구성되어 있는데 조직 접합 시 이러한 두 가지 성분을 같은 양으로 섞으면 피브리노겐이 피브린으로 변형되면서 혈액응고인자 XIII에 의하여 피브린이 교차 결합되어 피브린 복합체의 피브린 응괴가 형성되는 원리를 이용한다[13-17].
최근 수술 기법의 발전과 인공수정체 도수계산 공식의 발전으로 인하여 술 후의 굴절력 예측이 보다 정확해졌으며, 술 후 굴절 상태에 대한 예측과 결과가 환자의 수술 만족도에도 큰 영향을 미치게 되었다. 수술 후에 시기능을 판단하는 척도에는 눈부심 등 주관적 증상의 여부, 대비감도의 변화, 원주값 등 여러 가지가 있겠지만, 그중에서 술 후 굴절력이 가장 중요한 척도이며 따라서 술 후 굴절 상태에 대한 평가가 중요하다. 이전 연구에 따르면 수술 후 전방깊이와 안축장의 크기는 비례관계에 있다고 보고되었으며, 술 전 전방깊이가 얕거나 안축장이 짧은 경우에는 술 후 전방깊이가 더 얕게 형성되어 근시 편위를 보이고 긴 경우에는 술 후 전방깊이가 더 깊게 형성되어 원시 편위를 보였다. 이를 통해 안축장이 짧은 안이 긴 안에 비해서 술 후 전방깊이가 상대적으로 예상 정도보다 큰 변화를 일으키는 원인으로 생각하였다. 실제로 안축장이 짧고, 전방깊이가 얕은 경우 술 후 통계적으로 유의하게 큰 굴절이상을 보였다고 한다[30]. 짧은 안축장에서는 작은 측정 오류도 큰 굴절 이상을 유발하게 되므로, 짧은 안축장을 가진 환자, 특히 전방깊이가 얕은 눈에서는 술 전 측정 오류의 가능성을 꼭 감안해야 한다[31,32].
본 연구 결과로 인공수정체 이탈 환자에 대한 치료로 피브린 접착제를 이용한 공막 내 인공수정체고정술은 수술의 편의성을 높일 수 있는 장점이 있으며 봉합사를 이용한 공막고정의 단점인 인공수정체의 뒤틀림, 봉합사의 노출, 봉합사의 분해로 인한 합병증을 줄일 수 있는 것으로 생각된다. 피브린 접착제를 이용한 공막 내 인공수정체고정술 후 최대교정시력, 구면값, 구면렌즈대응치의 유의한 향상으로 시력호전 효과를, 술 후 원주값의 유의한 변화가 없음으로 인공수정체의 뒤틀림과 난시의 유발이 낮음을 추정할 수 있었다. 또한 안축장의 길이와 전방깊이의 차이를 고려했을 때 술 후 최대교정시력, 구면값, 구면렌즈대응치의 유의한 향상을 보였으며 이는 시력호전의 효과가 있음을 확인하였다. 술 후 1개월과 술 후 6개월의 시기능 품질을 대변할 수 있는 구면렌즈대응치를 비교하였을 때 그 변화가 크지 않았음을 통해 장기적인 시기능 품질의 안정성을 기대할 수 있는 술기로 생각된다.
본 연구의 제한점으로는 연구가 후향적으로 진행되어 수술 후 환자가 장기간 경과 관찰되지 않아 단기 임상 결과밖에 얻을 수 없었기에 추가적인 합병증에 대한 평가가 불가능하였고 인공수정체의 기울어짐이나 중심이탈에 대한 합병증 평가를 위해 Purkinje image나 Scheimpflug imaging을 이용한 객관적 측정이 이루어지지 않은 점이 있다. 연구 분석에 포함된 모든 공막내 인공수정체고정술을 조직 접착제를 사용하여 시행한 환자에 한정하였기 때문에, 환자군의 수가 적다는 점과 임의로 군을 나누어 시기능 품질의 변화를 시간에 따라 비교 분석하였기에 다른 대조군과의 비교가 불가능하였다는 점도 있다. 따라서 더욱 유의한 결과를 얻기 위해서는 더 많은 환자를 대상으로 연구를 시행하고 대조군으로 봉합사를 이용한 환자군을 선정하여 전향적으로 계획된 연구가 필요할 것이라 생각된다.
이전 연구에 따르면 봉합사를 사용한 공막고정술군에서 술 후 염증(48%), 안압상승(40%), 각막부종(32%), 유리체출혈(12%)의 합병증과 공막사 노출(2안)을 보였으며 무봉합 공막고정술군에서 술 후 염증(16%), 안압상승(16%), 각막부종(16%), 유리체출혈(12%)의 합병증과 인공수정체 지지부 노출(1안)을 보였음이 보고되었다[33]. 본 연구에서는 술 후 합병증으로 haptic slippage (11%), IOL dislocation (7%), optic capture (2%)로 확인되었으며 이는 본 연구에서 사용된 술기의 경우 수술적 편의를 도모하여 수술 시간의 단축을 기대할 수 있고, 봉합사 사용으로 인한 염증 유발의 위험성이 적어 나타난 결과로 추측된다. 반면 안축장의 길이가 증가함에 따라 인공수정체의 안정적인 고정과 관련된 합병증이 증가함을 확인할 수 있었으며, 이는 술기에 사용된 인공수정체의 전체 직경은 일정한데 비하여 수술 환자의 안구길이가 길어질수록 인공수정체의 전체 직경이 증가하는 형태로 잡아당겨져 공막 내에 고정되므로 안정성 측면에 영향을 주었을 것으로 추측된다. 이를 바탕으로 안축장의 길이가 긴 환자에서 인공수정체의 안정적인 고정을 도모할 수 있는 방법에 대한 추가 연구가 필요할 것이다.
또한 기본적으로 백내장수술의 기왕력이 있는 환자에서 안축장과 전방깊이의 정확한 측정에 변수가 있다는 점도 고려해야 한다. 실제 IOL master®이 기존의 접촉식 초음파에 비해 정확한 생체계측이 가능하다고 보고되었지만 검사 당시 환자의 협조도에 따라 결과가 달라질 수 있는 변수가 존재한다. 주시에 따라 발생하는 조절에 의해 수정체의 이동이 유발되고 그로 인하여 광학축과 시축의 차이가 생겨 측정 오차가 발생할 수 있다는 점도 고려해야 한다.
술기의 특성을 고려하였을 때 인공수정체가 온전한 수정체낭의 안정적인 지지를 받지 못하는 상태이고 실제로 예상했던 위치에 정확하게 위치시키는 것이 어렵다는 변수도 있다. 술기에 사용한 인공수정체는 MN60AC AcrySof® (Alcon Inc.)으로 광학부 직경은 6.0 mm, 전체 직경은 13.0 mm의 형태로 공막고정술에 사용되는 인공수정체의 지지부의 특성이 제품군에 따라 형태, 길이, 폭 등 다양한 요소에서 차이가 있다는 점도 오차에 영향을 줄 수 있다. 또한 술기 중 결막부착을 위해 피브린 접착제를 사용하였는데, 생체조직접착제는 수일에서 수주간 뛰어난 생적합성, 생분해성을 보이며 염증 반응을 일으키지 않고 독성이 적은 편이지만 대부분 단백질 추출물로 이루어져 있기 때문에 잠재적으로 면역 반응을 일으킬 위험이 있어 술 후 생길 수 있는 합병증에 대한 지속적인 관찰을 고려해야 한다. 결론적으로 조직접착제를 사용한 공막내 인공수정체고정술은 안축장의 길이와 전방깊이의 측정값 차이를 고려하였을 때 비교적 안정적인 임상경과를 보임을 연구를 통해 확인할 수 있었으며, 환자의 상태를 고려해 공막내 인공수정체고정술을 시행할 때 봉합사를 사용한 술기가 어려운 상황에서 선택할 수 있는 대체 술기로 사용할 수 있음을 확인할 수 있었다.
Notes
Conflict of Interest
The authors have no conflicts to disclose.
References
Biography
손현우 / Hyeon Woo Son
메리놀병원 안과
Department of Ophthalmology, Maryknoll Hospital