 |
 |
| J Korean Ophthalmol Soc > Volume 62(5); 2021 > Article |
|
ĻĄŁļ¼Ėņ┤łļĪØ
ļ¬®ņĀü
ļ░▒ļé┤ņןņłśņłĀ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ļ│ĆĒÖöņÖĆ ņØ┤ņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö ņ×äņāüņĀü ņÜöņØĖļōżņŚÉ ļīĆĒĢ┤ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
ļīĆņāüĻ│╝ ļ░®ļ▓Ģ
ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”Ø ņŚåņØ┤ ņ┤łņØīĒīīņłśņĀĢņ▓┤ņ£ĀĒÖöņłĀ ļ░Å ņØĖĻ│ĄņłśņĀĢņ▓┤ņéĮņ×ģņłĀņØä ņŗ£Ē¢ēĒĢ£ ņ┤Ø 62ļ¬ģ ĒÖśņ×É, 95ņĢłņØä ļīĆņāüņ£╝ļĪ£ ĒøäĒ¢źņĀü ņØśļ¼┤ĻĖ░ļĪØ ļČäņäØņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņłśņłĀ ņĀä, ņłśņłĀ 1ņŻ╝ Ēøä, 1ļŗ¼ Ēøä, 2ļŗ¼ ĒøäņØś ņØ┤ļ»Ėņ¦Ćņ”ØĻ░Ģ-ļ╣øĻ░äņäŁļŗ©ņĖĄņ┤¼ņśüņØś ļŗ©ļ®┤ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦Ćņłśļź╝ ĻĄ¼ĒĢśņśĆļŗż. ļ¦łņĘ© ļ░®ļ▓Ģ, ļŗ╣ļć©/Ļ│ĀĒśłņĢĢņØś ņ£Āļ¼┤, ņ┤łņØīĒīī ņäĖĻĖ░/ņŗ£Ļ░äņŚÉ ļö░ļźĖ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦Ćņłś ļ│ĆĒÖöņØś Ļ┤ĆĻ│äļź╝ ļČäņäØĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ļ¦łņĘ© ļ░®ļ▓Ģ, ļŗ╣ļć©/Ļ│ĀĒśłņĢĢņØś ņ£Āļ¼┤ņŚÉ Ļ┤ĆĻ│äņŚåņØ┤ ņłśņłĀ ņĀäĻ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ņłśņłĀ 1ņŻ╝ ĒøäĻ╣īņ¦Ć ņ”ØĻ░ĆĒĢ£ ņØ┤ĒøäļĪ£ 2ļŗ¼Ļ╣īņ¦Ć ņłśņłĀ ņĀä ņłśņżĆņ£╝ļĪ£ Ļ░ÉņåīĒĢśņśĆļŗż. ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ņĀÉņĢłļ¦łņĘ©ļź╝ Ē¢łĻ▒░ļéś ĻĖ░ņĀĆņ¦łĒÖśņØ┤ ņŚåļŹś ĻĘĖļŻ╣ņŚÉņä£ ņłśņłĀ ņĀäĻ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ņłśņłĀ 1ļŗ¼ ĒøäĻ╣īņ¦Ć ņ”ØĻ░ĆĒĢśņśĆļŗżĻ░Ć ņØ┤Ēøä ņłśņłĀ ņĀä ņłśņżĆņ£╝ļĪ£ Ļ░ÉņåīĒĢśņśĆņ£╝ļéś, ņłśņłĀ ņĀä ĻĄ¼Ēøäļ¦łņĘ©ļź╝ ņŗ£Ē¢ēĒ¢łĻ▒░ļéś ļŗ╣ļć©ļéś Ļ│ĀĒśłņĢĢņØ┤ ņ׳ļŹś ĻĘĖļŻ╣ņØś ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ņłśņłĀ ņĀäĻ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ņłśņłĀ 2ļŗ¼ ĒøäĻ╣īņ¦Ć ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśņśĆļŗż.
ABSTRACT
Purpose
To investigate clinical factors affecting subfoveal choroidal thickness (SFCT) and choroidal vascularity index (CVI) after cataract surgery.
Methods
A retrospective medical record review was performed of 62 patients (95 eyes) who underwent cataract surgery. The SFCT and CVI were calculated based on cross-section measurements obtained from enhanced depth imaging-optical coherence tomography preoperatively and postoperatively at 1 week, 1 month, and 2 months. The changes in SFCT and CVI were analyzed with respect to anesthesia, diabetes mellitus (DM), hypertension (HTN), and phaco power/time.
Results
Regardless of anesthesia, DM, or HTN, SFCT had increased at 1 week postoperatively and continued to decrease up to 2 months postoperatively. In the case of topical anesthesia and patients without DM or HTN, the CVI was significantly higher at 1 month postoperatively, but was followed by a steady reduction up to the 2-month follow-up. In the case of retrobulbar anesthesia and patients with DM or HTN, the CVI increased up to 2 months postoperatively.
ņ┤łņØīĒīīņłśņĀĢņ▓┤ņ£ĀĒÖöņłĀņØä ņØ┤ņÜ®ĒĢ£ ļ░▒ļé┤ņןņłśņłĀņØĆ ņĢłĻ│╝ņŚÉņä£ ļ¦żņÜ░ ĒØöĒĢśĻ▓ī ņØ┤ļŻ©ņ¢┤ņ¦ĆļŖö ņłśņłĀņØ┤ļŗż[1]. ļ¦źļØĮļ¦ēņØĆ Ļ▓░ņ▓┤ņĪ░ņ¦ü, ņŗĀĻ▓ĮĻ│╝ ļ®£ļØ╝ļŗīņäĖĒżļ┐ÉņĢäļŗłļØ╝ ļ¦Øļ¦ē ņÖĖņĖĄņŚÉ ņśüņ¢æĻ│╝ ņé░ņåīļź╝ Ļ│ĄĻĖēĒĢśļŖö ĒÆŹļČĆĒĢ£ ĒśłĻ┤Ćņ£╝ļĪ£ ņØ┤ļŻ©ņ¢┤ņĀĖ ņ׳ļŗż[2,3]. ņĄ£ĻĘ╝ enhanced depth imaging (EDI) optical coherence tomography (OCT)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļ¦źļØĮļ¦ēņØś ĻĖ░ņ¦łĻ│╝ ĒśłĻ┤ĆņĖĄņŚÉ ļīĆĒĢ£ Ļ┤Ćņ░░ņØ┤ Ļ░ĆļŖźĒĢ┤ņ¦Ćļ®┤ņä£ ļ¦źļØĮļ¦ēņØś ļ│ĆĒÖöņŚÉ ļīĆĒĢ£ ļŗżņ¢æĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż[4,5]. ĒŖ╣Ē׳, ņĢłĻ│╝ņŚÉņä£ Ļ░Ćņן ĒØöĒĢśĻ▓ī ņŗ£Ē¢ēļÉśļŖö ļ░▒ļé┤ņןņłśņłĀ ĒøäņŚÉ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗ś ļ░Å ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņŚÉ ļīĆĒĢ┤ ļŗżņ¢æĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ ņ׳ļŗż[1,6-12]. ņ¢┤ļ¢ż ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ░▒ļé┤ņןņłśņłĀ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśĻ░Ć ņ”ØĻ░ĆĒĢ£ļŗżļŖö Ļ▓░Ļ│╝Ļ░Ć ņ׳ļŗż[1,6,8,11,12]. ĻĘĖļ¤¼ļéś ņØ╝ļČĆņŚÉņä£ļŖö ļ│ĆĒÖöĻ░Ć ņŚåļŗżļŖö ņāüļ░śļÉ£ Ļ▓░Ļ│╝Ļ░Ć ņ׳ņ¢┤ ņĢäņ¦üĻ╣īņ¦Ć ņĀĢļ”ĮļÉ£ Ļ▓░Ļ│╝ļŖö ņŚåļŗż[7,9,10]. ļśÉĒĢ£, ļ░▒ļé┤ņןņłśņłĀ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ļ│ĆĒÖöņŚÉ ļīĆĒĢ£ ņÜöņØĖļōżņŚÉ Ļ┤ĆĒĢ£ ņŚ░ĻĄ¼ļŖö ņĢäņ¦üĻ╣īņ¦Ć ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåļŗż. ņØ┤ņŚÉ ļ│Ė ņĀĆņ×ÉļōżņØĆ ļ░▒ļé┤ņןņłśņłĀ ņĀä ļ¦łņĘ© ļ░®ļ▓Ģ, Ļ│ĀĒśłņĢĢĻ│╝ ļŗ╣ļć©, ĻĘĖļ”¼Ļ│Ā ņłśņłĀ ņżæ ņé¼ņÜ®ĒĢ£ ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņŗ£Ļ░ä Ļ░ÖņØĆ ņ×äņāüņĀü ņÜöņØĖļōżņØ┤ ļ░▒ļé┤ņןņłśņłĀ ĒøäņŚÉ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēņØś ļæÉĻ╗śņÖĆ ĒśłĻ┤Ć ņ¦ĆņłśņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņŚÉ ļīĆĒĢ┤ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
ļ│Ė ņĀĆņ×ÉļōżņØĆ 2019ļģä 1ņøöļČĆĒä░ 2019ļģä 11ņøöĻ╣īņ¦Ć Ļ░ĆĒå©ļ”ŁļīĆĒĢÖĻĄÉ ļČĆņ▓£ņä▒ļ¬©ļ│æņøÉņŚÉņä£ ĒĢ®ļ│æņ”Ø ņŚåļŖö ļŗ©ņł£ ļ░▒ļé┤ņןņŚÉ ļīĆĒĢ┤ ņ┤łņØīĒīīņłśņĀĢņ▓┤ņ£ĀĒÖöņłĀ ļ░Å Ēøäļ░®ļé┤ ņØĖĻ│ĄņłśņĀĢņ▓┤ņéĮņ×ģņłĀņØä ņŗ£Ē¢ēļ░øņØĆ ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ĒøäĒ¢źņĀüņ£╝ļĪ£ ņØśļ¼┤ĻĖ░ļĪØņØä ņĪ░ņé¼ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĒÖśņ×ÉņØś ņŚ░ĻĄ¼ ļÅÖņØśļź╝ ļ®┤ņĀ£ļ░øņĢśņ£╝ļ®░, Ļ░ĆĒå©ļ”ŁļīĆĒĢÖĻĄÉ ļČĆņ▓£ņä▒ļ¬©ļ│æņøÉ ņ×äņāüņŚ░ĻĄ¼ņŗ¼ņØśņ£äņøÉĒÜī(Insititutional Review Board, IRB)ņØś ņŖ╣ņØĖņØä ļ░øņĢä ņ¦äĒ¢ēļÉśņŚłļŗż(IRB ņŖ╣ņØĖ ļ▓łĒśĖ: HC20RASI0089). ļ¬©ļōĀ Ļ│╝ņĀĢņØĆ ĒŚ¼ņŗ▒ĒéżņäĀņ¢Ė(Declaration of Helsinki)ņØä ņżĆņłśĒĢśņśĆļŗż.
ļ░▒ļé┤ņןņłśņłĀņØĆ 5ļģä ņØ┤ņāüņØś ņłśņłĀ Ļ▓ĮĒŚśņØä Ļ░Ćņ¦ä ņłÖļĀ©ļÉ£ ņłĀņ×É 2ņØĖņŚÉ ņØśĒĢ┤ ņŗ£Ē¢ēļÉśņŚłļŗż. ļ░▒ļé┤ņןņłśņłĀņŚÉ ņØ┤ņÜ®ļÉ£ ņØĖĻ│ĄņłśņĀĢņ▓┤ļŖö ļ¬©ļæÉ Tecnis 1-Piece aspheric acrylic posterior chamber intraocular lens (ZCB00┬«; Johnson & Johnson, Inc. Santa, CA, USA)ļź╝ ņé¼ņÜ®ĒĢśņśĆļŗż. ņłśņłĀ ņĀäĒøäņÖĆ ņłśņłĀ ļÅäņżæņŚÉ ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”ØņØĆ ļ░£ņāØĒĢśņ¦Ć ņĢŖņĢśļŗż. ņłśņłĀ ņŗ£Ļ░äņØĆ ļīĆļץ 15-20ļČäĻ░Ćļ¤ē ņåīņÜöļÉśņŚłļŗż. ņłśņłĀ ņĀä ļ¦łņĘ©ļŖö ņĀÉņĢłļ¦łņĘ© Ēś╣ņØĆ ĻĄ¼Ēøäļ¦łņĘ©ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņĀÉņĢłļ¦łņĘ©ļŖö Proparacaine hydrochloride 0.5% (Alcaine┬«; Novartis, Basel, Switzerland)ļź╝ ņłśņłĀ ņ¦üņĀä 2-5ļ░®ņÜĖ ņłśņłĀņĢłņŚÉ ņĀÉņĢłĒĢśņśĆļŗż. ĻĄ¼Ēøäļ¦łņĘ©ļŖö Lidocaine hydrochloride 2% (Lidocaine┬«; Huons. Co. Ltd., Seongnam, Korea)ņÖĆ Bupivacaine Hydrochloride 0.5% (Pucaine┬«; REYON Pharmaceutical Co., Ltd., Seoul, Korea)ļź╝ 7:3 ļ╣äļĪ£ Ēś╝ĒĢ®ĒĢśņŚ¼ 1.5-2 mL Ļ░Ćļ¤ēņØä ĻĄ¼ĒøäņŚÉ ņŻ╝ņ×ģĒĢ£ Ēøä, 10-15ļČäĻ░Ćļ¤ē ļłłņØä ņĢĢļ░ĢĒĢśņśĆļŗż. Ļ░üļ¦ēņĀłĻ░£ļÅä 2.75 mm (Clear cut┬«; Alcon, Fort Worth, TX, USA)ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ Ēł¼ļ¬ģĻ░üļ¦ēņĀłĻ░£ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ņĀÉĒāäļ¼╝ņ¦łļĪ£ Hyaluronic acid 1.5% (Hyalu┬«; Hanmi Pharm Co. Ltd., Seoul, Korea)ļź╝ ņĀäļ░®ņŚÉ ņŻ╝ņ×ģĒĢśĻ│Ā ņøÉĒśĢņĀäļéŁņĀłĻ░£ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. ĒÅēĒśĢņŚ╝ņĢĪ(BSS┬«, Alcon, Fort Worth, TX, USA)ņØä ņé¼ņÜ®ĒĢśņŚ¼ ņłśļĀźļČäļ”¼ņłĀĻ│╝ ņłśļĀźļČäņĖĄņłĀņØä ĒĢśņśĆļŗż. ņłśņĀĢņ▓┤ņ£ĀĒÖöņłĀ ĻĖ░Ļ│ä(Infiniti┬«; Alcon, Fort Worth, TX, USA)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņłśņĀĢņ▓┤ļéŁ ļé┤ņØś ņłśņĀĢņ▓┤ļź╝ ņ£ĀĒÖöĒĢśĻ│Ā, ņ×öļźśĒö╝ņ¦łņØĆ Ļ┤ĆļźśĒØĪņ×ģĻĖ░ļĪ£ ņĀ£Ļ▒░ĒĢśņśĆļŗż. ņØĖĻ│ĄņłśņĀĢņ▓┤ļź╝ ņ╣┤ĒŖĖļ”¼ņ¦ĆņÖĆ ņŻ╝ņ×ģĻĖ░ņŚÉ ņןņ░®ĒĢśĻ│Ā ņłśņĀĢņ▓┤ļéŁ ļé┤ņŚÉ ņéĮņ×ģĒĢśņśĆļŗż. ņłśņłĀ Ēøä 1ļŗ¼Ļ░ä 0.5% Moxifloxacin hydrochloride (Vigamox┬«; Novartis, Basel, Switzerland)ņÖĆ Prednisolone acetate 1% (Predforte┬«; Allercan, Inc., Chicago, IL, USA)ļź╝ Ļ░üĻ░ü 4ĒÜī/ņØ╝ ņłśņłĀņĢłņŚÉ ņĀÉņĢłĒĢśņśĆļŗż.
ĒÖśņ×ÉņØś ļ¦źļØĮļ¦ēņØĆ ņłśņłĀ ņĀä, ņłśņłĀ 1ņŻ╝ Ēøä, 1ļŗ¼ Ēøä ĻĘĖļ”¼Ļ│Ā 2ļŗ¼ ĒøäņØś EDI-OCT ņ┤¼ņśüļ▓Ģ(Cirrus HDŌĆæOCT 4000┬«; Carl Zeiss Meditec AG, Inc., Dublin, CA, USA)4,5,13ņØä ņØ┤ņÜ®ĒĢśņŚ¼ Ļ▓Ćņé¼ĒĢśņśĆļŗż. ņäĀĒāØļÉ£ ņØ┤ļ»Ėņ¦ĆļŖö ImageJ ņåīĒöäĒŖĖņø©ņ¢┤(http://imagej.nih.gov/ij, version2.0.0-rc-69/1.52, National Institute of Health, Bethesda, MD, USA)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņØ┤ņ¦äĒÖö(Binarizaion)ĒĢśņśĆļŗż(Fig. 1) [14-17]. ļ¦źļØĮļ¦ēņØś ļ▓öņ£äļŖö OCT ņżæ ņŗ£ņŗĀĻ▓Įņ£ĀļæÉņÖĆ ĒÖ®ļ░śņśżļ¬®ņØä Ļ░ĆļĪ£ņ¦Ćļź┤ļŖö ļŗ©ļ®┤ņŚÉņä£ ļ¦Øļ¦ēņāēņåīņāüĒö╝ņØś ļ░öĻ╣źņ¬Į Ļ▓ĮĻ│äņŚÉņä£ Ļ│Ąļ¦ēņØś ņĢłņ¬Į Ļ▓ĮĻ│äļĪ£ ĒĢśņśĆļŗż[2]. OCT ļŗ©ļ®┤ņØś ļ¦źļØĮļ¦ē ļ▓öņ£ä ļé┤ņŚÉņä£ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗ś(subfoveal choroidal thickness), ļ¦źļØĮļ¦ēĒśłĻ┤Ćļé┤Ļ▓Į ļäōņØ┤(luminal area), ņĀäņ▓┤ ļ¦źļØĮļ¦ē ļäōņØ┤(total choroidal area) ļ░Å ļ¦źļØĮļ¦ēĒśłĻ┤Ćņ¦Ćņłś(choroidal vascularity index)ļź╝ ņĖĪņĀĢĒĢśņśĆļŗż(Fig. 1A) [14-17]. ņäĀĒāØļÉ£ OCT ļŗ©ļ®┤ņØä ImageJņØś Polygon toolņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĀäņ▓┤ ļ¦źļØĮļ¦ē ļäōņØ┤ļź╝ ņäĀĒāØĒĢśņśĆļŗż(Fig. 1B). ļ¬ģņĢöņØä ņĪ░ņĀĢĒĢśņŚ¼ region of interest (ROI) managerņŚÉ ņ×ģļĀźĒĢśņśĆĻ│Ā, ņØ┤ļ»Ėņ¦Ćļź╝ 8 bitļĪ£ ļ│ĆĒÖśĒĢśņŚ¼ NiblackŌĆÖs auto local thresholdļĪ£ ņØ┤ņ¦äĒÖöĒÖöņśĆļŗż(Fig. 1C). ņØ┤ņ¦äĒÖöļÉ£ ņØ┤ļ»Ėņ¦ĆļŖö RGB ņØ┤ļ»Ėņ¦ĆļĪ£ ļŗżņŗ£ ļ│ĆĒÖśĒĢśņŚ¼ Threshold color toolļĪ£ ņ¢┤ļæÉņÜ┤ ĒöĮņģĆņØä ROI managerņŚÉ ņĀĆņןĒĢśņśĆļŗż(Fig. 1D). ROI managerņŚÉ ņ×ģļĀźļÉ£ ņ┤Ø 2Ļ░Ćņ¦Ć ņØ┤ļ»Ėņ¦Ćļź╝ AND operationĒĢśņŚ¼ ļ¦źļØĮļ¦ēĒśłĻ┤Ćļé┤Ļ▓Į ļäōņØ┤ļź╝ ĻĄ¼ĒĢśņśĆļŗż(Fig. 1D). ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ļ¦źļØĮļ¦ēĒśłĻ┤Ćļé┤Ļ▓Į ļäōņØ┤ņÖĆ ņĀäņ▓┤ ļ¦źļØĮļ¦ē ļäōņØ┤ņØś ļ╣äļĪ£ ĻĄ¼ĒĢśņśĆļŗż(Fig. 1E). Ļ░ÖņØĆ ļ░®ļ▓Ģņ£╝ļĪ£ 95ņĢłņØś ļ¬©ļōĀ ņØ┤ļ»Ėņ¦Ćļź╝ Ļ│äņé░ĒĢśņśĆļŗż.
ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņŗ£Ļ░äņØĆ ņłśņłĀ Ēøä ņłśņĀĢņ▓┤ņ£ĀĒÖöņłĀ ĻĖ░Ļ│ä(Infiniti┬«, Alcon)ņŚÉņä£ ņĀ£Ļ│ĄļÉ£ ņĀĢļ│┤ļź╝ ņØ┤ņÜ®ĒĢśņśĆļŗż. ņ┤łņØīĒīīņØś ņäĖĻĖ░ļŖö ĒÖöļ®┤ņŚÉ ņĀ£Ļ│ĄļÉ£ equivalent average ultrasonic power Ļ░ÆņØä ņØ┤ņÜ®ĒĢśņśĆļŗż. ņ┤łņØīĒīīņØś ņŗ£Ļ░äņØĆ ĻĖ░Ļ│äņØś ĒÖöļ®┤ņŚÉ total longitudinal power on timeņØä ņé¼ņÜ®ĒĢśņśĆļŗż.
ĒåĄĻ│äņĀü ļČäņäØņØĆ SPSS version 23.0 (IBM Inc., Armonk, NY, USA) ņåīĒöäĒŖĖņø©ņ¢┤ļź╝ ņØ┤ņÜ®ĒĢśņśĆļŗż. ļ¬©ļōĀ ņĖĪņĀĢņ╣śņØś ĒÅēĻĘĀĻ░ÆņØä Ļ░üĻ░üņØś ļČäņäØņŚÉ ĒÖ£ņÜ®ĒĢśņśĆļŗż. ņłśņłĀ ņĀäĒøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ņĖĪņĀĢņ╣śļź╝ ļ╣äĻĄÉĒĢśĻĖ░ ņ£äĒĢ┤ ļ¦łņĘ© ļ░®ļ▓Ģ, ļŗ╣ļć©ņØś ņ£Āļ¼┤, ĻĘĖļ”¼Ļ│Ā Ļ│ĀĒśłņĢĢņØś ņ£Āļ¼┤ņŚÉ ļö░ļØ╝ ļīĆņØæĒæ£ļ│Ė t-Ļ▓ĆņĀĢņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņŗ£Ļ░äņŚÉ ĒØÉļ”äņŚÉ ļö░ļźĖ Ļ░ü ļ│Ćņłś(ļ¦łņĘ© ļ░®ļ▓Ģ, ļŗ╣ļć©ņØś ņ£Āļ¼┤, ĻĘĖļ”¼Ļ│Ā Ļ│ĀĒśłņĢĢņØś ņ£Āļ¼┤)ņŚÉ ļö░ļØ╝ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ļ│ĆĒÖöņŚÉ ņ░©ņØ┤Ļ░Ć ņ׳ļŖöņ¦Ćļź╝ ĻĘĖļŻ╣ļ│äļĪ£ ļ╣äĻĄÉĒĢśĻĖ░ ņ£äĒĢ┤ Boferroniļ▓ĢņØä ņØ┤ņÜ®ĒĢ£ ļ░śļ│Ą ņĖĪņĀĢ ļČäņé░ļČäņäØ(repeated measures analysis of variance)ņØä ņé¼ņÜ®ĒĢśņśĆļŗż. ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśĻ░Ć ņłśņłĀ ņżæ ņé¼ņÜ®ĒĢ£ ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņŗ£Ļ░äĻ│╝ ņ¢┤ļ¢ż ņāüĻ┤ĆĻ┤ĆĻ│äļź╝ Ļ░¢ļŖöņ¦Ć ĒÖĢņØĖĒĢśĻĖ░ ņ£äĒĢ┤ Pearson ņāüĻ┤ĆĻ│äņłśļź╝ ņØ┤ņÜ®ĒĢśņśĆļŗż. ļ¬©ļōĀ Ļ▓ĮņÜ░ņŚÉņä£ p-valueĻ░Ć 0.05ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśļŗż ĒĢ┤ņäØĒĢśņśĆļŗż.
ņ┤Ø 62ļ¬ģņØś 95ņĢłņØ┤ ņŚ░ĻĄ¼ņŚÉ ĒżĒĢ©ļÉśņŚłļŗż. ļé©ņ×É ĒÖśņ×É 30ļ¬ģņØś 48ņĢł, ņŚ¼ņ×É ĒÖśņ×É 32ļ¬ģņØś 47ņĢłņØ┤ņŚłļŗż(Table 1). ņ¢æņĢłņØĆ 33ņĢłņØä ņĪ░ņé¼ĒĢśņśĆļŗż(Table 1). ĒÅēĻĘĀ ņŚ░ļĀ╣ņØĆ 68.0 ┬▒ 10.0ņäĖ(46-87ņäĖ)ņśĆļŗż(Table 1). ņØ┤ ņżæ 25ņĢł(26.3%)ņØĆ ņĀÉņĢłļ¦łņĘ©, 42ņĢł(44.2%)ņØĆ ĻĄ¼Ēøäļ¦łņĘ©ļź╝ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā, ļéśļ©Ėņ¦Ć 28ņĢł(29.5%)ņØĆ Ļ░ÖņØĆ ĻĖ░Ļ░ä ņłśņłĀņØä ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņØĆ ļ░śļīĆņĢłņØś ĻĖ░ļĪØņØä ĒÖĢņØĖĒĢśņśĆļŗż(Table 1). ņłśņłĀņØä ņŗ£Ē¢ēĒĢ£ 67ņĢł ņżæ ĻĖ░ņĀĆņ¦łĒÖśņ£╝ļĪ£ ļŗ╣ļć©Ļ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ļŖö 31ņĢł(46.3%)ņØ┤ņŚłĻ│Ā, Ļ│ĀĒśłņĢĢņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ļŖö 42ņĢł(62.7%)ņØ┤ņŚłļŗż(Table 1). ĻĄÉņ░©ļČäņäØņØä ņŗ£Ē¢ēĒĢśņŚ¼ ļ¦łņĘ© ļ░®ļ▓Ģ, ļŗ╣ļć©ņÖĆ Ļ│ĀĒśłņĢĢņØś ņ£Āļ¼┤ Ļ░äņŚÉ ņŚ░Ļ┤Ćņä▒ņØä ĒÖĢņØĖĒĢśņśĆņØä ļĢī, ņä£ļĪ£ ņ£ĀņØśĒĢ£ ņŚ░Ļ┤Ćņä▒ņØä ļ│┤ņØĖ Ļ▓āņØĆ ņŚåņŚłļŗż(Table 2).
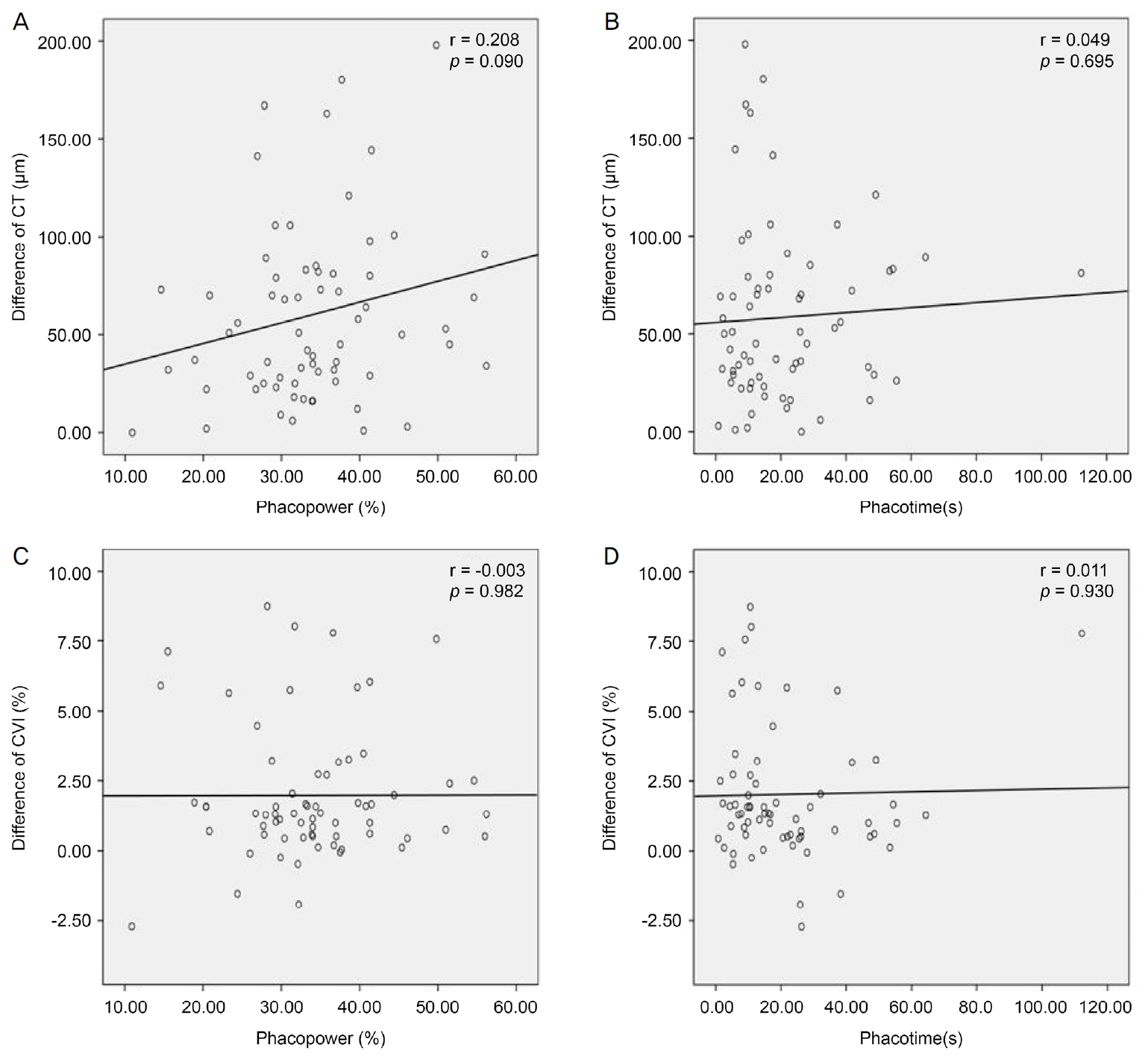
ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņØś ņŗ£Ļ░äņŚÉ ļö░ļźĖ ļ│ĆĒÖöļŖö ņłśņłĀĒĢ£ ņĀäņ▓┤ ļłłņŚÉņä£ ņłśņłĀ ņĀä 269.55 ┬▒ 42.86 ╬╝m, ņłśņłĀ 1ņŻ╝ Ēøä 328.48 ┬▒ 58.24 ╬╝m (p<0.001), 1ļŗ¼ Ēøä 324.24 ┬▒ 69.83 ╬╝m (p<0.001), 2ļŗ¼ Ēøä 313.31 ┬▒ 69.91 ╬╝m (p<0.001)ļĪ£ ņłśņłĀ 1ņŻ╝ ĒøäņŚÉ ņ”ØĻ░ĆĒĢ£ ņØ┤Ēøä ņ£ĀņØśĒĢśĻ▓ī Ļ░ÉņåīĒĢśļŖö Ļ▓░Ļ│╝ļź╝ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż(Table 3, Fig. 2A). ĒÖśņ×ÉĻĄ░ņØä ļ¦łņĘ© ļ░®ļ▓Ģ, Ļ│ĀĒśłņĢĢ ņ£Āļ¼┤ņŚÉ ļö░ļØ╝ ļéśļłäņŚłņØä ļĢīļŖö Ļ░ü ĻĄ░ ļé┤ņŚÉņä£ ņÜöņØĖņŚÉ ļö░ļźĖ ņ░©ņØ┤Ļ░Ć ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśņ¦Ćļ¦ī(Fig. 2B, D, Ļ░üĻ░ü p=0.421, p=0.281), ļŗ╣ļć© ņ£Āļ¼┤ņŚÉ ļö░ļØ╝ ļéś ļłäņŚłņØä ļĢīņŚÉļŖö ĻĘĖ ļ│ĆĒÖö ņ¢æņāüņØ┤ ļŗ╣ļć© ņ£Āļ¼┤ņŚÉ ļö░ļØ╝ ņ░©ņØ┤ļź╝ ļ│┤ņśĆļŗż(Fig. 2C, p=0.037). ļŗ╣ļć©Ļ░Ć ņŚåļŖö ĻĄ░ņŚÉņä£ļŖö ļ¦źļØĮļ¦ēļæÉĻ╗śņØś ļ│ĆĒÖöĻ░Ć ļŗ╣ļć©Ļ░Ć ņ׳ļŖö ĻĄ░ņŚÉņä£ ļ│┤ļŗż ņ£ĀņØśĒĢśĻ▓ī ņĀüĻ▓ī Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 2C).
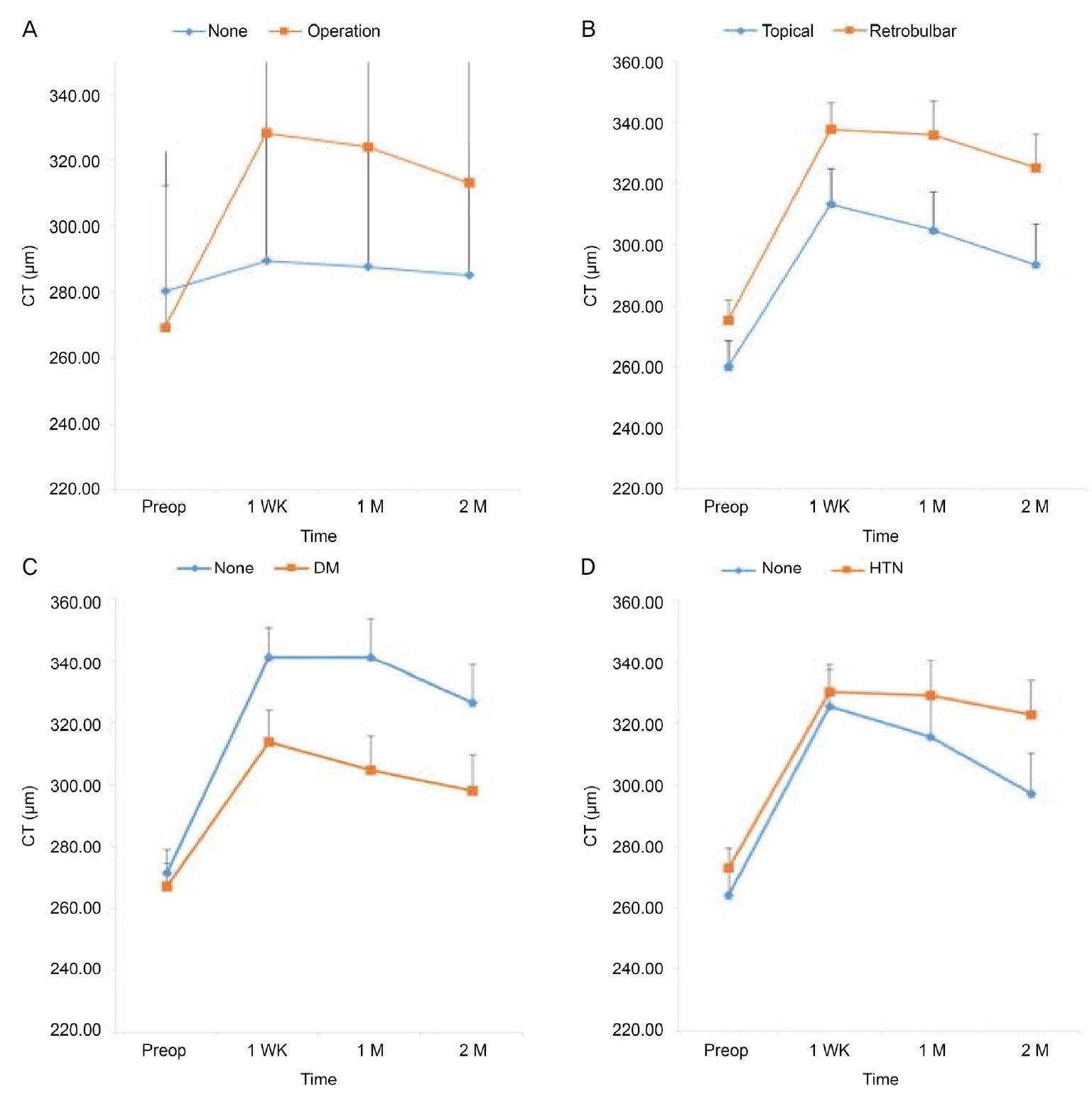
ĒÅēĻĘĀ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ņłśņłĀĒĢ£ ņĀäņ▓┤ ļłłņŚÉņä£ ņłśņłĀ ņĀä 59.82 ┬▒ 2.11%, ņłśņłĀ 1ņŻ╝ Ēøä 62.05 ┬▒ 1.79% (p<0.001), 1ļŗ¼ Ēøä 62.56 ┬▒ 1.95% (p<0.001), 2ļŗ¼ Ēøä 62.63 ┬▒ 2.28% (p<0.001)ļĪ£ ņłśņłĀ Ēøä ņ”ØĻ░ĆĒĢśļŖö ņ¢æņāüņØä ļ│┤ņśĆļŗż(Table 4, Fig. 3A). ņłśņłĀņØä ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņØĆ ļ░śļīĆņĢłņØś ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ņłśņłĀ Ēøä 1ņŻ╝ Ēøä, 1ļŗ¼ Ēøä ĻĘĖļ”¼Ļ│Ā 2ļŗ¼ ĒøäņØś ļ│ĆĒÖöļŖö ĒåĄĻ│äņĀüņ£╝ļĪ£ ļ¬©ļæÉ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśļŗż(Table 4, Ļ░üĻ░ü p=0.95, p=0.89, p=0.94) ļ¦łņĘ© ļ░®ļ▓ĢņŚÉ ļö░ļØ╝ ņłśņłĀ 1ņŻ╝ Ēøä, 1ļŗ¼ Ēøä ĻĘĖļ”¼Ļ│Ā 2ļŗ¼ ĒøäņØś ņłśņłĀ ņĀäĻ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ņĀÉņĢłļ¦łņĘ©ĻĄ░ņŚÉņä£ 2.49 ┬▒ 2.58%, 3.21 ┬▒ 2.55%, 2.83 ┬▒ 3.05%ļĪ£ ņłśņłĀ 1ļŗ¼ ĒøäņŚÉ ļ╣äĒĢ┤ 2ļŗ¼ ĒøäņŚÉ Ļ░ÉņåīĒĢśļŖö ņ£ĀņØśĒĢ£ ļ│ĆĒÖöļź╝ ļ│┤ņśĆņ£╝ļéś(Table 4, Fig. 3B, p<0.001), ņĀÉņĢłļ¦łņĘ©ņÖĆ ĻĄ¼Ēøäļ¦łņĘ©ļź╝ ņŗ£Ē¢ēĒĢ£ ĒÖśņ×É Ļ░äņŚÉ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦Ćņłś ļ│ĆĒÖö ņ¢æņāüņØś ņ░©ņØ┤ļŖö ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśļŗż(Fig. 3B, p=0.409). ļŗ╣ļć©ļéś Ļ│ĀĒśłņĢĢņØ┤ ņŚåļŖö ĒÖśņ×ÉĻĄ░ņŚÉņä£ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ņłśņłĀ 1ļŗ¼ ĒøäņŚÉ ļ╣äĒĢ┤ 2ļŗ¼ ĒøäņŚÉ Ļ░ÉņåīĒĢśļŖö ņ£ĀņØśĒĢ£ ļ│ĆĒÖöļź╝ ļ│┤ņśĆņ£╝ļéś(Table 4, Fig. 3C, D, p<0.001), ļŗ╣ļć©ļéś Ļ│ĀĒśłņĢĢņØ┤ ņ׳ļŖö ĒÖśņ×ÉĻĄ░Ļ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦Ćņłś ļ│ĆĒÖö ņ¢æņāüņØś ņ░©ņØ┤ļŖö ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśļŗż(Fig. 3D, Ļ░üĻ░ü p=0.682, p=0.10).
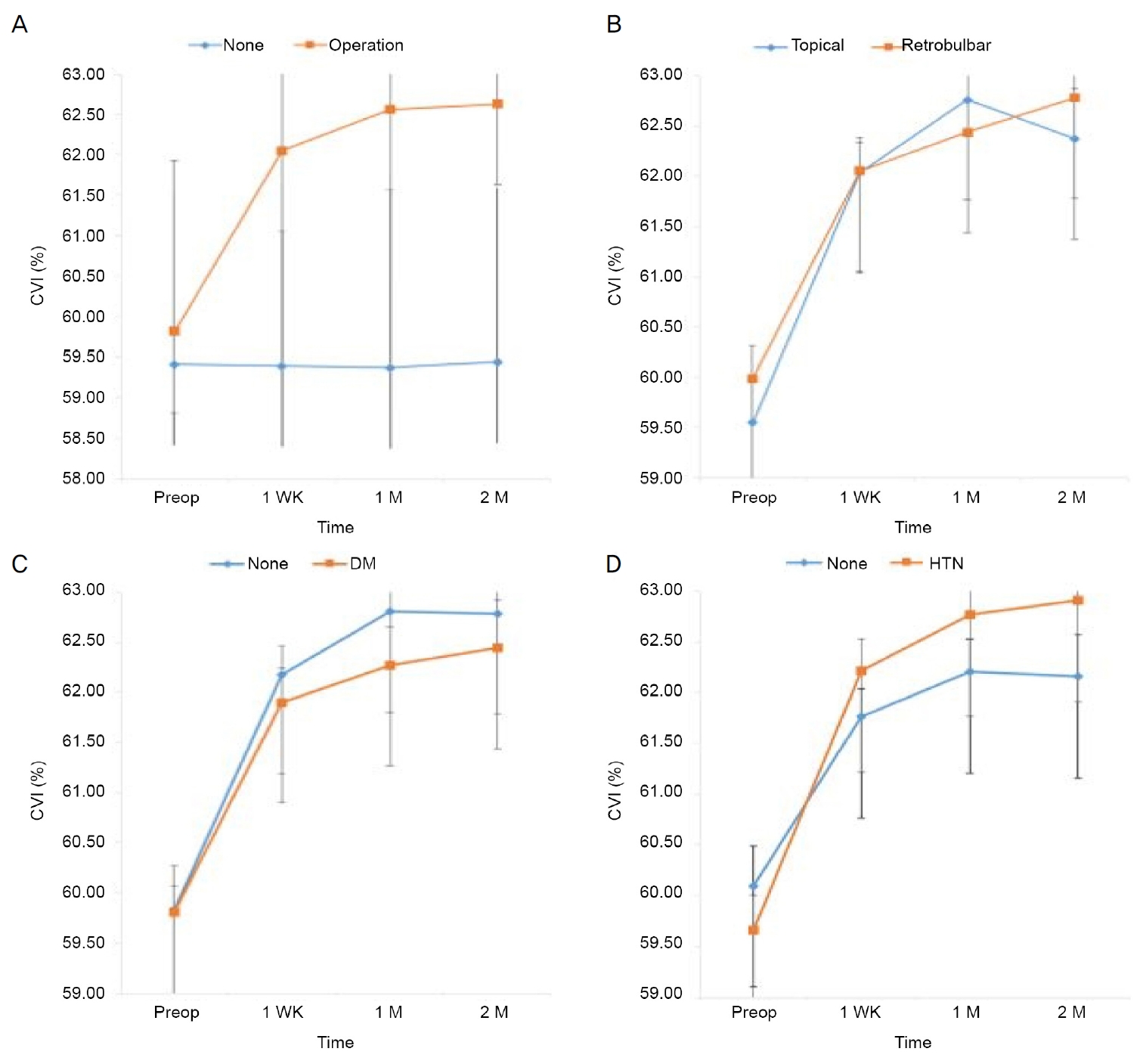
ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņłśņłĀ 1ņŻ╝ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗ś ļ│ĆĒÖöņØś Pearson ņāüĻ┤ĆĻ│äņłśļŖö 0.208ļĪ£ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśņ£╝ļ®░(Fig. 4A, p=0.090), ņ┤łņØīĒīīņØś ņŗ£Ļ░äĻ│╝ ņłśņłĀ 1ņŻ╝ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗ś ļ│ĆĒÖöņØś Pearson ņāüĻ┤ĆĻ│äņłśļŖö 0.049ļĪ£ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśļŗż(Fig. 4B, p=0.695). ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņłśņłĀ 1ņŻ╝ Ēøä ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦Ćņłś ļ│ĆĒÖöņØś Pearson ņāüĻ┤ĆĻ│äņłśļŖö -0.003ļĪ£ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśņ£╝ļ®░(Fig. 4C, p=0.982), ņ┤łņØīĒīīņØś ņŗ£Ļ░äĻ│╝ ņłśņłĀ 1ņŻ╝ Ēøä ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś Pearson ņāüĻ┤ĆĻ│äņłśļŖö 0.011ļĪ£ ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśļŗż(Fig. 4D, p=0.930).
ļ¦źļØĮļ¦ēņØĆ Ļ▓░ņ▓┤ņĪ░ņ¦ü, ņŗĀĻ▓Į, ļ®£ļØ╝ļŗīņäĖĒżĻ│╝ ĒśłĻ┤ĆļōżļĪ£ ņØ┤ļŻ©ņ¢┤ņ¦ä ņĪ░ņ¦üņ£╝ļĪ£ ļ¦Øļ¦ēņŚÉ ņśüņ¢æĻ│╝ ņé░ņåīļź╝ Ļ│ĄĻĖēĒĢĀ ļ┐É ņĢäļŗłļØ╝ ņĢłĻĄ¼ņØś ļīĆņé¼ņÖĆ ņś©ļÅäļź╝ ņĪ░ņĀłĒĢ┤ņŻ╝ļŖö ņżæņÜöĒĢ£ ņŚŁĒĢĀņØä ĒĢ£ļŗż[2,3,8,18]. ļ¦źļØĮļ¦ēņØś ļ│ĆĒÖöļŖö ņŚ░ļĀ╣Ļ┤ĆļĀ©ĒÖ®ļ░śļ│Ćņä▒, ļŗ╣ļć©ļ¦Øļ¦ēļ│æņ”Ø, ļ¦Øļ¦ēļČĆņóģ ĻĘĖļ”¼Ļ│Ā ņżæņŗ¼ņןņĢĪļ¦źļØĮļ¦Øļ¦ēļ│æņ”Ø ļō▒Ļ│╝ Ļ░ÖņØĆ ņŚ¼ļ¤¼ ļ¦Øļ¦ēņ¦łĒÖśļōżĻ│╝ Ļ┤ĆļĀ©ņØ┤ ņ׳ļŗż[1,8]. ņĄ£ĻĘ╝ EDI-OCTņØś ļ░£ņĀä ļŹĢļČäņŚÉ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗ś ļ░Å ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņŚÉ ļīĆĒĢ┤ņä£ļÅä ņŚ░ĻĄ¼ļōżņØ┤ ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż[1,3,6-12]. ĒĢśņ¦Ćļ¦ī ļ│┤Ļ│ĀļÉśļŖö Ļ▓░Ļ│╝ļōżņŚÉ ņ░©ņØ┤Ļ░Ć ņ׳ļŗż. Chen et al [1]ņØĆ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśĻ░Ć ņłśņłĀ Ēøä 3ļŗ¼Ļ╣īņ¦Ć ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢśĻ▓ī ņ”ØĻ░ĆĒĢ£ļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░, Ohsugi et al [3]ņØĆ ņłśņłĀ ņ¦üĒøäļČĆĒä░ 1ņŻ╝Ļ╣īņ¦Ć ņ”ØĻ░ĆĒĢśļŗż ņØ┤Ēøä ļŗżņŗ£ Ļ░ÉņåīĒĢ£ļŗżĻ│Ā ĒĢśņśĆļŗż. ĒĢ£ĒÄĖ, Falc├Żo et al [9]ņØĆ ņłśņłĀ Ēøä 1ļŗ¼Ļ╣īņ¦Ć ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ļ│ĆĒÖöĻ░Ć ņŚåļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.
ņØ┤ņ▓śļ¤╝ ņØ┤ņĀä ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļōż ņé¼ņØ┤ņŚÉ ņ░©ņØ┤Ļ░Ć ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ, ļ│Ė ņĀĆņ×ÉļōżņØĆ ļ░▒ļé┤ņןņłśņłĀ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣Ā ņłś ņ׳ļŖö ņäĖļČĆ ĒĢŁļ¬®ļōżņØä ĻĄ¼ļČäĒĢśņŚ¼ ņłśņłĀ ņĀä, ņłśņłĀ 1ņŻ╝ Ēøä, ņłśņłĀ 1ļŗ¼ Ēøä ĻĘĖļ”¼Ļ│Ā ņłśņłĀ 2ļŗ¼ ĒøäņØś ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦Ćņłśļź╝ EDI-OCTļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļ│ĆĒÖöļź╝ ņĖĪņĀĢĒĢśņśĆļŗż. ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ¦źļØĮļ¦ēĒśłĻ┤ĆņĖĄņŚÉ ļ»Ėņ╣śļŖö ņÜöņØĖļōżņŚÉ Ļ┤ĆĒĢ£ ņŚ░ĻĄ¼ļŖö ņĢäņ¦üĻ╣īņ¦Ć ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåĻ│Ā ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś ļ│ĆĒÖöļŖö ņŚ¼ļ¤¼ ļ¦Øļ¦ēņ¦łĒÖśĻ│╝ Ļ┤ĆļĀ©ņØ┤ ņ׳ļŗż[1,8]. ļö░ļØ╝ņä£ ņ×äņāüņĀü ņÜöņØĖņŚÉ ļö░ļØ╝ ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ¦źļØĮļ¦ēĒśłĻ┤ĆņĖĄņØś ļ│ĆĒÖöļź╝ ņĢīņĢäļ│┤ļŖö Ļ▓āņØĆ ņČöĒøä ņŚ¼ļ¤¼ ļ¦Øļ¦ēņ¦łĒÖśņØś ņ£äĒŚśņØä ņĢīņĢäļ│╝ ņłś ņ׳ņ£╝ļ»ĆļĪ£ ņØśņØśĻ░Ć ņ׳ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ļ¦łņĘ© ļ░®ļ▓ĢĻ│╝ Ļ│ĀĒśłņĢĢ ņ£Āļ¼┤ņŚÉ Ļ┤ĆĻ│äņŚåņØ┤ ņłśņłĀ 1ņŻ╝ Ēøä ņ”ØĻ░ĆĒĢśņśĆļŗżĻ░Ć ņØ┤Ēøä Ļ░ÉņåīĒĢśļŖö ņ¢æņāüņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłņ£╝ļ®░, Ohsugi et al [3]Ļ│╝ ņ£Āņé¼ĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż[1,6,9]. ĒÖśņ×ÉĻĄ░ņØä ļ¦łņĘ© ņóģļźś ļ░Å Ļ│ĀĒśłņĢĢ ņ£Āļ¼┤ļĪ£ ļéśļłäņŚłņØä ļĢī ĻĘĖ ļ│ĆĒÖö ņ¢æņāüņØś ņ░©ņØ┤ļŖö ņ£ĀņØśĒĢśņ¦Ć ņĢŖņĢśņ¦Ćļ¦ī, ļŗ╣ļć©ņØś ņ£Āļ¼┤ļĪ£ ĒÖśņ×Éļź╝ ļ╣äĻĄÉĒĢśņśĆņØä ļĢī ĻĘĖļŻ╣ Ļ░äņŚÉļÅä ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņśĆļŗż. ņØ┤ļŖö ļŗ╣ļć©ņØś ņ£Āļ¼┤ņŚÉ ņāüĻ┤ĆņŚåņØ┤ ļ¦źļØĮļ¦ēļæÉĻ╗śĻ░Ć ņłśņłĀ Ēøä 3ļŗ¼Ļ╣īņ¦Ć ņ”ØĻ░ĆĒĢśļŖö ņ¢æņāüņØä ļ│┤ņśĆņ¦Ćļ¦ī, ļæÉ ĻĘĖļŻ╣ Ļ░äņŚÉ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗżļŖö Yip et al [6]Ļ│╝ļŖö ļŗżļźĖ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż. ĒĢśņ¦Ćļ¦ī ļ│Ė ņĀĆņ×ÉļōżņØĆ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļ¦īņØä ņĖĪņĀĢĒĢśņśĆņ¦Ćļ¦ī, Yip et al [6]ņØĆ ņżæņŗ¼ņÖĆņĢäļל, ļ╣äņĖĪĻ│╝ ņØ┤ņĖĪņ£╝ļĪ£ ņżæņŗ¼ņÖĆņĢäļלņŚÉņä£ 500 ╬╝m ļ¢©ņ¢┤ņ¦ä ņ¦ĆņĀÉĻ╣īņ¦Ć ņ┤Ø 3ņ¦ĆņĀÉņØś ļ¦źļØĮļ¦ēļæÉĻ╗śņØś ĒÅēĻĘĀĻ░Æņ£╝ļĪ£ Ļ│äņé░ĒĢśņśĆĻĖ░ņŚÉ ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ņÖĆ ņ░©ņØ┤Ļ░Ć ņ׳ņØä ņłś ņ׳ņ£╝ļ®░, ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśĻ╣īņ¦Ć ĒżĒĢ©ĒĢ£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļŹö ĒżĻ┤äņĀü ļ¦źļØĮļ¦ē ļ│ĆĒÖöļź╝ ĒÖĢņØĖ Ļ░ĆļŖźĒĢĀ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż.
ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ¦źļØĮļ¦ēņØś ļæÉĻ╗ś ļ│ĆĒÖöņŚÉ ļīĆĒĢ┤ ņĢäņ¦üĻ╣īņ¦Ć ĒÖĢņØĖļÉ£ ĻĖ░ņĀäņØĆ ņŚåļŗż. ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ░®ņłśņŚÉ ņ”ØĻ░ĆļÉ£ ĒöäļĪ£ņŖżĒāĆĻĖĆļ×Ćļöś, ņä▒ņןņØĖņ×É ļō▒ņØś ņŚ¼ļ¤¼ ņŚ╝ņ”ØņØĖņ×ÉĻ░Ć ņ£Āļ”¼ņ▓┤Ļ░ĢņØä ĒåĄĻ│╝ĒĢ£ Ēøä, ļ¦Øļ¦ēĻ│╝ ļ¦źļØĮļ¦ēņŚÉ ļÅäļŗ¼ĒĢśņŚ¼ ĒśłņĢĪļ¦Øļ¦ēņןļ▓Į(blood-retinal barrier)ņØä ĒīīĻ┤┤ĒĢśļ®┤ņä£ ļ¦źļØĮļ¦ēļæÉĻ╗śņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣£ļŗżĻ│Ā ņāØĻ░üļÉśĻ│Ā ņ׳ļŗż[1,3,19]. ļŗ╣ļć©Ļ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ ņØ┤ļ»Ė ņ£Āļ”¼ņ▓┤Ļ░Ģļé┤ proinflammatory ņé¼ņØ┤ĒåĀņ╣┤ņØĖņØś ņ”ØĻ░Ć ļō▒ņØś ļ│ĆĒÖöĻ░Ć ņØ╝ņ¢┤ļéś ņ׳ņ£╝ļ®░, ĒśłĻ┤ĆņØś Ēł¼Ļ│╝ņä▒ņØ┤ ļŹö ņĘ©ņĢĮĒĢśņŚ¼ ļŗ╣ļć©Ļ░Ć ņŚåļŖö Ļ▓ĮņÜ░ļ│┤ļŗż ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēņØś ļ│ĆĒÖöĻ░Ć ļŹö ņ£ĀņØśĒĢśĻ▓ī ļ░£ņāØĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üĒĢ┤ ļ│╝ ņłś ņ׳ļŗż. ļö░ļØ╝ņä£ ļŗ╣ļć©Ļ░Ć ņ׳ļŖö ĒÖśņ×ÉņŚÉņä£ ļ░▒ļé┤ņןņłśņłĀņØä ĒĢśņśĆņØä ļĢī ņŗĀņāØĒśłĻ┤Ć, ņŚ░ļĀ╣Ļ┤ĆļĀ©ĒÖ®ļ░śļ│Ćņä▒, ļŗ╣ļć©ļ¦Øļ¦ēļ│æņ”Ø, ļ¦Øļ¦ēļČĆņóģ ļō▒Ļ│╝ Ļ░ÖņØĆ ļ¦Øļ¦ēņ¦łĒÖśņØś ņ£äĒŚśņØ┤ ņ”ØĻ░ĆĒĢĀ Ļ▓āņØä ņāØĻ░üĒĢĀ ņłś ņ׳ļŗż[1,8].
ņĀÉņĢłļ¦łņĘ©ļź╝ ņŗ£Ē¢ēĒ¢łĻ▒░ļéś ļŗ╣ļć©ļéś Ļ│ĀĒśłņĢĢņØ┤ ņŚåļŖö ĒÖśņ×ÉĻĄ░ņØś ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ņłśņłĀ 1ņŻ╝ ņØ┤Ēøä ņ¦ĆņåŹņĀüņ£╝ļĪ£ Ļ░ÉņåīĒĢśņśĆĻ│Ā, ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ļ¬©ļæÉ ņłśņłĀ 1ļŗ¼ ĒøäĻ╣īņ¦Ć ņ£ĀņØśĒĢśĻ▓ī ņ”ØĻ░ĆĒĢśņśĆļŗżĻ░Ć Ļ░ÉņåīĒĢśļŖö ļ│ĆĒÖöļź╝ ļ│┤ņśĆļŗż. ĻĄ¼Ēøäļ¦łņĘ©ļź╝ ņŗ£Ē¢ēĒĢśĻ▒░ļéś ļŗ╣ļć©ļéś Ļ│ĀĒśłņĢĢņØ┤ ņ׳ļŖö ĒÖśņ×ÉĻĄ░ņŚÉņä£ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ņłśņłĀ 1ņŻ╝ ņØ┤Ēøä ņ¦ĆņåŹņĀüņ£╝ļĪ£ Ļ░ÉņåīĒĢśņ¦Ćļ¦ī ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ļ¬©ļæÉ ņłśņłĀ 2ļŗ¼Ļ╣īņ¦Ć ņ£ĀņØśĒĢśĻ▓ī ņ”ØĻ░ĆĒĢśņśĆļŗż. ņØ┤ņ▓śļ¤╝ ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ņ¢æņāüņØ┤ ņØ╝ņ╣śĒĢśņ¦Ć ņĢŖļŖö Ļ▓āņØĆ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ņłśņłĀ 1ņŻ╝ ĒøäļČĆĒä░ ņĀĢņāüĒÖöļÉśņ¦Ćļ¦ī, ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś ņ”ØĻ░ĆļÉ£ ņ┤Ø ļ®┤ņĀüņØĆ ņĀĢņāüĒÖöļÉśļŖö ļŹ░ ņŗ£Ļ░äņØ┤ ļŹö Ļ▒Ėļ”¼ĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ņāØĻ░üĒĢ┤ ļ│╝ ņłś ņ׳ļŗż.
ĻĘĖļÅÖņĢł ļ░▒ļé┤ņןņłśņłĀ ņØ┤Ēøä ļ¦źļØĮļ¦ēņØś ļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ļ│ĆĒÖöņŚÉ ļīĆĒĢ£ ņŚ¼ļ¤¼ ņŚ░ĻĄ¼ļōżņŚÉņä£ ņØ┤ļōż ļ│ĆĒÖö ņøÉņØĖņŚÉ ļīĆĒĢ£ Ļ░ĆņäżļĪ£ ņłśņłĀ ņżæ ņé¼ņÜ®ĒĢ£ ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņŗ£Ļ░äņØ┤ ņŚ░Ļ┤Ć ņ׳ņØä Ļ▓āņØ┤ļØ╝ļŖö ņØśļ¼ĖļōżņØä ņĀ£ņŗ£ĒĢśņśĆļŗż[1,6]. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņ┤łņØīĒīīņØś ņäĖĻĖ░ļéś ņŗ£Ļ░äņØĆ ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļéś ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ļ│ĆĒÖöņŚÉ ņśüĒ¢źņØä ņŻ╝ņ¦Ć ņĢŖņĢśļŗż. ņłśņłĀ ņżæ ļ░£ņāØĒĢśļŖö ļ¼╝ļ”¼ņĀü ņÜöņØĖņØĆ ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś ļ│ĆĒÖöņŚÉ ņśüĒ¢źņØä ņŻ╝ņ¦Ć ņĢŖņĢä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļéś, ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņŚÉļÅä ņśüĒ¢źņØä ņŻ╝ņ¦Ć ņĢŖļŖö Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż[1,19]. ĒĢśņ¦Ćļ¦ī ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņ┤łņØīĒīīņØś ņé¼ņÜ®ņØ┤ ĻĘ╣ļŗ©ņĀüņ£╝ļĪ£ ļ¦ÄņØĆ ņä▒ņłÖ ļ░▒ļé┤ņןņØĆ ļ░░ņĀ£ļÉśņŚłĻĖ░ņŚÉ ņØ┤ņŚÉ ļīĆĒĢ┤ņä£ļŖö ņČöĒøä ĒÖĢņØĖņØ┤ ļŹö ĒĢäņÜöĒĢśļŗż.
ļ│Ė ņŚ░ĻĄ¼ļŖö ļ¬ć Ļ░Ćņ¦Ć ĒĢ£Ļ│äņĀÉņØ┤ ņ׳ļŗż. ļ©╝ņĀĆ ĒøäĒ¢źņĀü ņØśļ¼┤ĻĖ░ļĪØ ļČäņäØņ£╝ļĪ£ ļ░▒ļé┤ņןņłśņłĀ ņĀäĒøä EDI-OCTņØś ĻĖ░ļĪØņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░Ļ░Ć ĒĢ£ņĀĢņĀüņØ┤ņŚłĻĖ░ņŚÉ, Ļ┤Ćņ░░ ļīĆņāüĻĄ░ņØ┤ 62ļ¬ģņØś 95ņĢłņ£╝ļĪ£ ņĀüļŗżļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż. ļæÉ ļ▓łņ¦ĖļĪ£, Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ĻĖ░Ļ░äņØ┤ ņłśņłĀ Ēøä 2Ļ░£ņøöļĪ£ ņ¦¦ļŗżļŖö ņĀÉĻ│╝ ĒÖśņ×ÉĻ░Ć Ļ░Ćņ¦ä Ļ│ĀĒśłņĢĢņØ┤ļéś ļŗ╣ļć©ņØś ņŚ¼ļČĆļ¦īņØä ĒÖĢņØĖĒĢśĻ│Ā ņ¦łĒÖśņØś ņżæņ”ØļÅäļéś ņĪ░ņĀł ņĀĢļÅäņŚÉ ļīĆĒĢśņŚ¼ ĒÖĢņØĖĒĢśņ¦Ć ņĢŖņĢśļŗżļŖö ĒĢ£Ļ│äņĀÉļÅä ņ׳ļŗż. ņäĖ ļ▓łņ¦ĖļĪ£ļŖö OCTļź╝ ņ┤¼ņśüĒĢśļŖö ņŗ£Ļ░äņØä ņØ╝ņĀĢĒĢśĻ▓ī ņĀĢĒĢĀ ņłś ņŚåņ¢┤ņä£ ĒÖśņ×É Ļ░äņØś ļ¦źļØĮļ¦ēņØś ņØ╝ņżæ ļ│ĆļÅÖņŚÉ ļīĆĒĢ┤ Ļ│ĀļĀżĒĢśņ¦Ć ļ¬╗ĒĢ£ ņĀÉļÅä ņØ┤ ņŚ░ĻĄ¼ņØś ĒĢ£Ļ│äņØ┤ļŗż[1-3,18,20]. ļäż ļ▓łņ¦ĖļĪ£, ĻĖ░ņłĀņĀüņØĖ ņĖĪļ®┤ņŚÉņä£ EDI-OCTņāüņŚÉņä£ ļ¦źļØĮļ¦ēņØś ļäōņØ┤ņÖĆ ĒśłĻ┤ĆņĖĄņØä ņåīĒöäĒŖĖņø©ņ¢┤ņāüņŚÉņä£ ņ×ÉļÅÖņ£╝ļĪ£ ņĖĪņĀĢĒĢĀ ņłś ņŚåĻ│Ā ņłśļÅÖņ£╝ļĪ£ ņĖĪņĀĢĒĢ┤ņĢ╝ Ē¢łļŗż[14-17]. ļśÉĒĢ£, OCT ņżæ ņŗ£ņŗĀĻ▓Įņ£ĀļæÉņÖĆ ĒÖ®ļ░śņśżļ¬®ņØä Ļ░ĆļĪ£ņ¦Ćļź┤ļŖö ļŗ©ļ®┤ļ¦īņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢņØä ĒĢśņśĆĻĖ░ņŚÉ ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś ĻĮłļ”¼ ĒśĢĒā£ļéś ĒśłĻ┤ĆņØś ĻĄ¼ļČĆļ¤¼ņ¦ä ļ®┤ņĀü ļō▒ņØĆ ļ░śņśüļÉśņ¦Ć ņĢŖņĢśļŗż. ļö░ļØ╝ņä£ ņĪ░ĻĖł ļŹö ļ¦ÄņØĆ ĒÖśņ×ÉĻĄ░ņØś 6Ļ░£ņøö ņØ┤ņāüņØś ļŹ░ņØ┤Ēä░Ļ░Ć ĒĢäņÜöĒĢśļ®░, ļ¦źļØĮļ¦ēņØś ņ×ģņ▓┤ņĀüņØĖ ļČĆļČäņØś ļ®┤ņĀüņØä ļ░śņśüĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ ĒĢäņÜöĒĢśļŗż[6,20].
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ░▒ļé┤ņןņłśņłĀ Ēøä, ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śņÖĆ ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśņØś ļ│ĆĒÖöņÖĆ ļ│ĆĒÖöņŚÉ ņśüĒ¢źņØä ņżä ņłś ņ׳ļŖö ļ¦łņĘ©ļ░®ļ▓Ģ, ļŗ╣ļć©ņÖĆ Ļ│ĀĒśłņĢĢņØś ņ£Āļ¼┤, ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņŗ£Ļ░ä ļō▒ ņ×äņāüņĀü ņÜöņØĖļōżĻ│╝ņØś Ļ┤ĆĻ│äļź╝ ņé┤ĒÄ┤ļ│┤ņĢśļŗż. ļ░▒ļé┤ņןņłśņłĀ Ēøä ņżæņŗ¼ņÖĆņĢäļל ļ¦źļØĮļ¦ēļæÉĻ╗śļŖö ņ×äņāüņĀü ņÜöņØĖĻ│╝ ņāüĻ┤ĆņŚåņØ┤ ņłśņłĀ ņĀäĻ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ņłśņłĀ 1ņŻ╝ Ēøä ņ”ØĻ░ĆĒĢśņśĆļŗżĻ░Ć ņØ┤Ēøä Ļ░ÉņåīĒĢśļŖö ņ¢æņāüņØä ļ│┤ņśĆĻ│Ā, ļ¦źļØĮļ¦ēĒśłĻ┤Ć ņ¦ĆņłśļŖö ņ×äņāüņĀü ņÜöņØĖņŚÉ ļö░ļØ╝ ņłśņłĀ 2ļŗ¼ ĒøäĻ╣īņ¦Ć ņ”ØĻ░ĆĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĒÖĢņØĖĒĢ£ ņ×äņāüņĀü ņÜöņØĖļōż ņżæņŚÉņä£ ļŗ╣ļć©ņØś ņ£Āļ¼┤Ļ░Ć ļ░▒ļé┤ņןņłśņłĀ Ēøä ļ¦źļØĮļ¦ēĒśłĻ┤ĆņØś ļ│ĆĒÖö ņ¢æņāüņŚÉ ņśüĒ¢źņØä ņŻ╝ļŖö ņÜöņØĖņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. ņłśņłĀ ņżæ ņé¼ņÜ®ĒĢ£ ņ┤łņØīĒīīņØś ņäĖĻĖ░ņÖĆ ņŗ£Ļ░äņØĆ ņłśņłĀ Ēøä ļ¦źļØĮļ¦ēĒśłĻ┤ĆņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØ┤ ņĀüņŚłļŗż.
Figure┬Ā1.
The technique of image binarization for choroid with Niblack auto local threshold tool. (A) The original enhanced depth imaging-optical coherence tomography scan. Choroidal thickness (red arrow). (B) The total choroidal area of scan passing thorough the fovea. (C) Image binarization by ImageJ. (D) The image was reconverted to RGB image showing dark areas (luminal area, red arrow) and light areas (stromal area, red arrowhead). (E) The binarized image over the original image.

Figure┬Ā2.
Mean choroidal thinckness (CT) in the change over time. Mean CT (╬╝m) depending on receiving operation, type of anesthesia, and the presence of diabetic mellitus (DM) or hypertension (HTN) before surgery, 1 week (WK), 1 month (M), and 2 months after surgery. There are significant changes over time (all p < 0.001). (A) CT increased and then decreased after 1 week, regardless of the operation received. There was a significant difference in the change over time between the two groups (p < 0.001). (B) CT increased and then decreased after 1 week, regardless of the type of anesthesia. There was no significant difference in the change over time between the two groups (p = 0.421). (C) CT increased and then decreased after 1 week, regardless of the presence of DM. There was a significant difference in the change over time between the two groups (p = 0.037). (D) CT increased and then decreased after 1 week, regardless of the presence of HTN. There was no significant difference in the change over time between the two groups (p = 0.281). Data was compared with preoperative value by repeated measure analysis of variance with BonferroniŌĆÖs method.
Figure┬Ā3.
Mean choroidal vascularity index (CVI) in the change over time. Mean CVI (%) depending on receiving operation, type of anesthesia, and the presence of diabetic mellitus (DM) or hypertension (HTN) before surgery, 1 week (WK), 1 month (M) and 2 months after surgery. There are significant changes over time (All p < 0.001). (A) CVI continued to increase up to 2 months. There was a significant difference in the change over time between the two groups (p < 0.001). (B) Within topical anesthesia, CVI increased and then decreased after 1 month. Within retrobulbar anesthesia, CVI continued to increase up to 2 months. There was no significant difference in the change over time between the two groups (p = 0.409). (C) Without DM, CVI increased and then decreased after 1 month. With DM, CVI continued to increase up to 2 months. There was no significant difference in the change over time between the two groups (p = 0.682). (D) Without HTN, CVI increased and then decreased after 1 month. With HTN, CVI continued to increase up to 2 months. There was no significant difference in the change over time between the two groups (p = 0.10). Data was compared with preoperative value by repeated measure analysis of variance with BonferroniŌĆÖs method.
Figure┬Ā4.
Scatterplots showing the correlation in the difference at postop 1 week. (A) Correlation between phacoemulsification power (%) and the difference of choroidal thickness (CT) at postop 1 week (r = 0.208, p = 0.090). (B) Correlation between phacoemulsification time(s) and the difference of CT at postop 1 week (r = 0.049, p = 0.695). (C) Correlation between phacoemulsification power (%) and the difference of choroidal vascularity index (CVI) at postop 1 week (r = -0.003, p = 0.982). (D) Correlation between phacoemulsification time(s) and the difference of CVI at postop 1 week (r = 0.011, p = 0.930). Data was compared with difference of CT or CVI in postop 1 week by Pearson Correlation Coefficient. Phacopower is the equivalent average ultrasonic power (FP3) which is the ratio of cumulative dissipated energy (CDE) to ultrasonic total time. CDE is calculated as: (longitudinal time ├Ś average longitudinal power) + (torsional time ├Ś 0.4 ├Ś average torsional amplitude). The factor 0.4 represents approximate reduction of heat dissipated at incision as compared to conventional phaco. Phacotime is the total longitudinal power on time.
Table┬Ā1.
Patient demographics and clinical characteristics of the subjects
Table┬Ā2.
Association between the type of anesthesia and the presence of past history
| Parameter | Anesthesia | DM | HTN |
|---|---|---|---|
| Anesthesia | - | 0.468 | 0.163 |
| DM | 0.468 | - | 0.826 |
| HTN | 0.163 | 0.826 | - |
Table┬Ā3.
Preoperative CT and postoperative variance of CT
| Parameter | Preoperative | Variance in postop 1 week | p-value* | Variance in postop 1 month | p-value* | Variance in postop 2 months | p-value* |
|---|---|---|---|---|---|---|---|
| Eyes without op (n = 28) | 280.43 ┬▒ 42.39 | 9.25 ┬▒ 31.98 | 0.14 | 7.429 ┬▒ 28.44 | 0.18 | 4.89 ┬▒ 36.39 | 0.48 |
| Eyes with op (n = 67) | 269.55 ┬▒ 42.86 | 58.93 ┬▒ 44.92 | <0.001 | 54.689 ┬▒ 6.86 | <0.001 | 43.76 ┬▒ 54.05 | <0.001 |
Table┬Ā4.
Preoperative CVI and postoperative variance of CVI
| Parameter | Preoperative | Variance in postop 1 week | p-value* | Variance in postop 1 month | p-value* | Variance in postop 2 months | p-value* | |
|---|---|---|---|---|---|---|---|---|
| Eyes without op (n = 28) | 59.41 ┬▒ 2.12 | -0.02 ┬▒ 1.31 | 0.951 | -0.04 ┬▒ 1.57 | 0.890 | 0.03 ┬▒ 1.87 | 0.940 | |
| Eyes with op (n = 67) | 59.82 ┬▒ 2.11 | 2.23 ┬▒ 2.32 | <0.001 | 2.74 ┬▒ 2.47 | <0.001 | 2.81 ┬▒ 2.77 | <0.001 | |
| Depending on anesthesia | ||||||||
| ŌĆā | Topical (n = 25) | 59.55 ┬▒ 2.11 | 2.49 ┬▒ 2.58 | <0.001 | 3.21 ┬▒ 2.55 | <0.001 | 2.83 ┬▒ 3.05 | <0.001 |
| Retrobulbar (n = 42) | 59.99 ┬▒ 2.12 | 2.07 ┬▒ 2.17 | <0.001 | 2.45 ┬▒ 2.42 | <0.001 | 2.79 ┬▒ 2.63 | <0.001 | |
| Depending on DM | ||||||||
| None DM (n = 36) | 59.83 ┬▒ 2.60 | 2.34 ┬▒ 2.22 | <0.001 | 2.97 ┬▒ 2.51 | <0.001 | 2.95 ┬▒ 2.60 | <0.001 | |
| DM (n = 31) | 59.81 ┬▒ 1.39 | 2.09 ┬▒ 2.46 | <0.001 | 2.46 ┬▒ 2.44 | <0.001 | 2.63 ┬▒ 2.98 | <0.001 | |
| Depending on HTN | ||||||||
| None HTN (n = 25) | 60.10 ┬▒ 1.97 | 1.67 ┬▒ 1.99 | <0.001 | 2.11 ┬▒ 2.15 | <0.001 | 2.06 ┬▒ 2.43 | <0.001 | |
| HTN (n = 42) | 59.66 ┬▒ 2.20 | 2.56 ┬▒ 2.46 | <0.001 | 3.11 ┬▒ 2.60 | <0.001 | 3.25 ┬▒ 2.89 | <0.001 | |
REFERENCES
1) Chen H, Wu Z, Chen Y, et al. Short-term changes of choroidal vascular structures after phacoemulsification surgery. BMC Ophthalmol 2018;18:81.



3) Ohsugi H, Ikuno Y, Ohara Z, et al. Changes in choroidal thickness after cataract surgery. J Cataract Refract Surg 2014;40:184-91.


4) Spaide RF, Koizumi H, Pozzoni MC. Enhanced depth imaging spectral-domain optical coherence tomography. Am J Ophthalmol 2008;146:496-500.


5) Querques G, Lattanzio R, Querques L, et al. Enhanced depth imaging optical coherence tomography in type 2 diabetes. Invest Ophthalmol Vis Sci 2012;53:6017-24.


6) Yip VC, Laude A, Tan KA, et al. A longitudinal study of choroidal changes following cataract surgery in patients with diabetes. Diab Vasc Dis Res 2019;16:369-77.


7) Brito PN, Rosas VM, Coentr├Żo LM, et al. Evaluation of visual acuity, macular status, and subfoveal choroidal thickness changes after cataract surgery in eyes with diabetic retinopathy. Retina 2015;35:294-302.


8) Shahzad R, Siddiqui MAR, Zafar S, et al. Choroidal thickness changes following cataract surgery using swept source optical coherence tomography. Can J Ophthalmol 2018;53:60-4.


9) Falc├Żo MS, Gon├¦alves NM, Freitas-Costa P, et al. Choroidal and macular thickness changes induced by cataract surgery. Clin Ophthalmol 2014;8:55-60.


10) Noda Y, Ogawa A, Toyama T, Ueta T. Long-term increase in subfoveal choroidal thickness after surgery for senile cataracts. Am J Ophthalmol 2014 158:455-9. e1.


11) Zeng S, Liang C, He Y, et al. Changes of subfoveal choroidal thickness after cataract surgery: a meta-analysis. J Ophthalmol 2018;2018:2501325.



12) Gudauskiene G, Matuleviciute I, Mockute R, et al. Changes in subfoveal choroidal thickness after uncomplicated cataract surgery. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2019;163:179-83.


13) Margolis R, Spaide RF. A pilot study of enhanced depth imaging optical coherence tomography of the choroid in normal eyes. Am J Ophthalmol 2009;147:811-5.


14) Tan KA, Laude A, Yip V, et al. Choroidal vascularity index-a novel optical coherence tomography parameter for disease monitoring in diabetes mellitus? Acta Ophthalmol 2016;94:e612-6.


15) Agrawal R, Li LK, Nakhate V, et al. Choroidal vascularity index in Vogt-Koyanagi-Harada disease: an EDI-OCT derived tool for monitoring disease progression. Transl Vis Sci Technol 2016;5:7.

16) Sonoda S, Sakamoto T, Yamashita T, et al. Choroidal structure in normal eyes and after photodynamic therapy determined by binarization of optical coherence tomographic images. Invest Ophthalmol Vis Sci 2014;55:3893-9.


17) Schindelin J, Arganda-Carreras I, Frise E, et al. Fiji: an open-source platform for biological-image analysis. Nat Methods 2012;9:676-82.


18) Kinoshita T, Mitamura Y, Shinomiya K, et al. Diurnal variations in luminal and stromal areas of choroid in normal eyes. Br J Ophthalmol 2017;101:360-4.


-
METRICS

-
- 0 Crossref
- 0 Scopus
- 2,613 View
- 96 Download
- Related articles
-
Clinical Results after Phacoemulsification in Mature Cataract.2016 June;57(6)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



