앞허혈시신경병증 환자에서 뇌자기공명영상으로 확인한 측두동맥염
Temporal Arteritis with Diagnostic Brain Magnetic Resonance Imaging
Article information
Abstract
목적
동맥염성 앞허혈시신경병증에서 측두동맥 조직검사 대신 뇌자기공명영상으로 측두동맥염을 진단하고 치료한 증례를 보고하고자 한다.
증례요약
83세 여자 환자가 2주 전부터 발생한 우안 시력저하, 4개월 전부터 시작된 후두부 통증과 저작장애를 주소로 내원하였다. 초진 시 최대교정시력 우안 0.1로 시력저하와 상대구심동공운동장애를 보였다. 시야검사에서 하측수평시야결손과 안저검사에서 상측 시신경유두의 창백과 부종 그리고 면화반이 있었다. 혈액검사상 적혈구침강속도, C반응단백, 류마티스인자 상승 및 형광항핵항체(fluorescent antinuclear antibody) 양성이었다. 표재성 측두동맥의 혈관강을 확인할 수 있는 고해상도 뇌자기공명영상에서 측두동맥의 혈관강폐쇄로 혈관내 신호소실이 나타나지 않아서 측두동맥염에 의한 앞허혈시신경병증 의심하에 고용량 스테로이드 정주치료 후 1주일 뒤 우안 시력 0.9, 중심시야 호전을 보였다. 경구 스테로이드 감량 및 azathioprine 병용 후 11개월째 우안 시력 0.9, 호전된 중심시야가 악화 없이 잘 유지되었다.
결론
앞허혈시신경병증이 의심되는 환자에서 뇌자기공명영상으로 측두동맥 내경의 이상을 확인하여 측두동맥염으로 진단하고, 스테로이드와 면역억제제 치료를 통하여 시력과 시야장애가 호전되었다.
Trans Abstract
Purpose
To report a case of arteritic anterior ischemic optic neuropathy diagnosed with brain magnetic resonance imaging (MRI) for temporal arteritis instead of temporal artery biopsy.
Case summary
An eighty-three years old female visited our clinic for right blurred vision for 2 weeks ago with occipital headache for 4 months and mastication problems. Initial best corrected visual acuity was 0.1 in right eye. She had right inferior altitudinal visual field defect and superior pale optic disc swelling with few cotton wool spots were checked. In serologic tests, erythrocyte sedimentation rate, C reactive peptide, and rheumatoid factor were increased, and fluorescent antinuclear antibody was positive. We performed high resolution brain MRI which could find superficial temporal artery’s luminal signal. In MRI image, we could find loss of intraluminal signal intensity void with total luminal obstruction. We assumed as arteritic anterior ischemic optic neuropathy and high dose intravenous steroid was done. Visual acuity of right eye was 0.9 and central scotoma was improved 1 week after intravenous steroid. We changed to oral steroid with tapering and added oral azathioprine. After 11 months of oral steroid use, her visual acuity was 0.9 in right eye and inferior altitudinal visual field defect was much improved.
Conclusions
A patient suspected anterior ischemic optic neuropathy was diagnosed by brain MRI with abnormalities in superficial temporal artery. Visual acuity and visual field defect were improved by steroid and immunosuppressive treatment for arteritic anterior ischemic optic neuropathy.
측두동맥염(temporal arteritis)은 측두동맥, 후두동맥 등 표재성 뇌혈관의 만성 육아종성 염증으로 거대세포동맥염(giant cell arteritis)이라고 하기도 한다. 측두동맥염이 뒤섬모체동맥을 침범하여 동맥염성 앞허혈시신경병증(arteritis anterior ischemic optic neuropathy)이 발생한다[1,2]. 측두동맥염의 임상양상은 주로 두통, 두피 압통, 발열 및 턱 관절 파행, 하지 관절 파행 등 관절 증상이 있으며 30%에서 시각 증상을 보이며 15%에서 시력저하를 일으키는 것으로 알려져 있다[2]. 임상적으로 측두동맥염을 강하게 시사하는 진단 기준으로는 새롭게 발생한 국소적인 두통, 턱 관절 파행, 표재성 측두동맥 촉진 시 압통, 적혈구침강속도(erythrocyte sedimentation rate) 상승 등이 있다[3]. 그러나 측두동맥염의 확진 방법은 측두동맥생검이다. 측두동맥생검은 특이도가 높아 진단적 가치가 높은 검사이나 생검 조직의 양이 불충분하거나 단안 침범인 경우 등위음성이 나올 수 있어 임상적 증상과 연관시켜 진단에 사용해야 한다[4]. 생검 결과에서는 특징적으로 동맥벽의 림프구, 대식세포 그리고 거대세포에 의한 혈관벽의 염증을 조직검사에서 확인할 수 있다[4]. 측두동맥생검은 일반적으로 안전한 것으로 알려져 있지만 생검의 합병증으로, 두피괴사, 안면신경손상 등이 있을 수 있다[4]. 국내에서는 동맥염성 앞허혈시신경병증이 매우 드문 질환으로 해부학적, 기술적인 숙련도가 부족하고 앞허혈시신경병증 환자에서 측두동맥염의 감별 진단을 위해 생검을 시도하기 쉽지 않을 것으로 추측된다. 뇌자기공명영상 기술의 발달로 1 mm 이하의 해상도로 표재성 두개동맥(superficial cranial artery)을 시각화할 수 있고, 측두동맥염이 비교적 흔한 서구에서는 이를 이용한 방법이 진단적 가치가 있음이 연구되고 있다[5]. 본 논문은 동맥염성이 의심되는 앞허혈시신경병증 환자에서 국내에서 처음으로 고해상도 뇌자기공명영상을 이용하여 측두동맥염으로 진단한 1례를 보고하고자 한다.
증례보고
고혈압 이외에 기저질환이 없었던 83세 여자 환자가 2주 전에 발생한 우안 시력저하를 주소로 내원하였다. 4개월 전부터 지속된 후두부 두통과 저작장애로 신경과와 치과 진료를 받는 중이었다. 신경과에서 시행한 신경학적 검사 및 뇌자기공명영상에서 정상으로 두통에 대한 특별한 원인질환은 없었다고 한다. 과거력상 결핵약 등 시력저하를 유발할 수 있는 약물 복용력은 없었다. 안과 초진 시 최대교정시력 우안 0.1, 좌안 0.9로 우안 시력이 저하되어 있었고 우안 상대구심동공운동장애를 보였다. 안압은 비접촉식 안압계로 우안 14 mmHg, 좌안 11 mmHg였고, 안저검사에서 시신경유두 상측의 경미한 창백 시신경유두부종과 면화반 소견(Fig. 1A), 험프리시야검사에서 우안 하측수평시야결손(Fig. 2A)이 관찰되었다. 빛간섭단층촬영에서는 우안 망막신경섬유층 두께가 좌안과 비교하면 약간 증가한 소견을 보였다(Fig. 2B). 혈액검사상 적혈구침강속도(erythrocyte sedimentation rate [ESR], 116 mm/hr), C반응단백(C reactive peptide [CRP], 32.34 mg/L), 류마티스인자(rheumatoid factor [RF], 22.27 IU/mL)가 상승 및 형광항핵항체(fluorescent antinuclear antibody) 양성이었고 혈소판 수치의 상승은 없었다. Fibrinogen 검사는 시행하지 않았다. 또한 매독, 결핵 등 감염 혈청 검사 결과는 모두 음성이었다. 이개 앞쪽 관자놀이 근처에 측두동맥염에서 보이는 전형적인 결절성 측두동맥 촉진은 되지 않았으나, 외상측 이마에 튀어나온 사행성 동맥이 일부 관찰되었다(Fig. 1B).

Fundus photography and a photograph of right side preauricular area and temporal forehead at first visit. (A) Right fundus shows cotton wool spot, pale optic disc and edema on the superior rim. (B) Engorged superficial vessel was found (arrow).
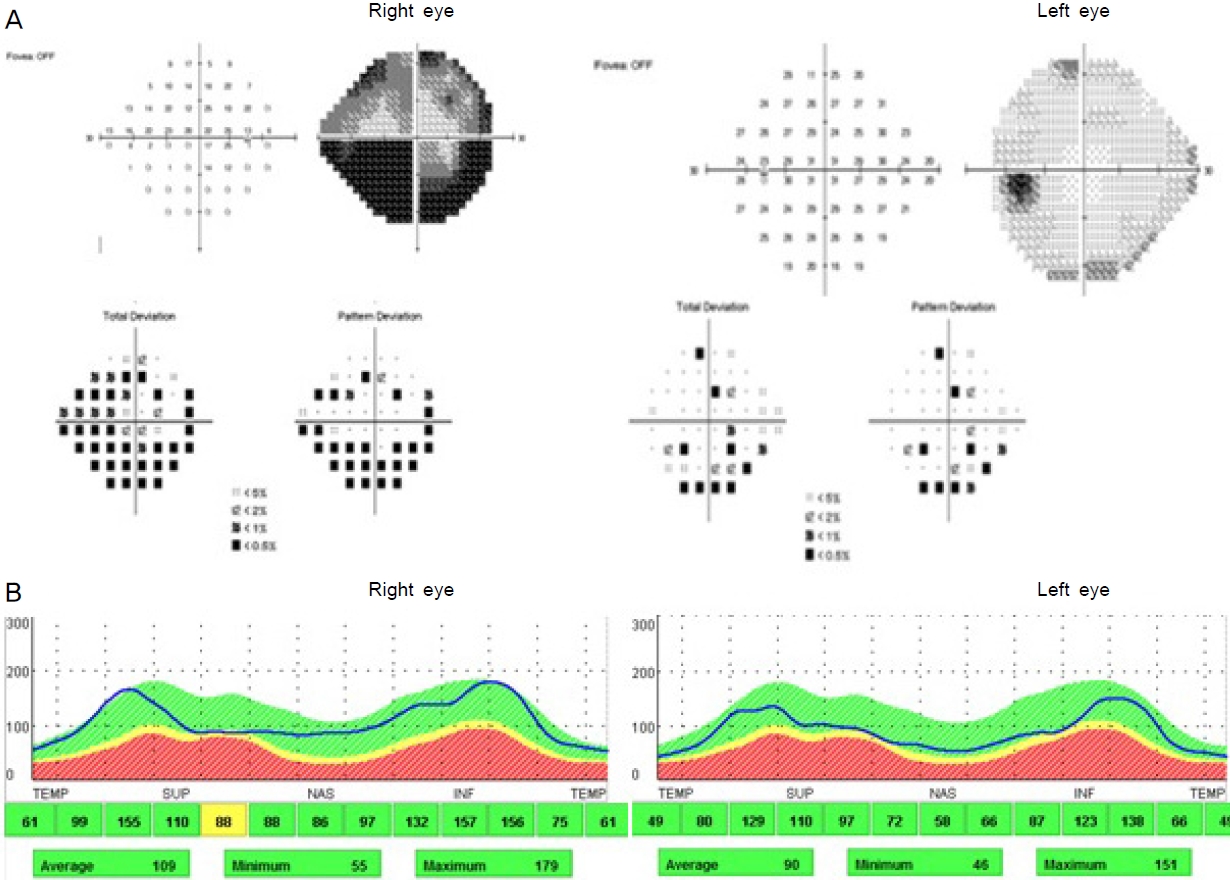
Visual field test and optical coherence tomography at initial ophthalmic examination. (A) Inferior altitudinal visual field defect in right eye was found. (B) Retinal nerve fiber layer (RNFL) of right eye was relatively thick compared to RNFL of left eye.
동맥염성 앞허혈시신경병증 의심하에 영상의학과에 표재성 두개동맥을 관찰할 수 있는 고해상도 뇌자기공명영상검사를 의뢰하였고, 검사 결과를 기다리지 않고 입원하여 6시간 간격으로 250 mg methylprednisone (하루 1 g)의 고용량 스테로이드 정주치료를 3일간 시행하였다.
진단을 위해 고해상도 뇌자기공명영상을 시행하였다. 고해상도 뇌자기공명영상은 3-Tesla system을 기반으로 시행되었으며 2D T1 가중영상은 SPACE (Siemens Healthcare, Erlangen, Germany)로부터 획득하였다. 영상 촬영의 지표는 repetition time 720 ms, echo time 12 ms, echo train length 1, fractional anisotropy 70°, Matrix 1,024 × 768, field of view 200 × 200 mm, pixel spacing 0.19 × 0.19 mm, acquisition time 1 minute 42 second 그리고 number of excitation 1이었다. 총 57 mm의 거리를 3 mm 두께와 공간으로 20개의 단면으로 촬영하였고, T1 가중 지방억제 영상은 같은 지표로 체중 kg당 0.1 mmol의 gadolinium 조영제(Gadovist®, Schering AG, Berlin, Germany) 주입 후 1분 뒤 촬영하였다.
뇌자기공명영상에서 뇌실질내 병변은 없었고 시신경과 안와도 정상 소견을 보였다(Fig. 3A). 표재성 측두동맥의 혈관내 공간폐쇄가 관찰되었는데, 정상 측두동맥은 뇌자기공명영상에서 혈관벽의 조영증강이 흰색으로, 혈류의 흐름에 따른 혈관강 내 신호소실(signal void)이 검은색으로 확인될 수 있으나(Fig. 3B), 본 증례의 환자에서는 혈관벽이 비후하고 혈관강이 막혀 신호소실을 확인할 수 없었다(Fig. 3C, D). 이를 바탕으로 측두동맥염 및 이로 인한 앞허혈시신경병증을 진단할 수 있었다. 스테로이드 정주 종료 시점에 최대교정시력은 우안 0.1, 좌안 0.9로 변동 없었으나 시야검사상 중심부 시야결손이 호전되었고(Fig. 4A), 저작장애는 계속 있으나 후두부 두통은 개선되었다. 퇴원 후 1 mg/kg 용량의 경구 스테로이드로 전환하고 외래로 경과 관찰하기로 하였다. 일주일 후 외래 방문 시 시력은 우안 0.9, 좌안 1.0으로 호전되었고, 환자는 저작장애도 좋아졌다고 하였다.

High resolution brain magnetic resonance imaging (MRI) of superficial temporal arteries and orbital section of high resolution brain MRI (fat suppression coronal view) after high dose intravenous steroid. (A) It shows normal optic nerve and orbital structure. (B) Transversal post-contrast fat-suppressed T1-weighted image on MRI shows the superficial temporal arteries of normal patient (C), the intraluminal signal intensity void with arterial wall enhancement (white arrow). (C, D) Anterior arteritic ischemic optic neuropathy patient in this study. The arterial lumen is near totally occluded as loss of intra luminal signal intensity void (empty arrows).
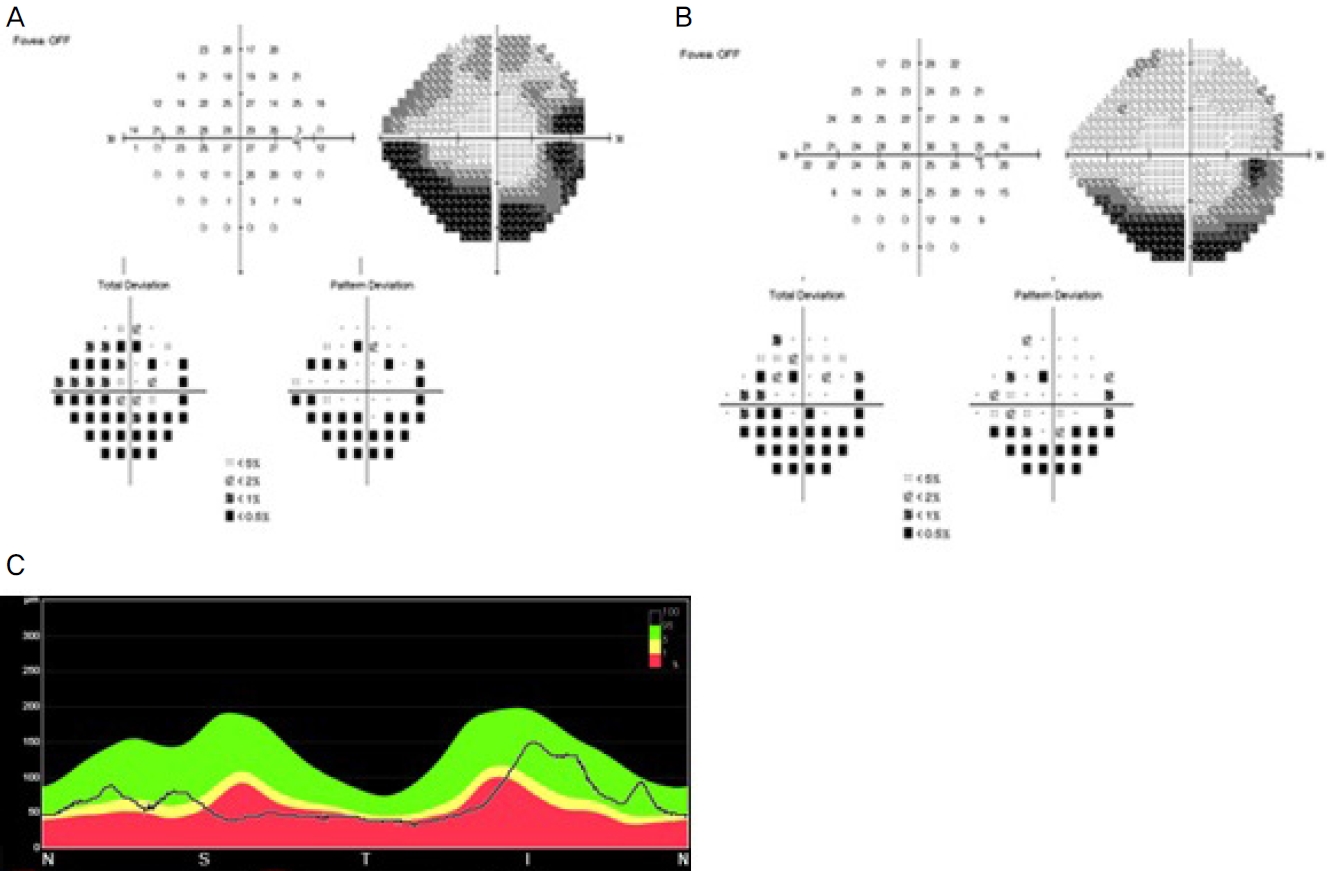
Visual field test and optical coherence tomography (OCT) in right eye after high dose intravenous steroid and at last visit. (A, B) Visual field test shows improved inferior altitudinal visual field defect after intravenous steroid (A) and shows well maintained visual field improvement at last visit (B). (C) OCT shows retinal nerve fiber layer thinning at last visit.
이후 경구 스테로이드를 두 달에 걸쳐 서서히 감량하고 두 달 후부터 경구 스테로이드 15 mg과 azathioprine 75 mg을 병용하다가 퇴원 후 9개월째에 경구 스테로이드는 중단하고 azathioprine만 복용하였다. 퇴원 후 11개월째 마지막 내원 시 azathioprine 75 mg을 복용 중이었고, 최대교정시력은 우안 0.9, 좌안 1.0, 시야검사에서는 우안 중심시야의 호전은 잘 유지되었다(Fig. 4B). 빛간섭단층촬영에서는 우안 시신경 망막신경섬유층의 결손이 보였다(Fig. 4C).
고 찰
앞허혈시신경병증은 동맥염성(arteritic)과 비동맥염성(nonarteritic)으로 분류한다. 두 질환은 치료 및 예후가 매우 다르므로 감별 진단이 중요하다. 동맥염성 앞허혈시신경병증의 원인이 되는 측두동맥염 또는 거대세포동맥염은 중간 크기 이상의 표재성 혈관을 침범하는 자가면역 혈관염으로 혈관벽 전층의 육아종성 염증으로 인한 혈관 내막 비후로 혈관강의 폐색을 유발한다. 주로 50세 이상, 70-80세의 백인 여성에서 호발하며 대부분 편측성이지만 조기에 스테로이드 치료를 하지 않을 경우 30% 이상에서 양측으로 진행하고 영구적인 시력소실로 이어질 수 있다[6]. 동맥염성 앞허혈시신경병증은 안전수지(count finger) 이하의 시력소실이 약 54%로, 이러한 시력저하의 발생이 약 26%로 알려진 비동맥염성 앞허혈시신경병증에 비해 심한 시력저하가 관찰된다. 또한 치료에도 불구하고 시력회복은 15% 정도밖에 되지 않는다. 그러나 증상 발생 24시간 이내 치료를 시작하는 경우 58%까지 시력회복을 기대할 수 있으므로 무엇보다 조기 스테로이드 치료가 중요하다[7,8]. 동맥염성 앞허혈시신경병증은 시력예후가 좋지 않은 편이나, 본 증례에서는 스테로이드 치료 후 빠른 시력 및 시야의 호전을 보였다. 그러나 일반적으로 동맥염성 앞허혈시신경병증은 시력예후가 좋지 않은 편이므로, 본 증례에서처럼 스테로이드 치료 후 비교적 빠른 시력 및 시야의 호전을 보이는 경우 비전형적인 시신경염을 감별하여야 한다. 비전형적인 시신경염의 대표적인 원인으로는 결핵, 매독 등 감염성 질환과 자가면역 또는 결체조직 질환이 있을 수 있으나, 시행한 혈액 검사 및 류마티스 내과와의 협진을 통해 이러한 원인들은 배제하였다[8].
측두동맥염의 치료 원칙은 스테로이드[9]이며 경구 스테로이드와 정주 스테로이드를 사용할 수 있으나 조기 고용량 정주 스테로이드 치료가 빠른 시력회복과 스테로이드 감량 시 재발을 줄이는 데 도움을 주어 조기 고용량 정주 스테로이드 치료 후 수개월에서 1년간 천천히 감량을 시행한다. 이는 측두동맥염에서 재발이 흔하며 경구 스테로이드를 1년간 천천히 감량해도 최소 43%에서 재발을 경험한다고 알려져 있으며 첫 1년 이내의 재발이 전체 재발 중 55%를 차지하여[10,11] 정주 스테로이드 치료 후 경구 스테로이드로의 전환 시 신중하고 천천한 감량이 중요하다[11,12]. 앞서 말한 것처럼 감량에 있어 중요한 것은 재발과 부작용을 최소화하는 것인데, 스테로이드와 면역억제제의 병용이 유용하다고 알려져 있다[13]. 본 증례에서도 안전한 스테로이드 감량을 위해 azathioprine을 추가하여 사용하였고, 마지막 내원까지 11개월 동안 재발 및 치료에 따른 특별한 부작용은 없었다.
측두동맥염을 시사하는 여러 가지 진단적 단서들로는 안저검사상 백묵같이 흰 창백 유두부종(chalky-white pale optic disc edema), 양측침범, 면화반(cotton-wool spot)이나 망막경색(retinal infarction) 같은 동반된 망막 혹은 맥락막동맥허혈(concurrent signs of retinal or choroidal circulation ischemia) 등이 있으며, 전신 증상으로 두통, 이마관자부위 통증, 체중 감소, 턱관절 파행이 동반된다. 동맥염성 앞허혈시신경병증의 확진 수단인 측두동맥생검은 측두동맥염이 한국인에서 발생률이 매우 낮은 질환이므로 생검의 해부학적 위치나 기술적인 면의 경험이 부족하고, 의심되는 증례에서 감별 진단을 위해 즉시 시행하기 어려운 경우가 많을 것이라 생각된다.
서구에서는 류마티스질환 분야에서 다발성 근염(polymyalgia rhuematica)의 원인으로, 측두동맥염 등의 자가면역질환을 진단하기 위한 기준들을 제시하였고 이 중 영상의학 영역에서도 다양한 시도가 이루어졌다. 그중 하나가 고해상도 뇌자기공명영상으로 표재성 측두동맥의 혈관강의 신호를 직접 확인하는 것이다[14]. 혈관강의 신호를 다룬 타 연구에 의하면, 뇌자기공명영상에서 표재성 측두동맥의 혈관강 내 신호소실 및 혈관벽 비후 소견을 4가지 단계로 분류하였는데, 혈관벽 비후의 두께 0.5 mm를 기준으로 그보다 얇은 경우 혈관벽의 조영증강이 없으면 grade 0 ,약간의 조영증강이 있으면 grade 1으로 정의하였다. 또한 0.6 mm 이상의 혈관벽 비후와 혈관벽의 명확한 조영증강은 grade 3, 0.7 mm 이상의 혈관벽 비후와 혈관벽의 강한 조영증강은 grade 4로 정의하였다[5]. 본 증례는 혈관벽 비후가 0.7 mm 이상 및 강한 조영증강으로 혈관강 내 신호소실이 확인되지 않는 영상 소견으로 grade 4에 해당한다고 볼 수 있다.
서구에서 시행한 연구들에서 임상양상과 혈액검사를 바탕으로 제시한 임상적 진단 기준을 이용한 측두동맥염의 진단에 비해 magnetic resonance imaging (MRI)의 특이도는 97.0%, 민감도는 80.6%였다. 반면 생검의 경우 민감도는 77.8%로 MRI보다 낮았으나 특이도는 100%였다[5]. 본 연구의 증례에서는 임상적 진단 기준에 의한 동맥염성 앞허혈시신경병증이 비교적 확실하였지만, 진단이 모호하고 다른 질환이 의심되는 소견들이 있다면 생검과 MRI를 함께 사용함으로써 진단의 정확도를 높일 수 있을 것이다. 하지만 생검, MRI 모두 특이도보다 민감도가 낮은 검사로, 위음성 가능성을 염두에 두어야 하고 임상적으로 의심된다면 거대세포동맥염을 배제하여서는 안 되며, MRI나 생검을 단독으로 사용할 경우 이러한 검사들이 음성이라도 진단의 착오가 있을 수 있어 주의를 요한다.
본 증례의 임상적 소견을 살펴보면, 본 증례에서는 측두동맥염의 특징적인 이마관자부위 통증은 없었으나 후두부 두통이 있었는데, 다른 연구에서는 이마관자놀이 외에도 후두동맥(occipital artery)이 위치한 부위의 목통증, 후두부 통증 등 다양한 위치의 표재성 뇌동맥염에 의한 새로운 양상의 두통에서 측두동맥염을 의심할 수 있다고 보고되었다[6,14]. 본 증례의 환자는 수평시야결손이 있는 시력저하, 창백 유두부종과 면화반 등의 안저 소견, 후두부 두통, 저작 장애, CRP, ESR 상승 등을 바탕으로 앞허혈시신경병증의 동맥염성 원인을 의심할 수 있었다. 확진을 위한 측두동맥 생검은 시행하지 않고, 고해상도 뇌자기공명영상을 통해 측두동맥의 혈관강 내 신호소실, 혈관벽의 조영증강이 없어지고 혈관이 폐쇄된 소견을 바탕으로 측두동맥염으로 진단하였고, 스테로이드 정주 치료 및 장기간의 경구 스테로이드 및 면역억제제 병용을 통해 시력 및 시야결손의 회복을 얻을 수 있었다. 고해상도 뇌자기공명영상을 통해 표재성 뇌혈관을 직접 관찰하여, 동맥생검 없이 측두동맥염에 의한 동맥염성 앞허혈시신경병증으로 진단한 증례를 보고함으로써, 진단과 적절한 치료를 위한 뇌자기공명영상의 활용을 제시하고자 하였다.
Notes
Conflict of Interest
The authors have no conflicts to disclose.
References
Biography
장준혁 / Joon Hyuck Jang
한림대학교성심병원 안과
Department of Ophthalmology, Hallym University Sacred Heart Hospital
