유리체절제술과 백내장병합수술에서 후낭절개술군과 대조군의 전방깊이와 굴절력 변화
Changes of Anterior Chamber Depth and Refractive Error after Phacovitrectomy with and without Posterior Capsulotomy
Article information
Abstract
목적
유리체절제술과 백내장병합수술 시 유리체절단침을 이용하여 후낭절개술을 동시에 시행한 경우와 시행하지 않은 경우에 전방깊이 및 굴절력 변화를 확인하고자 하였다.
대상과 방법
유리체절제술과 백내장병합수술 시 유리체절단침을 이용한 후낭절개술을 받은 20명 20안, 병합수술은 시행하고 후낭절개술은 시행하지 않은 환자 20명 20안을 대조군으로 선정하였다. 술 전, 술 후의 전방의 깊이는 샤임플러그 사진기(Pentacam®)를 이용하였으며, 술 후 굴절력은 자동각막굴절측정기를 이용하여 예측한 굴절력과 차이를 비교하였다.
결과
후낭절개술을 시행한 군에서 술 전 전방깊이는 2.56 ± 0.233 mm, 술 후 1개월째 3.54 ± 0.366 mm, 3개월째 3.71 ± 0.424 mm로 측정되었다. 대조군에서는 술 전 2.53 ± 0.204 mm였으며, 술 후 1개월 3.09 ± 0.197 mm, 3개월째 2.95 ± 0.295 mm로 측정되었다. 술 전 유의한 차이는 없었으며 술 후 1, 3개월째는 두 군 간에 유의한 차이가 관찰되었다. 후낭절개술은 시행한 군에서 예측 굴절력은 -0.32 ± 0.124 diopters (D)였고, 술 후 3개월째 -0.62 ± 0.132 D로 측정되었으며 대조군에서는 예측 굴절력은 -0.33 ± 0.142 D였고, 술 후 3개월째 -0.91 ± 0.292 D로 측정되었고 3개월째 두 군 간에 유의한 차이가 관찰되었다.
결론
유리체절제술과 백내장병합수술 시 유리체절단침을 이용한 후낭절개술은 술 후 3개월까지 대조군과 비교해 볼 때 근시화 및 인공수정체의 전방이동을 방지할 수 있는 방법으로 고려해 볼 수 있다.
Trans Abstract
Purpose
To compare the effect on changes in anterior chamber depth (ACD) and refractive error between subjects after combined phacovitrectomy with posterior capsulotomy using a vitrectomy probe and control subjects after combined phacovitrectomy without posterior capsulotomy.
Methods
A total of 20 eyes of 20 subjects who underwent combined phacovitrectomy with posterior capsulotomy using a vitrectomy probe were compared with 20 eyes of 20 control subjects who underwent only phacovitrectomy without posterior capsulotomy. The ACD was measured with Scheimpflug imaging (Pentacam ®; OCULUS Optikgeräte GmbH, Wetzlar, Germany) before and after surgery. Also the preoperative desired refraction and postoperative refraction were compared using an auto keratorefractometor.
Results
The preoperative ACD of subjects with posterior capsulotomy was 2.56 ± 0.233 mm. The ACD was 3.54 ± 0.366 mm and 3.71 ± 0.424 mm at one and three months after surgery in subjects with posterior capsulotomy. The preoperative ACD of subjects without posterior capsulotomy was 2.53 ± 0.204 mm. The ACD was 3.09 ± 0.197 mm and 2.95 ± 0.295 mm at one and three months after surgery in subjects without posterior capsulotomy. There was no significant difference between the two groups in preoperative ACD, but ACD at one and three months after surgery was significantly different between the two groups.The desired refractory error was -0.32 ± 0.124 D in subjects with posterior capsulotomy, and -0.33 ± 0.142 D in the control group.The postoperative refraction was -0.62 ± 0.132 D in patients who underwent phacovitrectomy with posterior capsulotomy, and -0.91 ± 0.292 D in the control group. There was a significant difference in refraction three months after the surgery.
Conclusions
Combined phacovitrectomy with posterior capsulotomy using a vitrectomy probe may be a useful way to prevent myopic change caused by anterior migration of an intraocular lens compared with control subjects, without posterior capsulotomy, for three months after surgery.
최근 수술기구 및 술기의 발전으로 유리체절제술의 빈도가 증가하고 있으나 유리체절제술 중 안내 충전물의 사용이 백내장을 진행시키는 것으로 알려져 이차적으로 백내장수술이 필요한 경우가 많다[1]. 한 번의 수술로 짧은 시간 내에 시력을 회복할 수 있다는 장점 때문에 최근에는 유리체절제술과 백내장병합수술이 많이 사용되고 있고[2,3], 병합수술 이후 가장 흔한 합병증으로 후낭혼탁이 있으며 10%에서 51%까지 발생한다고 보고되고 있다[4-9]. 이러한 후낭혼탁은 수정체낭의 수축을 유발하고 인공수정체의 안정성 및 위치에 영향을 줄 수 있다. 야그레이저후낭절개술이 대표적인 치료로 알려져 있으나 인공수정체에 손상이 발생하거나 안압상승 등의 합병증이 나타날 수 있으며 비문증으로 인한 주관적인 불편감을 호소하는 경우가 있다[10].
최근에는 병합수술 중에 유리체절제침을 이용한 후낭절개술을 동시 시행하기도 하며 후낭혼탁을 예방하는 안전하고 효과적인 방법으로 소개되고 있다[11]. 저자들의 이전 연구에서 다양한 환자를 대상으로 유리체절제술과 백내장 병합수술 시 유리체절단침을 이용하여 후낭절개술을 동시에 시행한 경우 수술 후 전방깊이가 깊어짐과 근시성 굴절력 변화를 확인하였으나 대조군 비교는 시행하지 않았다[12]. 본 연구에서는 망막전막 환자만을 대상으로 병합수술 중 후낭절개술 시행군과 대조군을 비교하여 전방깊이와 굴절력 변화를 비교해 보고자 한다.
대상과 방법
2017년 1월에서 2019년 12월까지 본원에서 망막전막으로 유리체절제술과 백내장병합수술을 시행 받은 환자 중 3개월 이상 경과 관찰을 시행한 환자의 의무기록을 토대로 후향적으로 분석하였다. 본 연구는 본원의 임상연구윤리위원회의 승인하에 진행되었다(승인 번호: 2018-11-016). 유리체절제술 및 백내장병합수술을 시행하면서 유리체절단침을 이용한 후낭절개술을 받은 20명 20안과 유리체절제술 및 백내장병합수술을 시행하면서 후낭절개술을 시행하지 않은 20명 20안을 대상으로 분석하였다. 이전에 안과 수술력 및 망막전막 외 안과 병력이 있는 경우, 술 중 수정체소대의 이상, 술 중 실리콘 기름을 주입한 경우, 술 중 후낭파열이 일어나거나 섬모체고랑에 인공수정체를 삽입한 경우, 술 후 안내염증이 발생한 경우는 연구에 포함시키지 않았다. 모든 수술은 한 명의 술자(I.Y.C.)가 시행하였다. 본 연구에 사용된 수술 방법 및 검사 스케줄은 이전 보고와 같은 방법으로 진행하였다[12]. 유리체절제술은 전신마취 또는 구후부마취 후 3개의 공막 천자를 통한 섬모체 평면부에 시행하고, 백내장수술은 투명각막절개를 통해 초음파수정체유화술을 시행하였다. 모든 환자에서 인공수정체는 1-piece 비구면 아크릴 인공수정체를 사용하였으며(ZCB00 TECNIS®; Abbott Medical Optics Inc., Santa Ana, CA, USA), 인공수정체는 수정체낭에 삽입 후 공막 천자 부위를 통해 유리체절단침을 이용하여 후낭에 약 4.0 mm 크기의 원형의 후낭절개술을 시행하였으며 대조군에서는 이 과정이 생략되었다. 모든 환자들은 시력, 세극등현미경, 안압, 자동각막굴절계, 안저검사를 시행하였고 샤임플러그사진기(Pentacam®; OCULUS Optikgeräte GmbH, Wetzlar, Germany)를 이용하여 전방깊이를 술 전, 술 후 1개월, 3개월째에 측정하였다. 스펙트럼영역 빛간섭단층촬영기(HRA Spectralis+OCT; Heidelberg Engineering, Heidelberg, Germany)를 이용하여 술 전 단층촬영을 시행하였다. 또한 IOL Master® (Carl Zeiss, Jena, Germany)를 이용하여 안구 길이 측정을 술 전 및 술 후 3개월째에 시행하였다. 검사는 산동 상태로 동일하게 시행하였고, 동일한 검사자가 시행하였다. 인공수정체의 도수 결정은 SRK-T 공식을 이용하였고, 굴절력은 spherical equivalent로 계산하였다. 통계적 검정은 Mann-Whitney U-test를 이용하였다. 모든 통계 분석은 SPSS (version 21.0, software for windows; IBM Corp., Armonk, NY, USA)를 이용하였으며, p값이 0.05 미만인 경우에 통계적으로 유의하다고 판단하였다.
결 과
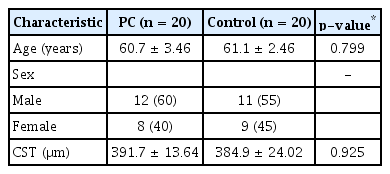
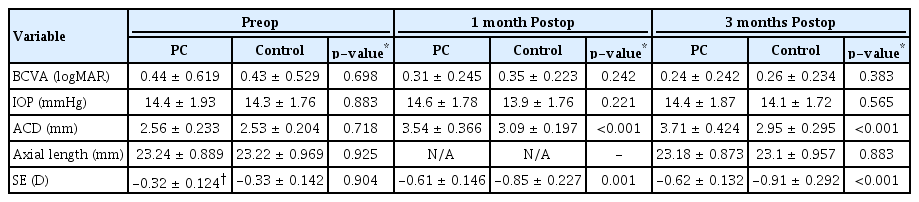
후낭절개술을 시행한 군은 남자가 12명, 여자 8명이었으며 평균 나이는 60세였다. 대조군은 남자 11명, 여자 9명이었고 평균 나이는 61세였으며 두 군에서 의미 있는 차이는 없었다. 또한 술 전 중심황반부두께와 전방깊이, 안축장길이 및 굴절력도 의미 있는 차이는 없었다(Table 1, 2).
후낭절개술을 시행한 군에서 술 전 최대교정시력은 logMAR 0.44 ± 0.619였으며 술 후 1개월에 logMAR 0.31 ± 0.245, 3개월에 logMAR 0.24 ± 0.242로 측정되었다. 대조군에서는 술 전 logMAR 0.43 ± 0.529 술 후 1개월에 logMAR 0.35 ± 0.223, 3개월에 logMAR 0.26 ± 0.234로 측정되었다. 후낭절개술을 시행한 군에서 대조군에 비해 1개월, 3개월째 시력상승은 있었으나 통계적으로 의미 있는 차이는 관찰되지 않았다(Table 2). 후낭절개술을 시행한 군에서 술 전 안압은 14.4 ± 1.93 mmHg였으며 술 후 1개월 14.6 ± 1.78 mmHg, 3개월째 14.4 ± 1.87 mmHg, 대조군에서는 술 전 14.3 ± 1.76 mmHg, 술 후 1개월 13.9 ± 1.76 mmHg, 3개월째 14.1 ± 1.72 mmHg로 측정되었고 유의한 안압의 차이는 나타나지 않았다(Table 2).
수술 전후의 전방깊이의 변화를 살펴보면 후낭절개술 시행군에서 술 전 전방깊이는 2.56 ± 0.233 mm였으며 술 후 1개월에 3.54 ± 0.366 mm, 술 후 3개월에 3.71 ± 0.424 mm로 관찰되었다. 대조군에서는 술 전, 1개월, 술 후 3개월째 각각 2.53 ± 0.204 mm, 3.09 ± 0.197 mm, 2.95 ± 0.295 mm로 측정되었다. 술 전에는 두 군에서 유의한 차이가 없었으며 1개월째(p<0.001), 3개월째(p<0.001)에는 유의한 차이가 확인되었다(Table 2). 후낭절개술 시행군에서 술 전 안구 길이는 23.24 ± 0.889 mm였으며 수술 후 3개월째 안구 길이는 23.18 ± 0.873 mm로 측정되었으며 대조군에서는 길이는 23.22 ± 0.969 mm였으며 수술 후 3개월째 안구 길이는 23.1 ± 0.957 mm로 유의한 차이는 없었다(Table 2).
굴절력의 변화 양상을 보면, 후낭절개술 시행군에서 술 전 목표 굴절력은 -0.32 ± 0.124 diopters (D)였으며 술 후 1개월째 -0.61 ± 0.142 D, 술 후 3개월째는 -0.62 ± 0.132 D로 측정되었다. 대조군에서는 술 전 -0.33 ± 0.142 D였으며 술 후 1개월째 -0.85 ± 0.227 D, 술 후 3개월째는 -0.91 ± 0.292 D로 측정되었다. 술 전에는 두 군 간 유의한 차이는 없었으며 1개월(p=0.001), 3개월째(p<0.001) 두 군 간에 유의한 차이가 있었다(Table 2). 모든 환자에서 술 후 3개월까지 인공수정체의 위치 이상, 고안압증 및 신생혈관녹내장, 중심부황반부종, 유리체출혈, 안내염 등의 합병증은 관찰되지 않았다.
고 찰
후낭혼탁은 백내장수술 후의 가장 흔한 합병증으로 유리체절제술 및 충전물의 사용이 후낭혼탁을 일으키는 것으로 알려져 왔다[8]. 유리체절제술 시 백내장병합수술을 시행한 경우 후낭혼탁이 많이 발생하게 되며 이를 치료하기 위해 야그레이저후낭절개술이 널리 이용되고 있다. 야그레이저후낭절개술은 비교적 안전한 시술로 알려져 있지만 인공수정체 손상, 비문증을 일으켜 주관적인 불편감이 나타나게 되거나, 낭포황반부종, 앞유리체혼탁, 망막박리, 안내염 등의 합병증도 발생 가능한 것으로 알려져 있다[10]. 따라서 Sato et al [11]은 유리체절제술과 백내장병합수술에서 유리체절제침을 이용한 후낭절개술을 처음 기술하였고 이러한 후 낭혼탁에 대한 합병증을 줄일 수 있는 방법으로 소개하였다. 본 저자들도 이전 보고에서 다양한 질환을 대상으로 병합수술을 한 경우에 전방깊이 및 굴절력에 대해 보고한 바 있으며 전방의 안정성을 확인함과 동시에 의미 있는 근시성 변화를 확인하였다[12]. 이번 연구는 망막전막 환자만 분석하여 질환에 따른 수정체낭의 수축 등 다른 변수를 줄일 수 있었으며 대조군을 설정하여 비교하였으며 그 결과 대조군에 비하여 술 후 전방깊이가 통계학적으로 의미 있게 유지된것으로 확인되었다.
Stifter et al [13]이 보고한 백내장수술에서 후낭절개술을 동시에 시행한 경우 대조군에 비해 전방의 깊이가 깊게 유지되었고 대조군에서는 술 전보다는 전방깊이가 깊어지나 후 낭절개술 시행군과 비교하여 수정체낭의 수축으로 인한 전방이 좁아지고 인공수정체의 전방이동을 보고하였다. 저자들의 연구에서도 전방의 깊이는 유리체절제술과 백내장병합수술 시 후낭절개술을 동시에 시행한 군에서 대조군에 비하여 술 후 3개월까지 안정적으로 유지되는 것을 확인하였다. 대조군에서는 앞의 연구와 유사하게 술 전보다는 전방의 깊이가 깊어졌지만, 후낭절개술 시행군에 비하여 3개월까지 전방의 깊이가 좁게 측정되었다. 이는 대조군에서 수정체낭수축으로 인한 전방깊이 변화가 심하게 발생하고, 후낭절개술 시행군에서는 전방깊이 변화가 적게 발생하는 것으로 생각되며 인공수정체의 안정성을 나타내는 지표로 생각된다.
이전 연구에서 백내장수술 시 후낭절개수술을 동시 시행한 경우 통계적으로 의미는 없었지만 수술 후 1개월째 경한 근시성 변화가 있었다고 보고하였으며[13], 유리체절제술과 백내장병합수술 시 경한 근시 이동이 보고된 적 있으며, 병합수술과 동시에 후낭절개술을 시행한 경우에도 경한 근시 이동이 나타남을 여러 연구에서 보고하고 있다[14-16]. 하지만 국내 보고에서 유리체절제술과 백내장병합수술 중 후낭절제술을 시행한 군에서는 경한 원시성 변화, 대조군에서는 경한 근시성 변화로 반대의 내용이 보고된 적도 있다[17]. 이처럼 아직까지 유리체절제술과 백내장병합수술에서 후낭절개술을 시행하는 경우 경한 근시 이동이 다수로 보고되고 있지만 명확한 원인은 밝혀지지 않았다. 다양한 가설이 제시되고 있으며 유리체와 전방수의 굴절 계수의 차이, 안구 길이의 변화, 후낭의 지지 역할 파괴에 의한 후방 압력에 의한 인공수정체 앞쪽으로의 이동 등의 가설이 제시되었다[16,18,19]. 이러한 이전의 연구들은 대부분 수정체낭의 수축으로 인한 근시화, 유리체절제술과 후낭절개술 시행 시에는 후부의 밀어내는 힘으로 인하여 경한 근시화 변화가 가능할 것이라는 가설을 지지하고 있다. 본 저자들의 연구에서는 후낭절개술군과 대조군 모두 근시화가 되었으나 대조군에서 후낭절개술군에 비하여 유의하게 크게 근시화가 되었다. 이는 전방깊이와 연관지어 생각해볼 때 후낭절개술 시행군에서는 후낭절개 시행 부위로 후부압력 및 충전물질로 인한 인공수정체의 앞쪽 이동으로 경한 근시화가 가능할 것으로 생각되며, 대조군에서는 상대적으로 후부압력에 의한 인공수정체의 전방이동은 적겠지만 수정체낭의 수축을 가져와 더 심한 근시화를 유발하는 것으로 생각된다. 이를 통해 후방 압력과 충전물에 의한 인공수정체의 이동은 약 0.3 D 정도의 미미한 수준인 것으로 보이며 그보다는 후낭절개술을 시행하지 않을 경우에 발생하는 낭 수축으로 인한 인공수정체의 안정성 이상 및 전방이동으로 인한 근시화가 더 큰 영향을 주는 것으로 생각된다. 이번 연구는 망막전막 환자만을 한정적으로 연구하여 기저질환으로 인한 낭 수축을 배제할 수 있었다. 또한 후낭절개술을 시행한 경우 펜타캠을 통해 확인한 결과 전방깊이가 깊어짐과 동시에 경한 근시화가 관찰되고 대조군에서 더 큰 근시성 변화 및 좁은 전방을 확인하여 후낭절개술 이후 발생하는 근시화에 대한 하나의 가설로 고려해볼 만한 가치가 있다.
본 연구의 제한점으로 대상자의 수가 적어 결과를 일반화하기는 어려운 점이 있으며, 경과 관찰 기간이 3개월까지로 장기적인 결과를 관찰하지 않아 추후 장기간의 연구가 필요할 것으로 생각된다. 또한 전방깊이의 변화에 따른 근시화의 정도가 일치하여 인공수정체의 전방이동은 확인하였으나 수정체낭 수축 및 후낭혼탁 정도는 평가하지 않아 수정체낭 수축과 전방깊이, 근시화의 직접적인 연관성에 대해서는 추후 추가적인 분석이 필요할 것으로 생각된다. 결론적으로 본 연구는 유리체절제술 및 백내장병합수술 후 유리체절제침을 이용하여 후낭절개술을 시행한 후 펜타캠 이용한 전방깊이의 변화와 굴절력 변화를 측정한 후속연구로 망막전막환자를 대상으로 시행하여 다른 변수를 제거하였고, 대조군과 비교하여 봤을 때 유리체절제침을 이용한 후낭절제술을 시행 시 인공수정체의 위치 변화 및 굴절력 변화를 방지할 수 있는 한 가지 방법으로 고려해봐야 한다.
Notes
Conflict of Interest
The authors have no conflicts to disclose.
References
Biography
조용운 / Yong Wun Cho
경상대학교 의과대학 경상대학교병원 안과학교실
Department of Ophthalmology, Gyeongsang National University Hospital, Gyeongsang National University College of Medicine