 |
 |
| J Korean Ophthalmol Soc > Volume 61(8); 2020 > Article |
|
국문초록
대상과 방법
섬유주절제술 후 경과 관찰 기간이 최소 6개월 이상인 환자들을 대상으로 양막이식술 시행 여부에 따라 양막이식술군과 대조군으로 나누고 Kaplan-Meier 생존 분석을 통해 수술 성적에 미치는 영향에 대해 분석하였다. 수술 성공은 안압하강제를 사용하지 않고 안압이 18 mmHg 이하이고 안압이 20% 이상 하강한 경우로 정의하였고, 양막이식술 여부에 따라 합병증 발생 빈도와 여과포 형태를 분석하였다.
결과
양막이식술군은 46명 52안, 대조군은 33명 43안이었다. 양막이식술군과 대조군의 수술 후 12개월 성공률은 각각 94.2%, 85.8%로 유의한 차이는 없었다(p=0.121). 양막이식술군의 수술 전 평균 안압은 30.2 ± 9.8 mmHg에서 수술 후 마지막 방문시 11.6 ± 4.2 mmHg으로 감소하였고(p<0.001), 대조군의 수술 전 평균 안압 29.7 ± 7.4 mmHg에서 수술 후 마지막 방문시 12.2 ± 4.5 mmHg으로 감소하였다(p<0.001). 술 전 안압, 술 후 마지막 안압, 그리고 합병증 발생 빈도는 두 군 간에 유의한 차이는 없었다. 무혈관 낭포성 여과포가 양막이식술군에서는 관찰되지 않았으나, 대조군 8안(18.6%)에서 관찰되었다(p=0.002).
ABSTRACT
Purpose
To evaluate the short-term clinical outcomes of trabeculectomy with amniotic membrane transplantation (AMT) and mitomycin C (MMC) in patients with primary open-angle glaucoma (POAG).
Methods
This was a retrospective, comparative, and consecutive case series study. We reviewed the medical records of patients with POAG who underwent trabeculectomy with AMT and MMC and compared the surgical outcomes according to AMT with Kaplan-Meier survival analysis. All patients had follow-up of ≥6 months. Surgical success was defined as an intraocular pressure (IOP) ≤18 mmHg and IOP reduction ≥20% without medication. We evaluated the frequency of complications and bleb morphology according to AMT.
Results
A total of 95 eyes of 79 patients were included; 52 eyes of 46 patients with AMT (AMT group) and 43 eyes of 33 patients without AMT (control group). The cumulative probability of success after trabeculectomy was 94.2% and 85.8% after one year for the AMT and control groups, respectively (p = 0.121). Mean IOP decreased from 30.2 ± 9.8 mmHg preoperatively to 11.6 ± 4.2 mmHg at the final visit in the AMT group (p < 0.001). Mean IOP decreased from 29.7 ± 7.4 mmHg preoperatively to 12.2 ± 4.5 mmHg at the final visit in the control group (p < 0.001). Preoperative and final IOP were not significantly different between the two groups. Complications were comparable between the groups. However, avascular cystic bleb was more frequent in the control group (18.6%) than in the AMT group (0%) (p = 0.002).
1960년대에 처음 소개된 섬유주절제술은 현재까지도 조절되지 않는 녹내장 환자를 위한 수술적 치료의 표준적인 방법으로 시행되고 있다[1,2]. 섬유주절제술의 목적은 전방으로부터 결막하 또는 테논낭 아래 공간으로 방수의 배출로를 형성하는 것이다[1,3]. 섬유주절제술의 실패는 내측공막절개부의 폐쇄와 공막편 부위의 흉터 그리고 상공막과 결막하의 섬유화 반흔 조직의 형성 등에 의해 공막 절개부를 통한 방수의 흐름이 폐쇄되어 발생할 수 있다[1,3]. 이러한 수술 실패는 섬유모세포에서 근섬유모세포로의 분화로 인한 섬유화와 관련이 있고, 섬유화를 억제하고 섬유주절제술의 성공률을 높이기 위해서 5-fluorouracil (FU)과 mitomycin-C (MMC)와 같은 항섬유화제제가 일반적으로 사용되고 있다[4,5]. 비록 MMC나 5-FU의 보조적 사용이 섬유주절제술의 수술 성공률을 높였으나, 여과포 누출과 여과포 관련 감염의 위험 또한 증가한다고 보고되고 있다[6,7]. 더욱이 정상안 압녹내장 환자의 결막은 원발개방각녹내장 환자의 결막보다 더 얇고 섬유주절제술 후 저안압 발생, 여과포 감염 등의 합병증의 위험도가 더 높다고 알려져 있다[8,9].
이전에 섬유주절제술을 실패하였거나 신생혈관녹내장, 위수정체 녹내장과 같은 난치성 녹내장 환자에서 MMC와 양막이식술을 함께 시행한 섬유주절제술은 안압하강에 효과적이었다고 보고되었다[10,11]. 또한, MMC와 양막이식술을 함께 시행한 섬유주절제술은 양막이식술을 시행하지 않은 경우에 비해 수술 성공률이 더 높고, 합병증의 빈도는 더 낮다고 보고되었다[3,12]. 양막을 이용한 섬유주절제술의 높은 성공률은 양막의 항염증, 항섬유화, 그리고 항혈관화 작용과 관계가 있다고 알려져 있다[3,10-12]. 이러한 특징들로 인해 이론적으로 양막은 섬유주절제술에서 섬유화를 줄이기 위한 이상적인 보조제로 생각될 수 있다[3]. Li et al [13]은 동결보존양막의 기질표면과 양막의 기질 추출물에서 배양된 섬유모세포는 근섬유모세포로의 분화가 억제되었을 뿐만 아니라, 동결보존양막의 기질표면과 양막의 기질 추출물에서 배양된 근섬유모세포가 섬유모세포로 다시 회복되었다고 보고하였다. Lee et al [14]은 토끼를 이용한 동물 실험에서 양막을 이용하여 아메드밸브삽입술을 시행하고 섬유성막을 조직병리학적으로 분석한 결과 양막이식술군의 섬유성막에서 근섬유모세포층의 두께가 대조군보다 더 얇음을 보고하여 양막의 항섬유화 효과를 확인하였다. 하지만 아직까지 국내에서 원발개방각녹내장 환자에서 양막을 이용한 섬유주절제술의 임상성적을 보고한 연구는 없었다. 이에 본 연구에서 원발개방각녹내장 환자에서 양막이식술을 병행한 섬유주절제술의 단기 임상성적을 알아보고자 하였다.
본 연구는 섬유주절제술을 시행받고 최소 6개월 이상 경과 관찰한 원발개방각녹내장 환자들을 대상으로 양막이식술 병행 여부를 포함한 의무기록을 후향적으로 분석하였다. 이 연구는 인간 대상 연구를 위한 헬싱키 선언에 따라 수행되었고, 부산대학교병원 임상시험위원회로부터 승인을 받았다(승인 번호: 1910-011-084).
수술을 시행한 모든 환자에서 최대교정시력(best corrected visual acuity), 세극등현미경검사, 골드만압평안압계를 이용한 안압 측정, 전방각경검사, 산동안저검사, 시신경과 망막신경섬유층 촬영(AFC-210; Nidek, Gamagori, Japan), 시야검사(Humphrey Field Analyzer, Swedish interactive threshold algorithm standard C24-2; Carl Zeiss Meditec, Inc. Dublin, CA, USA), 빛간섭단층촬영검사(Cirrus HD-OCT, Carl Zeiss Meditec), 그리고 여과포 상태에 대한 전안부 사진 촬영 등을 포함한 철저한 안과 검사를 시행하였다.
원발개방각녹내장은 녹내장성 시신경 손상과 이와 연관된 시야결손이 있는 경우, 전방각은 개방되어있고, 치료 전 안압이 >21 mmHg인 경우로 정의하였다. 정상안압녹내장은 녹내장성 시신경 변화 혹은 망막신경섬유층의 결손이 있고 이와 관련된 시야결손이 있는 경우와 전방각은 개방되어 있고, 오전 9시부터 5시까지 2시간 간격으로 측정한 치료 전 안압이 ≤21 mmHg인 경우로 정의하였다. 녹내장성 시신경 손상은 시신경유두 함몰비 ≥0.7, 양안의 시신경 유두 함몰비 차이 ≥0.2, 시신경유두테의 패임이나 얇아짐, 시신경유두 출혈, 시신경 섬유결손 중 1가지 이상이 확인된 경우로 정의하였고, 녹내장성 시야 결손은 신뢰할 수 있는 두 번의 연속적인 시야 검사에서 Glaucoma hemifield test가 “outside normal limit”이 나타날 때, 또는 pattern deviation plot에서 활 모양 영역에 있는 3개 이상 점의 역치가 정상의 5% 미만에서 나타나고 그중 한 점이 1% 미만일 때이거나, pattern standard deviation (PSD) <5% 경우로 정의하였다[15]. 시신경, 황반 또는 시야에 영향을 미칠 수 있는 안과적 혹은 신경과적 질환이 있는 경우는 연구에서 제외하였다. 섬유주절제술은 최대약물요법으로 안압 조절에 실패하거나 최대약물치료에도 불구하고 시신경 손상 혹은 시야 결손이 진행하는 경우에 시행하였다[9].
섬유주절제술은 1명의 수술자(J.W.L)에 의해서 시행되었다. 국소마취하에 원개기저결막편 형성을 위해 각막윤부 결막을 5-6 mm로 절개하여 결막과 테논낭을 결막낭 쪽으로 박리를 하고, 3 × 3 mm 크기, 2/3 공막 두께, 사다리꼴 모양의 공막편을 만들었다. 0.4 mg/mL의 희석된 MMC를 적신 Weck-cell 스펀지를 테논낭과 공막 사이에 2-3분 동안 접촉시킨 다음 스펀지를 제거하고 약 20 mL의 평형염기용액으로 세척을 시행하였다. 내측공막절개술을 시행하고 이를 통하여 주변홍채를 절제한 후 미리 공막편의 뒤쪽 모서리에 설치해둔 9-0 나일론 봉합사(Ethicon Inc., Johnson & Johnson, Somerville, NJ, USA)로 두 군데 개봉 봉합을 시행하여 공막편을 원위치에 봉합하였다.
이후 양막이식술을 병행한 군에서는 20 × 20 mm 정도 크기로 단층의 양막을 결막/테논낭 아래에 기저막쪽이 아래로 향하고 기질층을 위로 향하도록 위치시키고 각막 윤부쪽의 양막 부위를 10-0 나일론 봉합사(Ethicon Inc., Johnson & Johnson)로 두 군데 공막에 고정하였다(Fig. 1). 양막은 시판 중인 동결보존양막 제품(MS Amnion, MS BIO Inc., Seongnam, Korea)을 영하 40°C 이하의 냉동고에 보관하였다가 사용하였다.
이후 결막은 양쪽에서 10-0 나일론 봉합사(Ethicon Inc., Johnson & Johnson)를 이용하여 테논과 함께 공막에 고정봉합을 시행하였다. 전방천자 부위를 통해 평형염기용액을 주입하여 전방을 형성시키고 공막편을 통한 방수의 유출 정도와 결막 봉합 부분을 통한 방수 누출이 있는지 확인하였다. 수술 후 Levofloxacin (CravitⓇ, Santen Pharm, Co., Osaka, Japan), Prednisolone acetate (PredbellⓇ, CKD Pharm, Co., Seoul, Korea) 점안액을 사용하였고, 안압과 여과포의 상태에 따라 안구지압과 개봉봉합사 제거를 시행하였다.
수술 후 매번 방문 시마다 골드만압평안압과 최대교정시력을 측정하고, 사용하는 안압하강제 수와 합병증 발생 여부를 기록하였고, Indiana Bleb Appearance Grading Scale (IBAGS) [16]에 따라 여과포의 높이(Bleb height, H)와 범위(Horizontal extent, E), 혈관분포 정도(Vascularity, V), 여과포누출 정도(Seidel test, S)를 평가하여 여과포의 형태에 대해 분석하였다. 여과포의 높이 H0는 여과포의 상승 없이 평평한 경우, H1은 낮은 여과포 상승, H2는 중등도의 여과포 상승, H3는 높은 여과포 상승으로 분류되었다[16]. 여과포의 범위는 여과포의 수평 너비를 나타내고 E0는 1시각 미만, E1은 1시각 이상 2시각 미만, E2는 2시각 이상 4시각 미만, E3는 4시각 이상인 경우로 분류하였다[16]. 혈관분포 정도 V0는 미세낭포가 보이지 않는 무혈관 흰색(avascular white) 여과포, V1은 미세낭포가 보이는 무혈관 낭포성(avascular cystic) 여과포, V2는 경도 혈관분포, V3는 중등도 혈관분포, V4는 울혈된 혈관을 가진 과도한 혈관분포로 분류하였다[16]. 여과포의 누출 정도는 Seidel 검사에서 여과포 표면에서 방수의 누출이 나타나는 정도에 따라 3가지로 분류하여 S0는 여과포 누출이 없는 경우, S1은 형광물질도포 후 5초 이내에 흘러나오는 방수의 누출없이 여과포 표면의 여러 작은 지점에서 결막을 통한 누출이 보이는 경우(multiple pinpoint leak), S2는 형광물질 도포 후 5초 이내에 방수의 흐름이 보이는 누출(streaming aqueous leak)로 분류하였다[16].
섬유주절제술의 성공은 수술 후 안압하강제를 사용하지 않는 조건에서 안압이 18 mmHg 이하이고 수술 전에 비하여 안압이 20% 이상 하강한 경우로 정의하였다[17]. 수술 후 2번의 연속된 방문에서 성공 기준을 만족하지 못하는 경우와 2번의 연속된 방문에서 안압이 5 mmHg 이하인 경우, 광각인지를 못하는 경우, 안압 조절을 위해 녹내장수술이 필요한 경우를 수술 실패로 정의하였다[17]. 주사침을 이용한 여과포 복원술(Bleb needling)은 수술 실패로 간주하지 않았다[18]. 저안압은 수술 후 6주 이상 경과 관찰 후 2번의 연속된 검사에서 골드만압평 안압이 5 mmHg 이하인 경우로 정의하였으며, 지속되는 저안압은 수술 후 3개월 이상 경과 관찰 후 3번 이상의 연속적인 검사에서 골드만압평안압계로 측정한 안압이 5 mmHg 이하인 경우로 정의하였다[18].
통계 방법으로 데이터의 정규성을 검정하기 위해 Kolmogorov-Smirnov test를 시행하였다. 양막이식술을 병행한 군(양막이식술군)과 병행하지 않은 군(대조군)의 연속형 변수 비교를 위해 Mann-Whitney U-test를 사용하였고, 수술 전후 변수를 비교를 위해 Wilcoxon signed rank test를 사용하였다. 범주형 자료의 분석은 Chi-squared test 혹은 Fisher’s exact test를 이용하였다. 수술 성공률은 Kaplan-Meier 생존 분석을 사용하였고, Log-rank test를 이용하여 양막이식술을 병행한 군과 병행하지 않은 군의 수술 성공률을 비교하였다. 통계학적인 분석은 윈도우용 SPSS 19.0 (SPSS Inc., Chicago, IL, USA)을 이용하였고, p-value가 0.05 미만일 경우를 통계적으로 유의한 것으로 간주하였다.
총 79명 95안의 원발개방각녹내장 환자가 섬유주절제술을 시행 받았다. 양막이식술군은 46명 52안, 양막이식술을 시행하지 않은 대조군은 33명 43안이었다. 섬유주절제술 후 평균 경과 관찰 기간은 양막이식술군이 1.2 ± 0.4년, 대조군이 1.1 ± 0.1년이었다(p=0.601). 나이, 성별, 술 전 수정체 상태, 중심각막두께, 안축장길이, 구면대응치, 수술 전 평균 안압, 수술 전 사용한 평균 안압하강제 수와 시야검사의 PSD는 두 군 간에 통계적으로 유의한 차이가 없었다(모든 p≥0.127) (Table 1). 수술 전 측정한 최대교정시력, 시야검사의 Visual Field Index, mean deviation는 대조군이 양막이식술군보다 유의하게 더 낮았다(모든 p≤0.007) (Table 1).
수술 후 마지막 방문에서 측정한 평균 안압은 수술 전 안압에 비해 양막이식술군에서 30.2 ± 9.8 mmHg에서 11.6 ± 4.2 mmHg으로 58.4% 감소하였다(p<0.001) (Table 2). 수술 후 마지막 방문에서 측정한 평균 안압은 수술 전 안압에 비해 대조군에서 29.7 ± 7.4 mmHg에서 12.2 ± 4.5 mmHg으로 57.0% 감소하였다(p<0.001) (Table 2). 수술 전 안압을 포함하여 수술 후 안압을 월별로 비교 분석하였을 때, 각 시기별로 두 군 간에 통계적으로 유의한 차이는 없었다(Fig. 2).
마지막 방문 시 사용한 안압하강제의 평균 개수는 수술 전과 비교하여 양막이식술군과 대조군 모두에서 통계적으로 유의하게 감소하였다(모든 p<0.001) (Table 2). 수술 전 그리고 수술 후 마지막 방문 시의 평균 최대교정시력은 양막이식술군과 대조군 모두 수술 후 유의한 차이가 없었다(각각 p=0.649, p=0.693) (Table 2).
맥락막 삼출, 전방 얕아짐, 그리고 저안압이 각각 2안씩 양막이식술 군과 대조군에서 발생하였다(모든 p=1.000). 저안압 교정을 위해 경결막 공막편 봉합(transconjunctival scleral flap suture)은 양막이식술군 3안(5.77%), 대조군 4안(9.30%)에서 시행하였다(p=0.698). 주사침을 이용한 여과포 복원술(Bleb needling)은 양막이식술군 9안(17.31%), 대조군 5안(11.62%)에서 시행하였다(p=0.565) (Table 3). 수술 후 마지막 경과 관찰에서 2줄 이상의 시력저하가 양막이식술군에서는 관찰되지 않았고, 대조군 2안(4.65%)에서 발생하였다(p=0.202). 안구내염을 포함한 여과포 관련 감염은 두 군 모두에서 경과 관찰 기간 동안 발생하지 않았다.
Kaplan-Meier 생존 분석 결과, 수술 12개월 후 수술 성공률은 양막이식술군은 94.2%, 대조군은 85.8%였다. 두 군의 수술 성공률을 Log rank 분석 방법을 이용하여 비교한 결과, 양막이식술의 시행 여부에 따른 수술 성공률의 유의한 차이는 없었다(p=0.121) (Fig. 3).
섬유주절제술 후 여과포의 형태를 IBAGS에 따라 분류하여 두 군을 비교 분석하였다. 양막이식술군에서 여과포의 높이는 73.1%가 H2, 15.4%가 H1, 11.5%가 H3이었고, 대조군에서 여과포의 높이는 65.1%가 H2, 25.6%가 H1, 9.3%가 H3이었다(p=0.466). 여과포의 범위는 양막이식술군은 65.4%가 E2, 26.9%가 E3, 7.7%가 E1이었고, 대조군은 60.5%가 E2, 30.2%가 E3, 9.3%가 E1이었다(p=0.855). 혈관분포 정도는 양막이식술군은 90.4%가 V2, 7.7%가 V3, 1.9%가 V4이었고, 대조군은 18.6%가 V1, 76.7%가 V2, 4.7%가 V3였다. 무혈관 낭포성 여과포로 분류되는 V1은 양막이식술군에서는 관찰되지 않은 반면 대조군에서는 8안(18.6%)에서 관찰되었다(p=0.002) (Table 4).
양막이식술군 52안을 원발개방각녹내장 43안과 정상안압녹내장 9안으로 분류하여 IBAGS에 따라 여과포 형태를 비교 분석한 결과 여과포의 높이, 범위와 혈관분포 정도는 두 군 간 통계적으로 유의한 차이가 없었다(각각 p=0.709, p=1.000, p=0.630) (Table 5). Kaplan-Meier 생존 분석 결과, 수술 12개월 후 수술 성공률은 원발개방각녹내장군은 95.0%, 정상안압녹내장군은 88.9%였고, 두 군의 수술 성공률을 Log rank 분석 방법을 이용하여 비교한 결과, 수술 성공률의 유의한 차이는 없었다(p=0.939).
양막이식술군의 대표 증례인 71세 남성 원발개방각녹내장 환자는 본원에서 우안에 양막이식술을 병행한 섬유주절제술을 시행받고 수술 후 2년 동안의 경과 관찰 기간 동안 안압은 성공적으로 조절되었고, 합병증 발생은 없었다. 우안의 여과포는 중등도의 상승 높이, 4시간의 너비, 경도의 혈관분포 소견을 보였고, 방수 누출은 없었다(Fig. 4A). 대조군의 대표 증례인 82세 남성 원발개방각녹내장 환자는 본원에서 좌안에 양막이식술 없이 섬유주절제술을 시행받고 수술 후 2년 동안의 경과 관찰 기간 동안 안압은 성공적으로 조절되었다. 그러나 좌안의 여과포는 무혈관 낭포 소견을 보였다(Fig. 4B).
본 연구에서 원발개방각녹내장 환자에서 섬유주절제술과 동시에 시행한 양막이식술이 섬유주절제술의 임상성적에 미치는 영향을 알아보기 위해 양막이식술군과 양막이식술을 시행하지 않은 대조군을 비교 분석하였다. 두 군 모두에서 섬유주절제술 후 수술 전에 비하여 마지막 방문 시 안압은 유의하게 감소하였다. 수술 전, 수술 후 1, 3, 6, 9, 12개월에 두 군 간의 안압을 비교하였을 때, 수술 전 안압을 포함하여 두 군 간 유의한 차이는 없었다. 양막이식술군과 대조군의 수술 후 1년 성공률은 각각 94.2%, 85.8%로 수술 성공률의 유의한 차이는 없었다(p=0.121). 합병증의 발생 빈도 역시 두 군 간에 통계적으로 유의한 차이는 없었으나, 여과포 형태 측면에서 무혈관 낭포성 여과포가 양막이식술군에서는 관찰되지 않은 반면 대조군에서는 8안(18.6%)에서 관찰되었다(p=0.002).
본 연구에서 시행한 양막이식술을 병행한 섬유주절제술의 수술 후 1년의 성공률은 이전의 보고들과 유사하다[3,12]. Sheha et al [3]은 치료에 반응하지 않는 신생혈관녹내장, 이전 섬유주절제술이 실패한 녹내장, 위수정체 녹내장과 같은 난치성 녹내장 환자에서 MMC와 양막이식술을 병행한 섬유주절제술이 MMC만 이용한 섬유주절제술에 비해 성공률이 더 높고 합병증 발생 빈도는 더 낮았다고 보고하였다. 성공 기준을 안압하강제를 사용하지 않고 안압이 22 mmHg 미만으로 정의하였을 때, MMC와 양막이식술을 병행한 군은 1년 후 성공률은 80%였고, MMC만 이용한 군은 40%였다(p=0.03) [3]. 합병증 측면에서도 저안압이 MMC만 이용한 군은 3안(16.7%)에서 동반되었으나 양막이식술을 병행한 군은 발생하지 않았고, 테논낭포형성이 MMC만 이용한 군은 7안(38.9%), 양막이식술을 병행한 군은 1안(5.3%)에서 발생하였다고 보고하였다[3]. Yadava et al [12]도 원발개방각녹내장과 원발폐쇄각녹내장 환자에서 성공 기준을 안압하강제를 사용하지 않고 안압이 16 mmHg 미만인 경우로 정의하였을 때, MMC와 양막이식술을 병행한 군은 수술 후 1년 성공률은 85%이고, MMC만을 이용한 군은 60%로 양막이식술을 병행한 군의 성공률이 더 높았다고 보고하였다(p=0.04) [12].
본 연구에서 무혈관 낭포성 여과포가 양막이식술군에서는 관찰되지 않았으나, 양막이식술을 병행하지 않은 대조군에서는 8안(18.6%)에서 관찰되었다(p=0.002). MMC나 5-FU의 보조적 사용이 섬유주절제술의 수술 성공률을 높였으나, 무혈관 낭포성 여과포, 여과포 누출, 그리고 여과포 관련 감염의 증가와 관련있는 것으로 보고되었다[6,7]. Well et al [20]은 MMC를 이용한 섬유주절제술을 시행한 환자에서 원개기저결막편으로 수술한 17안 중 5안(29%)에서 낭포성 여과포가 동반되었다고 보고하였고, 국내에서도 MMC를 사용하여 원개기저결막으로 수술한 섬유주절제술 후 31안 중 5안(16.1%)에서 무혈관 낭포성 여과포가 형성됨을 보고하였다[21]. 특히 이전의 연구들에서 MMC를 사용하여 시행한 섬유주절제술 후 발생한 여과포 관련 감염안 모두에서 낭포성 여과포가 관찰된다고 보고되었고, 무혈관 낭포성 여과포의 존재 자체가 여과포 관련 감염 발생의 중요한 위험인자로 알려져 있다[22,23].
본 연구에서 무혈관 낭포성 여과포가 양막이식술군에서는 관찰되지 않았고, 이와 같은 결과는 이전에 양막이식술을 병행한 섬유주절제술의 임상성적을 보고한 연구들의 결과와 유사하다. Sheha et al [3]은 MMC와 양막이식술을 병행하여 섬유주절제술을 시행한 군에서는 넓고, 정상 혈관 분포를 가진 여과포가 관찰되는 반면, 양막이식술을 시행하지 않은 대조군에서는 무혈관 낭포성 여과포가 관찰된다고 하였다. Sarnicola et al [24]도 이전 섬유주절제술이 실패한 환자에서 양막이식술을 병행한 섬유주절제술을 시행한 결과 2년의 경과 관찰 기간 동안 무혈관 낭포성 여과포가 발생하지 않았고, 성공 기준을 안압하강제를 사용하지 않고 안압이 21 mmHg 미만인 경우로 정의하였을 때 95%의 수술 성공률을 보고하였다. 그리고 양막이식술을 병행한 섬유주절제술을 한 여과포의 상태를 IBAGS에 따라 분석하여 대부분(95%)이 H2, E2, V3, S0 정도로 중등도의 높이와 2시간에서 4시간 범위, 혈관분포를 가지고 있었다고 보고하였다[24]. 본 연구에서도 양막이식술을 병행한 군에서 IBAGS 분류에 따라 분석한 여과포 형태는 H2 (73.1%), E2 (65.4%), V2 (90.4%), S0 (100%)로 대부분 중등도 높이와 혈관 분포, 그리고 2시간에서 4시간 범위의 여과포를 관찰할 수 있었다.
특히, 조직검사에서 정상안압녹내장 환자의 결막기질두께는 64 ± 31 µm로 원발개방각녹내장의 결막기질두께 103 ± 44 µm보다 더 얇으므로 섬유주절제술 후 여과포 감염의 위험성이 더 높다고 보고하였고[8], Jongsareejit et al [9]은 정상 안압녹내장 환자 39명에서 MMC를 이용한 섬유주절제술 후 안압은 유의하게 하강하였으나 여과포 누출 1안, 여과포염 2안이 발생했다고 보고하였다. 이에 본 연구에서는 양막이식술을 병행한 군을 정상안압녹내장군과 원발개방각녹내장군으로 분류하여 비교 분석한 결과, 모든 군에서 경과 관찰 기간 동안 여과포 누출, 무혈관 낭포성 여과포, 여과포 감염 혹은 안구내염이 발생하지 않았고, 수술 성공률뿐 아니라 여과포 형태 측면에서도 여과포의 높이, 범위와 혈관분포 정도가 두 군 간에 통계적으로 유의한 차이가 없었다. 그러나, 본 연구에서 정상안압녹내장 환자는 9안으로 원발개방각녹내장 환자 43안에 비해 수가 적어 두 군의 임상성적을 비교하기에 제한점이 있을 것으로 생각된다.
이전 연구들과 본 연구 모두에서 양막이식술을 병행한 섬유주절제술은 성공적인 안압하강 효과를 가지고, 형성된 여과포는 중등도의 높이와 너비, 그리고 정상 혈관분포를 가지는 것으로 나타났다[3,12,24]. 이는 양막의 항염증, 항섬유화, 항혈관화 작용을 뒷받침하는 결과로 생각되고, 이식된 양막이 여과포 벽의 일부분으로 작용하여 무혈관 낭포성 여과포 발생을 방지하고 결막하 흡수를 통한 방수 유출을 촉진시키는 역할을 할 것으로도 생각된다[25]. 양막은 배양된 정상 결막 및 익상편의 섬유모세포에서 Transforming growth factor-β의 신호 전달을 하향 조절하여 항섬유화 작용과 관련이 있다고 보고되었다[26,27]. 또한 양막은 다형핵세포의 침윤을 막고 대식세포의 세포자멸사를 촉진하여 강력한 항염증 효과를 발휘하는 것으로 알려져 있다[28].
본 연구에서 양막이식술을 병행한 섬유주절제술 후 무혈관 낭포성 여과포는 발생하지 않고 넓게 확산되어 있고 중등도의 높이와 정상 혈관분포를 가지는 여과포가 관찰되었는데, 이와 같은 결과는 양막이식술을 병행한 섬유주절제술 후 여과포 내의 구조와 안압 조절에 대해서 초음파생체현미경을 이용하여 분석한 Nakamura et al [25]의 연구 결과와 유사하다. Nakamura et al [25]은 양막이식술을 병행한 섬유주절제술 후 형성된 여과포는 결막하 액체 공간의 높이가 높을수록, 양막이식술을 시행하지 않은 섬유주절제술 후 형성된 여과포는 여과포 벽의 반사력이 낮을수록 장기적으로 양호한 안압 조절과 연관이 있다고 보고하였고, 양막이식술을 병행한 섬유주절제술에서 방수의 유출은 결막을 통과하는 경로(transconjunctival pathway)보다는 주로 결막하 흡수(subconjunctival pathway)에 의해 일어난다고 추정하였다[25]. 따라서, 이전의 연구 결과들과 본 연구의 결과를 종합하여 유추해볼 때, 양막이식술을 병행한 섬유주절제술의 경우 방수의 유출은 주로 결막하 흡수와 관련되어 무혈관 낭포성 여과포의 형성을 방지하고 넓고 정상 혈관분포를 가진 여과포의 형성과 관련된다고 생각할 수 있다.
본 연구의 제한점으로 양막이식군과 대조군 사이에성별, 나이, 경과 관찰 기간, 술 전 수정체 상태, 시력, 안압, 사용 안약 개수, 중심각막두께, 안축장의 길이, 당뇨, 고혈압의 과거력 유무에는 통계적으로 유의한 차이가 없었으나, 시야검사에서 대조군이 양막이식술군보다 녹내장 손상이 더 진행된 상태였다.
섬유주절제술 후 방수가 누출되는 얇은 여과포의 조직분석연구에서 술잔 세포의 수가 감소되어 있음이 보고되었고[29], 오랜 기간 동안 안약의 사용이 결막 술잔 세포 밀도 감소와 관련이 있을 수 있다고 보고되었다[30]. 따라서, 본 연구의 결과 해석 시 오랜 기간의 약물 사용이 여과포 형태에 미치는 영향을 고려하여야 할 것으로 생각된다. 그러나, 본 연구에 포함된 환자들의 수술 전 안압하강제의 평균 사용 기간은 양막이식군은 3.2 ± 3.0년, 대조군은 4.8 ± 5.2년으로 통계적으로 유의한 차이는 없었다(p=0.104, Mann-Whitney U-test). 그리고 양막이식술을 병행한 섬유주절제술 후 1년 간의 단기 임상성적을 분석한 것으로 그 경과 관찰 기간이 비교적 짧고 대상 환자 수가 적은 점을 들 수 있다. 따라서 더 많은 환자를 대상으로 장기적인 경과 관찰 연구가 필요할 것으로 생각된다.
본 연구의 또 다른 제한점으로는 여과포 내부 구조 분석을 위한 전안부 빛간섭단층촬영검사를 시행하지 못한 점을 들 수 있다. 여과포에 대한 빛간섭단층촬영검사를 시행하여 삽입된 양막과 여과포의 관계, 그리고 변화 양상을 분석하여 두 군 간 수술 성공에 미치는 여과포 형태를 이해할 수 있을 것으로 기대된다. 본 연구에서 시행한 세극등현미경검사에 의한 여과포의 육안적 특성 분석은 여과포의 기능과 밀접한 연관성이 있으나, 수술 후 장기적인 수술 성공 혹은 실패와 관련된 여과포의 내부 구조를 관찰할 수 없다는 단점이 있다[31-37]. Jung et al [32]은 방수유출장치를 삽입한 76명의 환자에서 여과포에 대한 전안부 빛간섭단층촬영검사를 시행하여 여과포 벽의 최대 그리고 최소 두께가 술 후 최대 안압과 관련이 있고, 여과포 벽의 최대 두께가 수술의 성공과 관련이 있음을 보고하였다. Jung et al [33]은 방수유출장치를 삽입한 52명의 환자에서 술 후 6개월 동안 연속적으로 여과포에 대한 전안부 빛간섭단층촬영검사를 시행하여 술 후 1개월에 고안압기를 가진 환자군에서 1개월째 안압이 가장 높고 여과포 벽의 반사력이 최대였음을 보고하였다. Cho et al [38]은 여과포에 대한 3차원적 전안부 빛간섭단층촬영검사를 시행하여 레이저개봉봉합사 시행 후 안압의 감소는 여과포 내 액체 공간의 높이, 여과포의 두께, 여과포의 강도, 그리고 여과부 넓이의 증가와 관련이 있음을 보고하였다. Park and Ahn [39]은 원개기저결막편 섬유주절제술을 시행한 68안의 환자에서 안구 마사지 전과 후에 여과포에 대한 전안부 빛간섭단층촬영검사를 시행하여 수술 후 6개월에 안구 마사지 후 안압은 감소하고 빛간섭단층촬영검사에서 여과포의 유의한 변화가 있었고, 안압의 변화는 여과포 내부 공간의 수평 길이, 수직 길이, 높이, 여과포 전체 높이, 그리고 미세낭포의 수와 관련이 있음을 보고하였다. 또한, 섬유주절제술 후 여과포에 대한 빛간섭단층촬영검사와 여과포의 육안적인 특성을 동시에 분석한 이전 연구에 의하면, 여과포 특성을 육안적으로 분석하는 임상검사보다 빛간섭단층촬영검사에서 주사침을 이용한 여과포복원술을 필요로 하는 섬유성 피막을 더 일찍 발견할 수 있었음을 보고하여 세극등현미경검사로는 관찰할 수 없는 여과포의 심부 구조를 분석하기 위해 전안부 빛간섭단층촬영검사의 중요성을 강조하였다[37].
섬유주절제술의 성공은 내측 공막절개 부위를 통한 일정하고 제어된 방수의 누출과 결막 여과포의 안전성에 영향을 받는다고 알려져 있다[40]. 이식된 양막은 여과포 벽의 한부분으로 작용하여 앞서 언급한 항염증, 항섬유화, 그리고 항혈관 작용으로 공막절개 부위를 통한 방수의 일정한 흐름에 영향을 미칠 뿐만 아니라 여과포 벽에 가해지는 압력을 완화하여 여과포의 안전성에도 기여할 것으로 판단된다. 본 연구를 통하여 양막이식술을 병행한 섬유주절제술은 무혈관 낭포성 여과포, 여과포 관련 감염 발생 없이 안정적이고 효과적으로 안압을 하강시킬 수 있음을 알 수 있었다.
Figure 1.
Amniotic membrane transplantation was performed during trabeculectomy. 20 × 20 mm single layer of cryopreserved amniotic membrane was placed with stromal side facing up under the tenon’s capsule. The amniotic membrane was secured to the lateral side of scleral flap with two interrupted 10-0 nylon sutures.
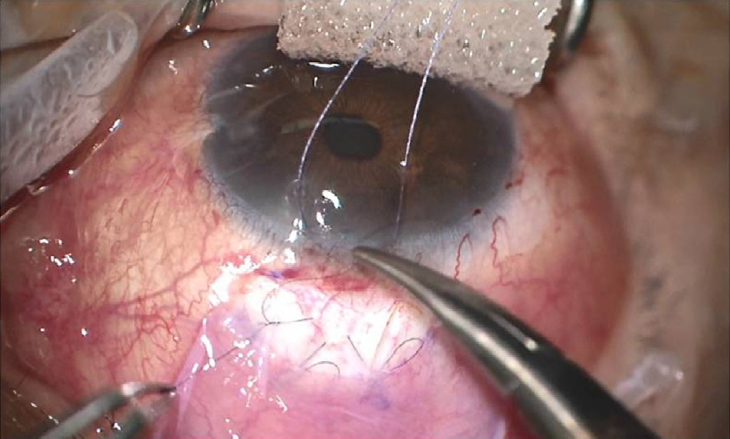
Figure 2.
Changes in mean intraocular pressure after trabeculectomy with or without amniotic membrane transplantation. Intraocular pressure at each time point was not significantly different between the two groups during entire study period. The figures indicate the number of patients followed-up at the time (with amniotic membrane transplantation/without amniotic membrane transplantation). The errors bars are 95% confidence intervals (mean ± standard error × 1.96). IOP = intraocular pressure; AMT = amniotic membrane transplantation.
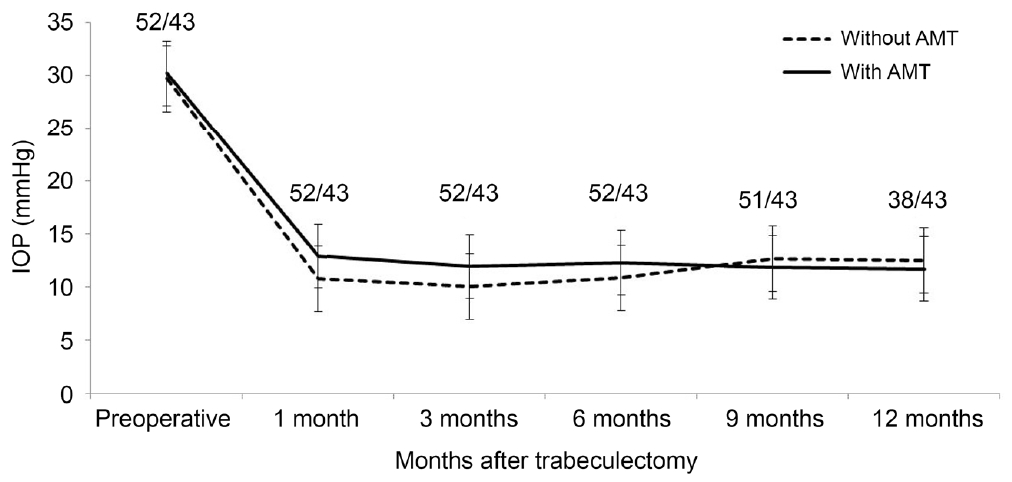
Figure 3.
Cumulative probabilities of surgical success after trabeculectomy with or without amniotic membrane transplantation in primary open-angle glaucoma. Success rate was not statistically significantly different between the two groups (Mantel-Cox log rank test). The mean (standard error) complete success rates at the first year of follow-up was 94.2% (3.2) for trabeculectomy with amniotic membrane transplantation group and 85.8% (5.4) for trabeculectomy without amniotic membrane transplantation group (p= 0.121). AMT = amniotic membrane transplantation.
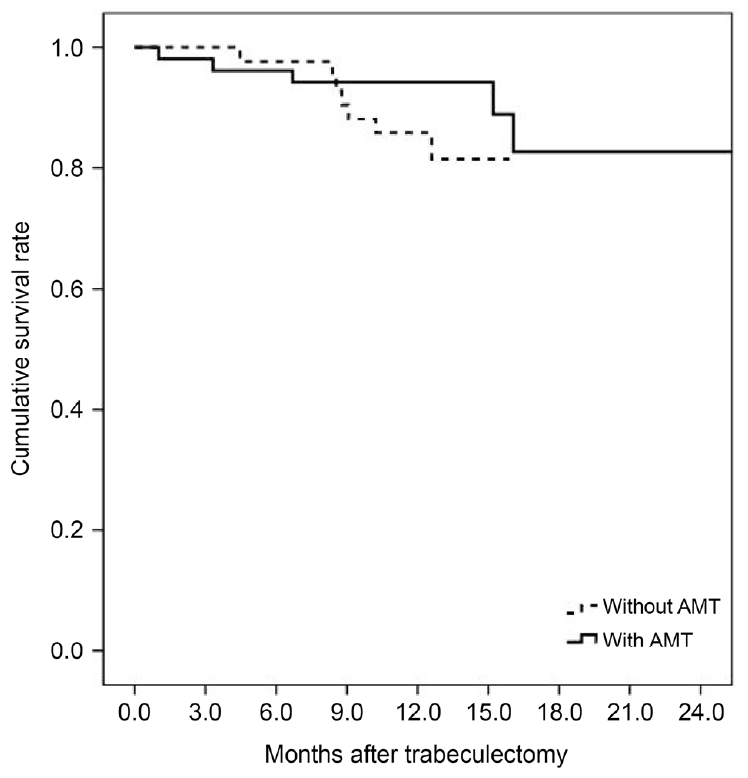
Figure 4.
Bleb photograph images of representative cases after trabeculectomy with and without amniotic membrane transplantation. A 71-year-old man had trabeculectomy with amniotic membrane transplantation on the right eye two years ago (A) and an 82-year-old man had trabeculectomy alone on the left eye two years ago (B). (A) Bleb photograph in the right eye shows bleb with medium height (H2), 4-clock hour extent (E3) and mild vascularity (V2). Intraocular pressure of the right eye was 14 mmHg. (B) Bleb photograph in the left eye shows avascular cystic bleb (V1) with high height (H3) and 2-clock hour extent (E2). Intraocular pressure of the left eye was 12 mmHg.

Table 1.
Demographics and clinical characteristics of patients with primary open-angle glaucoma with or without amniotic membrane transplantation
| Characteristic | With amniotic membrane transplantation | Without amniotic membrane transplantation | p-value |
|---|---|---|---|
| Number of eyes (patients) | 52 (46) | 43 (33) | - |
| Follow-up time (years) | 1.20 ± 0.36 | 1.08 ± 0.07 | 0.601* |
| Age (years) | 63.23 ± 16.96 | 58.15 ± 18.19 | 0.127* |
| Sex | 0.294† | ||
| Male | 30 (65.2) | 18 (54.5) | |
| Female | 16 (34.8) | 15(45.5) | 0.684† |
| Eye laterality | |||
| Right | 23 (44.2) | 21 (48.8) | |
| Left | 29 (55.8) | 22 (51.2) | |
| Diabetes mellitus | 16 (30.8) | 13 (30.2) | 1.000† |
| Hypertension | 21 (67.7) | 10 (23.3) | 0.084† |
| Preoperative lens status | 1.000† | ||
| Phakic | 26 (50.0) | 21 (48.8) | |
| Pseudophakic | 26 (50.0) | 22 (51.2) | |
| Central corneal thickness (μm) | 529.52 ± 36.59 | 533.40 ± 51.35 | 0.503* |
| Axial length (mm) | 24.87 ± 2.18 | 24.57 ± 2.29 | 0.346* |
| Spherical equivalent (diopters) | -2.45 ± 3.90 | -1.92 ± 2.20 | 0.991* |
| Preoperative IOP (mmHg) | 30.17 ± 9.76 (15-59) | 29.67 ± 7.41 (14-47) | 0.928* |
| Number of preoperative medications | 3.98 ± 0.64 (1-5) | 3.95 ± 0.61 (2-5) | 0.833† |
| Preoperative visual acuity (logMAR) | 0.27 ± 0.44 (3-0) | 0.66 ± 0.77 (3-0) | 0.007* |
| Visual field parameter | |||
| Visual Field Index (%) | 52.38 ± 31.30 | 33.88 ± 27.26 | 0.004* |
| Mean deviation (dB) | -16.75 ± 8.94 | -22.14 ± 7.78 | 0.004* |
| Pattern standard deviation (dB) | 7.58 ± 3.97 | 8.30 ± 4.11 | 0.422* |
Counting fingers at 30 cm was considered equivalent to the Snellen value 20/2,000, which corresponds to a logMAR of 2.0. Hand motion acuity was considered equivalent to the Snellen value 20/20,000, which corresponds to a logMAR of 3.0 [19]. Values are presented as mean ± standard deviation (range) or number (%) unless otherwise indicated.
IOP = intraocular pressure; logMAR = logarithm of the minimum angle of resolution.
Table 2.
Preoperative and postoperative intraocular pressure, number of glaucoma medication, visual acuity in patients who underwent trabeculectomy with or without amniotic membrane transplantation
| Preoperative | Postoperative | p-value* | |
|---|---|---|---|
| With amniotic membrane | |||
| IOP (mmHg) | 30.17 ± 9.76 (1559) | 11.58 ± 4.18 (631) | <0.001 |
| IOP reduction (%) | - | 58.40 ± 18.16 | - |
| Number of medication | 3.98 ± 0.64 (1-5) | 0.19 ± 0.79 (0-4) | <0.001 |
| Visual acuity (logMAR) | 0.27 ± 0.44 (3-0) | 0.27 ± 0.47 (3-0) | 0.649 |
| Without amniotic membrane transplantation | - | - | - |
| IOP (mmHg) | 29.67 ± 7.41 (1447) | 12.21 ± 4.52 (525) | <0.001 |
| IOP reduction (%) | - | 57.02 ± 16.45 | - |
| Number of medication | 3.95 ± 0.61 (2-5) | 0.35 ± 0.92 (04) | <0.001 |
| Visual acuity (logMAR) | 0.66 ± 0.77 (3-0) | 0.67 ± 0.75 (3-0) | 0.693 |
Table 3.
Complications after trabeculectomy with or without amniotic membrane transplantation in patients of primary open-angle glaucoma
| Postoperative complication | With amniotic membrane transplantation | Without amniotic membrane transplantation | p-value* |
|---|---|---|---|
| Shallow anterior chamber | 2 (3.85) | 2 (4.65) | 1.000 |
| Choroidal effusion | 2 (3.85) | 2 (4.65) | 1.000 |
| Hypotony | 2 (3.85) | 2 (4.65) | 1.000 |
| Transconjunctival scleral flap suture | 3 (5.77) | 4 (9.30) | 0.698 |
| Bleb needling | 8 (15.38) | 5 (11.62) | 0.565 |
| Decrease of visual acuity | 0 | 2 (4.65) | 0.202 |
Table 4.
Comparison of bleb morphology based on Indiana Bleb Appearance Grading Scale after trabeculectomy with or without amniotic membrane transplantation
| With amniotic membrane transplantation | Without amniotic membrane transplantation | p-value* | ||
|---|---|---|---|---|
| Bleb height (H0-H3) | 1 | 8 (15.4) | 11 (25.6) | 0.466 |
| 2 | 38 (73.1) | 28 (65.1) | - | |
| 3 | 6 (11.5) | 4 (9.3) | - | |
| Horizontal extent (E0-E3) | 1 | 4 (7.7) | 4 (9.3) | 0.855 |
| 2 | 34 (65.4) | 26 (60.5) | - | |
| 3 | 14 (26.9) | 13 (30.2) | - | |
| Vascularity (V0-V4) | 1 | 0 | 8 (18.6) | 0.002 |
| 2 | 47 (90.4) | 33 (76.7) | - | |
| 3 | 4 (7.7) | 2 (4.7) | - | |
| 4 | 1 (1.9) | 0 | - |
Table 5.
Comparison of bleb morphology based on Indiana Bleb Appearance Grading Scale after trabeculectomy with amniotic membrane transplantation in primary open-angle glaucoma versus normal-tension glaucoma
| Primary open-angle glaucoma | Normal-tension glaucoma | p-value* | ||
|---|---|---|---|---|
| Bleb height (H0-H3) | 1 | 7 (16.3) | 1 (11.1) | 0.709 |
| 2 | 30 (69.8) | 8 (88.9) | - | |
| 3 | 6 (14.0) | 0 | - | |
| Horizontal extent (E0-E3) | 1 | 3 (7.0) | 1 (11.1) | 1.000 |
| 2 | 28 (65.1) | 6 (66.7) | - | |
| 3 | 12 (27.9) | 2 (22.2) | - | |
| Vascularity (V0-V4) | 2 | 39 (90.7) | 8 (88.9) | 0.630 |
| 3 | 3 (7.0) | 1 (11.1) | - | |
| 4 | 1 (2.3) | - | - |
REFERENCES
1) Khaw PT, Chiang M, Shah P, et al. Enhanced trabeculectomy-the moorfields safer surgery system. In: Bettin P, ed. Glaucoma Surgery, 1st ed. Basel: Karger Publishers, 50:2012;1-28.
2) Gong D, Jun L, Tsai JC. A quantitative analysis of the relationship between Medicare payment and service volume for glaucoma procedures from 2005 through 2009. Ophthalmology 2015;122:1049-55.


3) Sheha H, Kheirkhah A, Taha H. Amniotic membrane transplantation in trabeculectomy with mitomycin C for refractory glaucoma. J Glaucoma 2008;17:303-7.


4) Lama PJ, Fechtner RD. Antifibrotics and wound healing in glaucoma surgery. Surv Ophthalmol 2003;48:314-46.


5) Yoon PS, Singh K. Update on antifibrotic use in glaucoma surgery, including use in trabeculectomy and glaucoma drainage implants and combined cataract and glaucoma surgery. Curr Opin Ophthalmol 2004;15:141-6.


6) DeBry PW, Perkins TW, Heatley G, et al. Incidence of late-onset bleb-related complications following trabeculectomy with mitomycin. Arch Ophthalmol 2002;120:297-300.


7) Higginbotham EJ, Stevens RK, Musch DC, et al. Bleb-related endophthalmitis after trabeculectomy with mitomycin C. Ophthalmology 1996;103:650-6.


8) Van Ginderdeuren R, Vandewalle E, Pinto LA, et al. The conjunctiva in normal tension glaucoma patients is thinner than in primary open-angle glaucoma patients: a comparative histologic study. J Glaucoma 2016;25:e546-9.


9) Jongsareejit B, Tomidokoro A, Mimura T, et al. Efficacy and complications after trabeculectomy with mitomycin C in normal-tension glaucoma. Jpn J Ophthalmol 2005;49:223-7.



10) Drolsum L, Willoch C, Nicolaissen B. Use of amniotic membrane as an adjuvant in refractory glaucoma. Acta Ophthalmol Scand 2006;84:786-9.


11) Eliezer RN, Kasahara N, Caixeta-Umbelino C, et al. Use of amniotic membrane in trabeculectomy for the treatment of glaucoma: a pilot study. Arq Bras Oftalmol 2006;69:309-12.



12) Yadava U, Jaisingh K, Dangda S, et al. Simultaneous use of amniotic membrane and mitomycin C in trabeculectomy for primary glaucoma. Indian J Ophthalmol 2017;65:1151-5.



13) Li W, He H, Chen YT, et al. Reversal of myofibroblasts by amniotic membrane stromal extract. J Cell Physiol 2008;215:657-64.



14) Lee JW, Park WY, Kim EA, Yun IH. Tissue response to implanted ahmed glaucoma valve with adjunctive amniotic membrane in rabbit eyes. Ophthalmic Res 2014;51:129-39.


15) Foster PJ, Buhrmann R, Quigley HA, Johnson GJ. The definition and classification of glaucoma in prevalence surveys. Br J Ophthalmol 2002;86:238-42.



16) Cantor LB, Mantravadi A, WuDunn D, et al. Morphologic classification of filtering blebs after glaucoma filtration surgery: the Indiana Bleb Appearance Grading Scale. J Glaucoma 2003;12:266-71.


17) Fontana H, Nouri-Mahdavi K, Lumba J, et al. Trabeculectomy with mitomycin C: outcomes and risk factors for failure in phakic open-angle glaucoma. Ophthalmology 2006;113:930-6.


18) Gedde SJ, Schiffman JC, Feuer WJ, et al. Treatment outcomes in the tube versus trabeculectomy (TVT) study after five years of follow-up. Am J Ophthalmol 2012 153:789-803. e2.



19) Holladay JT. Proper method for calculating average visual acuity. J Refract Surg 1997;13:388-91.


20) Wells AP, Cordeiro MF, Bunce C, Khaw PT. Cystic bleb formation and related complications in limbus-versus fornix-based conjunctival flaps in pediatric and young adult trabeculectomy with mitomycin C. Ophthalmology 2003;110:2192-7.


21) Lee BH, Choi WS, Lee JW, Lee KW. Bleb morphology of fornixbased versus limbus-based conjunctival flaps in trabeculectomy with mitomycin C. J Korean Ophthalmol Soc 2011;52:1461-9.

22) Mochizuki K, Jikihara S, Ando Y, et al. Incidence of delayed onset infection after trabeculectomy with adjunctive mitomycin C or 5-fluorouracil treatment. Br J Ophthalmol 1997;81:877-83.



23) Rai P, Kotecha A, Kaltsos K, et al. Changing trends in the incidence of bleb-related infection in trabeculectomy. Br J Ophthalmol 2012;96:971-5.


24) Sarnicola V, Millacci C, Ibanez PT, et al. Amniotic membrane transplantation in failed trabeculectomy. J Glaucoma 2015;24:154-60.


25) Nakamura M, Naka M, Tatsumi Y, et al. Filtering bleb structure associated with long-term intraocular pressure control after amniotic membrane-assisted trabeculectomy. Curr Eye Res 2012;37:239-50.


26) Tseng SC, Li DQ, Ma X. Suppression of transforming growth factor-beta isoforms, TGF-beta receptor type II, and myofibroblast differentiation in cultured human corneal and limbal fibroblasts by amniotic membrane matrix. J Cell Physiol 1999;179:325-35.


27) Lee SB, Li DQ, Tan DT, et al. Suppression of TGF-ß signaling in both normal conjunctival fibroblasts and pterygial body fibroblasts by amniotic membrane. Curr Eye Res 2000;20:325-34.


28) Li W, He H, Kawakita T, et al. Amniotic membrane induces apoptosis of interferon-γ activated macrophages in vitro. Exp Eye Res 2006;82:282-92.


29) Francis BA, Du LT, Najafi K, et al. Histopathologic features of conjunctival filtering blebs. Arch Ophthalmol 2005;123:166-70.


30) Broadway DC, Chang LP. Trabeculectomy, risk factors for failure and the preoperative state of the conjunctiva. J Glaucoma 2001;10:237-49.


31) Singh M, Chew PT, Friedman DS, et al. Imaging of trabeculectomy blebs using anterior segment optical coherence tomography. Ophthalmology 2007;114:47-53.


32) Jung KI, Lim SA, Park HYL, Park CK. Visualization of blebs using anterior-segment optical coherence tomography after glaucoma drainage implant surgery. Ophthalmology 2013;120:978-83.


33) Jung KI, Park H, Jung Y, Park CK. Serial changes in the bleb wall after glaucoma drainage implant surgery: characteristics during the hypertensive phase. Acta Ophthalmol 2015;93:e248-53.


34) Kokubun T, Kunikata H, Tsuda S, et al. Quantification of the filtering bleb’s structure with anterior segment optical coherence tomography. Clin Exp Ophthalmol 2016;44:446-54.


35) Kokubun T, Tsuda S, Kunikata H, et al. Anterior-segment optical coherence tomography for predicting postoperative outcomes after trabeculectomy. Curr Eye Res 2018;43:762-70.


36) Tsutsumi-Kuroda U, Kojima S, Fukushima A, et al. Early bleb parameters as long-term prognostic factors for surgical success: a retrospective observational study using three-dimensional anteriorsegment optical coherence tomography. BMC Ophthalmol 2019;19:155.




37) Waibel S, Spoerl E, Furashova O, et al. Bleb morphology after mitomycin-C augmented trabeculectomy: comparison between clinical evaluation and anterior segment optical coherence tomography. J Glaucoma 2019;28:447-51.


38) Cho HK, Kojima S, Inoue T, et al. Effect of laser suture lysis on filtration openings: a prospective three-dimensional anterior segment optical coherence tomography study. Eye (Lond) 2015;29:1220-5.




39) Park HYL, Ahn MD. Imaging of trabeculectomy blebs with Visante anterior segment optical coherence tomography after digital ocular compression. Jpn J Ophthalmol 2012;56:38-45.



40) Choplin NT, Traverso CE. Atlas of Glaucoma, 1st ed. London: CRC press, 2014;241-52.
-
METRICS

- Related articles
-
Clinical Characteristics of First-Degree Relatives with Primary Open-Angle Glaucoma.2015 March;56(3)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



