 |
 |
| J Korean Ophthalmol Soc > Volume 65(1); 2024 > Article |
|
국문초록
대상과 방법
2015년 10월부터 2021년 3월까지 백내장수술만 시행한 환자 228명의 228안을 분석하였다. 수술 전 LENSTAR로 9가지 공식의 예측 굴절값을 구하였다. 수술 후 2달째 실제 굴절값을 2가지 intraocular lens의 종류, 안축장, Keratometry (K)값에 따라 나누어 굴절값의 오차(mean prediction error, ME)와 절대오차(mean absolute error, MAE), 절대오차의 중간값(median absolute error, MedAE), MAE가 ± 0.50 diopters (D), ± 0.75 D, ± 1.00 D 이내 비율을 구하였다.
결과
두 인공수정체 모두 MAE는 Haigis가 가장 높은 정확도를 보였으며 그 다음 Barrett Universal II (Barrett II)와 Olsen이었다. MAE가 0.50 D 이내 비율 가장 높은 공식은 Haigis였다. AXL≥25 mm 20안에서 MAE는 Hoffer Q가 가장 정확하였고 그 다음은 Olsen과 Barrett II였다. MAE가 0.50 D 이내 비율이 높은 공식은 Hoffer Q였다. K≥46 D 24안에서 MAE와 MedAE는 Haigis가 정확하였으며 그 다음은 Barrett II였다. MAE가 0.50 D 이내 비율이 높은 공식은 Holladay, Barrett II, Haigis 순이었다.
ABSTRACT
Methods
This study is retrospective consecutive case series. A total of 228 eyes of 228 patients who underwent uncomplicated cataract surgery between October 2015 and March 2021 were included. The accuracy of nine IOL calculation formulas (Kane, Emmetropia verifying optical version, Hill-radial basis function, Olsen, Barrett Universal II [Barrett II], Haigis, Holladay, Hoffer, and SRK/T) was compared and analyzed using differences between the predicted refractive power and actual refractive power at 2 months after cataract surgery. Mean prediction error (ME), mean absolute error (MAE), median absolute error (MedAE), and the percentage of eyes that were within ± 0.50 diopters (D), ± 0.75 D, and ± 1.00 D of the target refraction were calculated for each formula.
Results
For all eyes, Haigis formula was the most accurate in MAE, followed by Barrett II formula. Comparing the probability of MAE within 0.50 D, Haigis formula showed the highest accuracy. A total of 20 eyes of 20 patients had more than 25 mm axial length. Regarding MAE, Hoffer Q was the most accurate, followed by the Olsen formula. Comparing the probability of MAE within 0.50 D, the Hoffer Q formula was the most accurate. A total of 24 eyes of 24 patients had more than 46 D keratometry. Regarding MAE and MedAE, Haigis was the most accurate, followed by the Barrett II formula. Comparing the probability of MAE within 0.5 D, Holladay formula was the most accurate.
백내장수술에 있어서 수술 중 사용할 인공수정체(intraocular lens, IOL)의 도수를 계산하고 결정하는 것은 중요하다. 수술 후 최상의 굴절값을 얻기 위해 현재까지 여러 가지의 인공수정체 도수를 계산하는 공식이 개발되었다.1-3 기존 공식은 안구에서 측정된 매개변수를 사용하고 유효한 수정체 위치(effective lens position, ELP) 예측에 중점을 두었다. SRK/T 및 Holladay 1 공식은 ELP를 계산하기 위해 안축장(axial length, AXL) 및 각막곡률(keratometry, K)을 사용하였다.4,5 Hoffer Q 공식은 수술 후 ELP 추정을 위해 전방깊이(anterior chamber depth, ACD), AXL 및 K를 사용하였다.6,7 Haigis 공식은 ACD 및 AXL을 사용하였고 Holladay 2 공식은 ELP를 계산하기 위해 각막곡률, 각막윤부직경(whiteto-white, WTW), 굴절값, ACD 및 AXL을 사용하였다.8 Barrett Universal II 공식(Barrett II)은 해부학적 깊이를 통해 ELP를 결정하고, IOL 주 평면의 물리적 위치와 관련된 렌즈 계수를 활용하고, 인공수정체에 대한 주 평면의 변화를 계산하였다.9 Olsen and Hoffmann10은 인공수정체의 수술 후 위치를 결정하는 수정체의 수술 전 두께 비율을 나타내는 C상수를 사용하였다. 이러한 기존 공식은 정확한 안구 모델과 복잡한 수학 공식이 필요하다.11 따라서 공식에 사용되는 매개변수의 수가 증가해왔고 공식 또한 복잡해졌다. 그럼에도 불구하고 거대 각막, 공막화 각막 등 비정상적인 모양을 가진 눈에서는 굴절이상이 발생할 수 있으며, 더 정확한 공식이 개발되어야 한다.12
최근 개발된 Hill-Radial Basis Function (Hill-RBF) 공식은 패턴인식, 자가학습 또는 자가조직화, 경계모델을 통한 자가검증, 빅데이터 실습 등 인공신경망을 이용하여 인공수정체의 도수를 계산한다.13 가장 큰 장점인 인공신경망의 핵심은 관찰된 데이터로부터 학습하고 원하는 근사 함수를 생성하는 능력이다. 14 Emmetropia verifying optical version 2.0 (EVO 2.0) 공식은 정시화 이론에 기반한 새로운 두꺼운 렌즈 공식으로 최근 개발되었다.15 또한 Kane 공식은 인공지능의 회귀분석과 이론적인 광학을 기반으로 한 요소를 이용한 새로운 공식이다.16 여러 연구가 보고되었지만, 이 공식들의 정확성을 검증하는 것이 필요하다. 이에 본 연구에서는 굴절이상 예측을 위한 Hill-RBF, Kane 및 EVO 2.0 공식을 포함한 9개의 IOL 도수 계산 공식의 정확도를 평가하였다.
이 후향적 연구는 헬싱키선언의 원칙에 따라 수행되었으며 임상심사위원회의 검토 및 승인을 받았다. 연구의 후향적 특성으로 인해 정보에 입각한 동의에 대한 요구사항이 면제되었으며 2015년 10월부터 2021년 3월까지 내원한 환자들의 진료차트를 후향적으로 검토하였다. 이 연구에는 2가지의 IOL (SN60WF, Alcon Inc., Fort Worth, TX, USA; ZCB00, AMO Inc., Santa Ana, CA, USA)로 수정체유화술 및 후방 인공수정체삽입술을 받은 228명의 환자 228안이 포함되었다. IOL 고랑 삽입술, IOL 공막고정술 또는 유리체절제술을 병행한 환자는 제외하였다. 각막혼탁, 각막이영양증, 원추 각막 또는 망막이상이 있는 환자 또한 제외되었다. 표본 수 산출은 검정력 0.80, 유의수준 0.05에서 ClinCalc calculator를 사용하였으며 두 그룹 비교 시 총 125명의 대상이 필요한 것으로 나타났다. 전체 환자군은 IOL 종류에 따라 ALCON® SN60WF (Alcon Inc.)와 TECNIS® ZCB00 (AMO Inc.) 두 군으로 분류하였을 때와 AXL을 기준으로 <25.0 mm와 ≥25.0 mm 또는 K값을 기준으로 <46 diopters (D)와 ≥ 46 D로 나누었을 때를 각 공식별로 나누어 비교 분석하였다. 17-19 ALCON® SN60WF 및 TECNIS® ZCB00를 삽입한 모든 백내장수술은 결막하 마취 후 상측 투명각막 절개(2.75 mm)로 백내장초음파유화술을 시행하였고, 수술 절개창은 봉합하지 않고 절개창의 각막수화를 시행한 후 수술을 종료하였다.
수술 전 환자의 안축장(AXL), 각막곡률, 중앙각막두께, 전방깊이, 렌즈 두께, 각막윤부직경(WTW)을 LENSTAR (LS900, Gaag-Streit AG, Koeniz, Switzerland)를 이용하여 측정하였다. 인공수정체 도수 계산은 Hill-RBF, Olsen, Barrett II, Haigis, Holladay, Hoffer Q, and SRK/T 공식을 LENSTAR를 이용하였으며 Kane, EVO 2.0 공식은 online calculator를 사용하였다. 공식별 상수는 User Group for Laser Interference Biometry (ULIB) web site에서 제공되는 최적화된 인공수정체 상수를 사용하였다.19,20
대부분의 환자에서 목표 굴절값은 약간의 근시화였다(+0.0 D to -0.50 D). 실제 술 후 굴절값은 TOPCON KR-800으로 수술 후 최소 2개월 후에 측정하였다. 9개의 인공수정체 계산 공식(Hill-RBF, Kane, EVO 2.0, Olsen, Barrett II, Haigis, Holladay 2, Hoffer, SRK/T)의 정확도를 수술 후 2개월 시점에서 실제 굴절력과 수술 전 예상 굴절력의 차이를 비교 분석하였다. 굴절예측오차(prediction error, PE)는 각 공식에 대한 실제 수술 후 굴절 결과와 예상 굴절(실제 수술 후 굴절-예측 굴절)의 차이로 계산하였다. 평균 예측오차(mean prediction error, ME)와 표준편차(standard deviation [SD] of PE), 평균 절대오차(mean absolute error, MAE) 및 절대오차의 중앙값(median absolute error, MedAE)을 각 공식에 대해 계산하였다. 목표 굴절의 ± 0.5 D, ± 0.75 D, ± 1.0 D 내에 포함된 비율을 각 공식별로 평가하였다.
각 공식별 ME가 0을 벗어난 정도를 평가하기 위해 일표본 t-검정 또는 Wilcoxon signed-rank test를 사용하였다. ME와 MAE 비교를 위해 Friedman test와 Bonferroni correction with Wilcoxon test를 시행하였으며 목표 굴절의 ± 0.5 D, ± 0.75 D, ± 1.0 D 내로 포함된 비율을 비교하기 위해 Cochran Q test와 McNemar test를 시행하였다. 통계학적 분석은 SPSS 28.0 (IBM Corp., Armonk, NY, USA)을 이용하였고, p값이 0.05 미만인 경우를 통계학적으로 유의하다고 정의하였다.
대상 인원은 228명 228안으로, ALCON® SN60WF (1-piece acrylic IOL)가 87명 87안, TECNIS® ZCB00 (1-piece acrylic IOL)이 141명 141안이었다. 환자의 인구통계학적 정보 및 술 전 측정변수를 Table 1에 기술하였다. 인공수정체는 모두 1-piece acryclic IOL이고, 전체 크기는 13.0 mm, 광학부 크기는 6.0 mm로 동일하였다(Table 2).
TECNIS® ZCB00군에서 ME를 비교하였을 때 모든 공식 중에서 Kane (0.011 ± 0.528 D)이 가장 정확하였으며 이어서 Olsen과 Barrett II (-0.017 ± 0.502 D and -0.039 ± 0.498 D) (Table 3)의 정확도가 높았다. EVO 2.0 공식의 ME는 0.085 ± 0.500 D였다. Holladay, Hoffer Q, SRK-T는 근시화된 결과를 보였다(-0.163 ± 0.509 D, -0.111 ± 0.518 D, and -0.189 ± 0.538 D). MAE를 비교하였을 때, Haigis 공식이 가장 정확하였으며(0.395 ± 0.327 D) 그 다음으로 Barrett II (0.400 ± 0.296 D)와 Olsen (0.395 ± 0.308 D)이었다(Table 3). MAE에서 Haigis는 Holladay와 SRK/T 공식보다 유의하게 정확도가 높았으며(p=0.041 and p=0.001) (Table 3), SRK/T 공식이 가장 많은 오차를 보였다(0.468 ± 0.324 D). MedAE에서는 Haigis가 제일 정확하였고(0.290 D), 그 다음 Kane과 EVO 2.0이었다(0.310 D) (Table 3). MAE가 0.50 D 이내인 비율을 비교해 보았을 때 Barrett II 공식(70.2%)이 가장 높은 비율을 보였고, 그 다음은 Olsen 공식(68.8%)과 EVO 2.0 공식(68.8%)이었다(Table 4). Barrett II 공식은 SRK/T 공식과 유의한 차이를 보였다(p=0.002, McNemar test) (Table 4). MAE가 1.0 D 이내인 비율은 Barrett II가 94.3%였으나 다른 공식과 유의한 차이는 없었다.
ALCON® SN60WF에서 ME를 비교하였을 때 모든 공식 중에서 Barrett II (0.027 ± 0.461 D)로 가장 정확하였으며 이어서 SRK/T과 Haigis (-0.031 ± 0.496 D and -0.044 ± 0.452 D) (Table 3)의 정확도가 높았다. EVO 2.0 공식의 ME는 0.277 ± 0.450 D였다. Barrett II를 제외한 모든 공식은 근시화된 결과를 보였다(Table 3). MAE를 비교하였을 때, Haigis 공식이 가장 정확하였으며(0.344 ± 0.293 D) 그 다음으로 Hoffer Q (0.358 ± 0.312 D)와 Holladay (0.359 ± 0.303 D)였다(Table 3). MAE에서 Haigis는 Holladay와 SRK/T 공식보다 유의하게 정확도가 높았다(p=0.042 and p=0.016) (Table 3). MedAE에서는 Hoffer Q가 제일 정확하였고(0.240 D), 그 다음 Barrett II와 Haigis였다(0.280 D). MAE가 0.50 D 이내인 비율에서 Haigis 공식이 가장 정확하였으며(75.9%) 이는 Kane 공식과 유의한 차이를 보였다(p=0.035, McNemar test) (Table 4). MAE가 1.0 D 이내인 비율은 Hoffer Q가 97.7%였으나 다른 공식과 유의한 차이는 없었다(Table 4). TECNIS® ZCB00과 ALCON® SN60WF 두 가지 IOL 사이에 각 공식별 유의미한 차이는 나타나지 않았다(Table 3).
전체 228명을 AXL 따라 두 군으로 나누었을 때 각 군의 술 전 측정변수를 Table 5에 기술하였다. AXL이 더 긴 군에서 유의하게 전방의 깊이가 더 깊고 각막곡률은 더 낮았다(p=0.001, p=0.006, Mann-Whitney test). AXL<25 mm (208안)인 경우 ME를 기준으로 Barrett II 공식이 -0.013 ± 0.487 D로 가장 정확하였으며 Hill-RBF (-0.020 ± 0.525 D), Olsen (-0.023 ± 0.500 D) 순이었다(Table 6). MAE에서는 Haigis (0.374 ± 0.290 D)가 가장 정확도가 높았으며 그 다음으로는 Olsen (0.386 ± 0.310 D)과 Barrett II (0.387 ± 0.300 D)였다(Table 6). MedAE에서는 Haigis가 가장 정확하였고(0.290 D), 그 다음 Barrett II였다(0.300 D). MAE의 0.5 D 이내 비율에서 Haigis (70.2%)와 Barrett II (70.2%)가 가장 높았으며 SRK/T는 62.5%였다(Table 6). MAE 0.5 D 이내 비율은 SRK/T 공식은 유의하게 Haigis와 Barrett II 공식보다 낮았다(p=0.024, p=0.012, McNemar test).
AXL ≥25 mm (20안)인 눈의 경우, Holladay 공식이 ME에서 가장 정확하였고(-0.017 ± 0.555 D), Barrett II (-0.020 ± 0.461 D)과 SRK/T 공식(-0.049 ± 0.591 D)이 그 뒤를 이었다(Table 6). Hoffer Q 공식은 다른 공식과 달리 원시화(0.109 ± 0.457 D)된 결과를 보였다(p<0.05) (Table 5). MAE의 경우, Hoffer Q 공식이 가장 정확하고(0.347 ± 0.225 D), Olsen (0.374 ± 0.390 D), Barrett II (0.378 ± 0.360 D)가 그 다음이었다. SRK/T (0.488 ± 0.510 D) 및 Holladay (0.446 ± 0.360 D)는 Hoffer Q보다 유의하게 낮았다(p=0.029 and p=0.019, Wilcoxon rank test) (Table 6). MedAE에서는 Hoffer Q가 가장 정확하였고(0.300 D), 그 다음 Barrett II, Holladay, Kane은 동일하였다(0.360 D) (Table 5). 0.5 D 이내의 MAE 비율을 비교하면 Olsen (80.0%)이 가장 높은 정확도를 보였고, Hoffer Q는 75.0%, SRK/T는 50.0%였다(Table 6).
전체 228명을 K값에 따라 두 군으로 나누었을 때 각 군의 술 전 측정변수를 Table 5에 기술하였다. K값이 더 큰 군에서 유의하게 안축장이 짧았다(p<0.001, Mann-Whitney test). K<46 D (204안)인 경우 ME를 기준으로 Barrett II 공식이 0.001 ± 0.493 D로 가장 정확하였으며 Hill-RBF (-0.023 ± 0.527 D), Olsen (-0.040 ± 0.499 D) 순이었다(Table 7). MAE에서는 Haigis (0.387 ± 0.318 D)가 가장 정확도가 높았으며 그 다음으로는 Olsen (0.389 ± 0.315 D)과 Barrett II (0.395 ± 0.295 D)였다(Fig. 1, Table 7). MedAE에서는 Haigis가 가장 정확하였다(0.310 D). MAE의 0.5 D 이내 비율에서 Hoffer Q (70.1%)가 가장 높았으며 Barrett II (69.1%)와 Haigis (69.1%)가 그 다음이었고 SRK/T는 61.8%였다(Table 7). MAE 0.5 D 이내 비율은 SRK/T 공식은 유의하게 Hoffer Q와 Barrett II 공식보다 낮았다(p=0.005, p=0.018, McNemar test).
K ≥ 46 D (24안)인 눈의 경우, Haigis 공식이 ME에서 가장 정확하였고(0.032 ± 0.381 D), Hill-RBF (-0.047 ± 0.438 D)와 Olsen 공식(0.056 ± 0.411 D)이 그 뒤를 이었다(Table 7). MAE의 경우, Haigis 공식이 가장 정확하고(0.278 ± 0.263 D), Barrett II (0.309 ± 0.234 D), Olsen (0.345 ± 0.230 D)이 그 다음이었다. SRK/T (0.481 ± 0.329 D)는 Haigis보다 유의하게 낮았다(p=0.010, Wilcoxon rank test) (Fig. 1, Table 7). MedAE에서는 Haigis가 가장 정확하였고(0.235 D), 그 다음 Barrett II (0.245 D)와 Hoffer Q (0.275 D) 순이었다(Table 7). 0.5 D 이내의 MAE 비율을 비교하면 Holladay (83.3%)가 가장 높은 정확도를 보였고, Haigis는 79.2%, Barrett은 79.2% SRK/T는 58.3%였다(Table 7).
IOL 도수 계산의 주요 오류 원인은 측정 오류이다.21 때문에 안구 생체계측기는 더 정확한 생체 매개변수를 측정하기 위해 개발되어 왔으며 공식들은 정확도를 높이기 위해 더 많은 매개변수를 추가하며 발전되었다.11 Olsen 및 Barrett II 공식과 같은 최근에 개발된 공식은 더 정확한 IOL 도수 계산을 위해 각막윤부직경(WTW), K값, AXL, ACD, lens thickness 및 central corneal thickness를 사용하였고,15 인공지능을 사용하는 Hill-RBF 공식, Kane과 EVO 2.0 등의 새로운 공식도 개발되었다.22,23 이에 본 연구에서는 IOL 도수 계산 공식의 정확성을 비교하였다. ME, MAE 및 MedAE, 0.5 D 내의 백분율을 사용하여 공식의 정확도를 비교하였다. 각 지표에 따라 공식의 정확도에 차이가 있었다. ME는 쉽게 오차값을 계산할 수 있지만 양수 혹은 음수값으로 표시되기 때문에 서로 상쇄될 수 있어 공식의 정확도를 반영하지 못한다.24,25 따라서 오차의 절대 수치인 MAE가 ME보다 공식의 정확도를 더 많이 반영한다.24 또한 공식의 정확도는 목표에 대한 근접성을 통해 평가할 수 있으며, 이는 0.5 D 내의 비율로 측정할 수 있다.26 한편 MAE 또한 중앙값을 멀리 벗어나는 케이스가 추가되면 평균값을 크게 움직일 수 있으므로 MedAE가 정확도 평가에 더 유리할 수 있다.27
본 연구에서, 평균 ME는 공식에 따라 -0.014 D에서 -0.124 D 사이였고, 이는 -0.04 D에서 0.49 D인 이전 연구와 일치하였다. 28,29 평균 MAE는 공식에 따라 0.376 D에서 0.441 D까지 분포하였고 이는 0.309 D에서 0.433 D인 이전 연구와 일치하였다.28-31 MedAE는 0.290 D에서 0.355 D까지였으며 이는 0.160 D에서 0.310 D인 이전 연구와 일치하였다.17 한편 MAE가 0.5 D 이내 비율은 공식에 따라 57.4% (SRK/T)에서 83.3% (Holladay)까지였는데 각각 이전 연구와 일치하였다.28,30-32 이러한 값의 차이는 공식의 정확도를 반영할 수 있다. 이 연구에서 Barrett II은 모든 환자에게 가장 정확하였고 Haigis가 그 다음이었다. Melles et al30은 Barrett II이 가장 정확하고, Olsen과 Haigis가 그 다음이라고 보고하였다. Tang et al33은 Hill-RBF 공식이 가장 낮은 MAE (0.384 D)를 보였다고 하였으며 0.5 D (75.5%) 내 비율에서도 Barrett II 또는 Holladay 2 공식보다 더 정확하다고 보고하였다. Savini et al34은 Kane 공식이 예측오차 <0.25 D (41%)로 두 번째로 높은 정확도를 보였고 Haigis 공식이 <0.25 D (56%)를 보였으며 대체로 모든 공식이 좋은 결과를 보였다고 보고하였다.
인공수정체 도수 계산의 정확성에 가장 큰 영향을 미치는 인자는 AXL로 알려져 있다.1 이에 본 연구에서는 AXL에 따른 공식의 정확도를 비교하였다. AXL 25 mm를 기준으로 분류하였는데 기존 연구에서도 이 기준으로 분류한 바가 있다.17,35,36 Haigis 공식은 AXL <25 mm로 일반적인 눈에서 가장 정확하였고, Barrett II가 그 다음이었다. Tang et al33은 Hill-RBF 공식이 0.5 D (77.6%) 이내의 비율이 더 높고 Barrett II 또는 Holladay 공식보다 더 정확하다고 보고하였다. Pereira et al37은 EVO 2.0이 0.25 D (50.0%)와 0.5 D (76.6%) 내에서 높은 비율을 보였고, Kane 공식은 0.25 D (49.0%)와 0.5 D (77.7%) 내에서 높은 비율을 보였음을 보고하였다. AXL (>25 mm)이 긴 눈의 경우, Hoffer Q 공식이 가장 정확하였고, Olsen과 Barrett II이 그 다음이었다. Tang et al33은 Holladay 공식(65.3%)이 긴 눈에 가장 정확하다고 보고하였다. Guo et al38은 AXL ≥ 29.0 mm의 눈을 대상으로 EVO 2.0, Kane, SRK/T, Barrett Universal II, Haigis, Olsen 등 6개의 IOL 계산식을 비교한 결과 EVO 2.0, Kane, Barrett II, Olsen 공식의 정확도가 SRK/T 및 Haigis 공식보다 우수한 것으로 보고하였다. Melles et al30은 Olsen과 Barrett II 공식이 긴 눈에서 가장 정확하다는 것을 보여주었다. 그러나 이러한 연구는 EVO 2.0, Kane 및 Hill-RBF와 같은 새로 개발된 공식을 사용하지 않았다. Cheng et al39은 Kane 공식이 highly myopia (AXL>26 mm)에서 MAE가 0.34 D, extremely myopia (AXL>30 mm)에서 MAE가 0.31 D로 가장 높은 정확도를 보였다고 하였다. 본 연구에서는 긴 안축장에서 Olsen과 Barrett II의 정확도가 높았으며 이는 이전 연구와 일치하였다.30,38 한편 Hoffer Q가 가장 높은 정확도를 보였으나 유의한 차이를 보이지는 않았다. Hoffer Q 공식은 이론적인 인공수정체(IOL) 도수 공식에 대한 인공수정체 전방깊이(ACD)를 예측하기 위해 개발되었으며 맞춤형 ACD, 축 길이 및 각막 곡률에 따라 결정되며40 기존 문헌들에서는 Hoffer Q는 짧은 안축장에서 다른 공식에 비해 높은 정확도를 보였다.41 본 연구에서 사용된 LENSTAR 900의 광학적 생체 측정 방법을 이용한 정확한 전방깊이의 측정이 Hoffer Q의 예측오차를 줄였을 수 있다.42
K값 또한 인공수정체의 도수 계산의 정확성에 영향을 미치는 인자 중의 하나이다.1,43 K값(<46 D)이 일반적인 눈의 경우, MAE와 MedAE에서 Hagis 공식이 가장 정확하였고, Hoffer Q와 Barrett II가 그 다음이었다. K값(≥46 D)이 큰 환자군에서 또한 MAE와 MedAE에서 Haigis가 가장 정확하였으며 이어서 Barrett II와 Olsen이 정확도가 높았다. Röggla et al41에 따르면 K값이 크거나 일반적인 군 모두 MedAE 기준으로 Haigis의 정확도가 가장 높았다고 보고하였다.
인공수정체 도수 계산의 정확도에 대해 Barrett II와 Kane 공식이 우수하다는 결과들이 기존에 보고되었다.28,29,32,34 다른 보고들에서는 기존 공식 중에서는 Haigis가 전반적으로 높은 정확도를 보이거나,13,28,36 신세대공식과 비슷한 정도의 우수한 결과를 보여주었다.13,15,16,32 이는 Barrett II와 Haigis의 정확도가 높게 나온 본 연구와 일치한다. 한편 MAE가 1.0 D 이상의 굴절놀람(refractive surprise)을 보였던 환자는 총 11명이었다(Table 8). 2번 환자는 술 안의 automatic refraction (AR)으로 측정한 K값과 렌즈스타로 측정한 K값이 1.0 D 이상 차이가 났고 5번 환자의 경우 AR로 측정한 K값이 방문 시마다 변동이 심하였다. 4번 환자는 양안의 렌즈스타로 측정한 K값이 1.0 D 이상 차이 났다. 6번 환자는 양안의 각막난시가 2.5 D 이상 차이가 났으며 8번 환자는 렌즈스타로 측정한 K값이 41로 매우 낮았고 11번 환자는 46.67로 높았다. The Royal College of Ophthalmologists에서 발행한 Cataract Surgery Guidelines에 따르면 안축장이 21.2 mm 미만, 26.6 mm 이상일 경우, mean K값이 41 D 이하, 47 D 이상일 경우, 각막난시가 2.5 D 이상일 경우, 양안의 안축장이 0.7 mm 이상 차이나는 경우, 양안의 Mean 값이 0.9 D 이상 차이나는 경우 측정의 오류일 가능성이 있어 재검사를 권장하고 있다.44 11명의 환자와 전체 환자군을 비교하였을 때 유의한 차이를 보이는 공통된 인자는 찾을 수 없었으나 개개인별로 위와 같은 특징들을 보였다.
본 연구는 몇 가지 제한점을 가지고 있는데 첫 번째로는 constant optimization을 생략하고 ULIB에서 제공하는 최적화된 상수를 사용하였다. Constant optimization은 결국 각 공식별 굴절예측 값을 정확히 하기 위한 것이며 또한 공식별 정확도를 조금 더 객관적으로 비교하기 위해 평균 예측오차율을 영점 조절하는 것이다. 본 연구에서는 MAE, MedAE, 0.5 D 이내 포함된 비율, 평균 예측오차의 표준편차(SD of PE)를 비교하였으며 이들의 결과값이 일치하였다. 두 번째는 술 후 굴절값의 측정 시기를 2개월 시점으로 하였으나 환자마다 굴절값이 안정되는 시기의 차이가 있었을 것으로 보인다. 또한, 굴절값 측정에 사용한 자동굴절검사 기계의 경우 환자의 협조도에 따라 오차가 발생하였을 수 있으며 이에 따른 예측오차가 발생할 수 있을 것으로 보인다. 본 연구에서는 기존 문헌들에 비해 공식별 0.5 D 이내 비율이 낮은 경향을 보인 이유일 수 있을 것이다. 하지만 0.75 D, 1.0 D 이내 비율은 비슷한 수준으로 나타났다. 마지막으로 긴 안축장의 환자군이 20명으로 비교적 작으며 25 mm를 기준으로 분류하여 정상 안축장 길이의 환자군과 충분한 차이를 보이지 않았을 수 있다. 기존 논문에서는 안축장을 25 mm를 기준으로 분류하기도 하지만 26 mm를 기준으로 분류한 경우가 많다.17,35,36,45,46 이는 짧은 안축장에서 우세하다고 알려진 Hoffer Q가 높은 정확도를 보인 이유일 수도 있다. 마지막으로 수술 전 biometry 측정 시 오차가 의심되는 환자들이 있었으며 MAE가 1.0 D 이상 차이나는 원인이 되었을 수 있다. 평균값을 벗어나는 수치나 양안의 차이를 보이는 경우 수술 전 재검사가 필요할 것이다.
결론적으로, Barrett II 공식이 모든 환자에게 가장 정확하였고, Haigis 공식이 그 다음이었다. Haigis 공식은 AXL <25 mm인 일반적인 눈에서 가장 정확하였고, Barrett II 공식이 그 뒤를 이었다. AXL이 긴 눈의 경우, Hoffer Q 공식이 가장 정확하였고, Olsen 공식과 Barrett II 공식 순이었다. 각막곡률이 높은 환자군에서는 Haigis와 Barrett II의 정확도가 높았다. AI를 이용한 IOL 파워 공식의 정확도는 여전히 기존 공식에 비해 떨어지지만, 인공신경망은 많은 양의 데이터를 학습하고 분석할 수 있으며 추론 능력도 높아지고 있기 때문에 앞으로 정확도가 향상될 것으로 기대된다.
Acknowledgments
This research was supported by the National Research Foundation of Korea (NRF-2023R1A2C2002674).
Figure 1.
MAE according to AXL or mean K and biometric formula. MAE = mean absolute error; AXL = axial length; K = keratometry; D = diopters.
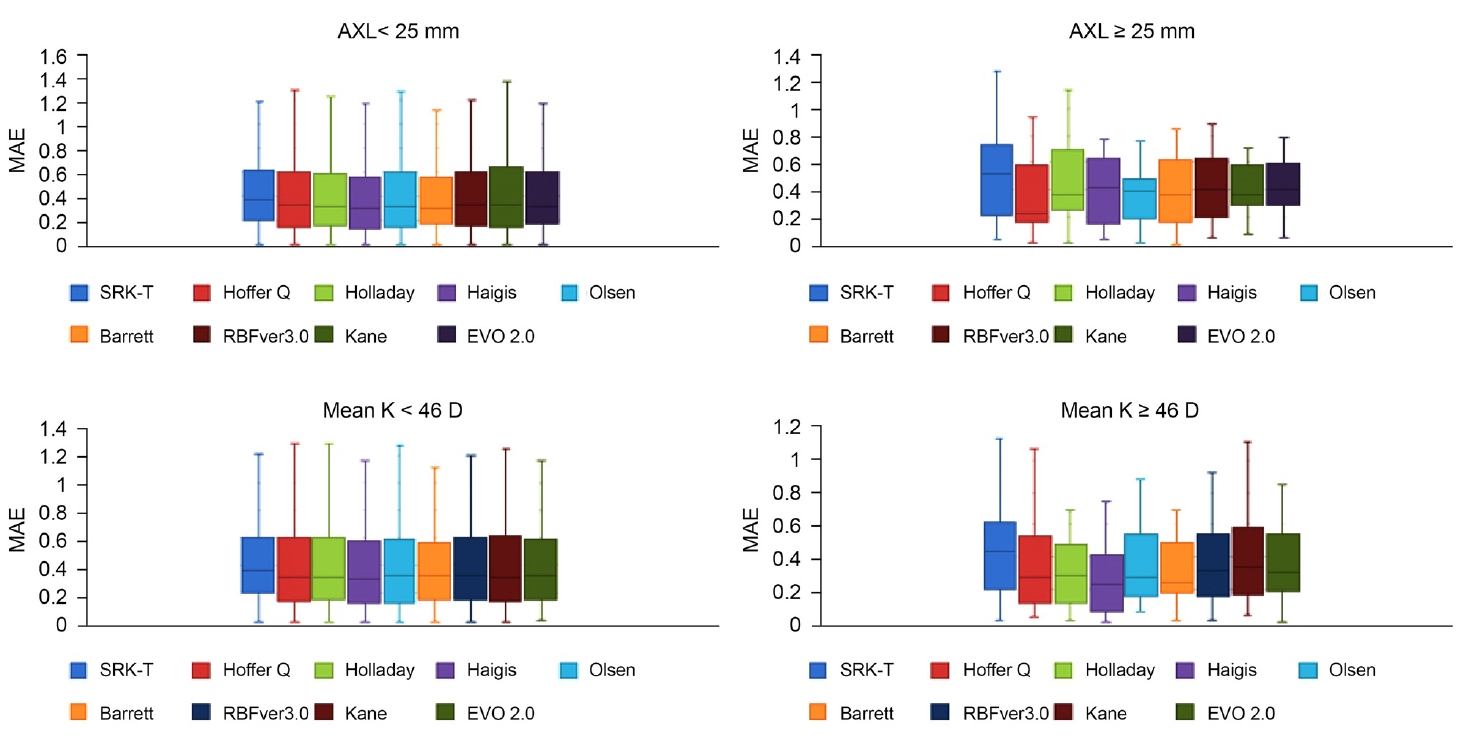
Table 1.
Patient demographic and clinical characteristics for each IOL groups
| ALCON® SN60WF | TECNIS® ZCB00 | p-value | |
|---|---|---|---|
| Number of patients (eyes) | 87 (87) | 141 (141) | - |
| Sex, male:female | 31:56 | 47:94 | 0.724 |
| Age (years) | 72.78 ± 6.78 | 68.33 ± 10.02 | 0.000* |
| Preoperative refraction (SE) | -0.299 ± 0.51 | -0.45 ± 0.72 | 0.145 |
| Axial length (mm) | 23.53 ± 1.01 | 23.62 ± 1.02 | 0.515 |
| Central corneal thickness (µm) | 528.58 ± 29.33 | 539.19 ± 31.21 | 0.012* |
| Aqueous depth (mm) | 2.54 ± 0.40 | 2.59 ± 0.43 | 0.434 |
| Anterior chamber depth (mm) | 3.07 ± 0.40 | 3.11 ± 0.39 | 0.426 |
| Lens thickness (mm) | 4.60 ± 0.34 | 4.54 ± 0.38 | 0.223 |
| Mean keratometry (D) | 44.00 ± 1.38 | 44.31 ± 1.46 | 0.112 |
Table 2.
Information of two types of IOLs
Table 3.
Refractive prediction errors, SD of PE, MAE, and MedAE for SN60WF and ZCB00 IOL
Table 4.
Percentage of eyes within certain range of prediction Error for SN60WF and ZCB00 IOL
| Formula |
ALCON® SN60WF |
TECNIS® ZCB00 |
||||
|---|---|---|---|---|---|---|
| ±0.50 D (%) | ± 0.75 D (%) | ± 1.00 D (%) | ±0.50 D (%) | ± 0.75 D (%) | ± 1.00 D (%) | |
| SRK/T | 67.8* | 86.2 | 95.4 | 57.4 | 83.0 | 92.2 |
| Hoffer Q | 74.7 | 88.5 | 97.7 | 67.4 | 87.2 | 92.9 |
| Holladay | 73.6 | 88.5 | 95.4 | 65.2 | 85.1 | 91.5 |
| Haigis | 75.9 | 92.0 | 96.6 | 66.7 | 85.1 | 94.3 |
| Olsen | 69.0 | 88.5 | 96.6 | 68.8 | 87.2 | 95.7 |
| Barrett | 70.1 | 92.0 | 96.6 | 70.2 | 87.9 | 94.3 |
| Hill-RBF | 73.6 | 87.4 | 95.4 | 64.5 | 81.6 | 95.0 |
| Kane | 63.2 | 81.6 | 92.0 | 66.7 | 85.1 | 95.0 |
| EVO 2.0 | 67.8 | 87.4 | 94.3 | 68.8 | 86.5 | 94.3 |
Table 5.
Patient demographic and clinical characteristics for axial length (AXL) and keratometry (K) groups
| AXL < 25 mm (n = 208) | AXL ≥ 25 mm (n = 20) | p-value | K < 46 D (n = 204) | K ≥ 46 D (n = 24) | p-value | |
|---|---|---|---|---|---|---|
| Axial length (mm) | 23.38 ± 0.75 | 25.81 ± 0.64 | 0.000* | 23.70 ± 1.00 | 22.62 ± 0.53 | 0.000* |
| Central corneal thickness (µm) | 533.51 ± 30.30 | 546.50 ± 35.71 | 0.099 | 534.68 ± 31.52 | 539.08 ± 25.07 | 0.501 |
| Anterior chamber depth (mm) | 2.54 ± 0.38 | 3.40 ± 0.38 | 0.001* | 3.10 ± 0.40 | 3.07 ± 0.34 | 0.635 |
| Lens thickness (mm) | 4.59 ± 0.37 | 4.45 ± 0.41 | 0.109 | 4.57 ± 0.39 | 4.51 ± 0.37 | 0.599 |
| Mean keratometry (D) | 44.21 ± 1.45 | 43.34 ± 1.08 | 0.006* | 43.91 ± 1.23 | 46.61 ± 0.40 | 0.000* |
| White to white (mm) | 10.97 ± 1.52 | 11.59 ± 0.77 | 0.192 | 11.11 ± 1.23 | 10.30 ± 2.66 | 0.053 |
Table 6.
Refractive prediction errors, SD, MAE, and MedAE, percentage of eyes within certain range of prediction error for two groups (AXL < 25 mm, AXL ≥ 25 mm)
| Formula | ME (D) | SD (D) | MAE (D) | MedAE (D) | ± 0.50 D (%) | ± 0.75 D (%) | ± 1.00 D (%) |
|---|---|---|---|---|---|---|---|
| AXL < 25 mm | |||||||
| SRK/T | -0.136 | 0.522 | 0.436* | 0.360 | 62.5† | 85.1 | 93.3 |
| Hoffer Q | -0.114 | 0.501 | 0.395 | 0.320 | 69.7 | 88.5 | 94.2 |
| Holladay | -0.131 | 0.490 | 0.397 | 0.310 | 68.8 | 87.0 | 92.8 |
| Haigis | -0.093 | 0.485 | 0.374 | 0.290 | 70.2 | 87.0 | 94.7 |
| Olsen | -0.023 | 0.500 | 0.386 | 0.310 | 67.8 | 87.5 | 95.7 |
| Barrett | -0.013 | 0.487 | 0.387 | 0.300 | 70.2 | 88.9 | 94.7 |
| Hill-RBF | -0.020 | 0.525 | 0.407 | 0.325 | 68.3 | 83.7 | 94.7 |
| Kane | -0.127 | 0.545 | 0.428 | 0.320 | 65.4 | 82.2 | 93.3 |
| EVO 2.0 | -0.048 | 0.517 | 0.403 | 0.310 | 69.2 | 86.1 | 93.8 |
| AXL ≥ 25 mm | |||||||
| SRK/T | -0.049 | 0.591 | 0.488 | 0.510 | 50.0 | 75.0 | 95.0 |
| Hoffer Q | 0.109 | 0.457 | 0.347 | 0.225 | 75.0 | 80.0 | 100.0 |
| Holladay | -0.017 | 0.555 | 0.446 | 0.360 | 65.0 | 80.0 | 95.0 |
| Haigis | -0.147 | 0.440 | 0.389 | 0.410 | 70.0 | 95.0 | 100.0 |
| Olsen | -0.108 | 0.419 | 0.374 | 0.390 | 80.0 | 90.0 | 100.0 |
| Barrett | -0.020 | 0.461 | 0.378 | 0.360 | 70.0 | 95.0 | 100.0 |
| Hill-RBF | -0.073 | 0.496 | 0.414 | 0.400 | 70.0 | 90.0 | 100.0 |
| Kane | -0.093 | 0.446 | 0.404 | 0.360 | 65.0 | 100.0 | 100.0 |
| EVO 2.0 | -0.109 | 0.459 | 0.421 | 0.395 | 60.0 | 95.0 | 100.0 |
Table 7.
Refractive prediction errors, SD, MAE, and MedAE, percentage of eyes within certain range of prediction error for two groups (K < 46 D, K ≥ 46 D)
| Formula | ME (D) | SD (D) | MAE (D) | MedAE (D) | ± 0.50 D (%) | ± 0.75 D (%) | ± 1.00 D (%) |
|---|---|---|---|---|---|---|---|
| K < 46 D | |||||||
| SRK/T | -0.092 | 0.529 | 0.436† | 0.365 | 61.8* | 84.3 | 93.6 |
| Hoffer Q | -0.089 | 0.504 | 0.395 | 0.320 | 70.1 | 87.3 | 95.1 |
| Holladay | -0.106 | 0.503 | 0.406 | 0.320 | 66.7 | 85.8 | 93.1 |
| Haigis | -0.113 | 0.488 | 0.387 | 0.310 | 69.1 | 86.8 | 95.1 |
| Olsen | -0.040 | 0.499 | 0.389 | 0.330 | 68.6 | 87.3 | 95.6 |
| Barrett | 0.001 | 0.493 | 0.395 | 0.330 | 69.1 | 88.7 | 94.6 |
| Hill-RBF | -0.023 | 0.527 | 0.411 | 0.330 | 67.6 | 83.8 | 94.6 |
| Kane | -0.121 | 0.540 | 0.427 | 0.320 | 64.7 | 84.3 | 93.6 |
| EVO 2.0 | -0.048 | 0.514 | 0.406 | 0.330 | 68.6 | 87.7 | 94.1 |
| K ≥ 46 D | |||||||
| SRK/T | -0.438 | 0.384 | 0.481† | 0.435 | 58.3* | 83.3 | 91.7 |
| Hoffer Q | -0.138 | 0.452 | 0.359 | 0.275 | 70.8 | 91.7 | 91.7 |
| Holladay | -0.241 | 0.402 | 0.358 | 0.285 | 83.3 | 91.7 | 91.7 |
| Haigis | 0.032 | 0.381 | 0.278 | 0.235 | 79.2 | 95.8 | 95.8 |
| Olsen | 0.056 | 0.411 | 0.345 | 0.275 | 70.8 | 91.7 | 100.0 |
| Barrett | -0.143 | 0.360 | 0.309 | 0.245 | 79.2 | 95.8 | 100.0 |
| Hill-RBF | -0.047 | 0.438 | 0.353 | 0.320 | 75.0 | 87.5 | 100.0 |
| Kane | -0.149 | 0.489 | 0.413 | 0.340 | 70.8 | 79.2 | 95.8 |
| EVO 2.0 | -0.098 | 0.479 | 0.399 | 0.310 | 66.7 | 79.2 | 95.8 |
Table 8.
Refractive surprise patient demographic and clinical characteristics
AXL = axial length; Diff. AXL = difference in axial length between fellow eyes; K value = keratometry; Diff. K value = difference in mean keratometry between fellow eyes; Corneal Astig. = corneal astigmatism; ACD = anterior chamber depth; CCT = central corneal thickness; LT = lens thickness; F = female; M = male.
REFERENCES
1) Kane JX, Chang DF. Intraocular lens power formulas, biometry, and intraoperative aberrometry: a review. Ophthalmology 2021;128:e94-114.


2) Goto S, Maeda N, Ohnuma K, et al. Preliminary demonstration of a novel intraocular lens power calculation: the O formula. J Cataract Refract Surg 2022;48:1305-11.



3) Fram NR, Masket S, Wang L. Comparison of intraoperative aberrometry, OCT-based IOL formula, Haigis-L, and masket formulae for IOL power calculation after laser vision correction. Ophthalmology 2015;122:1096-101.


4) Vander Mijnsbrugge J, Fils JF, Jansen J, et al. The role of the vitreous body in effective IOL positioning. Graefes Arch Clin Exp Ophthalmol 2018;256:1517-20.



5) Aristodemou P, Knox Cartwright NE, Sparrow JM, Johnston RL. Formula choice: Hoffer Q, Holladay 1, or SRK/T and refractive outcomes in 8108 eyes after cataract surgery with biometry by partial coherence interferometry. J Cataract Refract Surg 2011;37:63-71.


6) Yang S, Whang WJ, Joo CK. Effect of anterior chamber depth on the choice of intraocular lens calculation formula. PLoS One 2017;12:e0189868.



7) Eom Y, Kang SY, Song JS, et al. Comparison of Hoffer Q and Haigis formulae for intraocular lens power calculation according to the anterior chamber depth in short eyes. Am J Ophthalmol 2014;157:818-24.e2.


8) Miraftab M, Hashemi H, Fotouhi A, et al. Effect of anterior chamber depth on the choice of intraocular lens calculation formula in patients with normal axial length. Middle East Afr J Ophthalmol 2014;21:307-11.



9) Gatinel D, Debellemanière G, Saad A, et al. Determining the theoretical effective lens position of thick intraocular lenses for machine learning-based IOL power calculation and simulation. Transl Vis Sci Technol 2021;10:27.

10) Olsen T, Hoffmann P. C constant: new concept for ray tracing-assisted intraocular lens power calculation. J Cataract Refract Surg 2014;40:764-73.


11) Xia T, Martinez CE, Tsai LM. Update on intraocular lens formulas and calculations. Asia Pac J Ophthalmol (Phila) 2020;9:186-93.



12) Ong APC, Zhang J, Vincent AL, McGhee CNJ. Megalocornea, anterior megalophthalmos, keratoglobus and associated anterior segment disorders: a review. Clin Exp Ophthalmol 2021;49:477-97.



13) Carmona GonzálezD, Palomino Bautista C. Accuracy of a new intraocular lens power calculation method based on artificial intelligence. Eye (Lond) 2021;35:517-22.



14) Sramka M, Slovak M, Tuckova J, Stodulka P. Improving clinical refractive results of cataract surgery by machine learning. PeerJ 2019;7:e7202.




15) Zhao J, Liu LP, Cheng HH, et al. Accuracy of eight intraocular lens power calculation formulas for segmented multifocal intraocular lens. Int J Ophthalmol 2020;13:1378-84.



16) Szalai E, Toth N, Kolkedi Z, et al. Comparison of various intraocular lens formulas using a new high-resolution swept-source optical coherence tomographer. J Cataract Refract Surg 2020;46:1138-41.


17) Sánchez-Liñan N, Pérez-Rueda A; Parrón-Carreño T, et al. Evaluation of biometric formulas in the calculation of intraocular lens according to axial length and type of the lens. Sci Rep 2023;13:4678.


18) Dong J, Zhang Y, Zhang H, et al. Comparison of axial length, anterior chamber depth and intraocular lens power between IOLMaster and ultrasound in normal, long and short eyes. PLoS One 2018;13:e0194273.



19) Charalampidou S, Cassidy L, Ng E, et al. Effect on refractive outcomes after cataract surgery of intraocular lens constant personalization using the Haigis formula. J Cataract Refract Surg 2010;36:1081-9.


20) Scholtz SK, Schwemm M, Eppig T, et al. Benefits and new features of a modern international internet database "IOLCon" for updated and optimized IOL constants and IOL specifications. Klin Monbl Augenheilkd 2021;238:996-1003.


21) Olsen T. Sources of error in intraocular lens power calculation. J Cataract Refract Surg 1992;18:125-9.


22) Ryu S, Jun I, Kim TI, et al. Accuracy of the Kane formula for intraocular lens power calculation in comparison with existing formulas: a retrospective review. Yonsei Med J 2021;62:1117-24.




23) Voytsekhivskyy OV, Hoffer KJ, Savini G, et al. Clinical accuracy of 18 IOL power formulas in 241 short eyes. Curr Eye Res 2021;46:1832-43.


24) Jasman AA, Shaharuddin B, Noor RA, et al. Prediction error and accuracy of intraocular lens power calculation in pediatric patient comparing SRK II and Pediatric IOL Calculator. BMC Ophthalmol 2010;10:20.




25) Wlaź A, Kustra A, Rozegnal-Madej A, Zarnowski T. Intraocular lens power calculations in eyes with pseudoexfoliation syndrome. Sci Rep 2021;11:19071.


26) Ferreira TB, Ribeiro P, Ribeiro FJ, O'Neill JG. Comparison of methodologies using estimated or measured values of total corneal astigmatism for toric intraocular lens power calculation. J Refract Surg 2017;33:794-800.


27) Hoffer KJ, Aramberri J, Haigis W, et al. Protocols for studies of intraocular lens formula accuracy. Am J Ophthalmol 2015;160:403-5.e1.


28) Shammas HJ, Shammas MC, Jivrajka RV, et al. Effects on IOL power calculation and expected clinical outcomes of axial length measurements based on multiple vs single refractive indices. Clin Ophthalmol 2020;14:1511-9.


29) Zhang Y, Li T, Reddy A, Nallasamy N. Gender differences in refraction prediction error of five formulas for cataract surgery. MC Ophthalmol 2021;21:183.


30) Melles RB, Holladay JT, Chang WJ. Accuracy of intraocular lens calculation formulas. Ophthalmology 2018;125:169-78.


31) Wallace HB, Misra SL, Li SS, McKelvie J. Predicting pseudophakic refractive error: Interplay of biometry prediction error, anterior chamber depth, and changes in corneal curvature. J Cataract Refract Surg 2018;44:1123-9.


32) Lwowski C, Pawlowicz K, Hinzelmann L, et al. Prediction accuracy of IOL calculation formulas using the ASCRS online calculator for a diffractive extended depth-of-focus IOL after myopic laser in situ keratomileusis. J Cataract Refract Surg 2020;46:1240-6.


33) Tang KS, Tran EM, Chen AJ, et al. Accuracy of biometric formulae for intraocular lens power calculation in a teaching hospital. Int J Ophthalmol 2020;13:61-5.



34) Savini G, Di Maita M, Hoffer KJ, et al. Comparison of 13 formulas for IOL power calculation with measurements from partial coherence interferometry. Br J Ophthalmol 2021;105:484-9.


35) Malik TG, Moin M, Alam R. A comparison of SRK/T formula with Hill RBF 2 and Barrett Universal II in the calculation of intraocular lens power. J Pak Med Assoc 2022;72:1373-7.


36) Razmjoo H, Atarzadeh H, Kargar N, et al. The comparative study of refractive index variations between Haigis, Srk/T and Hoffer-Q formulas used for preoperative biometry calculation in patients with the axial length >25 mm. Adv Biomed Res 2017;6:78.



37) Pereira A, Popovic MM, Ahmed Y, et al. A comparative analysis of 12 intraocular lens power formulas. Int Ophthalmol 2021;41:4137-50.



38) Guo C, Yin S, Qiu K, Zhang M. Comparison of accuracy of intraocular lens power calculation for eyes with an axial length greater than 29.0 mm. Int Ophthalmol 2022;42:2029-38.




39) Cheng H, Wang L, Kane JX, et al. Accuracy of artificial intelligence formulas and axial length adjustments for highly myopic eyes. Am J Ophthalmol 2021;223:100-7.


40) Hoffer KJ. The Hoffer Q formula: a comparison of theoretic and regression formulas. J Cataract Refract Surg 1993;19:700-12.


41) Röggla V, Langenbucher A, Leydolt C, et al. Accuracy of common IOL power formulas in 611 eyes based on axial length and corneal power ranges. Br J Ophthalmol 2021;105:1661-5.


42) Song JS, Yoon DY, Hyon JY, Jeon HS. Comparison of ocular biometry and refractive outcomes using IOL Master 500, IOL Master 700, and Lenstar LS900. Korean J Ophthalmol 2020;34:126-32.




43) Yin S, Guo C, Qiu K, et al. Assessment of the influence of keratometry on intraocular lens calculation formulas in long axial length eyes. Int Ophthalmol 2022;42:3211-9.



44) Scientific Department The Royal College of Ophthalmologists. Cataract Surgery Guidelines. The Royal College of Ophthalmologists: London, 2010;45.
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 475 View
- 58 Download
- Related articles
-
Incidence Rate and Risk Factors of Intraocular Lens Dislocation in South Korea2024 March;65(3)




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



